Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Infectio
Print version ISSN 0123-9392
Infect. vol.10 no.4 Bogotá Oct./Dec. 2006
REVISIÓN DE TEMA
Diagnóstico de la infección por el virus de la inmunodeficiencia humana
Diagnosis of human immunodeficiency virus
SIGIFREDO OSPINA O.1
1Médico, microbiólogo, epidemiólogo Jefe, Departamento de Epidemiología Hospitalaria, Hospital Universitario San Vicente de Paúl, Medellín, Colombia.
Fecha de recepción: 05/11/2006; fecha de aceptación; 29/11/2006
Resumen
La infección por el VIH y su consecuencia, el sida, se han podido conocer, seguir, y, en algunos casos, controlar, gracias a la disponibilidad de pruebas diagnósticas al acceso de la población. Una prueba diagnóstica en un individuo infectado asintomático puede significar muchos años de vida ganados y con buena calidad, al mismo tiempo que permite evitar nuevas infecciones. El diagnóstico de la infección por el VIH se establece al aislar el virus en cultivo, detectar el antígeno P24, medir la respuesta de anticuerpos o detectar su ácido nucleico. En este momento se dispone de diferentes tipos de pruebas en varios formatos, en general, con muy buena sensibilidad y especificidad. Después de realizar la asesoría previa a la prueba, el abordaje diagnóstico se inicia con una prueba presuntiva o de tamizaje, tipo ELISA, que luego debe confirmarse con una prueba más específica, tipo Western Blot. En algunos casos, como en el niño menor de 18 meses, es necesario recurrir a pruebas moleculares para establecer el diagnóstico. En este artículo se presenta una revisión actualizada de los diferentes métodos disponibles para el diagnóstico de la infección por el VIH, así como sus ventajas, desventajas y limitaciones.
Palabras clave: VIH, diagnóstico, prueba de tamizaje, prueba confirmatoria.
Abstract
HIV infection and AIDS, have been known, followed and controlled due to availability of diagnostic tests. An opportune diagnostic test in an asymptomatic patient might represent a good number of years with a high quality of life for an infected patient. HIV infection tests stands on the basis of the recognition of virus in a culture, or the presence of P24 antigen, the antibody response or detecting viral DNA. Currently, the available tests offer good specificity and sensitivity. After the pre-test assessment, diagnostic approach begins with a screening test that should be followed by a confirmatory test like Western blot. In the case of children younger than 18 months, molecular tests are needed. A current review of the diagnostic methods is presented, showing not only the known advantages but also the disadvantages and limitations of these tests.
Keywords: HIV, diagnosis, screening test, confirmatory test.
GENERALIDADES DEL VIRUS
El virus de la inmunodeficiencia humana (VIH) pertenece a la familia Retroviridae, género Lentivirinae. El genoma de los retrovirus consta de dos copias idénticas de ARN de cadena simple y está compuesto por tres genes principales, denominados gag, pol y env, los cuales codifican las proteínas del core, la envoltura y las enzimas. La organización de los genomas es siempre la misma, 5´-gag-pol-env-3´, y, según el retrovirus, hay genes accesorios que se sobreponen a los genes principales (1).
En general, los retrovirus se componen de: una envoltura formada por una glucoproteína de superficie y una proteína transmembrana; una cápside viral o core que incluye las proteínas de la matriz, cápside y nucleocápside; enzimas como la transcriptasa reversa, la proteasa y la integrasa, las cuales son muy importantes para la replicación del virus, y otras proteínas no esenciales (1).
La gran variabilidad del VIH y su capacidad de mutación y recombinación han llevado a la identificación de varios grupos y serotipos. El grupo M del VIH 1 se divide en subtipos de la A a la K; también, se han descrito el grupo O y el grupo N. Los virus del grupo M son los responsables de la pandemia y se encuentran en todo el mundo, mientras que los del grupo O están restringidos a ciertas áreas geográficas y son poco frecuentes. El grupo N se ha identificado en pocos individuos. Del VIH 2 se han identificado 5 subtipos, de la A a la E, y más recientemente, el F y el G (1).
DIAGNÓSTICO POR EL LABORATORIO
Las pruebas de laboratorio para el diagnóstico de la infección por el VIH están indicadas en adolescentes y adultos entre 13 y 64 años, que tienen o han tenido relaciones sexuales sin protección con pareja no estable, personas con antecedentes de infecciones de transmisión sexual, antecedente de tatuaje o piercing con instrumentos potencialmente contaminados, usuarios de drogas intravenosas, contactos de un caso positivo, solicitud voluntaria de la prueba, o pacientes de otras edades con claros factores de riesgo (2, 3). Debe ofrecerse a la mujer embarazada, como parte de su control prenatal. Las pruebas están igualmente indicadas en el niño hijo de una madre positiva, teniendo en cuenta la selección de la prueba, según la edad, y en los padres cuando se detecta primero el niño (4).
A muchas personas infectadas asintomáticas, la prueba diagnóstica de VIH les da no sólo la posibilidad de una mayor supervivencia sino que contribuye a que no disemine la infección a otros (5).
En Colombia, el Decreto 1543 de 1997 del Ministerio de Salud establece que la prueba para VIH sólo podrá efectuarse previo consentimiento de la persona o cuando la autoridad sanitaria competente lo determine. El fin de esto es poder brindarle a la persona una adecuada asesoría antes de la realización de la misma (6). Más recientemente, el mismo Ministerio adoptó, en la Resolución 003342 del 22/ 09/2006, las guías de práctica clínica basadas en la evidencia para la prevención, el diagnóstico y el tratamiento de pacientes con VIH/sida (7).
El diagnóstico de la infección VIH se establece, además de los criterios clínicos y epidemiológicos, detectando anticuerpos, antígeno o ácido nucleico, o aislándolo en cultivo. A continuación se describen los diferentes tipos de pruebas disponibles, sus ventajas y sus limitaciones.
PRUEBAS PARA DETECCIÓN DE ANTICUERPOS
La producción de anticuerpos contra el VIH ocurre después de un período inicial de intensa replicación viral, con altos niveles de ARN y antígeno P24; se asume que, como en todas las infecciones virales, primero aparece la inmunoglobulina M y, luego, la G (8).
Las pruebas para detección de anticuerpos contra el VIH se dividen en: pruebas de tamizaje o presuntivas, las cuales poseen una alta sensibilidad y buena especificidad, y las pruebas confirmatorias, cuya característica es la alta especificidad.
Las pruebas para la detección de anticuerpos pueden clasificarse de la siguiente manera, según su generación: pruebas de primera generación, que usan lisados virales como antígeno y que se acompañan de alta frecuencia de falsos positivos; pruebas de segunda generación, que usan proteínas recombinantes del VIH, péptidos sintéticos o ambos como antígenos; pruebas de tercera generación, que usan péptido/proteína recombinantes; y pruebas de cuarta generación, que se basan en la detección simultánea de anticuerpos y complejos inmunes antígeno P24/anticuerpo y tienen una alta sensibilidad y especificidad (1, 10).
El tiempo de positividad para las pruebas de anticuerpos de tercera generación es de 20,3 días (IC95%, 8 - 32,5); Las pruebas de cuarta generación disminuyen el tiempo de detección en 3 a 5 días. Con las pruebas de tercera y cuarta generación, el 50% de los infectados pueden detectarse en las primeras tres semanas de la infección, un 45% de los restantes en los primeros dos meses y el otro 5% en seis meses o más (1).
La muestra que se utiliza para la detección de anticuerpos es de suero o plasma, aunque se dispone de pruebas que utilizan hisopado de mucosa gingival o yugal (saliva), orina o secreciones vaginales.
Pruebas rápidas para detección de anticuerpos.
Existen otros formatos para la detección de anticuerpos, los cuales emplean el flujo lateral o capilar de la muestra a través de un soporte sólido para permitir la interacción con un antígeno incorporado y utilizan la unión indirecta, el antígeno de captura, la aglutinación, la cromatografía o tipo "sándwich"; incluye controles para identificar la reactividad inespecífica. La muestra usualmente es sangre total, no se requiere equipo para su lectura y se puede conservar a temperatura ambiente. Son muy útiles en situaciones de emergencia, como al momento del parto o en accidentes de riesgo biológico. Debe tenerse en cuenta que son pruebas de tamizaje y que tienen las mismas limitaciones de período de ventana y que toda prueba reactiva debe confirmarse, máxime que su resultado es de tipo cualitativo (8).
Prueba de aglutinación de partículas para detección de anticuerpos. Son pruebas que se basan en la unión de los anticuerpos del VIH presentes en el suero del paciente, con pequeñas partículas que contienen antígeno del virus en la superficie, bajo el principio tipo sándwich de las pruebas de tercera generación. Estas pruebas tienen una alta sensibilidad y, relativamente, buena especificidad, por lo que son muy útiles como pruebas de tamizaje en áreas de limitados recursos, ya que son rápidas, simples y no requieren equipos (8).
PRUEBAS SEROLÓGICAS PARA LA DETECCIÓN DE ANTÍGENO
En la infección temprana existe un corto período en el que hay presencia del antígeno p24 del VIH-1 en ausencia de anticuerpos contra el mismo. Este antígeno puede detectarse por técnicas de ELISA. Algunos métodos incorporan un ajuste al pH o tratamiento con calor para separar los complejos p24-anti p24 y, así, mejorar la sensibilidad de la prueba (8).
La positividad de la prueba de antígeno p24 se detecta en un tiempo estimado de 26,4 días (IC95%, 12,6 - 38,7) (1).
La prueba de detección de antígeno tiene tres limitantes: en primer lugar, la presencia de anticuerpos puede llevar a la detección de niveles bajos o a falsos negativos; la otra situación es la presencia de inmunoglobulina específica, anticuerpos similares al factor reumatoideo, los cuales pueden hacer un puente entre el antígeno de captura y los trazadores, y causar detección en demasía o falsos positivos; el tercer problema es la baja sensibilidad de la prueba.
PRUEBAS EN CASA
Desde los comienzos de la epidemia se ha planteado la necesidad de una estrategia que permita un acceso fácil y anónimo de las personas a la prueba. En algunos países, existe la posibilidad para el paciente de adquirir de manera anónima un sistema para toma de muestra, previa consejería, y los resultados le son reportados con un código vía telefónica por un asesor.
También se han diseñado pruebas para realizar en casa. Sin embargo, éstas no se han aprobado por los organismos internacionales, ya que adolecen de la consejería antes y después de la prueba.
PRUEBAS EN MUESTRAS DIFERENTES A SANGRE, SUERO O PLASMA
Las secreciones de la cavidad oral contienen niveles detectables de anticuerpos contra el VIH-1, aunque en una proporción 1.000 veces inferior a la del suero. La muestra consiste en un hisopado de las encías y la mucosa yugal, y se utiliza en formatos tipo ELISA. Se han reportado falsos negativos en pacientes bajo terapia y falsos positivos, por lo que este tipo de pruebas siempre deben confirmarse por otra prueba (8, 11). En el comercio, existen formatos para muestras como orina y secreción vaginal, las cuales tienen la ventaja de la facilidad de la toma de la muestra. La prueba en secreción vaginal se recomienda para víctimas de abuso sexual, ya que los anticuerpos contra el VIH pueden detectarse en los espermatozoides y el líquido seminal. En general, tienen buena sensibilidad y especificidad, pero toda prueba reactiva requiere de una confirmatoria (12).
INTERPRETACIÓN DE LOS RESULTADOS DE LAS PRUEBAS DE TAMIZAJE
Cuando se analizan los resultados de las pruebas de tamizaje, debe tenerse en cuenta la posibilidad de falsos positivos por otros trastornos, la posibilidad de falsos negativos en las fases iniciales o finales por baja producción de anticuerpos, infecciones silenciosas que cursan con replicación viral pero sin desarrollo de anticuerpos, las limitantes de la prueba para detectar variantes como grupo 0 o para detectar VIH 2. Una transfusión masiva puede generar un falso negativo por efecto de la dilución.
Los falsos negativos pueden presentarse en las etapas iniciales de la infección cuando aún no hay producción de anticuerpos o están en muy baja cantidad, en las etapas terminales cuando hay un franco deterioro del sistema inmune y baja producción de anticuerpos, o cuando el paciente ha recibido terapia antirretroviral tempranamente (8).
Los falsos positivos son más comunes que los falsos negativos y se pueden presentar por problemas técnicos, multiparidad, alcoholismo, enfermedad reumática, trastornos hemorrágicos congénitos, sífilis, neurocisticercosis, infección aguda por dengue, malaria y hepatitis B, vacunación reciente para hepatitis B o rabia (8).
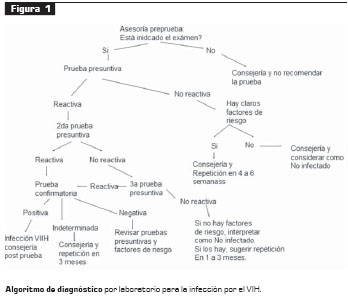
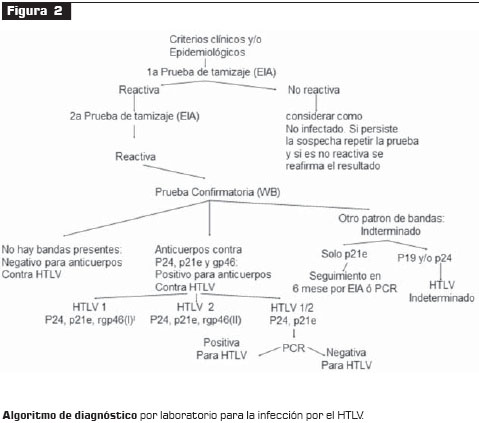
Toda prueba presuntiva reactiva debe repetirse, preferiblemente en una muestra diferente; si ésta es reactiva, se pasa a la prueba confirmatoria, pero, si es negativa, se realiza una tercera prueba presuntiva; la decisión se toma con base en dos resultados de tres, así: dos reactivas va a prueba confirmatoria, dos negativas se considera como no infectado y va a consejería, o se cita el paciente para una nueva prueba en cuatro semanas (figura 1 y figura 2).
PRUEBAS CONFIRMATORIAS PARA LA INFECCIÓN POR EL VIH
Como su nombre lo indica, estas pruebas están orientadas a confirmar la presencia de la infección por el VIH en un paciente con una prueba presuntiva doblemente reactiva, por lo que tienen una alta especificidad. Se basan en la detección de anticuerpos contra el virus o sus componentes.
WESTERN BLOT
El Western blot es la técnica más ampliamente utilizada y consiste en que las proteínas constitutivas del virus se separan por electroforesis y, luego, se transfieren a un papel de nitrocelulosa.
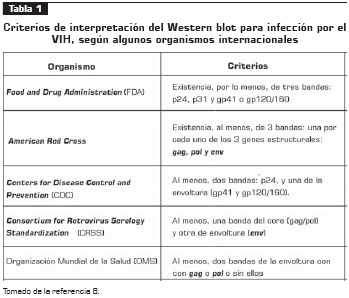
Estas proteínas fijadas son expuestas al suero del paciente, en el cual los anticuerpos específicos se unen a las proteínas presentes dando un patrón de bandas, cuya interpretación depende del criterio que se adopte en el laboratorio de acuerdo con lo definido por organismos internacionales, los cuales se presentan en la tabla 1.
El resultado de la prueba de Western blot se informa como negativo cuando hay ausencia total de bandas; como indeterminado, cuando no cumple los criterios definidos en la tabla 1 y no es egativo, y positivo cuando cumple los criterios, de acuerdo con el que se haya adoptado. El resultado indeterminado puede deberse a un período inicial de seroconversión o a un falso positivo, sobre todo cuando se trata de una sola banda, usualmente la p24. Este tipo de hallazgo puede estar en relación con lupus eritematoso sistémico, tiroiditis de Hashimoto, linfoma no Hodgkin, histiocitosis, muestra con elevada bilirrubina, hemólisis, factor reumatoideo, gammapatía policlonal, hemodiálisis, anticuerpos HLA y otras enfermedades infecciosas, incluso la infección por HTLV-1. Los antígenos clase II expresados en células H9 usadas para la propagación del VIH pueden ser igualmente causa de un Western blot indeterminado (8).
Una prueba de Western blot para VIH 1 sugestiva de infección por el VIH 2, debe ser confirmarse por un Western blot específico para VIH 2 o por pruebas que involucren proteínas recombinantes específicas. En algunos casos es necesario hacer PCR para ambos virus.
INMUNOFLUORESCENCIA
La inmunofluorescencia indirecta se ha utilizado ampliamente como prueba confirmatoria para la infección por el VIH-1 y lo siguen haciendo laboratorios con amplia experiencia con la prueba. Su desempeño es bueno pero requiere de personal debidamente entrenado para su lectura y de microscopio de fluorescencia (8, 9).
PRUEBAS PARA DETECCIÓN DE ÁCIDOS NUCLEICOS
Las técnicas de detección de ácidos nucleicos se utilizan para diagnóstico sólo en el caso de niños menores de 18 meses. En algunos casos se han utilizado para aclarar resultados indeterminados por los otros métodos. Su principal uso está en el seguimiento de la infección y el de la terapia (8).
Existen diferentes pruebas para detectar el ácido ribonucleico (ARN) del virus, tales como la amplificación por reacción en cadena de la polimerasa (PCR), la amplificación basada en la secuencia de ácido nucleico (NASBA), ahora disponible en tiempo real, y el ADN ramificado (bDNA).
Las diferentes técnicas disponibles comercialmente y aprobadas por los organismos competentes tienen un muy buen nivel de correlación (13, 14).
La prueba de PCR para ADN proviral se hace positiva 26,4 días (IC95%, 12,6 - 38,7) después de la infección. La PCR para ARN en plasma es positiva en promedio a los 31 días (IC95%, 16,7 - 45,3) (1).
TÉCNICAS VIROLÓGICAS PARA DETECTAR EL VIRUS
El cultivo del virus puede utilizarse para establecer el diagnóstico, pero requiere de una infraestructura con un alto nivel de bioseguridad y es poco sensible cuando se utiliza suero o plasma. Las células mononucleares de sangre periférica son más adecuadas, especialmente si están reducidas o agotadas de CD8+.
DIAGNÓSTICO DE LA INFECCIÓN POR EL VIH EN EL NIÑO
En el niño que ha adquirido la infección por transmisión vertical, las pruebas de detección de anticuerpos no son útiles antes de los 18 meses de edad; esto se debe al paso pasivo de anticuerpos de la madre, los cuales permanecen durante ese tiempo. Sin embargo, muestras pareadas al mes y a los 4 meses pueden ser de utilidad para ver el aumento de título. No obstante, las técnicas recomendadas son las de detección del ácido nucleico o aislamiento viral; las primeras son las usualmente recomendadas y utilizadas. Una tercera parte de los pacientes son detectados por PCR en los primeros 10 días de vida, el 50% en las primeras cuatro semanas y el resto en los siguientes dos meses (8, 15).
En el niño mayor de 18 meses se pueden utilizar las mismas pruebas diagnósticas que se utilizan en el adulto.
Tomado de la referencia 8.
REFERENCIAS
1. Schüpbach J. Human immunodeficiency viruses. En: Murria PR, Baron EJ, Jorgensen JH, Pfaller MA, Yolken RH, editores. Manual of Clinical Microbiology. 8th,edition. Washington, D.,C.: ASM Press; 2003. p.1253-81. [ Links ]
2. (Centers for Disease Control and Prevention. Revised recommendations for HIV screening of pregnant women. Perinatal counseling and guidelines consultation. MMWR2001;50(RR19):59-86. [ Links ]
3. Correa AL, Velásquez G. Síndrome de inmunodeficiencia adquirida y virus de la inmunodeficiencia humana. En: Restrepo A, Robledo J, Leiderman E, Restrepo M, Botero D, Bedoya VI, editores. Enfermedades infecciosas. Sexta edición. Medellín: CIB; 2003. p.642-69. [ Links ]
4. Centers for Disease Control and Prevention. Revised recommendations for HIV testing of adults, adolescents and pregnant women in health care settings. MMWR 2006;55(RR14):1-17. [ Links ]
5. Centers for Disease Control and Prevention. Twenty-five years of HIV/AIDS. United States. 1981-2006. MMWR 2006;55(21):585-9. [ Links ]
6. Ministerio de Salud Pública de Colombia. Decreto 1543 de 1997. Diario Oficial Nº 43062, del 17 de junio de 1997. [ Links ]
7. Ministerio de la Protección Social, República de Colombia. Guía para el manejo de VIH/SIDA basada en la evidencia. Colombia. Bogotá, 2005. [ Links ]
8. Maldarelli F. Diagnosis of human immunodeficiency virus infection. En: Mandell GL, Bennett JE, Dolin R. Mandell, Douglas and Bennett´s Principles and Practice of Infectious Diseases. 6th edition. Pittsburg:Elsevier, Churchill, Livingstone; 2005. p.1506-27. [ Links ]
9. Boshell J, Álvarez C, Marrugo S, Rojas MC, Rodríguez BM, González M, Gómez B. Indirect immunofluorescence as a supplementary test for confirming HIV-1 infection: the experience of the National Institute of Health, 1993-2000. Biomédica. 2002;22(1):30-8. [ Links ]
10. World Health Organization. Guidelines for HIV diagnosis and monitoring of antiretroviral therapy. WHO Project ICP BCT 001. December 2005. Disponible en: www.searo.who.int/LinkFiles/Publications_HLM-382 ev1.pdf. Fecha de consulta: 31/10/2006 [ Links ]
11. Centers for Disease Control and Prevention. Supplemental testing for confirmation of reactive oral fluid rapid HIV antibody tests. MMWR2005;54(50):1287-8. [ Links ]
12. Estrada S, Jaramillo A. El Laboratorio en el diagnóstico y seguimiento del paciente con VIH/SIDA. En: Betancur J, Correa AL, Estrada S, Orozco B. Manual de VIH/SIDA y otras infecciones de transmisión sexual. 1ª edición. 2005. p.6-16. [ Links ]
13. Olaya P, Díaz-Granados CA. Correlación y concordancia de tres técnicas de cuantificación de carga viral del VIH disponibles en Colombia. Biomédica. 2006;26:302-8. [ Links ]
14. Centers for Disease Control and Prevention. Guidelines for laboratory test result reporting of human immunodeficiency virus type 1 ribonucleic acid determination. Recommendations from a CDC Working Group. MMWR 2001;50(RR20). [ Links ]
15. Hernández M. Prevención, diagnóstico y tratamiento de la infección por el VIH en el niño. En: Betancur J, Correa AL, Estrada S, Orozco B. Manual de VIH/SIDA y otras infecciones de transmisión sexual. 1ª edición. 2005. p.17-34. [ Links ]