Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Infectio
Print version ISSN 0123-9392
Infect. vol.11 no.2 Bogotá Apr./June 2007
ARTÍCULO ORIGINAL
Reacción en cadena de la polimerasa: una contribución para el diagnóstico de la tuberculosis extrapulmonar y de las micobacteriosis
Polymerase chain reaction (PCR): a contribution for diagnosis of extrapulmonary tuberculosis and micobacteriosis
GLORIA PUERTO CLAUDIA M. CASTRO, WELLMAN RIBÓN*
* Grupo de Micobacterias, Subdirección de Investigación, Instituto Nacional de Salud, Bogotá, D. C., Colombia.
Fecha de recepción: 17/04/2007; fecha de aceptación; 05/07/2007
Resumen
Introducción. La Organización Mundial de la Salud define la tuberculosis extrapulmonar como la enfermedad tuberculosa localizada en cualquier órgano diferente a los pulmones y, la micobacteriosis, como la infección bacteriana producida por micobacterias no tuberculosas. El diagnóstico de tuberculosis extrapulmonar y micobacteriosis se hace fundamentalmente por el cultivo y la posterior identificación de la micobacteria por pruebas bioquímicas, así como por baciloscopia para el primer caso.
El cultivo de micobacterias presenta limitaciones, especialmente, por el tiempo de incubación que puede tardar hasta 12 semanas y por la sensibilidad para determinar la presencia del microorganismo. Actualmente, se utilizan herramientas moleculares que permiten disminuir el tiempo de diagnóstico. Entre ellas está la reacción en cadena de la polimerasa (PCR) que es una prueba rápida con buena sensibilidad y especificidad para la identificación de patógenos.
Objetivo. Implementar la (PCR) como apoyo para el diagnóstico de la tuberculosis extrapulmonar y la micobacteriosis, para disminuir el tiempo en la obtención de resultados y contribuir a la instauración de tratamientos oportunos para estas patologías.
Materiales y métodos. El estudio se llevó a cabo entre junio de 2005 y agosto de 2006. Se procesaron 57 muestras clínicas provenientes de 15 centros hospitalarios del país, analizadas por PCR para la secuencia de inserción IS6110 y para el gen hsp65. Se incluyeron datos clínicos del paciente, edad, sexo y prueba de VIH.
Resultados. Los resultados de amplificación para PCR IS6110 fueron positivos en 6 pacientes, lo que sugiere tuberculosis extrapulmonar, y para PCR hsp65, en igual número, lo que sugiere un proceso de micobacteriosis. Se confirmó el diagnóstico de tuberculosis meníngea en 4 (6,9%) pacientes, seguida por tuberculosis en piel y tuberculosis miliar, cada una en un (1,7%) paciente.
Se identificaron micobacterias no tuberculosas en 6 (10,3%) pacientes, así: 4 (7%) en esputo, 1 (1,75%) en secreción de abdomen y 1 (1,75%) en secreción de lesiones en piel. Un aislamiento de Mycobacterium chelonae de piel se asoció con un tratamiento previo con mesoterapia. No se encontró relación entre el estado de ¿portador de? VIH, con las patologías estudiadas.
Discusión. Se presenta la PCR como una buena ayuda diagnóstica, específicamente, por la obtención de resultados en un lapso de 3 días.
Palabras clave: infecciones por Mycobacterium, infecciones atípicas por Mycobacterium, reacción en cadena de la polimerasa, PCR.
Abastract
Introduction: The World Health Organization defines extrapulmonary tuberculosis as the disease located in any type of organ different from the lungs, and mycobacteriosis as the bacterial infection produced by environmental Mycobacteria. The diagnosis of extrapulmonary tuberculosis and mycobacteriosis is achieved fundamentally by culture and later identification of bacteria by biochemical tests, as well as by sputum smear for the first case.
Culture presents limitations specially related with the time of incubation that can last up to 12 weeks and with the sensitivity to the presence of the microorganism. Currently, molecular tools allow a decrease in the time of diagnosis. Among these tools, the polymerase chain reaction (PCR) is a rapid test with good sensitivity and specificity for the identification of pathogenic Mycobacteria.
Objective: To implement PCR as support to the diagnosis of extrapulmonary tuberculosis and mycobacteriosis to decrease the time in obtaining results and to contribute to the implementation of appropriate treatments for these diseases.
Materials and methods: The study was carried out between June 2005 and August 2006. 57 clinical samples of 15 hospitals throughout the country were analyzed by PCR for the sequence of insertion of IS6110 and for the gene hsp65. Clinical information of the patients, age, sex, and VIH test were included.
Results: Results of amplification for PCR IS6110 were positive in 6 patients suggesting extrapulmonary tuberculosis and for PCR hsp65 in an equivalent number, suggesting a process of mycobacteriosis. The study contributed to the diagnosis of meningeal tuberculosis in 4 (6.9%) patients, followed by skin tuberculosis and miliar tuberculosis each one with 1 (1.7%) patient.
We identified ¿non- Mycobacteryum tuberculosis? ¿lNMT? in 6 (10.3%) cases, which were differentiated as follows: 4 (7%) patients in sputum, 1 (1.75 %) patient in secretion of abdomen and 1 (1,75 %) patient in secretion of skin injuries. Mycobacterium chelonae isolation of the skin was associated with cosmetic mesotherapy. No relation was found between VIH status and the studied pathologies.
Discussion: This study shows PCR as a valuable diagnostic technique for patients, specifically for obtaining results within three days.
Key words: Mycobacterium infections, Mycobacterium infections atypical, polymerase chain reaction
INTRODUCCIÓN
A pesar de la disponibilidad de medicamentos desde 1940 para curar la tuberculosis, esta enfermedad producida por las micobacterias pertenecientes al complejo Mycobacterium tuberculosis ( M. tuberculosis, M. bovis, M. africanum, M. microti, M. tuberculosis subs. canettii, M. caprae y M. pinnipedii) ocasiona dos millones de muertes al año en el mundo y se estima que cerca de un tercio de la población mundial está infectada por el bacilo M. tuberculosis. Anualmente se reportan en promedio nueve millones de casos nuevos de la enfermedad (1). Las proyecciones indican que el impacto de la tuberculosis aumentará si no se toman de inmediato medidas de control en todos los países para reducir la transmisión, la morbilidad y la mortalidad de la enfermedad hasta que disminuya la amenaza para la salud pública (2).
En Colombia, para el año 2005, se reportaron al Sistema de Vigilancia Epidemiológica del Instituto Nacional de Salud (INS-SIVIGILA) 9.118 casos nuevos de tuberculosis para una incidencia de 22 casos por 100 mil habitantes, de los cuales, 84,1% fueron tuberculosis pulmonar, 0,5% tuberculosis meníngea y 15,4% correspondió a otras formas extrapulmonares (Instituto Nacional de Salud. Informe mensual de tuberculosis en Colombia. Agosto de 2006. Bogotá, D.C., INS, Subdirección de Vigilancia y Control en Salud Pública).
La tuberculosis extrapulmonar se presenta como consecuencia de la diseminación de M. tuberculosis a través de los vasos linfáticos o del torrente circulatorio a otros órganos; los que se afectan con mayor frecuencia son: las meninges, la pleura, la piel, los ganglios linfáticos, el abdomen, el aparato genitourinario, los riñones, la piel, las articulaciones y los huesos (3,4).
Según la guía de atención de la tuberculosis, existen diferentes criterios para el diagnóstico de la tuberculosis extrapulmonar, como son el estudio clínico, el estudio histopatológico, el criterio epidemiológico y el bacteriológico. El aislamiento del microorganismo en el cultivo es uno de los factores más importantes, pero presenta inconvenientes, especialmente por la sensibilidad, que va de 50% a 81% (5- 8), y por la espera en la identificación del microorganismo (6 a 12 semanas); este tiempo puede prolongarse debido a que las muestras clínicas de origen extrapulmonar son paucibacilares, situación Infectio 2007; 11(2): 87-94 que va en contra del pronóstico del paciente por la demora en la instauración del tratamiento adecuado (7,9-11).
Las micobacteriosis son patologías infecciosas producidas por micobacterias no tuberculosas, microorganismos de amplia distribución ambiental en agua y suelo. El aislamiento de estos microorganismos ahora es más frecuente por la epidemia del VIH-sida (12), por la persistencia de otras enfermedades que suprimen el sistema inmune, como el cáncer y la diabetes (13), y por el auge de los procedimientos estéticos (14,15). El diagnóstico de las micobacteriosis se basa, específicamente, en el aislamiento de la micobacteria en un medio de cultivo y su posterior identificación de especie por pruebas bioquímicas; estos procedimientos tardan varias semanas y en algunos casos la identificación de especie no es concluyente (16).
En Colombia existen pocos reportes de micobacterias no tuberculosas. En el Grupo de Micobacterias del Instituto Nacional de Salud, entre 1995 y 2003 se aislaron 213 micobacterias no tuberculosas, con mayor frecuencia, M. chelonae (23%), lo cual corrobora la importancia de la identificación y la determinación de especie de estos patógenos (17).
El desarrollo de pruebas rápidas basadas en biología molecular ha surgido como alternativa de ayuda para el diagnóstico de enfermedades infecciosas (11). Entre estas pruebas está la reacción en cadena de la polimerasa (PCR), que se presenta como un método rápido de gran sensibilidad (1 ng/ µl de ADN ) y especificidad, entre 98% y 100% para micobacterias del complejo M. tuberculosis (18). Entre los blancos genéticos de amplificación más comunes para la identificación de micobacterias, se presenta la secuencia de inserción IS 6110 específica de los miembros del complejo M. tuberculosis (19,20) y el gen hsp 65 ligado a la restricción específica del producto de amplificación conocido como metodología de ¿PRA? (análisis de restricción de los productos de PCR), que se ha descrito como una metodología rápida, económica y de fácil implementación para la identificación de micobacterias (16,21).
Teniendo en cuenta lo anterior, el Grupo de Micobacterias del INS utiliza la PCR para contribuir al diagnóstico de tuberculosis y micobacteriosis en muestras clínicas. El presente trabajo tuvo como objetivo utilizar la PCR en los blancos genéticos IS 6110 y hsp65, con el fin de ayudar en la detección de tuberculosis extrapulmonar y micobacteriosis, en pacientes atendidos en las entidades de salud del país que lo solicitaron, para confirmar la presencia e identificar la micobacteria en la muestra clínica analizada.
METODOLOGÍA
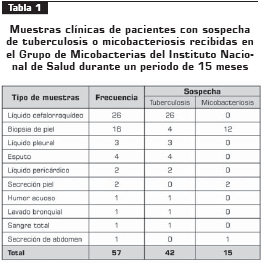
Población y muestras. El trabajo incluyó 57 pacientes a quienes se les sospechaba tuberculosis extrapulmonar o micobacteriosis; de cada uno de ellos se obtuvo igual número de muestras clínicas (tabla 1) que se remitieron al Grupo de Micobacterias del Instituto Nacional de Salud, entre junio de 2005 y octubre de 2006. Los especímenes clínicos fueron enviados de 15 instituciones de salud del país, 8 públicas y 7 privadas.
El médico remitente diligenció una ficha de recolección de datos de cada uno de los pacientes del estudio, en la cual se indagó sobre edad, sexo, reporte de HIV e impresión diagnóstica.
Extracción de ADN genómico de micobacterias.
El proceso de extracción de ADN se realizo según el protocolo descrito por Dick van Soolingen en 2002 (22). Las muestras de esputo se trataron con fosfato trisódico al 10%. Todas las muestras se centrifugaron a 4.000g durante 30 minutos; el sedimento obtenido se resuspendió en 400 µl de solución amortiguadora TE (0,01M Tris-HCl, 0,001M EDTA, pH 8) y se inactivó por ebullición durante 20 minutos. Luego, se adicionaron 50 µl de lisozima, 10 mg/ml (SIGMA) y se incubó a 37 °C durante 2 horas; posteriormente, se adicionaron 70 µl de SDS 10% (SIGMA) y 10 µl de proteinasa K de 10 mg/ml (SIGMA) y se incubó a 65 °C por 10 minutos; posteriormente, se agregaron 100 µl de NaCl 5M y CTABNaCl para incubar a 65 °C por 10 minutos. El ADN se extrajo mediante cloroformo:alcohol isoamílico (24:1), precipitado con isopropanol absoluto y fue resuspendido en solución amortiguadora TE 0,1X.
PCR para los miembros del complejo M. tuberculosis. Trece muestras se sometieron a la PCR específica para amplificar un fragmento de 245 pb de IS 6110 en una mezcla de reacción de 50 ìl que contenía una concentración de 25 ìM de cada uno de los iniciadores INS1 CGTGAGGGCATCGAGGTGGC3 e INS2 5GCGACGTAGGCGTCGGTGACAAA3 (Invitrogen ®), solución amortiguadora de PCR 10X (Invitrogen ®), MgCl2 25 mM (Invitrogen ®), 2,5 mM de cada desoxinucleósido trifosfato (Invitrogen ®), 1,25 U de TaqADN polimerasa (Invitrogen ®) y 10 ìl del ADN extraido de la muestra clínica (23). La reacción se llevó a cabo en un termociclador Mastercycler Eppendorf con desnaturación inicial de 96 ºC por 5 minutos, seguida por 40 ciclos de 94 ºC por 2 minutos, 60 ºC por 2 minutos y 72 ºC por 2 minutos y un ciclo final de 72 ºC por 7 minutos.
PCR para micobacterias no tuberculosas metodología de PRA. Se sometieron 44 muestras a una prueba de PCR para amplificar un fragmento de 439 pb del gen hsp65 en una mezcla de reacción de 50 ìl que contenía una concentración de 25 ìM de cada uno los iniciadores Tb11 5ACCAACGATGGTGTGTCCAT y Tb12 5CTTGTCGAACCGCATACCCT (Invitrogen ®), solución amortiguadora de PCR 10X (Invitrogen ®), MgCl2 25 mM (Invitrogen ®), 2,5 mM de cada desoxinucleósido trifosfato (Invitrogen ®), 2,5 U de TaqADN polimerasa y 10 ìl del AND extraído de la muestra clínica (24). La reacción se llevó a cabo en un termociclador Mastercycler Eppendorf con una desnaturación inicial de 95 ºC por 5 minutos, seguida por 40 ciclos de 94 ºC por 1 minuto, 65 ºC por 1 minuto y 72 ºC por 1 minuto, y un ciclo final de 72 ºC por 7 minutos.
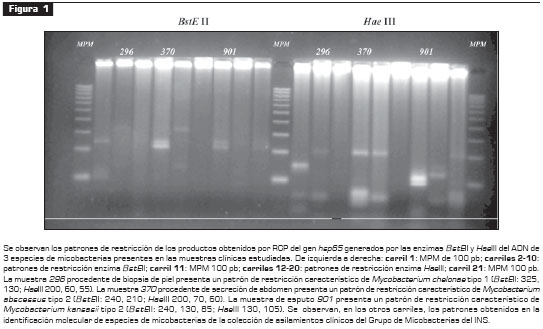
Los productos amplificados por PCR hsp65 se sometieron a digestión con las enzimas BstE II y Hae III (Sigma ®), por separado, en una mezcla de reacción de 25 ìl en agua que contenia el producto de PCR, solución amortiguadora SB 10X (Sigma ®), y SM 10X (Sigma ®), respectivamente, y una unidad de la enzima. Los productos de restricción obtenidos por PRA se visualizaron en gel de agarosa al 4% y su tamaño molecular se determinó con un patrón de peso molecular de 100 pb. Los patrones de restricción se analizaron usando el sitio de la red PRA site (http://app.chuv.ch/prasite/index.html).
Visualización de los productos amplificados. La amplificación de los blancos genéticos IS6110 y hsp65 se confirmó en geles de agarosa al 1,4% por corrido electroforético a 90 V/cm durante 20 minutos. Para determinar el tamaño molecular de los fragmentos de amplificación esperados se utilizó el marcador de peso molecular ØX174- Hae III.
Control de calidad de la PCR. Cada una de las pruebas se procesó con un control positivo para la amplificación de IS6110 y hsp65 utilizando ADN de la cepa de referencia M. tuberculosis H37Rv, un control negativo de amplificación con agua ultrapura estéril para determinar la ausencia de contaminación en el laboratorio y un control de inhibidores que consistió en adicionar una alícuota de ADN de M. tuberculosis H37Rv a la extracción de ADN de la muestra clínica, para corroborar la ausencia de inhibidores en la muestra que no permitieran amplificar un posible ADN micobacteriano presente (25).
Emisión de resultados. Los resultados de la PCR para las muestras clínicas se informaron a la entidad solicitante. El médico tratante estableció el diagnóstico definitivo.
RESULTADOS
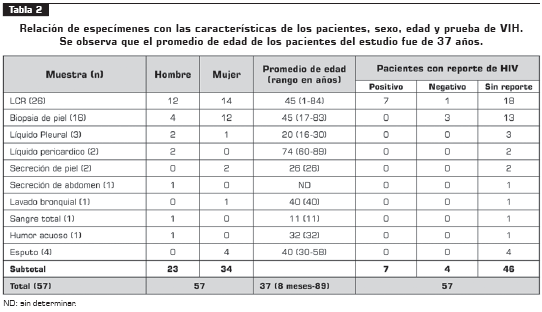
Características clínicas de los pacientes. La información sobre sexo, edad y reporte de VIH de los pacientes que ingresaron al estudio, se presentan en la tabla 2. Algunas historias clínicas no presentaban la información completa de la historia clínica, especialmente, la edad y el reporte de la prueba de VIH. No se supo si la falta de esta información se debió a que no se le formuló la pregunta al paciente o a que éste la omitió.
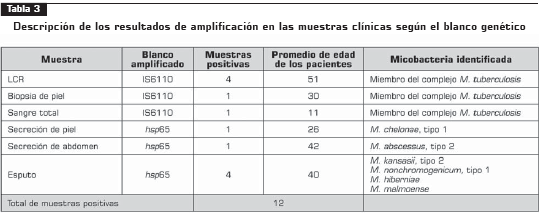
PCR IS6110 y hsp65. Doce de 57 muestras (21%) presentaron amplificación con alguno de los dos blancos genéticos: 6 muestras amplificadas por PCR IS6110, en las que se detectó la presencia de AND de miembros del complejo M. tuberculosis, y 6 muestras amplificadas con PCR hsp65, posteriormente fueron sometidas a análisis de restricción para la identificación de la micobacteria implicada; 45/57 (79%) de las muestras fueron negativas y no presentaron amplificación con ninguno de los dos blancos (tabla 3).
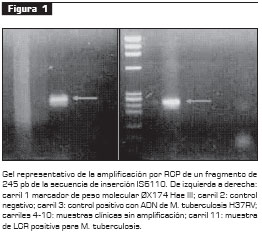
Los resultados de amplificación para IS6110 fueron positivos en 6 pacientes (10,5%), discriminados así: 4 (7%) con tuberculosis meníngea, 1 (1,75%) con tuberculosis en piel y 1 (1,75%) con tuberculosis diseminada ( véase figura 1).
Los resultados de la amplificación para hsp65 fueron positivos en las muestras clínicas de secreción de abdomen, esputo y secreción de piel en muslo, y se identificaron micobacterias no tuberculosas en 6 (10,5%) pacientes. Las identificadas fueron; M. abscessus, M. kansasii, M. nonchromogenicum, M. hiberniae, M. malmoense y M. chelonae (figura 2).
Ninguno de los 7 pacientes con reporte positivo para VIH presentó amplificación por PCR para IS6110 o para hsp65 en las muestras clínicas analizadas.
La edad promedio de los pacientes con PCR positiva para IS6110 fue de 40 años y para PCR hsp65 fue de 36 años.
Emisión de resultados. Los resultados de las amplificaciones por PCR fueron remitidos en su totalidad a las entidades para entrega directa a los familiares del paciente o se enviaron vía fax.
DISCUSIÓN
Los resultados de la PCR para IS6110 y para hsp65 se informaron tres días después de recibida la muestra; cuando se reportaba una PCR positiva, se investigaba el diagnóstico médico de los pacientes; en los 12 casos positivos, la clínica confirmó el diagnóstico de tuberculosis extrapulmonar o de micobacteriosis, con lo que se corroboró la contribución de la prueba en el diagnóstico.
La obtención de resultados por PCR en un lapso de 72 horas, tiempo necesario para realizar la extracción, amplificación y detección del AND micobacteriano, se presenta como una ventaja clínica para el manejo de los pacientes, teniendo en cuenta que los que se les sospechaba tuberculosis meníngea estaban hospitalizados en unidades de cuidado intensivo y requerían la pronta instauración del tratamiento (26).
Con PCR IS6110 se logró establecer la presencia de miembros del complejo M. tuberculosis. Aunque en este estudio no se logró la identificación de la especie implicada, por ser prioritaria la información oportuna al servicio médico debido al estado critico de salud de los pacientes; se recomienda utilizar otras metodologías moleculares como el spoligotyping para este fin; esta última, además de identificar la especie, permite establecer la familia a la que pertenece, su asociación con resistencia a medicamentos y la distribución nacional y mundial; de esta manera se logra orientar el tratamiento, en especial, si se sospecha de la presencia de un aislamiento con resistencia a los medicamentos de primera línea, como isoniacida, rifampicina, pirazinamida y etambutol (21,27).
El diagnóstico de tuberculosis meníngea en 4 pacientes, tuberculosis en piel y tuberculosis diseminada en 1 paciente, concuerda con los reportes previamente conocidos, en los cuales la tuberculosis meníngea es la presentación más común y la diseminada, la de menor frecuencia (27,28). En este estudio la amplificación de IS6110 confirmó el estado de infección del paciente; el criterio clínico, el epidemiológico y los resultados de las ayudas diagnósticas son los que orientan al médico sobre el curso de la enfermedad.
La edad promedio de los pacientes con muestras clínicas positivas para la amplificación de IS6110 para la detección de miembros del complejo M. tuberculosis fue de 30 años, situación concordante con la literatura donde se presenta el impacto de la tuberculosis en población joven económicamente activa (29).
Los diagnósticos de micobacteriosis fueron confirmados por criterio clínico. Las micobacteriosis se manifestaron en pacientes con edad promedio de 36 años, quienes generalmente presentaron dificultad en el tratamiento, como fue el caso de la paciente en cuya muestra de secreción de piel del muslo se identificó M. chelonae, a quien se le había diagnosticado micosis y sobreinfección con bacterias Gram positivas, sin respuesta al tratamiento. M. chelonae se ha recuperado como contaminante de heridas quirúrgicas, soluciones y equipos médicos; se asocia con procedimientos estéticos como cirugías plásticas y mesoterapia (30). La identificación de M. abscessus en la secreción de la lesión en el abdomen concuerda con la epidemiología de este microorganismo, que causa infecciones especialmente en piel y tejidos blandos, y es aislado con frecuencia (31).
M. kansasii, M. nonchromogenicum, M. hiberniae y M. malmoense, identificadas en esputo, son micobacterias que se recuperan con poca frecuencia de procesos infecciosos pulmonares, especialmente, en pacientes con algún grado de inmunosupresión; el conocimiento de estas especies causantes de infección micobacteriana en el pulmón llama la atención debido a que las muestras clínicas de esputo ingresaron con un diagnóstico presuntivo de tuberculosis pulmonar y se hizo un diagnóstico final de micobacteriosis; por lo tanto, es importante valerse de metodologías diagnósticas como las pruebas moleculares que ayuden a determinar la especie implicada, con el fin de instaurar el tratamiento adecuado y mejorar el estado general de los enfermos (12,17).
La amplificación de hsp65 y posterior identificación de la micobacteria no tuberculosa no se realizó en tres muestras seriadas como lo recomienda la Red Nacional de Laboratorios (17) debido, especialmente, a que las muestras clínicas fueron en su mayoría biopsias que se obtienen por procedimientos invasivos. El criterio médico fue el patrón para la instauración del tratamiento según la sintomatología del paciente.
Todas las muestras se procesaron con control positivo, negativo y de inhibidores, lo que permitió asegurar la ausencia de inhibidores (compuestos orgánicos e inorgánicos) en las muestras, que influyeran en la amplificación de un posible AND micobacteriano presente (25,32).
En el 2005 y en lo corrido del 2006 se reportaron al SIVIGILA sólo 2 casos de tuberculosis meníngea en Bogotá, lo que contrasta con los 4 casos confirmados en este estudio; no se tiene conocimiento del reporte de tuberculosis cutánea y miliar. La notificación de los casos de tuberculosis extrapulmonar se constituye en una necesidad prioritaria para el país, con el fin de permitir al SIVIGILA aplicar acciones de control tendientes a disminuir el impacto de la enfermedad (12).
No se encontró asociación de tuberculosis extrapulmonar y micobacteriosis con los pacientes positivos para VIH de este estudio; esta situación es de interés por los reportes de la literatura de la asociación entre estas dos enfermedades, en los cuales se describe que más de 50% de los pacientes positivos para VIH aumentan el riesgo de enfermedad tuberculosa y pueden enfermar de tuberculosis con el avance de la inmunosupresión (12,27). Esto lleva a sugerir que los pacientes que participaron de este estudio y que eran positivos para VIH, no presentaban estados avanzados de inmunosupresión.
Se pone en conocimiento del personal médico este tipo de metodologías moleculares de diagnóstico, las cuales permiten contribuir a la toma de decisiones y a la instauración de tratamientos adecuados; además, los laboratorios de diagnóstico clínico deben implementar técnicas básicas de biología molecular, como la PCR, de fácil acceso y bajos costos para contribuir al diagnóstico en un tiempo más corto.
Se sugiere continuar este tipo de estudios y avanzar hacia la implementación de la PCR en tiempo real, la cual presenta una mayor sensibilidad en cuanto a la detección del número de copias del posible AND micobacteriano que se encuentra en una muestra extrapulmonar (33), sin dejar de realizar la identificación microbiológica convencional (bacilos-copia y cultivo) establecida por el Programa Nacional de Tuberculosis del Ministerio de la Protección Social.
Financiación
Este trabajo fue financiado por el Instituto Nacional de Salud de Colombia, Subdirección de Investigación.
Correspondencia:
Wellman Ribón, Grupo de Micobacterias, Instituto Nacional de Salud, Avenida Calle 26 Nº 51-60, Bogotá, D. C., Colombia. Telefax: 220 0926 wribon@ins.gov.co
REFERENCIAS
1. WORLD HEALTH ORGANIZATION. Global Tuberculosis Control WHO Report. Geneva: WHO; 2006. [ Links ]
2. WORLD HEALTH ORGANIZATION. Un marco ampliado de DOTS para el control eficaz de la tuberculosis. Ginebra: WHO; 2002. [ Links ]
3. BROOKS G, BUTEL J, MORSE S. Microbiología médica de Jawetz, Melnick y Adelberg. 17ª edición. Ciudad de México: El Manual Moderno; 2002. [ Links ]
4. ORGANIZACIÓN PANAMERICANA DE LA SALUD. Definiciones de casos: tétanos neonatal y tuberculosis. Boletín Epidemiológico 2000; 21. Consultado: 30-01-07. Disponible en: http://www.paho.org/spanish/sha/be_v21n1-casos.htm [ Links ]
5. ANGEBY KA, ALVARADO-GÁLVEZ C, PINEDA-GARCÍA L, HOFFNER SE. Improved sputum microscopy for a more sensitive diagnosis of pulmonary tuberculosis. Int J Tuberc Lung Dis. 2000;4:684-7. [ Links ]
6. WARREN J, BHATTACHARYA M, DE ALMEIDA K, TRAKAS K, PETERSON L. A minimum 5.0 ml of sputum improves the sensitivity of acid-fast smear for M ycobacterium tuberculosis. Am J Respir Crit Care Med. 2000;161:1559-62. [ Links ]
7. DEL CASTILLO DURÁN Y, BODÍ SANTOS F, CASTANDER SERENTILL D, JUBERT MONTAPERTO P, ESPINOSA VALENCIA P, RABASSÓ SOLÉ C. Tuberculosis miliar en paciente tratado con instilaciones intravesicales de bacilo de Calmette-Guérin. Medicina Intensiva. 2006;30:116-9. [ Links ]
8. MINISTERIO DE SALUD. Guía de atención de la tuberculosis pulmonar y extrapulmonar. Bogotá: Ministerio de Salud; 2002. [ Links ]
9. VILLEGAS MV, LABRADA LA, SARAVIA NG. Evaluation of polymerase chain reaction, adenosine deaminase, and interferon ã in pleural fluid for the differential diagnosis of pleural tuberculosis. Chest. 2000;118:1355-64. [ Links ]
10. WIENER RS, DELLA-LATTA P, SCHLUGER NW. Effect of nucleic acid amplification for Mycobacterium tuberculosis on clinical decision making in suspected extrapulmonary tuberculosis. Chest. 2005;128:102-7. [ Links ]
11. FURIN JJ, JOHNSON JL. Recent advances in the diagnosis and management of tuberculosis. Curr Opin Pulm Med. 2005;11:189-94. [ Links ]
12. CASTIBLANCO C, RIBÓN W. Coinfección de tuberculosis en pacientes con VIH/SIDA: un análisis según las fuentes de información en Colombia. Infectio. 2006;10:232-42. [ Links ]
13. BARNES AI, ROJO S, MORETTO H. Prevalencia de micobacteriosis y tuberculosis en pacientes de un hospital de referencia de la provincia de Córdoba. Rev Argent Microbiol. 2004;36:170-3. [ Links ]
14. DEL SOLAR M, SALOMÓN M, BRAVO F, SEAS C, GOTUZZO E, CULQUI D, ET AL. Infección cutánea por micobacterias atípicas de crecimiento rápido (MACR) debido a mesoterapia cosmética. Reporte de casos y revisión de la literatura. Folia Dermatol Perú. 2005;16:127-35. [ Links ]
15. GIRA AK, REISENAUER AH, HAMMOCK L, NADIMINTI U, MACY JT, REEVES A, ET AL. Furunculosis due to M ycobacterium mageritense associated with footbaths at a nail salon. J Clin Microbiol. 2004;42:1813-7. [ Links ]
16. DEVALLOIS A, GOH KS, RASTOGI N. Rapid identification of mycobacteria to species level by PCR-restriction fragment length polymorphism analysis of the hsp65 gene and proposition of an algorithm to differentiate 34 mycobacterial species. J Clin Microbiol. 1997;35:2969-73. [ Links ]
17. GARZÓN MC, ORJUELA DL, NARANJO O, LLERENA C. Micobacterias no tuberculosas en Colombia 1995-2003. Inf Quinc Epidemiol Nac. 2005;10:161-76. [ Links ]
18. PIERSIMONI C, SCARPARO C. Relevance of commercial amplification methods for direct detection of Mycobacterium tuberculosis complex in clinical samples. J Clin Microbiol. 2003;41:5355-65. [ Links ]
19. CHAKRAVORTY S, TYAGI JS. Novel multipurpose methodology for detection of Mycobacteria in pulmonary and extrapulmonary specimens by smear microscopy, culture, and PCR. J Clin Microbiol. 2005;43:2697–702. [ Links ]
20. RIMEK D, TYAGI S, KAPPE R. Performance of an i s6110-based PCR assay and the cobas amplicor MTB PCR system for detection of Mycobacterium tuberculosis complex DNA in human lymph node samples. J Clin Microbiol. 2002;40:3089-92. [ Links ]
21. BURGOS MV, MÉNDEZ JC, RIBÓN W. Molecular epidemiology of tuberculosis: methodology and applications. Biomédica. 2004;24 (Suppl. 1):188-201. [ Links ]
22. SOOLINGEN DV, DE HASS PE, KREMER K. Restriction fragment length polymorphism (RFLP) typing of Mycobacteria. Bilthoven: National Institute of Public Health and the Environment; 2002. [ Links ]
23. OTAL I, SAMPER S, ASENSIO MP, VITÓRIA MA, RUBIO MC, GÓMEZ-LUS R, ET AL. Use of a PCR method based on IS6110 polymorphism for typing Mycobacterium tuberculosis strains from BACTEC cultures. J Clin Microbiol. 1997;35:273-7. [ Links ]
24. TELENTI A, MARCHESI F, BALZ M, BALLY F, BOTTGER EC, BODMER T. Rapid identification of Mycobacteria to the species level by polymerase chain reaction and restriction enzyme analysis. J Clin Microbiol. 1993;31:175-8. [ Links ]
25. CHAKRAVORTY S, SEN MK, TYAGI JS. Diagnosis of extrapulmonary tuberculosis by smear, culture, and PCR using universal sample processing technology. J Clin Microbiol. 2005;43:4357-62. [ Links ]
26. NAGESH BS SEHGAL S, JINDAL SK, ARORA SK. Evaluation of polymerase chain reaction for detection of Mycobacterium tuberculosis in pleural fluid. Chest .2001;119:1737-41. [ Links ]
27. GOLDEN MP, VIKRAM HR. Extrapulmonary tuberculosis: An overview. Am Fam Physician. 2005;72:1761-8. [ Links ]
28. SHAFER RW, KIM DS, WEISS JP, QUALE JM. Extrapulmonary tuberculosis in patients with human immunodeficiency virus infection. Medicine (Baltimore). 1991;70:384-97. [ Links ]
29. THE STOP TB INITIATIVE. The economic impacts of tuberculosis. Series. Presented at the Ministerial Conference, Amsterdam, March 22-24, 2000. [ Links ]
30. MEYERS HB, BROWN-ELLIOTT BA, MOORE D, CURRY J, TRUONG C, ZHANG Y, ET AL. An outbreak of Mycobacterium chelonae infection following liposuction. Clin Infect Dis. 2002;34:1500-7. [ Links ]
31. USLAN D, KOWALSKI T, WENGENACK N, VIRK A, WILSON J. Skin and soft tissue infections due to rapidly growing mycobacteria comparison of clinical features, treatment, and susceptibility. Arch Dermatol. 2006;142:1287-92. [ Links ]
32. HONORE-BOUAKLINE S, VINCENSINI JP, GIACUZZO V, LAGRANGE PH, HERRMANN JL. Rapid diagnosis of extrapulmonary tuberculosis by PCR: Impact of sample preparation and DNA extraction. J Clin Microbiol. 2003;41:2323-9. [ Links ]
33. PARASHAR D, CHAUHAN D, SHARMA V, KATOCH V. Applications of real-time PCR technology to mycobacterial research. Ind J Med Res. 2006;124:385-398. [ Links ]