Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Infectio
Print version ISSN 0123-9392
Infect. vol.14 no.2 Bogotá Apr./June 2010
1Instituto de Investigaciones Biológicas del Trópico, Universidad de Córdoba, Montería, Colombia
Recibido: 06/02/2009; Aceptado: 22/04/2010
Objetivo: Determinar las mutaciones del gen gyrA asociadas con la resistencia a fluoroquinolonas en Acinetobacter baumannii.
Materiales y métodos: Entre agosto de 2005 y febrero de 2007 se recolectaron 23 aislamientos de A. baumannii de una clínica privada de tercer nivel de Montería. Se investigaron los genes gyrA, parC y adeB; este último codifica para la bomba de salida. Se realizó secuenciación del ADN y, para el análisis de las secuencias, se usaron la base de datos GenBank y el motor de búsqueda BLASTX.
Resultados: La amplificación del gen gyrA en aislamientos de A. baumannii generó un fragmento de 343 pb, el cual presentó pérdida del sitio de restricción con la enzima Hinfl en 12/23 (52,1%) de los aislamientos resistentes a fluoroquinolonas. La secuenciación del fragmento mostró mutación puntual con el cambio de Ser-83 a Leu, código de acceso GenBank EU886740. No se encontraron mutaciones en el gen parC, ni la presencia de la bomba de salida Ade.
Conclusión: Los aislamientos de A. baumannii resistentes a fluoroquinolonas sugieren que la mutación del gen gyrA que codifica el cambio del aminoácido serina a leucina en el codón 83 de estos aislamientos, es responsable o, al menos, contribuye con la resistencia expresada a las fluoroquinolonas.
Palabras clave: Acinetobacter baumannii, fluoroquinolonas, gyrA, parC, adeB, Colombia
Abstract
Objective: Determine mutations in the gyrA gene associated to resistance to fluoroquinolones in A. baumannii.
Materials and methods: From August, 2005 to February, 2007, 23 A. baumannii isolates were collected in a third level private clinic in Monteria. Research on gyrA, parC and adeB genes was carried out, and the latter encodes for the efflux pump. DNA sequencing was performed, and the GenBank database and BLASTX search engine were used for sequence analysis.
Results: Amplification of the gyrA gene inA. baumannii isolates generated a 343pbfragment which presented loss of restrictionsite with the enzyme HinfI in 12/23 (52.1%) of the isolates resistant to fluoroquinolones. The fragment sequencing showed mutation characterized by the change of Ser-83 to Leu GenBank acces code EU886740. None of the isolates showed mutations in the parC gene or presence of the adeB efflux pump.
Conclusion: The A. baumannii isolates resistant to fluoroquinolones suggest that mutation of the gyrA gene encoding the serine amino acid change to leucine at codon 83 of these isolates is responsible or at least contributes to the mentioned resistance to fluoroquinolones.
Key words: A. baumannii, fluoroquinolones, resistance, gyrA, parC, adeB, Colombia.
Introducción
La incidencia de infecciones hospitalarias causadas por cepas de Acinetobacter baumannii resistentes a fluoroquinolonas ha aumentando en los últimos años, especialmente, en brotes en las unidades de cuidados intensivos UCI en las que el uso indiscriminado de antibióticos ha conllevado a la diseminación de clones resistentes (1,2). El uso de las fluoroquinolonas en un comienzo estaba indicado principalmente en infecciones respiratorias; posteriormente, fue utilizado en infecciones urinarias y otras patologías infecciosas, lo que posiblemente contribuyó al aumento de la resistencia (2)
En Estados Unidos y Europa, la resistencia a las quinolonas se encuentra alrededor de 20% (3,4). En Latinoamérica (5), la resistencia a las quinolonas está entre 50% y 70%, similar a lo que ocurre en Colombia (6). En el departamento de Córdoba se han encontrado porcentajes de resistencia de 60,5% (6); aunque estos reportes sólo señalan el perfil fenotípico, han contribuido al conocimiento de la epidemiología de la resistencia a las fluoroquinolonas. A pesar de la alta prevalencia, en Colombia no existen estudios conocidos que analicen, desde la perspectiva molecular, la resistencia a las fluoroquinolonas
Las mutaciones en los genes gyrA y parC, que codifican para la subunidad A de la ADN girasa y la subunidad C de la topoisomerasa IV, se encuentran en una zona llamada QRDR (quinolone-resistance-determining region) específica para cada subunidad, las cuales se han estudiado en A. baumannii (7). En gyrA, estas mutaciones afectan con mayor frecuencia la Ser83 y en segundo lugar la Asp87. En parC, las mutaciones afectan la Ser80 y, en segundo lugar, el Glu84. Una mutación conlleva a la disminución de la sensibilidad a las fluoroquinolonas y una doble mutación se asocia a elevados niveles de resistencia (8)
Las mutaciones en la secuencia de aminoácidos del gen gyrA y el parC se han encontrado con frecuencia en aislamientos clínicos de A. baumannii con resistencia a las quinolonas (9). No obstante, existen también otros factores importantes que conllevan a la resistencia a estos antimicrobianos, como los sistemas de salida adeB, AbeM y AdeIJK (10,11). Recientemente, se ha descrito un mecanismo tipo plásmido, determinado por el gen qnr en los aislamientos de Escherichia coli. Sin embargo, en A. baumannii este mecanismo aún no se ha descrito (12,13).
El objetivo de este trabajo fue investigar la presencia de mutaciones en gyrA asociadas con la resistencia a fluoroquinolonas en aislamientos de A. baumannii de una clínica privada de Montería
Materiales y métodos
Cepas bacterianas. Los 23 aislamientos de A. baumannii que se utilizaron en este estudio fueron recolectados en una clínica privada de III nivel de atención en Montería, entre agosto de 2005 y febrero de 2007. La identificación de A. baumannii se hizo por icroScan® Neg Combo Panel Type 44 (Dade Behring, CA, USA). Los aislamientos se obtuvieron de diferentes muestras clínicas: secreciones respiratorias (n=13), catéter (n=3), secreciones de heridas (n= 3), secreciones gástricas (n=1), líquido peritoneal (n=2) y orina (n=1). Los aislamientos se mantuvieron a -70°C en leche descremada (skim milk), antes del análisis molecular
Determinación de la concentración inhibitoria mínima. Se determinaron los patrones de resistencia mediante el método de concentración inhibitoria mínima (CIM), según las normas del Clinical and Laboratory Standards Institute (14). Los agentes antibacterianos fueron: ciprofloxacina y moxifloxacina. Se usaron como controles Escherichia coli ATCC 25922 y Pseudomonas aeruginosa ATCC 27853
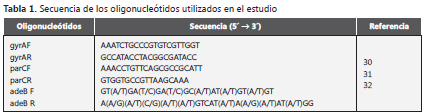
Amplificación y detección de genes de resistencia gyrA y parC y adeB. El ADN se obtuvo a partir del sobrenadante del cultivo a una concentración de 109 unidades formadoras de colonias (UFC) por ml, el cual se sometió a ebullición por 15 minutos y se centrifugó a 14.000g por 1 minuto. Los oligonucleótidos usados para amplificar la zona QRDR de los genes gyrA y parC, y el gen adeB que codifica para una bomba de salida de tipo RND, se muestran en la tabla 1. La detección de productos de ADN se hizo por tinción del gel con bromuro de etidio (0,5 mg/L) y posterior visualización en un fotodocumentador GE Healthcare (ImageQuant 100, Uppsala, Sweden)
Polimorfismo de longitud de fragmentos de restricción (RFLP). Veinte microlitros de los productos gyrA y parC se incubaron por 2,5 horas con 10 U de HinfI a 37°C. Los productos de la digestión se separaron mediante electroforesis a 80 V en NuSieve al 1,5% (Lonza, Rockland, ME, USA) más gel agarosa al 1%. Los productos que no mostraron restricción fueron secuenciados
Secuenciación de los productos PCR. Para confirmar los productos amplificados, los fragmentos se purificaron con el Wizard® SV Gel and PCR Clean-Up System (Promega, Madison, WI, USA), de acuerdo con las instrucciones del fabricante, y se secuenciaron directamente mediante el método dideoxi en un secuenciador automático de ADN MegaBACE 750 (Amersham, Biosciences)
El análisis de las secuencias se realizó con la base de datos GenBank del National Center for Biotechnology Information (NCBI) y el motor de búsqueda BLASTX (15). Las secuencias de genes relacionados y la secuencia de nucleótidos de los genes gyrA y parC se analizaron mediante el uso de múltiple alineación creada por Clustal W, versión 2.0.8 (16)
Resultados
Detección de la mutación en el gen gyrA y parC. La resistencia a las quinolonas se investigó por la búsqueda de mutaciones en los genes gyrA y parC de 23 aislamientos de A. baumannii con CIM para ciprofloxacina entre 0,5 y >64 μg/ml y CIM para moxifloxacina entre 0,5 y >64 μg/ml. La amplificación del gen gyrA en aislamientos de A baumannii sensibles a quinolona generó un fragmento de 343 pb, el cual se sometió a digestión con la enzima HinfI, y se produjeron dos fragmentos de 291 pb y 52 pb
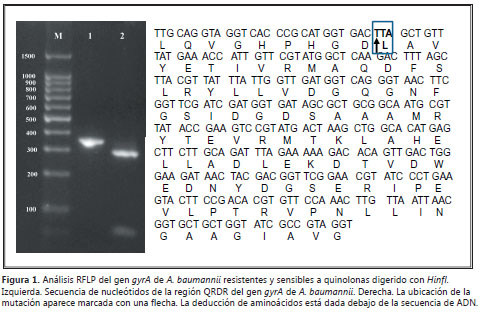
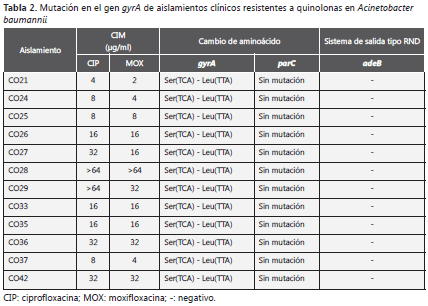
Sin embargo, no se presentó digestión del fragmento gyrA con HinfI en 12/23 (52,1%) aislamientos resistentes a quinolonas con CIM de ciprofloxacina mayor de 4 μg/ml. Los fragmentos sin sitio de restricción fueron purificados y secuenciados; estos mostraron 97% de homología con el gen gyrA y se encontró mutación puntual en el codón 83 dada por el cambio del nucleótido C a T, lo que codifica para el recambio del aminoácido serina a leucina (código de acceso, Gen- Bank EU886740) (figura 1). Las mutaciones en el gen gyrA que condujeron a cambios de aminoácidos en los aislamientos resistentes a quinolonas, se muestran en la tabla 2
El análisis del fragmento de 191 pb del gen parC con HinfI en aislamientos sensibles a las quinolonas y resistentes a ellas, generó dos fragmentos de 123 pb y 68 pb; la secuenciación del fragmento de 191 pb de todos los aislamientos mostró 100% de homología con el gen parC sin presencia de mutación (código de acceso, GenBank NC010400)
Detección de la bomba de salida adeB. No se produjo amplificación del gen adeB en los aislamientos (tabla 2).
Análisis bioinformático del gen gyrA Se realizó un alineamiento de la secuencia del gen gyrA de tres aislamientos de A. baumannii resistentes a las quinolonas de este estudio (CO-21, CO-24, CO-25), con la secuencia sin mutación del gen gyrA de A. baumannii (código de acceso GenBank X82165), y la secuencia con mutación (código de acceso, GenBank YP001712820), donde se demuestra que la mutación en la posición de la Ser-83 a Leu, estuvo dada por el cambio de C a T en la segunda posición del codón (tabla 3).
Discusión
La resistencia a las fluoroquinolonas en A. baumannii se ha asociado con mutaciones en el gen gyrA (17). Sin embargo, estas mutaciones en gyrA no explican por qué algunas cepas con la misma mutación presentan diferentes CIM a ciprofloxacina u otras fluoroquinolonas, lo que es posible por la presencia de mutaciones en la topoisomerasa IV como otro objetivo de las quinolonas. La determinación de la variación en la CIM para aislamientos de A. baumannii que muestran el mismo cambio de aminoácidos en la proteína gyrA podría derivarse de mutaciones en el gen parC, región equivalente a la QRDR de gyrA, o a la participación de bombas de salida
En este estudio la secuenciación del gen gyrA en los aislamientos clínicos para los que la CIM de ciprofloxacina fue de 1 μg/ml o menor, no mostró mutación puntual en el codón 83. Sin embargo, en los 12 aislamientos para los que la CIM de ciprofloxacina fue de 4 μg/ml o mayor, se presentó mutación en el codón 83 del gen gyrA, que resultó en el cambio del aminoácido serina a leucina, lo cual sugiere que este es el principal mecanismo implicado en la resistencia de estas bacterias a las fluoroquinolonas, debido a la ausencia de mutaciones en el gen parC y a la ausencia del sistema de salida adeB involucrado en la disminución de la sensibilidad a las fluoroquinolonas que puedan explicar las diferentes CIM expresadas a ciprofloxacina y moxifloxacina en los aislamientos de A. baumannii (10,18).
No obstante, a pesar de que los hallazgos muestran a la mutación en el gen gyrA como el único mecanismo de resistencia a las fluoroquinolonas, es posible que existan en estos aislamientos otros mecanismos de resistencia no contemplados en este estudio, como la bomba de salida de tipo MATE AbeM o el sistema de tipo RND AdeIJK (11,12,19). Aunque los genes de resistencia mediados por plásmidos, como el gen qnr, no se ha identificado en aislamientos de A. baumannii, podría considerarse su presencia como mecanismo de resistencia en este microorganismo (12).
De otra parte, las secuencias de aminoácidos obtenidas a partir de la secuenciación de los productos PCR de gyrA que no presentaron restricción con HinfI, se compararon mediante el uso de múltiple alineación creada por el uso de Clustal W, versión 2.0.8, con una secuencia sin mutación y otra con mutación obtenidas de la base de datos GenBank (16).
De esta manera, se estableció que las secuencias de los productos amplificados presentaron el cambio de Ser-83 a Leu, como se han descrito otros autores (22,18,20). Este cambio se ha asociado anteriormente con niveles de resistencia a ciprofloxacina intermedios a altos (CIM 4 a 128 μg/ml) (24), que corresponden con los niveles de resistencia a ciprofloxacina de las cepas de A. baumannii analizadas en el presente estudio.
Estos hallazgos sugieren que la resistencia a las quinolonas en A. baumannii multirresistentes depende de la modificación del destino conferida por sustituciones en la región QRDR del gen gyrA. Sin embargo, es importante mencionar que la presencia de la mutación Ser-83 incrementa la posibilidad de otras mutaciones en gyrA y parC (21). Aunque, Akasaka et al. (22) han informado que las mutaciones en el gen gyrB pueden jugar un papel importante en la resistencia a las fluoroquinolonas, debido a un posible aumento en la afinidad de estos antibióticos por esta subunidad a causa de una mutación en el codón 447 de la zona QRDR del gen gyrB (23).
Aunque los diferentes niveles de resistencia presentados en este estudio por los aislamientos de A. baumannii a la ciprofloxacina y a la moxifloxacina sugieren la presencia de mecanismos de resistencia a fluoroquinolonas distintos de gyrA, es importante mencionar que losestudios realizados en esta misma ciudad en 2002 mostraron porcentajes de resistencia de este microorganismo a las fluoroquinolonas del 50% (24).
Esto no es diferente de los resultados de este estudio donde se encontró un incrementó de sólo 2,1% en la resistencia, lo cual es suficientemente significativo debido a que esta resistencia aparece como consecuencia de un proceso gradual de mutación en los genes gyrA y parC, como también ocurre para los sistemas de salida. Así lo demuestra un estudio con P. aeruginosa en pacientes con fibrosis quística tratados con ciprofloxacina, realizado por Jalal et al. (25), en el cual el desarrollo de mutaciones de salida por MexCD-OprJ y MexEF-OprN como principal mecanismo de resistencia a las quinolonas, tomó cerca de tres años.
Por el contrario, con la resistencia mediada por la adquisición o transferencia horizontal de plásmidos de resistencia, transposones o integrones, el incremento en la CIM puede ocurrir de forma brusca en un tiempo corto como se presenta con la resistencia a antibióticos β-lactámicos y aminoglucósidos (26,27). En este estudio la resistencia expresada a las fluoroquinolonas fue más baja en relación con la resistencia mostrada a otras familias de antibióticos, como los aminoglucósidos, con 87,5% de resistencia y 68,7% de resistencia a los carbapenems (no se presentan los datos).
Las quinolonas ciprofloxacina y moxifloxacina son antimicrobianos de uso clínico importante en neumonías (28,29). Sin embargo, los resultados obtenidos en este estudio demuestran que el uso de estos antibióticos para tratar neumonías causadas por A. baumannii resultaría complicado, teniendo en cuenta que el gen gyrA presenta mutación que confiere resistencia a estos antibióticos en uno de cada dos aislamientos obtenidos. Esto podría conllevar al fracaso terapéutico, si estos antibióticos se utilizan para tratar las infecciones causadas por este microorganismo.
En conclusión, éste es el primer estudio que se lleva a cabo en Colombia sobre la detección molecular de la resistencia a fluoroquinolonas en A. baumannii. Los resultados permiten demostrar que los aislamientos de A. baumannii resistentes a las fluoroquinolonas son particularmente preocupantes, debido a que la resistencia a estos antibióticos, como fue encontrada en este estudio, stá dada por mutación cromosómica del gen gyrA.
Esto implica que, una vez adquirida, la resistencia es irreversible, lo que podría resultar en no usar estos antibióticos para tratar infecciones causadas por este microorganismo. Sin embargo, es posible que puedan existir mutaciones en el gen gyrB, o estar presentes otros sistemas de salida diferentes a los investigados en este estudio, que puedan contribuir a incrementar la CIM de las fluoroquinolonas. Los resultados también sugieren que la mutación del gen gyrA responsable de codificar el cambio del aminoácido serina a leucina en el codón 83 en aislamientos de A. baumannii, es responsable o, al menos, contribuye, con la resistencia expresada a las fluoroquinolonas.
A la Universidad de Córdoba por la financiación de este trabajo [código FMV 04-06; numeral: 1120223]. A Carlos Muskus por su valiosa ayuda en el análisis de las secuencias. Los resultados de este trabajo hacen parte de la tesis de maestría en Microbiología Tropical de Pedro Martínez R.
Correspondencia:
Salim Máttar V., Ph.D, Universidad de Córdoba, Instituto de Investigaciones Biológicas del Trópico, Universidad de Córdoba, Montería, Colombia Telefax: (574) 756-0710 mattarsalim@hotmail.com
http://www.unicordoba.edu.co/institutos/iibt/
1. Adams-Haduch J, Paterson D, Sidjabat H, Pasculle A, Potoski B, Muto C, et al. Genetic basis of multidrug resistance in Acinetobacter baumannii clinical isolates at a tertiary medical center in Pennsylvania. Antimicrobl Agents Chemother. 2008;52:3837-43. [ Links ]
2. Munoz-Price LS, Weinstein R. Acinetobacter infection. N Engl J Med. 2008;358:1271-81. [ Links ]
3. Karlowsky J, Draghi D, Jones M, Thornsberry C, Friedland I, Sahm D. Surveillance for antimicrobial susceptibility among clinical isolates of Pseudomonas aeruginosa and Acinetobacter baumannii from hospitalized patients in the United States, 1998 to 2001. Antimicrob Agents Chemother. 2003;47:1681-8. [ Links ]
4. Alós J. Quinolonas. Enferm Infecc Microbiol Clin. 2003;21:261-8. [ Links ]
5. Diomedis A. Infecciones por A. baumannii pan-resistentes. Consideraciones epidemiológicas y manejo antimicrobiano actualizado. Rev Chil Infect. 2005;22:298-320. [ Links ]
6. Martínez P, Mercado M, Máttar S. Determinación de blactamasas de espectro extendido en gérmenes nosocomiales del Hospital San Jerónimo, Montería. Colomb Med. 2003;34:196-205. [ Links ]
7. Hujer K, Hujer A, Endimiani A, Thomson J, Adams M, Goglin K, et al. Rapid determination of quinolone resistance in Acinetobacter spp. J Clin Microbiol. 2009;47:1436-42. [ Links ]
8. Mak J, Kim M, Pham J, Tapsall J, White P. Antibiotic resistance determinants in nosocomial strains of multidrugresistant Acinetobacter baumannii. J Antimicrob Chemother. 2009;63:47-54. [ Links ]
9. Hamouda A, Amyes S. Novel gyrA and parC point mutations in two strains of Acinetobacter baumannii resistant to ciprofloxacin. J Antimicrob Chemother. 2004;54:695-6. [ Links ]
10. Higgins P, Wisplinghoff H, Stefanik D, Seifert H. Selection of topoisomerase mutations and overexpression of adeB mRNA transcripts during an outbreak of Acinetobacter baumannii. J Antimicrob Chemother. 2004;54:821-3. [ Links ]
11. Damier-Piolle L, Magnet S, Brémont S, Lambert T, Courvalin P. AdeIJK, a resistance-nodulation-cell division pump effluxing multiple antibiotics in Acinetobacter baumannii. Antimicrob Agents Chemother. 2008;52:557-62. [ Links ]
12. Tran J, Jacoby G, Hooper D. Interaction of the plasmid-encoded quinolone resistance protein Qnr with Escherichia coli DNA gyrAse. Antimicrob Agents Chemother. 2005;49:118-25. [ Links ]
13. Peleg A, Seifert H, Paterson D. Acinetobacter baumannii: Emergence of a successful pathogen. Clin Microbiol Rev. 2008;21:538-82. [ Links ]
14. Clinical and Laboratory Standards Institute. Performance standards for antimicrobial susceptibility testing; 17th informational supplement. Wayne, PA: Clinical and Laboratory Standards Institute; 2007. [ Links ]
15. Altschul S, Gish W, Miller W, Myers E, Lipman D. Basic local alignment search tool. J Mol Biol. 1990;215:403-10. [ Links ]
16. Thompson J, Higgins D, Gibson T. CLUSTALW: improving the sensitivity of progressive multiple sequence alignment through sequence weighting, position-specific gap penalties and weight matrix choice. Nucleic Acids Res. 1994;22:4673-80. [ Links ]
17. Lin Y, Hsia K, Chen Y, Sheng W, Chang S, Liao M, et al. Genetic basis of multidrug resistance in Acinetobacter clinical isolates in Taiwan. Antimicrob Agents Chemother. 2010;54:2078-84. [ Links ]
18. Vila J, Ruiz J, Goñi P, Jiménez de Anta T. Quinoloneresistance mutations in the topoisomerase IV parC gene of Acinetobacter baumannii. J Antimicrob Chemother. 1997;39:757-62. [ Links ]
19. Jacoby G. Mechanisms of resistance to quinolones. Clin Infect Dis. 2005;41:S120-6. [ Links ]
20. Kyu J, Seon Y, Keun Y, Su B. Mutations in the gyrA and parC genes in ciprofloxacin-resistant clinical isolates of Acinetobacter baumanniiin Korea. Microbiol Immunol. 2005;49:647-53. [ Links ]
21. Oteo J, Campos J. Uso de quinolonas y resistencia. Enferm Infecc Microbiol Clin. 2004;22:201-3. [ Links ]
22. Akasaka T, Tanaka M, Yamaguchi A, Sato K. Type II topoisomerase mutations in fluoroquinolone-resistant clinical strains of Pseudomonas aeruginosa isolated in 1998 and 1999: role of target enzyme in mechanism of fluoroquinolone resistance. Antimicrob Agents Chemother. 2001;45:2263-8. [ Links ]
23. Heddle J, Maxwell A. Quinolone-binding pocket of DNA gyrAse: role of gyrB. Antimicrob Agents Chemother. 2002;46:1805-15. [ Links ]
24. Martínez P, Mercado M, Máttar S. Actividad in vitro de moxifloxacina comparada con otros antibióticos frente a aislamientos nosocomiales de dos hospitales de Colombia. Universitas Médica. 2004; 45:101-109. [ Links ]
25. Jalal S, Ciofu O, Hoiby N, Gotoh N, Wretlind B. Molecular mechanisms of fluoroquinolone resistance in Pseudomonas aeruginosa isolates from cystic fibrosis patients. Antimicrob Agents Chemother. 2000; 44: 710-712. [ Links ]
26. Moubareck C, Bremont S, Conroy M, Courvalin P, Lambert T. GES-11, a novel integron-associated GES variant in Acinetobacter baumannii. Antimicrob Agents Chemother. 2009;53:3579-81. [ Links ]
27. Nemec A, Dolzani L, Brisse S, van den Broek P, Dijkshoorn L. Diversity of aminoglycoside-resistance genes and their association with class 1 integrons among strains of pan-European Acinetobacter baumannii clones. J Med Microbiol. 2004;53:1233-40. [ Links ]
28. Lim T, Ledesma K, Chang K, Hou J, Kwa A, Nikolaou M, et al. Quantitative assessment of combination antimicrobial therapy against multidrug-resistant Acinetobacter baumannii. Antimicrob Agents Chemother. 2008;52:2898-904. [ Links ]
29. Drusano G, Preston S, Fowler C, Corrado M, Weisinger B, Kahn J. Relationship between fluoroquinolone area under the curve: minimum inhibitory concentration ratio and the probability of eradication of the infecting pathogen, in patients with nosocomial pneumonia. J Infect Dis. 2004;189:1590-7. [ Links ]
30. Vila J, Ruiz J, Goñi P, Marcos A, Jiménez De Anta T. Mutation in the gyrA gene of quinolone-resistant clinical isolates of Acinetobacter baumannii Antimicrobial Agents Chemother. 1995;39:1201-3. [ Links ]
31. Vila J, Ruiz J, Goñi P, Jiménez de Anta M. Detection of mutations in parC in quinolone-resistant clinical isolates of Escherichia coli. Antimicrob Agents Chemother. 1996;40: 491-3. [ Links ]
32. Magnet S, Courvalin P, Lambert T. Resistance-nodulationcell division-type efflux pump involved in aminoglucoside resistance in Acinetobacter baumannii strain BM4454. Antimicrob Agents Chemother. 2001;45:3375-80. [ Links ]














