Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Infectio
Print version ISSN 0123-9392
Infect. vol.15 no.2 Bogotá Apr./June 2011
1 Grupo de Inmunovirología, Universidad de Antioquia, Medellín, Colombia
Recibido: 03/12/2010; Aceptado: 08/06/2011
Resumen
Las estatinas son fármacos hipolipemiantes usados para controlar la aterogénesis y las enfermedades cardiovasculares originadas por hipercolesterolemia. Recientemente, se describieron varios efectos pleótropos de las estatinas, dependientes e independientes de la inhibición de la síntesis del colesterol, que van desde la regulación de la respuesta inmunitaria hasta la inhibición de la infección y la replicación viral. El tratamiento antirretroviral contra el VIH inhibe su replicación en las células infectadas, disminuyendo hasta niveles indetectables las copias del ARN viral en el plasma. Esto se asocia al incremento de los linfocitos T CD4+ circulantes y la disminución en la incidencia de infecciones oportunistas y en la mortalidad. Sin embargo, el costo y la complejidad del esquema antirretroviral, además de los efectos colaterales y la aparición de cepas resistentes, indican la necesidad de nuevos tratamientos para la infección por VIH. Como el VIH requiere del colesterol y las balsas de lípidos de la membrana celular para infectar las células blanco y cumplir su ciclo de replicación, se postula que las estatinas pueden ser una alternativa efectiva para ayudar al control de esta infección. La actividad anti-VIH de las estatinas no va dirigida contra las proteínas virales, muy variables por la mutabilidad del virus, sino que se centra en las células afectadas, bloqueando la infección por VIH y modulando su respuesta funcional; desde esta perspectiva, las estatinas evitarían la resistencia por mutaciones virales e intervendrían modulando la respuesta inmunitaria ampliamente alterada por el VIH.
Palabras clave: estatinas, inmunomodulación, actividad antiviral, virus de inmunodeficiencia humana.
Abstract
Statins are hypolipemiant drugs used for controlling atherogenesis and cardiovascular diseases caused by hypercholesterolemia. Recently, several pleiotropic effects of statins have been reported, whereas dependent or independent of downregulating cholesterol synthesis; these effects range from immune response modulation to inhibition of the infection and viral replication. The antiretroviral therapy against HIV inhibits viral replication in infected cells, decreasing to undetectable levels the number of viral RNA copies in plasma. Consequently, there is an increase in circulating CD4+ T-cell count, and a decrease in the incidence of opportunistic infections and mortality. However, the cost and complexity of antiretroviral regimens, the frequent side effects and the emergence of resistant strains, indicate the need of new approaches for HIV infection. Since HIV virions require of cholesterol in their envelope and the integrity of host membrane lipid rafts, in order to infect target cells and to perform several steps of their replication cycle, it has been proposed that the use of statins in HIV-1 infected patients can be an effective alternative to help control this infection. The anti-HIV activity of statins is not directed against viral proteins, which are highly variable due to viral mutations, but instead it focuses on cellular targets blocking their infection and regulating their functional responses. From this point of view, statins could avoid the emergence of resistant viral strains and intervene in the modulation of the highly altered immune responses.
Keywords: Statins, immunomodulation, antiviral activity, human immunodeficiency virus.
Introducción
Las estatinas son medicamentos conocidos por su propiedad para controlar la hipercolesterolemia y son ampliamente usadas para la prevención de enfermedades cardiovasculares (1,2). Las estatinas son análogos competitivos del substrato de la reductasa de la coenzima A 3-hidroxi- 3-metilglutarilo (HMG-CoA); esta enzima cataliza la conversión de HMG-CoA en ácido mevalónico (figura 1), precursor de la biosíntesis del colesterol y de los isoprenoides farnesilpirofosfato (FPP) y geranilgeranilpirofosfato (GGPP) (3).
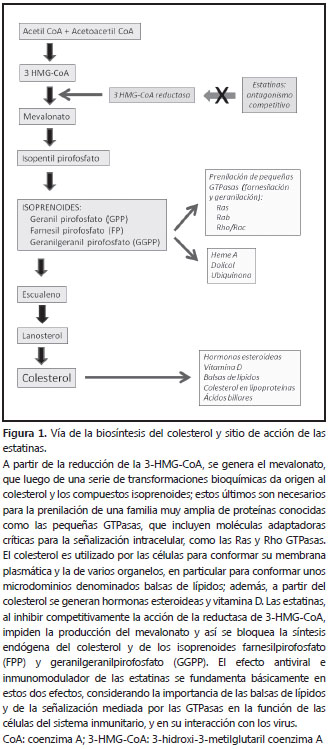
Al disminuir la concentración plasmática del colesterol, las estatinas también disminuyen la de las proteínas de baja densidad (Low Density Lipoproteins, LDL) circulantes; esto promueve una mayor expresión de los receptores para estas moléculas, lo cual facilita la depuración de las LDL del plasma y refuerza los efectos hipolipemiantes (4). Además, la menor producción de colesterol inducida por las estatinas, también se refleja en una reducción de la expresión en la superficie celular de los microdominios estructurales denominados “balsas de lípidos”, dominios que constituyen una especie de plataforma en la que convergen grupos de proteínas importantes para la activación y señalización celular (5-7).
El objetivo de esta revisión fue evaluar el conocimiento científico disponible sobre los efectos pleótropos de las estatinas, que van más allá de su acción hipolipemiante y que sustentan la potencial actividad inmunomoduladora, antiinfecciosa y anti-VIH de estos medicamentos. Para ello, se hizo una búsqueda en las bases de datos PubMed, Medline y Ovid, utilizando los siguientes términos: statin, pleiotropic effects, immunomodulation, infections, HIV. Se combinaron los términos, y se restringió la bibliografía a los artículos originales y a algunas revisiones publicadas en los últimos seis años.
Actividad inmunomoduladora de las estatinas
Además del efecto hipolipemiante dependiente de la inhibición de la biosíntesis del colesterol, se ha demostrado que las estatinas tienen otros efectos pleótropos que, en conjunto, llevan a acciones moduladoras de la respuesta inmunitaria y a una actividad antiviral (8-12). Las estatinas ejercen estos efectos inmunomoduladores por mecanismos muy diversos, que incluyen: la disminución en la formación de las balsas de lípidos y del reclutamiento de moléculas de comunicación intercelular en esos dominios; la inhibición de la señalización intracelular; la supresión de la secreción de citocinas proinflamatorias y de la expresión de moléculas de adhesión y coestimuladoras, y la alteración de la capacidad de las células dendríticas para inducir proliferación y activación de células T, entre otros (13).
Los isoprenoides FPP y GGPP son lípidos intracelulares requeridos para la prenilación de las proteínas; en este proceso, la unión de las proteínas a estos lípidos permite que ellas se ensamblen en la cara interior de la membrana celular, fenómeno que les permite ser funcionales.
Una de las familias de moléculas que es blanco de la prenilación por estos isoprenoides, es la de las pequeñas proteínas unidoras de trifosfato de guanosina (Guanosine Triphosphate, GTP), a la cual pertenecen varias subfamilias de proteínas de señalización intracelular, como las Rab, Ras, Rac y Rho GTPasas. Estas GTPasas participan en varios procesos intracelulares de señalización, con repercusiones en la funcionalidad de las células del sistema inmunitario al intervenir directamente en procesos como la motilidad y morfología de los leucocitos, el transporte intracelular de vesículas exocíticas y endocíticas, la fagocitosis y lisis de los microorganismos, el procesamiento y presentación de los antígenos, la activación y proliferación de los linfocitos, la función adhesiva y proinflamatoria del endotelio y las plaquetas, y la secreción de quimiocinas y otras citocinas (14-16). Así, al inhibir la síntesis de los isoprenoides, las estatinas modulan la prenilación de proteínas y su función, lo que afecta procesos muy importantes en el desarrollo de la respuesta inmunitaria (17).
Además, las estatinas se unen a un dominio específico de la molécula de adhesión LFA-1 (Leukocyte Function-Associated Molecule-1) y, de esta forma, bloquean de forma alostérica su interacción con la molécula ICAM-1 (Intercellular Adhesion Molecule-1); esta interacción es crucial para estabilizar el contacto entre la célula T y una célula presentadora de antígenos, y para regular el tráfico de leucocitos durante condiciones homeostáticas e inflamatorias (18-21). Las estatinas también inhiben la expresión inducible de las moléculas del complejo mayor de histocompatibilidad-II (Major Histocompatibility Complex-II, MHC-II) en las células endoteliales, respetando la expresión constitutiva en las células presentadoras de antígenos (10), fenómeno dependiente de una inadecuada geranilgeranilación de las Rho GTPasas que impide la actividad normal del citoesqueleto (12).
Por todos estos hallazgos, las estatinas han sido evaluadas como compuestos con beneficio potencial para el tratamiento de enfermedades diferentes a la hipercolesterolemia, la aterogénesis y las enfermedades cardiovasculares (22), como el rechazo del trasplante cardíaco y renal, el daño renal crónico, las enfermedades autoinmunitarias, las enfermedades neurológicas degenerativas crónicas, la sepsis y diversas enfermedades infecciosas (5,13,23-25).
Actividad antiviral de las estatinas
Los resultados de varios estudios han sugerido la utilidad de las estatinas para el tratamiento de las infecciones virales. En 1989 se publicaron dos investigaciones que demostraban el control del crecimiento celular por la inhibición de la reductasa de HMG-CoA, en células que fueron transformadas con el SV40 (Simian Virus 40) (26,27). Tres años después, se demostró que el tratamiento con lovastatina inhibía la correcta maduración de la proteína gPr90env del virus de la leucemia de ratón; en este caso, la gPr90env se quedaba secuestrada en compartimentos preGolgi y no sufría proteólisis en los complejos de Golgi, por mecanismos dependientes de la geranilgeranilación de Rab1p y Rab6p, impidiendo muy posiblemente las vías exocíticas (28).
La actividad antiviral de las estatinas también fue sugerida por estudios in vitro en cultivos celulares HEp-2 y en ratones infectados in vivo con el virus sincitial respiratorio sincitial (VRS), pero no en ratones infectados con viruela vacunoide (vaccinia virus) (29). Este efecto también pareció deberse a la inhibición en la síntesis de precursores para la prenilación de las Rho GTPasas. Es interesante que el uso de gemfibrosilo, otro agente que puede reducir la síntesis de colesterol y triglicéridos, no afectó la replicación viral, lo que indica que los mecanismos inhibitorios dependen de la prenilación de las Rho GTPasas y que, muy posiblemente, el colesterol no es un constituyente indispensable en la estructura del virus sincitial respiratorio.
A lo largo de la última década, se ha reactivado el interés por la actividad antiviral de los agentes hipolipemiantes e inhibitorios de la reductasa de HMG-CoA, que sugiere un uso potencial en el tratamiento de infecciones causadas por el virus de la influenza, del dengue, de la parainfluenza, de la hepatitis B y el citomegalovirus (30-34). Varios estudios también han demostrado actividad inhibitoria sobre la replicación del virus de la hepatitis C (VHC) (35-37); incluso, algunos autores sugieren, con base en los resultados obtenidos en sus modelos in vitro de replicación del virus de la hepatitis C, que las estatinas se pueden usar en tratamientos combinados con el interferón-α (35,38,39). Sin embargo, el compromiso de la función hepática durante esta infección hace discutible el uso de las estatinas en este grupo de pacientes, pues algunos de los efectos secundarios de las estatinas tienen fundamento en la toxicidad hepática (40-43). Además, y como se mencionó previamente, la estatinas aumentan la expresión de receptores para las LDL, las cuales también son usadas por el VHC para la entrada a los hepatocitos; por lo tanto, sería de esperarse que el uso de las estatinas pudiera aumentar la tasa de infección de las células blanco de este virus.
Actividad anti-VIH de las estatinas
La inmunopatogenia de la infección por el VIH implica varias interacciones entre el virus y el sistema inmunitario del huésped, con una destrucción temprana e irreversible del sistema inmunitario asociado a la mucosa del tubo digestivo, y un deterioro progresivo del resto de órganos linfoides primarios y (44) secundarios. Aunque hay activación de la respuesta inmunitaria innata y adaptativa (45), la infección es controlada con muy poco éxito. La replicación del VIH puede afectar el sistema inmunitario directamente por medio de la lisis de células infectadas o de su destrucción por la respuesta citotóxica, así como por el efecto inmunosupresor de proteínas virales como Nef, Vif y Vpr. Además, la infección crónica por el VIH se caracteriza por un estado de activación inmunitaria descontrolada que lleva a inmunosupresión y muerte acelerada de las células T CD4+, lo que contribuye al desarrollo de una inmunodeficiencia grave (45-47).
A pesar de más de 25 años de investigaciones dirigidas a buscar la manera de inducir una respuesta inmunitaria adaptativa protectora contra el VIH, no se han podido desarrollar tratamientos curativos o vacunas exitosas que prevengan esta infección. Actualmente, el tratamiento farmacológico mundialmente aceptado para el control de la infección por el VIH involucra la combinación de, al menos, tres agentes antirretrovirales en un esquema denominado terapia HAART (Highly Active Antiretroviral Therapy); se ha demostrado que en la mayoría de los infectados con el VIH, esta estrategia reduce significativamente la replicación viral, lo que lleva las concentraciones de ARN viral en plasma hasta niveles indetectables con los métodos de detección disponibles. Este efecto contribuye a que se restaure cuantitativamente y cualitativamente la inmunidad, aunque en un grado variable y no siempre completo, lo que se refleja en un incremento del conteo de células T CD4+ en sangre periférica; debido a la reconstitución inmunitaria, se aprecia una disminución de la incidencia de enfermedades oportunistas y reducción de la mortalidad (48). Sin embargo, cuando el esquema de la terapia HAART se suspende, la carga viral aumenta y el recuento de células T CD4+ disminuye, hasta niveles similares a los observados antes del inicio del tratamiento.
Pese a la potencia del esquema de la terapia HAART, este tratamiento antirretroviral administrado por largos períodos es incapaz de eliminar el VIH de los reservorios y no lleva a una completa restauración de la respuesta inmunitaria (49). Además, el alto costo y la complejidad de los esquemas de la terapia HAART, los efectos secundarios y la resistencia desarrollada por el VIH contra los medicamentos antirretrovirales, han indicado la necesidad inmediata de buscar otras estrategias terapéuticas adicionales.
Las investigaciones realizadas tanto in vivo como in vitro han demostrado que las estatinas tienen un potencial terapéutico para el control de la infección por el VIH, debido a que sus mecanismos de acción también incluyen una actividad antiviral que puede afectar diferentes estadios del ciclo de replicación del VIH, que van desde la inhibición del ingreso a las células blanco hasta un bloqueo en la gemación de las nuevas partículas virales (50-55). Es muy importante considerar que, por su mecanismo de acción, las estatinas son compuestos contra el VIH que no necesariamente atacan directamente el virión, sino que están dirigidos a las células blanco y a los otros efectos inmunopatogénicos indirectos de esta infección; por esta razón, un tratamiento anti- VIH con estatinas no tiene por qué, en teoría, constituir una presión selectiva para la aparición de cepas resistentes a estos medicamentos.
Los efectos biológicos de las estatinas sobre el metabolismo del colesterol, la función de las Rho GTPasas y sobre la molécula LFA-1, pueden interrumpir en varios pasos el ciclo de vida del VIH (figura 2). En primer lugar, la inhibición de la producción del colesterol por las estatinas puede tener múltiples efectos sobre la capacidad del VIH para producir infección, pues la necesidad del colesterol estructural en la membrana celular para la infección por el VIH ha sido claramente demostrada (56,57); cuando el colesterol de membrana se elimina por el tratamiento con β-ciclodextrina, se reduce considerablemente la capacidad infecciosa del VIH, impidiendo la fusión entre la membrana celular y la envoltura viral (51). Sin embargo, parece que la adhesión del virus a los receptores celulares no se afecta.
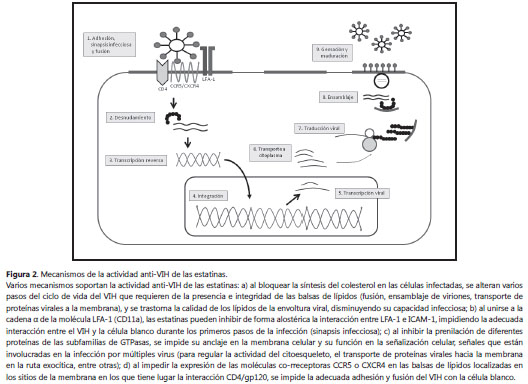
Por otro lado, la disminución de la síntesis del colesterol inhibe la capacidad de una célula para formar balsas de lípidos, y numerosos estudios han demostrado que el VIH requiere de las balsas de lípidos para pasar por los diferentes estadios de su replicación (55,56). Además, el análisis de la envoltura del VIH ha demostrado que los lípidos que conforman la envoltura viral son los mismos que se encuentran en las balsas de lípidos. La remoción del colesterol de membranas celulares o de la envoltura viral, inhibe la entrada del virus en cultivos primarios y líneas celulares (55, 58). Además, el desensamble de las balsas de lípidos inhibe la “transcitosis” del VIH a través de células endometriales HEC-1 o intestinales HT-29 (59).
Se ha demostrado que la proteína viral Nef se asocia al colesterol y transporta el colesterol recién sintetizado para incrementar la formación de balsas de lípidos, para hacer parte estructural de la envoltura del virión y promover el ensamblaje de nuevos viriones (60). Además, los diferentes fosfolípidos que conforman la envoltura también son regulados por la presencia de Nef. La expresión de Nef se correlaciona directamente con altos títulos virales y progresión de la enfermedad, pues la proteína Nef asociada a la balsas de lípidos media la activación de las células T, promoviendo la replicación y salida del VIH (61). Debido a que los viriones del VIH se ensamblan en dominios con balsas de lípidos, no es extraño que proteínas celulares pasen a ser parte estructural del VIH; también, se ha demostrado que moléculas de adhesión como LFA-1 e ICAM-1 se encuentran ensambladas en la envoltura viral (62).
La adhesión y la penetración del VIH se llevan a cabo mediante interacciones moleculares específicas entre las proteínas virales de envoltura y receptores y los correceptores presentes en la membrana de la célula blanco, lo que genera una serie de señales intracelulares que facilitan la infección viral (63). En particular, la localización simultánea del receptor CD4 en las balsas de lípidos es necesaria para la activación de p56-lck y posterior ingreso del VIH (56). La remoción del colesterol de la membrana de células mononucleares de sangre periférica reduce la localización simultánea de las moléculas CD4 y CXCR4 (64), necesaria para la infección con cepas X4 trópicas del VIH.
La fusión entre la envoltura viral y la membrana plasmática de la célula blanco es un paso posterior a la adhesión del VIH. A pesar de que el mecanismo completo de fusión de estas membranas no está completamente entendido, se ha visto que el colesterol presente en la envoltura viral es muy importante en este proceso (54). La capacidad del VIH para iniciar la fusión podría basarse en gran medida en la capacidad que tiene la proteína de envoltura gp41 para unirse al colesterol en las balsas de lípidos (65); la gp41 posee una secuencia señal que se une a dominios de lípidos, secuencia que al parecer es muy importante para la fusión de las membranas (66).
Otros procesos celulares dependientes del colesterol también juegan un papel importante en las etapas tardías del ciclo de vida del VIH, tales como el ensamble, la gemación, la morfología final del virión y su capacidad infecciosa (51). La disminución de la síntesis del colesterol en las células infectadas con el VIH da como resultado una significativa reducción en la liberación de virus, los cuales, además, presentan una capacidad infecciosa reducida (67). El colesterol de la envoltura del virión es adquirido de la célula huésped; se ha observado que los precursores Pr55Gag y Gag-Pol se ensamblan en complejos de lípidos resistentes a los detergentes (balsas de lípidos), aun antes de su transporte a la membrana celular (68). También, el sitio de liberación de las partículas virales está regulado por la distribución subcelular del colesterol (69). Es interesante que durante la gemación, las partículas del VIH incorporan moléculas de adhesión, como el ICAM- 1, debido a que existe una asociación entre los dominios citoplásmicos del ICAM-1 y Pr55Gag. La presencia de ICAM-1 en la envoltura viral aumenta la capacidad infecciosa del VIH (70).
Aparte de la ICAM-1, otras moléculas de adhesión, como LFA-1, ICAM-2 e ICAM-3, son expresadas en las balsas de lípidos de células infectadas con el VIH, y también, se encuentran en la envoltura de los viriones (71, 72); los niveles de expresión de estas moléculas de adhesión aumentan a medida que la enfermedad progresa (73). Se ha observado que el tratamiento previo del VIH con lovastatina inhibe su capacidad infecciosa por un bloqueo alostérico en un dominio específico de la cadena CD11a de LFA-1; esta inhibición de la infección es independiente del estado de activación de la molécula LFA-1 (19). Además, la inhibición de la prenilación de las Rho GTPasas puede regular negativamente la afinidad de la LFA-1 y atenuar varios aspectos de la respuesta inmunitaria, modificando o alterando vías de señalización intracelular (74-77). Estos hallazgos sugieren que la patogenia de la infección por el VIH puede ser modulada por las estatinas al actuar sobre la interacción ICAM-1/LFA-1, de manera que se impida la transmisión célula a célula del VIH (78,79).
La inhibición de la prenilación de las pequeñas Rho GTPasas por la lovastatina, parece ser otro de los mecanismos potencialmente benéficos en los pacientes infectados con el VIH (17), pues en el ciclo de replicación del VIH se ha demostrado la participación de las Rho GTPasas, así como de las Rab GTPasas. En la familia de las Rho GTPasas se han identificado cerca de 50 diferentes proteínas, como Cdc42, Rac1 y Rho, y, generalmente, cada una cumple con funciones específicas. Esta gran diversidad de proteínas no ha permitido identificar exactamente la participación específica de cada una de ellas en el ciclo de replicación del VIH. Sin embargo, se ha demostrado claramente que la inhibición de la geranilgeranilación de las Rho y de las Rab GTPasas (específicamente Rab11a), inhibe la producción del VIH en diferentes líneas celulares, como Jurkat, 293T, U1, U932 (17,50,80,81). Sin embargo, la incubación con estatinas lipofílicas como la lovastatina se asocia con una tasa mayor de transcripción de los genes virales, pero con un secuestro de sus productos a nivel intracelular (17,50); esto indica que la inhibición del VIH mediante el bloqueo de las pequeñas GTPasas también se puede deber a una deficiencia en los mecanismos de exocitosis. Es importante mencionar en este punto que, durante el proceso de salida del VIH de la célula huésped, el virus simula a las vesículas exocíticas en cuanto tamaño, composición de lípidos y composición proteica (82,83).
Recientemente se describió otro potencial mecanismo antiviral de las estatinas, que se puede sumar a la actividad anti-VIH de estos compuestos; se encontró que la lovastatina tiene capacidad de regular in vitro la expresión de CCR5 y RANTES en los linfocitos T CD4+ (84). Esta regulación, al parecer ejercida a nivel de la transcripción, da como resultado una mayor secreción de RANTES y una menor expresión de la molécula CCR5. Con estos efectos habría una clara inhibición de la infección por cepas R5 del VIH, mientras que no existiría efecto significativo sobre la infección por cepas X4 (84).
Los pocos estudios clínicos en que se ha evaluado la actividad anti-VIH de las estatinas in vivo, han arrojado resultados controversiales (17,85,86). En la investigación realizada por Del Real et al., seis individuos crónicamente infectados con el VIH, y que no habían recibido terapia HAART, recibieron lovastatina durante un mes como única medicación (17). Este corto tratamiento claramente redujo la carga viral e incrementó el conteo de células T CD4+. Además, luego de la suspensión del tratamiento con la lovastatina se observó, en ambos parámetros, una reversión hasta valores similares a los de antes de iniciar el tratamiento. En otra investigación llevada a cabo por Waters et al., se evaluó el efecto de las estatinas en individuos infectados con el VIH que tenían terapia HAART de inicio reciente; los resultados no demostraron diferencias significativas entre los que venían siendo tratados con estatinas y aquellos no tratados con estatinas (86). Además, se observó que las estatinas podrían tener un efecto tóxico sobre las células y atribuyeron el efecto anti-VIH in vitro más a esa actividad tóxica que a un verdadero efecto antiviral. En otro estudio observacional, no se encontraron cambios significativos en la carga viral y el conteo de células T CD4+ en aquellos pacientes positivos para VIH que fueron tratados con varios esquemas de inhibidores de proteasa y de transcriptasa inversa no análogos de nucleósido, en combinación con las estatinas (87).
Las interacciones farmacológicas entre las estatinas y los antirretrovirales usados en el esquema de la terapia HAART han sido estudiadas detalladamente (2,8,88-94). Es conocido que los medicamentos inhibidores de la proteasa viral también son inhibidores de la isoenzima hepática CYP3A y pueden, potencialmente, incrementar los niveles de estatinas, aumentando el riesgo de toxicidad muscular y hepática. Así, si se demuestran buenos efectos antivirales por el uso de las estatinas, las interacciones medicamentosas deben considerarse cuidadosamente en aquellos pacientes positivos para VIH que reciben esquemas de la terapia HAART.
Conclusiones Todos los hallazgos de los anteriores estudios in vitro e in vivo, ayudan a sustentar el potencial que tienen las estatinas para inhibir la infección por el VIH, gracias a que bloquean la síntesis del mevalonato (precursor del colesterol y los isoprenoides) y, en consecuencia, afectan varias etapas del ciclo de vida de este virus, tanto por mecanismos dependientes como independientes del colesterol. En ausencia de los lípidos generados en la vía del mevalonato, la adhesión y la fusión del VIH a la célula blanco se impiden al afectarse la flexibilidad de las membranas, debido a que se obstaculiza la formación y el agrupamiento de las balsas de lípidos, así como la expresión de los correceptores CCR5 y CXCR4 y, muy posiblemente, a que se altera la conformación y expresión de las moléculas de adhesión LFA-1 e ICAM-1.
Hasta el momento, se ha evidenciado que el VIH, al salir de la célula huésped, se lleva en su envoltura proteínas celulares como ICAM-1, que facilitan en cierto grado la infección. Sin embargo, no se sabe si la inhibición en la formación de balsas de lípidos por el tratamiento con estatinas tiene como consecuencia la ausencia de estas moléculas en la envoltura viral. Además, este bloqueo altera la señalización intracelular mediada por las Rho GTPasas, las cuales son las responsables de varios procesos de señalización celular y transporte intracelular de vesículas para el procesamiento de proteínas.
El control de la síntesis del mevalonato por medio de las estatinas representa una nueva posibilidad de intervenir sobre puntos críticos de la replicación del VIH, con nulo o mínimo riesgo de que aparezcan cepas resistentes a estos compuestos, por lo cual se postula como una nueva posibilidad terapéutica. Sin embargo, se necesitan los estudios básicos que definan si el tratamiento con estatinas lleva a la selección de cepas X4 del VIH o si no lo hace. Es completamente claro que los estudios in vitro con estatinas demuestran actividad anti-VIH y contra otros virus como el virus de la hepatitis C, pero estos hallazgos deben ser tomados aún con precaución, ya que los resultados de estudios clínicos en pacientes positivos para VIH son ambiguos, posiblemente por el pobre rigor y tamaño de la muestra de las investigaciones que se han publicado hasta el momento.
Se requieren con urgencia estudios clínicos controlados, aleatorios y doble ciego, para definir si lo que se ha observado in vitro se reproduce in vivo en pacientes infectados crónicamente con el VIH. Sin embargo, se debe tener en cuenta que en la mayoría de los individuos que reciben terapia HAART hay una disminución significativa de la carga viral, y que si en ellos se evalúa el efecto antiviral de las estatinas se podría enmascarar la inhibición mediada por las estatinas.
En consecuencia, la eficacia virológica y clínica de las estatinas debería ser evaluada en individuos positivos para VIH y asintomáticos que no hayan recibido ni estén recibiendo terapia HAART.
Reconocimientos Esta publicación fue posible gracias al apoyo financiero de Colciencias (proyecto 1115-40-820508).
Correspondencia: Edwin Andrés Higuita, Calle 62 N° 52-59, Torre 2, Laboratorio 532, Sede de Investigación Universitaria, Universidad de Antioquia, Medellín, Colombia. Teléfono: (4) 219- 6482. Dirección electrónica: andreshiguitad@gmail.com
Referencias
1. Calza L, Manfredi R, Chiodo F. Hyperlipidaemia in patients with HIV-1 infection receiving highly active antiretroviral therapy: Epidemiology, pathogenesis, clinical course and management. Int J Antimicrob Agents. 2003;22:89-99. [ Links ]
2. Calza L, Manfredi R, Chiodo F. Statins and fibrates for the treatment of hyperlipidaemia in HIV-infected patients receiving HAART. AIDS (London, England). 2003;17:851-9. [ Links ]
3. Illingworth DR, Tobert JA. HMG-CoA reductase inhibitors. Adv Protein Chem. 2001;56:77-114. [ Links ]
4. Downs JR, Clearfield M, Weis S, Whitney E, Shapiro DR, Beere PA, et al. Primary prevention of acute coronary events with lovastatin in men and women with average cholesterol levels: Results of AFCAPS/TexCAPS. Air Force/Texas Coronary Atherosclerosis Prevention Study. JAMA. 1998;279:1615-22. [ Links ]
5. Jury EC, Flores-Borja F, Kabouridis PS. Lipid rafts in T cell signalling and disease. Semin Cell Dev Biol. 2007;18:608-15. [ Links ]
6. Jury EC, Isenberg DA, Mauri C, Ehrenstein MR. Atorvastatin restores Lck expression and lipid raft-associated signaling in T cells from patients with systemic lupus erythematosus. J Immunol. 2006;177:7416-22. [ Links ]
7. Rao R, Logan B, Forrest K, Roszman TL, Goebel J. Lipids rafts in cytokine signaling. Cytok Growth Fact Rev. 2004;15:103-10. [ Links ]
8. Aberg JA, Zackin RA, Brobst SW, Evans SR, Alston BL, Henry WK, et al. A randomized trial of the efficacy and safety of fenofibrate versus pravastatin in HIV-infected subjects with lipid abnormalities: AIDS Clinical Trials Group Study 5087. AIDS Res Hum Retroviruses. 2005;21:757-67. [ Links ]
9. Fehr T, Kahlert C, Fierz W, Joller-Jemelka HI, Riesen WF, Rickli H, et al. Statin-induced immunomodulatory effects on human T cells in vivo. Atherosclerosis. 2004;175:83-90. [ Links ]
10. Kwak B, Mulhaupt F, Veillard N, Pelli G, Mach F. The HMG-CoA reductase inhibitor simvastatin inhibits IFN-gamma induced MHC class II expression in human vascular endothelial cells. Swiss Med Wkly. 2001;131:41-6. [ Links ]
11. Yilmaz A, Reiss C, Tantawi O, Weng A, Stumpf C, Raaz D, et al. HMGCoA reductase inhibitors suppress maturation of human dendritic cells: New implications for atherosclerosis. Atherosclerosis. 2004;172:85-93. [ Links ]
12. Kwak B, Mulhaupt F, Myit S, Mach F. Statins as a newly recognized type of immunomodulator. Nat Med. 2000;6:1399-402. [ Links ]
13. García PJ. Pleiotropic effects of statins: Moving beyond cholesterol control. Curr Atheroscler Rep. 2005;7:34-9. [ Links ]
14. Groves E, Dart AE, Covarelli V, Caron E. Molecular mechanisms of phagocytic uptake in mammalian cells. Cell Mol Life Sci. 2008;65:1957-76. [ Links ]
15. Heasman SJ, Ridley AJ. Mammalian Rho GTPases: New insights into their functions from in vivo studies. Nature Rev. 2008;9:690-701. [ Links ]
16. Scheele JS, Marks RE, Boss GR. Signaling by small GTPases in the immune system. Immunol Rev. 2007;218:92-101. [ Links ]
17. del Real G, Jiménez-Baranda S, Mira E, Lacalle RA, Lucas P, Gómez- Mouton C, et al. Statins inhibit HIV-1 infection by down-regulating Rho activity. J Exp Med. 2004;200:541-7. [ Links ]
18. Issekutz TB. Inhibition of lymphocyte endothelial adhesion and in vivo lymphocyte migration to cutaneous inflammation by TA-3, a new monoclonal antibody to rat LFA-1. J Immunol. 1992;149:3394- 402. [ Links ]
19. Kallen J, Welzenbach K, Ramage P, Geyl D, Kriwacki R, Legge G, et al. Structural basis for LFA-1 inhibition upon lovastatin binding to the CD11a I-domain. J Mol Biol. 1999;292:1-9. [ Links ]
20. Wallays G, Ceuppens JL. Ligation of leukocyte function-associated (LFA) molecule-1 provides an accessory signal for T-cell activation with pokeweed mitogen. Scand J Immunol. 1994;39:137-43. [ Links ]
21. Weitz-Schmidt G, Welzenbach K, Brinkmann V, Kamata T, Kallen J, Bruns C, et al. Statins selectively inhibit leukocyte function antigen-1 by binding to a novel regulatory integrin site. Nat Med. 2001;7:687- 92. [ Links ]
22. Blanco-Colio LM, Tunon J, Martín-Ventura JL, Egido J. Anti-inflammatory and immunomodulatory effects of statins. Kidney Int. 2003;63:12-23. [ Links ]
23. Campistol JM. Advances in transplantation and immunosuppression. Drug News Perspect. 1998;11:372-5. [ Links ]
24. McKay A, Leung BP, McInnes IB, Thomson NC, Liew FY. A novel antiinflammatory role of simvastatin in a murine model of allergic asthma. J Immunol. 2004;172:2903-8. [ Links ]
25. Vaughan CJ, Delanty N. Neuroprotective properties of statins in cerebral ischemia and stroke. Stroke. 1999;30:1969-73. [ Links ]
26. Larsson O, Engstrom W. The role of N-linked glycosylation in the regulation of activity of 3-hydroxy-3-methylglutaryl-coenzyme A reductase and proliferation of SV40-transformed 3T3 cells. Biochem J. 1989;260:597-600. [ Links ]
27. Larsson O, Barrios C, Latham C, Ruiz J, Zetterberg A, Zickert P, et al. Abolition of mevinolin-induced growth inhibition in human fibroblasts following transformation by simian virus 40. Cancer Res. 1989;49:5605-10. [ Links ]
28. Overmeyer JH, Maltese WA. Isoprenoid requirement for intracellular transport and processing of murine leukemia virus envelope protein. J Biol Chem. 1992;267:22686-92. [ Links ]
29. Gower TL, Graham BS. Antiviral activity of lovastatin against respiratory syncytial virus in vivo and in vitro. Antimicrob Agents Chemother. 2001;45:1231-7. [ Links ]
30. Carrillo-Esper R. Statins in influenza: Time for a controlled clinical study. Cirugía y Cirujanos. 2009;77:351-2. [ Links ]
31. Lin YL, Shiao MS, Mettling C, Chou CK. Cholesterol requirement of hepatitis B surface antigen (HBsAg) secretion. Virology. 2003;314:253-60. [ Links ]
32. Potena L, Frascaroli G, Grigioni F, Lazzarotto T, Magnani G, Tomasi L, et al. Hydroxymethyl-glutaryl coenzyme a reductase inhibition limits cytomegalovirus infection in human endothelial cells. Circulation. 2004;109:532-6. [ Links ]
33. Rothwell C, Lebreton A, Young Ng C, Lim JY, Liu W, Vasudevan S, et al. Cholesterol biosynthesis modulation regulates dengue viral replication. Virology. 2009;389:8-19. [ Links ]
34. Saladino R, Ciambecchini U, Nencioni L, Palamara AT. Recent advances in the chemistry of parainfluenza-1 (Sendai) virus inhibitors. Med Res Rev. 2003;23:427-55. [ Links ]
35. Ikeda M, Abe K, Yamada M, Dansako H, Naka K, Kato N. Different anti-HCV profiles of statins and their potential for combination therapy with interferon. Hepatology (Baltimore) 2006;44:117-25. [ Links ]
36. Mihaila R, Nedelcu L, Fratila O, Rezi EC, Domnariu C, Ciuca R, et al. Lovastatin and fluvastatin reduce viremia and the pro-inflammatory cytokines in the patients with chronic hepatitis C. Hepato-Gastroenterology. 2009;56:1704-9. [ Links ]
37. Ye J, Wang C, Sumpter R Jr, Brown MS, Goldstein JL, Gale M Jr. Disruption of hepatitis C virus RNA replication through inhibition of host protein geranylgeranylation. Proc Natl Acad Sci USA. 2003;100:15865-70. [ Links ]
38. Delang L, Paeshuyse J, Vliegen I, Leyssen P, Obeid S, Durantel D, et al. Statins potentiate the in vitro anti-hepatitis C virus activity of selective hepatitis C virus inhibitors and delay or prevent resistance development. Hepatology (Baltimore) 2009;50:6-16. [ Links ]
39. Harrison SA, Rossaro L, Hu KQ, Patel K, Tillmann H, Dhaliwal S, et al. Serum cholesterol and statin use predict virological response to peginterferon and ribavirin therapy. Hepatology (Baltimore) 2010;52:864-74. [ Links ]
40. Goldstein MR, Mascitelli L, Pezzetta F. Statins and hepatitis C virus: More caution and less enthusiasm. The American Journal of Gastroenterology. 2008;103:3207-8; author reply 8-9. [ Links ]
41. Khorashadi S, Hasson NK, Cheung RC. Incidence of statin hepatotoxicity in patients with hepatitis C. Clin Gastroenterol Hepatol. 2006;4:902-7. [ Links ]
42. Lonardo A, Loria P, Bertolotti M, Carulli N. Statins and HCV: A complex issue. Hepatology (Baltimore) 2007;45:257. [ Links ]
43. Tandra S, Vuppalanchi R. Use of statins in patients with liver disease. Current treatment options in cardiovascular medicine. 2009;11:272-8. [ Links ]
44. Montoya CJ, Moreno ME, Rugeles MT. Reacciones y alteraciones del sistema inmune durante la infección por el VIH-1. Infectio. 2006;10:250-65. [ Links ]
45. Cohen DE, Walker BD. Human immunodeficiency virus pathogenesis and prospects for immune control in patients with established infection. Clin Infect Dis. 2001;32:1756-68. [ Links ]
46. Giorgi JV, Liu Z, Hultin LE, Cumberland WG, Hennessey K, Detels R. Elevated levels of CD38+ CD8+ T cells in HIV infection add to the prognostic value of low CD4+ T cell levels: Results of 6 years of follow-up. J Acquir Immune Defic Syndr. 1993;6:904-12. [ Links ]
47. Hazenberg MD, Otto SA, van Benthem BHB, Roos MTL, Coutinho RA, Lange JMA, et al. Persistent immune activation in HIV-1 infection is associated with progression to AIDS. AIDS. 2003;17:1881-8. [ Links ]
48. Palella FJ, Delaney KM, Moorman AC, Loveless MO, Fuhrer J, Satten GA, et al. Declining morbidity and mortality among patients with advanced human immunodeficiency virus infection. N Engl J Med. 1998;338:853-60. [ Links ]
49. Finzi D, Hermankova M, Pierson T, Carruth LM, Buck C, Chaisson RE, et al. Identification of a reservoir for HIV-1 in patients on highly active retroviral therapy. Science. 1997;278:1295-300. [ Links ]
50. Amet T, Nonaka M, Dewan MZ, Saitoh Y, Qi X, Ichinose S, et al. Statin-induced inhibition of HIV-1 release from latently infected U1 cells reveals a critical role for protein prenylation in HIV-1 replication. Microbes and Infection/Institut Pasteur. 2008;10:471-80. [ Links ]
51. Campbell SM, Crowe SM, Mak J. Virion associated cholesterol is critical for the maintenance of HIV-1 structure and infectivity. AIDS (London, England). 2002;16:2253-61. [ Links ]
52. Carter GC, Bernstone L, Sangani D, Bee JW, Harder T, James W. HIV entry in macrophages is dependent on intact lipid rafts. Virology. 2009;386:192-202. [ Links ]
53. Corrales-Medina VF, Del Carpio F, Concha R, Symes S. Statins and HIV: Beyond the metabolic and cardiovascular benefit. J Acquir Immune Defic Syndr. 2005;39:503-4. [ Links ]
54. Guyader M, Kiyokawa E, Abrami L, Turelli P, Trono D. Role for human immunodeficiency virus type 1 membrane cholesterol in viral internalization. J Virol. 2002;76:10356-64. [ Links ]
55. Liao Z, Cimakasky LM, Hampton R, Nguyen DH, Hildreth JE. Lipid rafts and HIV pathogenesis: Host membrane cholesterol is required for infection by HIV type 1. AIDS Res. 2001;17:1009-19. [ Links ]
56. del Real G, Jiménez-Baranda S, Lacalle RA, Mira E, Lucas P, Gómez- Mouton C, et al. Blocking of HIV-1 infection by targeting CD4 to nonraft membrane domains. J Exp Med. 2002;196:293-301. [ Links ]
57. Waheed AA, Freed EO. The role of lipids in retrovirus replication. Viruses. 2010;2:1146-80. [ Links ]
58. Manes S, del Real G, Lacalle RA, Lucas P, Gómez-Mouton C, Sánchez- Palomino S, et al. Membrane raft microdomains mediate lateral assemblies required for HIV-1 infection. EMBO Rep. 2000;1:190- 6. [ Links ]
59. Alfsen A, Iniguez P, Bouguyon E, Bomsel M. Secretory IgA specific for a conserved epitope on gp41 envelope glycoprotein inhibits epithelial transcytosis of HIV-1. J Immunol. 2001;166:6257-65. [ Links ]
60. Zheng YH, Plemenitas A, Fielding CJ, Peterlin BM. Nef increases the synthesis of and transports cholesterol to lipid rafts and HIV-1 progeny virions. Proc Natl Acad Sci USA. 2003;1000:8460-5. [ Links ]
61. Wang JK, Kiyokawa E, Verdin E, Trono D. The Nef protein of HIV- 1 associates with rafts and primes T cells for activation. Proc Natl Acad Sci USA. 2000;97:394-9. [ Links ]
62. Bastiani L, Cecilia D, Fenyo EM, Laal S, Zolla-Pazner S. HIV phenotype correlates with the relative amounts of lymphocyte functionrelated molecule 1 (LFA-1) and major histocompatibility complex (MHC) class II in the virion envelope. AIDS (London, England). 2000;14:1523-31. [ Links ]
63. van der Goot FG, Harder T. Raft membrane domains: From a liquidordered membrane phase to a site of pathogen attack. Semin Immunol. 2001;13:89-97. [ Links ]
64. Viard M, Parolini I, Sargiacomo M, Fecchi K, Ramoni C, Ablan S, et al. Role of cholesterol in human immunodeficiency virus type 1 envelope protein-mediated fusion with host cells. J Virol. 2002;76:11584- 95. [ Links ]
65. Vincent N, Genin C, Malvoisin E. Identification of a conserved domain of the HIV-1 transmembrane protein gp41 which interacts with cholesteryl groups. Biochim Biophys. 2002;1567:157-64. [ Links ]
66. Saez-Cirion A, Nir S, Lorizate M, Agirre A, Cruz A, Pérez-Gil J, et al. Sphingomyelin and cholesterol promote HIV-1 gp41 pretransmembrane sequence surface aggregation and membrane restructuring. J Biol Chem. 2002;277:21776-85. [ Links ]
67. Liao Z, Graham DR, Hildreth JE. Lipid rafts and HIV pathogenesis: Virion-associated cholesterol is required for fusion and infection of susceptible cells. AIDS Res Hum Retroviruses. 2003;19:675-87. [ Links ]
68. Lee YM, Liu B, Yu XF. Formation of virus assembly intermediate complexes in the cytoplasm by wild-type and assembly-defective mutant human immunodeficiency virus type 1 and their association with membranes. J Virol. 1999;73:5654-62. [ Links ]
69. Lindwasser OW, Resh MD. Human immunodeficiency virus type 1 Gag contains a dileucine-like motif that regulates association with multivesicular bodies. J Virol. 2004;78:6013-23. [ Links ]
70. Fortin JF, Cantin R, Lamontagne G, Tremblay M. Host-derived ICAM- 1 glycoproteins incorporated on human immunodeficiency virus type 1 are biologically active and enhance viral infectivity. J Virol. 1997;71:3588-96. [ Links ]
71. Butini L, De Fougerolles AR, Vaccarezza M, Graziosi C, Cohen DI, Montroni M, et al. Intercellular adhesion molecules (ICAM)-1, ICAM-2, and ICAM-3 function as counter-receptors for lymphocyte function-associated molecule 1 in human immunodeficiency virus- mediated syncytia formation. Eur J Immunol. 1994;24:2191-5. [ Links ]
72. Tremblay MJ, Fortin JF, Cantin R. The acquisition of host-encoded proteins by nascent HIV-1. Immunol Today. 1998;19:346-51. [ Links ]
73. Park SW, Royal W, Semba RD, Wiegand GW, Griffin DE. Expression of adhesion molecules and CD28 on T lymphocytes during human immunodeficiency virus infection. Clin Diagn Lab Immunol. 1998;5:583-7. [ Links ]
74. Bolomini-Vittori M, Montresor A, Giagulli C, Staunton D, Rossi B, Martinello M, et al. Regulation of conformer-specific activation of the integrin LFA-1 by a chemokine-triggered Rho signaling module. Nature immunology. 2009;10:185-94. [ Links ]
75. Mor A, Dustin ML, Philips MR. Small GTPases and LFA-1 reciprocally modulate adhesion and signaling. Immunological reviews. 2007;218:114-25. [ Links ]
76. Nishibori M, Takahashi HK, Mori S. The regulation of ICAM-1 and LFA-1 interaction by autacoids and statins: A novel strategy for controlling inflammation and immune responses. J Pharmacol Sci. 2003;92:7-12. [ Links ]
77. Smith A, Bracke M, Leitinger B, Porter JC, Hogg N. LFA-1-induced T cell migration on ICAM-1 involves regulation of MLCK-mediated attachment and ROCK-dependent detachment. Journal of Cell Science. 2003;116(Pt 15):3123-33. [ Links ]
78. Hildreth JE, Orentas RJ. Involvement of a leukocyte adhesion receptor (LFA-1) in HIV-induced syncytium formation. Science. 1989;244:1075-8. [ Links ]
79. Pearce-Pratt R, Phillips DM. Studies of adhesion of lymphocytic cells: Implications for sexual transmission of human immunodeficiency virus. Biol Reprod. 1993;48:431-45. [ Links ]
80. Varthakavi V, Smith RM, Martin KL, Derdowski A, Lapierre LA, Goldenring JR, et al. The pericentriolar recycling endosome plays a key role in Vpu-mediated enhancement of HIV-1 particle release. Traffic (Copenhagen, Denmark). 2006;7:298-307. [ Links ]
81. Vidricaire G, Tremblay MJ. Rab5 and Rab7, but not ARF6, govern the early events of HIV-1 infection in polarized human placental cells. J Immunol. 2005;175:6517-30. [ Links ]
82. Booth AM, Fang Y, Fallon JK, Yang JM, Hildreth JE, Gould SJ. Exosomes and HIV Gag bud from endosome-like domains of the T cell plasma membrane. J Cell Biol. 2006;172:923-35. [ Links ]
83. Izquierdo-Useros N, Naranjo-Gómez M, Erkizia I, Puertas MC, Borras FE, Blanco J, et al. HIV and mature dendritic cells: Trojan exosomes riding the Trojan horse? PLoS Pathogens. 2010;6:e1000740. [ Links ]
84. Nabatov AA, Pollakis G, Linnemann T, Paxton WA, de Baar MP. Statins disrupt CCR5 and RANTES expression levels in CD4+ T lymphocytes in vitro and preferentially decrease infection of R5 versus X4 HIV-1. PLoS ONE. 2007;2:e470. [ Links ]
85. Probasco JC, Spudich SS, Critchfield J, Lee E, Lollo N, Deeks SG, et al. Failure of atorvastatin to modulate CSF HIV-1 infection: Results of a pilot study. Neurology. 2008;71:521-4. [ Links ]
86. Waters L, Stebbing J, Jones R, Mandalia S, Bower M, Stefanovic M, et al. The effect of statins on HIV rebound and blips. J Acquir Immune Defic Syndr. 2005;39:637-8. [ Links ]
87. Sklar PA, Masur H, Grubb JR, Voell J, Witek J, Ono A, et al. Pravastatin does not have a consistent antiviral effect in chronically HIV-infected individuals on antiretroviral therapy. AIDS (London, England). 2005;19:1109-11. [ Links ]
88. Aboulafia DM, Johnston R. Simvastatin-induced rhabdomyolysis in an HIV-infected patient with coronary artery disease. AIDS Patient Care STDS. 2000;14:13-8. [ Links ]
89. Benesic A, Zilly M, Kluge F, Weissbrich B, Winzer R, Klinker H, et al. Lipid lowering therapy with fluvastatin and pravastatin in patients with HIV infection and antiretroviral therapy: Comparison of efficacy and interaction with indinavir. Infection. 2004;32:229-33. [ Links ]
90. Bonnet F, Balestre E, Thiebaut R, Mercie P, Dupon M, Morlat P, et al. Fibrates or statins and lipid plasma levels in 245 patients treated with highly active antiretroviral therapy. Aquitaine Cohort, France, 1999-2001. HIV Med. 2004;5:133-9. [ Links ]
91. Hurlimann D, Chenevard R, Ruschitzka F, Flepp M, Enseleit F, Bechir M, et al. Effects of statins on endothelial function and lipid profile in HIV infected persons receiving protease inhibitor-containing antiretroviral combination therapy: A randomized double blind crossover trial. Heart. 2006;92:110-2. [ Links ]
92. Martínez E, Tuset M, Milinkovic A, Miro JM, Gatell JM. Management of dyslipidaemia in HIV-infected patients receiving antiretroviral therapy. Antivir Ther. 2004;9:649-63. [ Links ]
93. Penzak SR, Chuck SK, Stajich GV. Safety and efficacy of HMG-CoA reductase inhibitors for treatment of hyperlipidemia in patients with HIV infection. Pharmacotherapy. 2000;20:1066-71. [ Links ]
94. Sklar PA, Masur H, Grubb JR, Voell J, Witek J, Ono A, et al. Pravastatin does not have a consistent antiviral effect in chronically HIV-infected individuals on antiretroviral therapy. AIDS (London, England). 2005;19:1109-11. [ Links ]














