Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Infectio
Print version ISSN 0123-9392
Infect. vol.16 no.1 Bogotá Jan./Mar. 2012
1Laboratorio Médico Echavarría, Medellín, Colombia
2Universidad de Antioquia, Medellín, Colombia
3Sección de Biología Molecular, Bogotá; Laboratorio Médico Echavarría, Medellín, Colombia
Recibido: 11/07/2011; Aceptado: 08/02/2012
Resumen
Objetivo. El propósito del estudio fue evaluar el desempeño del método VERSANTHIV-1RNA 1.0 Assay® (kPCR) (Siemens), para la cuantificación de la carga viral en pacientes con VIH-1, en comparación con el método COBAS® AmpliPrep/COBAS TaqMan HIV-1 test®, v2.0 (Roche Diagnostics) (CAP/CTM).
Métodos. Las muestras fueron tomadas en dos tubos con EDTA, de 60 pacientes remitidos por el médico tratante para pruebas de carga viral como parte de su control de rutina de VIH/sida, y fueron procesadas para la cuantificación del ARN del VIH-1 por ambas técnicas. Se hizo análisis de regresión y se calcularon los coeficientes de correlación de Pearson, y los de correlación y concordancia de Lin. Se evalúo la concordancia entre las dos técnicas mediante el método de Bland-Altman.
Resultados. El promedio de la carga viral por el método CAP/CTM fue 3,2±1,4 long10 copias/ml y, por el método kPCR, 3,0±1,3 long10 copias/ml. El 86,7 % de muestras presentó diferencias entre los dos métodos, menores de 0,5 long10 copias/ml, y el 13,3 % presentó diferencias mayores. El coeficiente de correlación de Pearson entre los dos métodos fue de 0,97 (IC95% 0,95-0,99) y el índice kappa ponderado entre los dos métodos en diferentes rangos de concentración, fue de 0,91 (IC95% 0,87-0,96). El promedio de las diferencias entre las mediciones fue 0,22 long10 copias/ml (IC95% -0,45 a 0,89).
Conclusión. Las dos técnicas evaluadas fueron comparables, con el método kPCR se observaron resultados más bajos.
Palabras clave: VIH-1, carga viral, reacción en cadena de la polimerasa (PCR)
Abstract
Objective: The purpose of this study was to evaluate the performance of the kPCR VERSANT (™) 440 HIV-1RNA 3.0 Assay® (Siemens) method for the quantification of viral load in HIV-1 patients, compared to the COBAS AmpliPrep/COBASTaqMan HIV-1 test®, v. 2.0 (Roche Diagnostics) (CAP/CTM).
Methods: Samples were taken in 2 tubes with EDTA, in 60 patients referred by the attending physician for viral load tests as part of their routine control of HIV/AIDS, and were processed for quantification of HIV-1 RNA by both techniques. A regression analysis, the Pearson correlation coefficient and agreement of Lin were done. The agreement between the two techniques was evaluated with the Bland Altman analysis.
Results: The mean viral load by CAP/CTM was 3.2 ± 1.4 long10 copies/ml and by kPCR it was 3.0±1.3 10 copies/ml. Most samples (86.7%) showed differences between the two methods lower than 0.5 long10 copies/ml, and 13.3% presented greater differences. The Pearson correlation coefficient between the two methods was 0.97 (95% CI 0.95-0.99) and the weighted kappa index between the two methods, in different ranges of concentration, was 0.91 (95% CI 0.87-0.96). The average difference between measurements by both techniques was 0.22 long10 copies/ml, (IC 95% -0.45-0.89).
Conclusion: Both techniques were comparable, although lower values of viral load were observed with kPCR.
Key words: HIV-1, viral load, Polymerase Chain Reaction (PCR)
Introducción
La infección por virus de la inmunodeficiencia humana (VIH) y el síndrome de inmunodeficiencia adquirida (sida) son problemas de salud pública en aumento y Colombia no es ajena a este fenómeno, puesto que se encuentra entre las primeras 20 causas de años perdidos de vida saludable, en las edades de 15 a 49 años (1).
En este sentido, en el Plan Nacional de Respuesta ante el VIH/ 2008-2011, se ha propuesto, en tre otras metas para el año 2015, mantener la prevalencia de la infección por VIH por debajo de 1,2 %, aumentar el acceso a los medicamentos antirretrovirales y reducir la mortalidad por causa del sida (2). Dicho propósito implica mejorar el acceso al diagnóstico y tratamiento oportuno, así como el seguimiento de la evolución VIH/sida, mediante técnicas confiables.
Las pruebas de carga viral para VIH-1 son fundamentales en el seguimiento de los pacientes VIH/sida desde su evaluación inicial, así como durante el seguimiento en casos con terapia antirretroviral o sin ella, y se utilizan como guía para cambios en el plan de tratamiento, dado que los resultados de la cuantificación de la carga viral se correlacionan con la progresión del VIH/sida y con la respuesta a los antirretrovirales; además en casos especiales, contribuyen al diagnóstico inicial de infección aguda antes de la seroconversión (3-6).
En la actualidad se dispone de diferentes pruebas comerciales que permiten cuantificar la carga viral VIH-1, con diferencias en sensibilidad, linealidad, sitios blanco en el genoma del virus y métodos de amplificación. Las pruebas más recientes se basan en la metodología de la reacción de polimerasa en cadena (PCR) en tiempo real, las cuales han tenido amplia aceptación por parte de los laboratorios por su mayor sensibilidad, rango dinámico más amplio, altos niveles de automatización y mayor capacidad para cuantificar diferentes tipos y subtipos del VIH-1 (3,6,7).
En Colombia, los métodos comerciales de PCR en tiempo real más utilizados para cuantificación del VIH-1 son: COBAS AmpliPrep/COBAS TaqMan HIV-1 test®, v. 2.0 (Roche) (CAP/CTM), y Real Time HIV-1 Assay® (Abbott). En el último año se introdujo en el país la prueba de PCR en tiempo real VERSANT HIV-1 RNA 1.0 Assay® (kPCR), la cual tiene características similares a las anteriores (8).
La prueba PCR en tiempo real Cobas Ampliprep Taqman HIV-1®, v. 2.0, posee, como nuevas características, la capacidad de cuantificar VIH-1 -además del grupo M (subtipos A-H)- el grupo O y detectar desde 20 copias/ml. La prueba PCR en tiempo real, Versant HIV-1 RNA 1.0® (kPCR) también detecta el VIH-1 grupo M (subtipos A-H) y O y el límite de detección es de 35 copias/ml. En la tabla 1 se presentan las características más representativas de ambas pruebas (7,8).
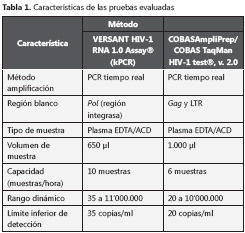
El objetivo de este estudio fue evaluar el desempeño del método kPCR, para la cuantificación de la carga viral en pacientes con VIH-1, en comparación con el método CAP/CTM; se hizo para busca aportar información sobre la eficiencia del método para el seguimiento de los pacientes con VIH-1/sida, con el propósito de evaluar el nuevo método kPCR en las condiciones específicas del laboratorio, que permita sacar conclusiones sobre la conmutabilidad de las dos pruebas, de modo que el nuevo método pueda ser intercambiado sin perder el poder diagnóstico.
Materiales y métodos
Se hizo una evaluación de prueba diagnóstica para cuantificación de carga viral VIH-1. Se incluyeron 60 pacientes del programa de control VIH/sida remitidos por el médico tratante para cuantificación de VIH-1. El número de muestras se estableció siguiendo las recomendaciones de la American Society for Microbiology (ASM) para la comparación de métodos de biología molecular, para pruebas aprobadas por la Food and Drug Administration (FDA) (9).
Las muestras utilizadas para la evaluación de las pruebas se obtuvieron de pacientes que habían sido remitidos por el médico tratante en el periodo comprendido entre agosto de 2010 y marzo de 2011, como parte de su control de rutina. Se siguieron las normas estrictas de bioseguridad en los procedimientos de toma de muestras y, de acuerdo con las directrices de la Resolución 8430 de 1993 del Ministerio de Salud, el estudio fue considerado sin riesgo, puesto que la prueba adicional para la técnica de comparación se hizo en la muestra de sangre ordenada por el médico tratante para el seguimiento del paciente. El proyecto fue aprobado por el Comité de Ética del laboratorio médico donde se llevó a cabo el estudio, y se garantizó la confidencialidad de la información.
Las muestras se tomaron en dos tubos con EDTA, se separó el plasma en la primera hora y se congeló a -20 °C hasta el momento del procesamiento. Las muestras se procesaron en la Sección de Biología Molecular del Laboratorio Médico Echavarría y se obtuvo la cuantificación del ARN del VIH-1 con la técnicas COBAS AmpliPrep/ COBAS TaqMan HIV-1 test®, v. 2.0 (CAP/ CTM) (Roche Molecular System, Inc., Branchburg, NJ, USA). y con VERSANT HIV-1 RNA 1.0 Assay (kPCR)® (Siemens Healthcare Diagnostics Inc., Deerfield, IL USA). El montaje de las muestras se hizo según recomendaciones del fabricante, tanto para el método kPCR como para CAP/CTM. Se registraron los datos de los resultados de ambas pruebas de todos los pacientes incluidos en el estudio, en número de copias/ ml y su conversión logarítmica (log10). El nuevo método (kPCR), se comparó con el método CAP/ CTM, utilizado de rutina en el laboratorio.
El análisis de los datos se hizo en SPSS® y EPIDATA ®. Se calcularon medidas de estadística descriptiva, como distribución de frecuencias, promedios y desviación estándar, para los resultados de las pruebas de carga viral, luego de su conversión en log10 en número de copias/ml. Para el análisis de los datos se tuvo en cuenta la recomendación de la American Society for Microbiology para la validación de pruebas diagnósticas de biología molecular para enfermedades infecciosas (9). Se elaboró un diagrama de dispersión y análisis de regresión para explorar la relación entre los dos métodos evaluados, se obtuvo la correlación entre ambas técnicas y se calculó el coeficiente de correlación y concordancia de Lin.
Para la evaluación de la concordancia, se obtuvieron las diferencias entre los resultados de los dos métodos en log10 del número de copias/ml para cada caso, así como el promedio de las diferencias y su desviación estándar, con lo cual se hizo el análisis de concordancia mediante el método de Bland-Altman.
Se obtuvo la distribución de frecuencias para los dos métodos según rango de concentración y se calculó el índice kappa ponderado (pesos cuadráticos). Los rangos incluidos fueron: <40, 41- 200, 201-400, 401-1.000, 1.001-10.000, 10.001- 100.000 y >100.000 copias/ml), los cuales corresponden a los utilizados por el laboratorio en estudios similares, y se incluyeron niveles de decisión clínicamente importantes.
Resultados
El valor promedio de las mediciones de la carga viral en las 60 muestras examinadas fue 3,2±1,4 log10 copias/ml, por el método CAP/CTM, y 3,0±1,3 log10 copias/ml, por el método kPCR. En la distribución de los resultados de las mediciones de la carga viral, se encontró que en 35 % de las muestras fue menor a 200 copias/ml por el método CAP/CTM, mientras que en 46,6 % de ellas estuvo en este rango por la kPCR; asimismo, se encontró que 50 % de las muestras estuvieron en rangos de concentración mayores a 1.000 copias/ml en el método CAP/CTM, en tanto que 43,3 % estuvo en este rango por el método kPCR. La distribución de frecuencias de la carga viral por rangos de concentración para los dos métodos en copias/ml y su conversión logarítmica se resume en la tabla 2.

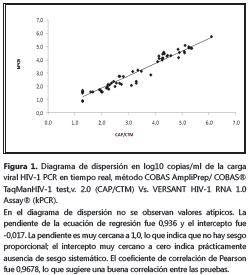
La figura 1 presenta el diagrama de dispersión de los resultados de carga viral para cada paciente, por las dos técnicas evaluadas. En el análisis de regresión entre los dos métodos se obtuvo una pendiente de 0,936 y una intercección de -0,017. El análisis de correlación arrojó un coeficiente de Pearson (ρ) de 0,968 (IC95% 0,950-0,982). El coeficiente de correlación y concordancia de Lin (Pc) fue de 0,957 (IC95% 0,934-0,976), con un factor de corrección de sesgo de 0,989.
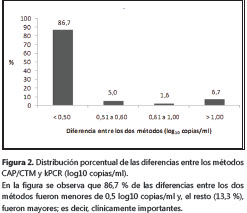
El 86,7 % de las muestras presentó diferencias entre los métodos CAP/CTM y kPCR, menores de 0,5 long10 copias/ml, y el 13,3 % presentó diferencias mayores, que son las consideradas clínicamente importantes. La figura 2 indica la distribución porcentual según las diferencias de carga viral en log10, entre ambas técnicas.
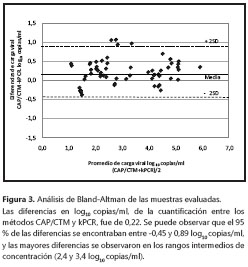
El gráfico de Bland-Altman permitió observar la diferencia entre las mediciones. La media de las diferencias fue de 0,22±0,33 long10 copias/ml. El 95 % de ellas se encontraba entre -0,45 y 0,89 long10 copias/ml (figura 3).
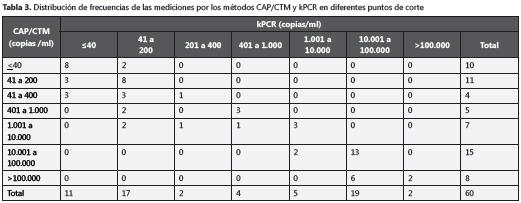
En el análisis de concordancia entre las dos técnicas, en los puntos de corte de <40, 41-200, 201-400, 401-1.000, 1.001-10.000, 10.001-100.000 y >100.000 copias/ml, se encontró un índice kappa ponderado de 0,91 (IC95% 0,86-0,96). En la tabla 3 se presenta la distribución de las mediciones para ambos métodos en los diferentes puntos de corte.
Discusión
Los nuevos métodos de PCR en tiempo real superan a las tecnologías de punto final, por su mayor exactitud y capacidad de cuantificar en un rango de concentración más amplio. Por tal razón, se consideran de elección en la evaluación inicial y en el control de pacientes de programas de VIH/sida. Se caracterizan por su gran sensibilidad, reducción del riesgo de contaminación y automatización de todas las etapas del proceso (6,10). Este tipo de pruebas, disponible en Colombia desde hace varios años, se utiliza de rutina en laboratorios de referencia.
En la búsqueda de pruebas diagnósticas más sensibles y confiables, se han introducido modificaciones a métodos ya existentes, como CAP/CTM, v. 2.0 (11), cuyo sistema de amplificación de múltiples blancos puede detectar desde 20 copias/ml. También, se han introducido otros nuevos como kPCR, que detecta desde 35 copias/ml y tiene gran capacidad para cuantificar subtipos, incluso aquellos del grupo O y formas circulantes recombinantes (12).
A pesar de los avances en los métodos diagnósticos para cuantificación de carga viral, en la práctica clínica se reconoce que los valores de carga viral en los rangos de concentración bajos, incluso cuando se comparan con otros basados en PCR en tiempo real, pueden presentar discrepancias (13-16).
Debido a la variabilidad en los resultados de las pruebas y a la posible presentación de incrementos transitorios e inesperados de carga viral en los pacientes (blips), en las últimas guías para el uso de agentes antirretrovirales en adultos y adolescentes infectados con VIH-1, se definió como falla virológica al resultado confirmado de carga viral mayor de 200 copias/ml, con el fin de controlar modificaciones innecesarias de tratamiento (6). No obstante, las diferencias entre métodos también se pueden observar en rangos intermedios y altos de carga viral, fenómeno menos explorado en los diferentes estudios. En esta comparación de métodos se observaron discrepancias importantes en los rangos intermedios de concentración (2,4 y 3,4 long10 copias/ml).
En el presente estudio, al comparar los resultados de la cuantificación de carga viral por ambos métodos, no se observaron valores atípicos en el diagrama de dispersión. La pendiente de la ecuación fue 0,936 y la intersección fue de -0,017. La pendiente es muy cercana a 1,0, lo cual indica que no hay sesgo proporcional; la intersección muy cercana a cero indica prácticamente ausencia de sesgo sistemático. El coeficiente de correlación de Pearson fue de 0,967, lo cual sugiere una buena correlación entre las pruebas y gran precisión; sin embargo, este hallazgo por sí solo no indica que las dos técnicas puedan ser intercambiables, para lo cual es necesario evaluar, además, la exactitud mediante el coeficiente de correlación y concordancia de Lin (9). El resultado del Pc de 0,957 (IC95% 0,934-0,976), con un factor de corrección de sesgo de 0,989 indica buena exactitud.
Una alta proporción (86,7 %) de resultados presentó diferencias menores de 0,5 long10 copias/ml, diferencia aceptada dentro del intervalo de tolerancia clínica (5,6). No obstante, se encontraron diferencias superiores a 0,5 long10 copias/ml en 13,3 % de los casos. Este hallazgo es bajo en comparación con las técnicas de punto final, en las cuales se han reportado diferencias de 36,4 % con Nuclisens Vs. kPCR, y de 35,3 % con bDNA Vs. kPCR. La mayoría de las discrepancias con este tipo de pruebas se describieron para el rango bajo (51 a 200 copias/ml) (17).
En cuanto a los métodos en tiempo real, Wagner, et al. reportaron discrepancias de 23,3 % al comparar kPCR con la versión anterior de CAP/CTM (v.1.5) (18). La comparación de kPCR con el método PCR en tiempo real de Abbott, no presentó discrepancias en el mismo estudio. Por otro lado, la comparación de CAP/CTM v1.5 con el método PCR en tiempo real de Abbott, ha mostrado discrepancias de 8,3 % al evaluar resultados con concentraciones menores de 200 copias/ml (19).
En el análisis de concordancia entre las dos técnicas con puntos de corte de <40, 41-200, 201-400, 401-1.000, 1.001-10.000, 10.001-100.000 y >100.000 copias/ml, se encontró un índice kappa ponderado de 0,91 (IC95% 0,87-0,96), lo que indica una buena concordancia. A pesar del bajo número de casos al distribuir los diferentes rangos de concentración, se observan más discrepancias en los rangos de concentración intermedios.
La mayoría de los estudios se han enfocado en las diferencias de métodos en los rangos bajos de concentración y en el límite inferior de detección; sin embargo, se han descrito discrepancias en los rangos altos de concentración (3,4 a 5,7 long10 copias/ml) al comparar CAP/CTM, v. 2.0, Vs. el método estándar Cobas Amplicor® (Roche), e incluso, reportaron diferencias superiores a 1,72 long10 copias/ml (20). En el presente estudio se observó una tendencia análoga en el rango intermedio (2,4 a 3,4 long10copias/ml); este hecho puede estar relacionado con la linealidad similar en ambos métodos, puesto que, al ser metodologías en tiempo real, desde el punto de vista teórico, se esperarían diferencias menores en los valores extremos.
Se sugiere la realización de estudios orientados a la comparación, en los rangos intermedios y altos de concentración, entre los métodos en tiempo real disponibles en Colombia, que aporten información útil para la toma de decisiones en pacientes que aún no inician tratamiento antirretroviral, considerando el impacto en costos que tendría para el sistema de salud, un resultado falsamente elevado.
Por último, aunque el establecer las causas de las diferencias entre los resultados de métodos diferentes no fue el objetivo del presente estudio, sí es importante mencionar algunos de los factores descritos en la literatura científica para explicar las discrepancias, entre los que se cuentan: la diversidad genética del VIH-1, las diferencias en el blanco utilizado, los efectos de la inhibición de la amplificación y la degradación de ARN, entre otros (7,8,19).
Se concluye que los dos métodos evaluados pueden ser intercambiables y, en consecuencia, la kPCR puede ser adecuada para el control de los pacientes VIH/sida remitidos al laboratorio, lo que se corroboró con el análisis de las diferencias entre las dos técnicas por el método de Bland-Altman (9,21). Se observaron resultados más bajos con kPCR y las diferencias observadas se identificaron en el rango intermedio de concentración.
En conclusión, a pesar de la alta concordancia entre las pruebas CAP/CTM y kPCR, hubo una tendencia a la cuantificación de valores más bajos de carga viral con el método kPCR. Asimismo, el método automatizado de kPCR es intercambiable con el método CAP/CTM en el seguimiento y control de pacientes VIH/sida.
Agradecimientos
Los autores agradecen a la empresa Siemens Health Care, por la donación de una parte de los reactivos para realizar el estudio.
Correspondencia: María Isabel Múnera-Jaramillo, Laboratorio Médico Echavarría, Carrera 43F N° 14-69, Medellín, Colombia. Teléfonos: (054) 311-4343 y (320) 6950-637. Dirección electrónica: mmunera@labechavarria.com, mmunera173@gmail.com
Referencias
1. Ministerio de la Protección Social. Carga de la enfermedad, Colombia 2005: resultados alcanzados. Documento técnico ass/1502-08. Bogotá, 2008. Fecha de consulta: 10 de junio de 2011. Disponible en: http://www.cendex.org.co/GPES/informes/PresentacionCarga_Informe.pdf. [ Links ]
2. Ministerio de la Protección Social, ONUSIDA. Plan Nacional de Respuesta al VIH y SIDA 2008-2011. Fecha de consulta: 10 de junio de 2011. Disponible en: http://www.unfpacolombia.org/home/unfpacol/public_htmlfile/plan_vihsida2008.pdf. [ Links ]
3. Nolte FS, Hill CE. Polymerase Chain Reaction and Other Nucleic acid Amplification Technology. In: McPherson RA, Pincus MR. Henry´s Clinical Diagnosis and Management by Laboratory Methods. 21 Ed. 2007 Saunders Elsevier Philadelphia. p. 1239-1249. [ Links ]
4. SterlingTR, Chaisson RE. Manifestaciones generales de la infección por el VIH. En: Mandell GL, Bennett JE y Dolin R. Enfermedades Infecciosas Principios y Práctica. 6ª. Edición, 2006. Elsevier Madrid, España, S.A. p.1547-1566. [ Links ]
5. Fundación para la investigación y desarrollo de la salud y la seguridad social (FEDESALUD) y Asociación Colombiana de Infectología (ACIN). Guía y modelo de atención del VIH/SIDA. Bogotá: Editorial Scripto Ltda.; 2006. [ Links ]
6. Panel on antiretroviral guidelines for adults and adolescents. Guidelines for the use of antiretroviral agents in HIV-1-infected adults and adolescents. Department of Health and Human Services. October 14, 2011; 1-174. Disponible: http://www.aidsinfo.nih.gov/ContentFiles/adultandadolescentGL.pdf.Consultado: 20 de febrero de 2012. [ Links ]
7. Wang S, Xu F, Demirci U. Advances in developing HIV-1 viral load assays for resource-limited settings. Biotecnology Advances. 2010;28:770-81. [ Links ]
8. González-Alba JM, Rodríguez-Domínguez M, Mateos-Lindemann ML. Determinación de la carga viral de VIH-1. Enferm Infecc Microbiol Clin 2011:29(Supl 3):47-50. [ Links ]
9. Burd E. Validation of laboratory developed molecular assays for infectious diseases. Clin Microbiol Rev. 2010;23:570-6. [ Links ]
10. Schumacher W, Frick E, Kauselmann M, Maier-Hoyle V, van der Vliet R, Babiel R. Fully automated quantitation of human immunodeficiency virus (HIV) type 1 RNA in human plasma by the COBAS AmpliPrep COBAS TaqMan system. J Clin Virol. 2007;38:304-12. [ Links ]
11. Paba P, Fabeni L, Ciccozzi M, Perno C, Ciotti M. Performance evaluation of the COBAS/TagMan HIV-1 v2.0 in HIV-1 positive patients with low viral load: A comparative study. J Virol Methods. 2011;173:399-402. [ Links ]
12. Ruelle J, Jnaoui K, Lefèvre I, Lamarti N, Goubau P. Performances and comparative evaluation of the automated VERSANT HIV-1 RNA 1.0 kinetic PCR molecular system (kPCR) for the quantitation of HIV-1 plasma viral load. J Clin Virol. 2008;44(Suppl.1)S17-32. [ Links ]
13. Wolff D, Gerritzen A. Comparison of the Roche COBAS Amplicor Monitor, Roche COBAS Ampliprep/COBAS TaqMan and Abbott Real Time assays for quantitation of hepatitis C virus and HIV RNA. Clin Chem Lab Med. 2008;46:917-22. [ Links ]
14. Gomes P, Palma AC, Cabanas J, Abecasis A, Carvalho AP, Ziermann R, et al. Comparison of the COBAS TAQMAN HIV-1 HPS with VERSANT(TM) 440 HIV-1 RNA 3.0 assay (bDNA) for plasma RNA quantitation in different HIV-1 subtypes. J Virol Methods. 2006;135:223-8. [ Links ]
15. Lohse N, Kronborg G, Gerstoft J, Larsen CS, Pedersen G, Pedersen C, et al. Virological control during the first 6-18 months after initiating highly active antiretroviral therapy as a predictor for outcome in HIV-infected patients: A Danish, population-based, 6-year followup study. HIV/AIDS. Clin Infect Dis. 2006;42:136-44. [ Links ]
16. Braun P, Ehret R, Wiesmann F, Frauke Z, Knickmann M, Ku R, et al. Comparison of four commercial quantitative HIV-1 assays for viral load monitoring in clinical daily routine. Clin Chem Lab Med. 2007;45:93-9. [ Links ]
17. Ruelle J, Jnaoui K, Lefèvre I, Lamarti N, Goubau P. Comparative evaluation of the VERSANT(TM) 440 ® HIV-1 RNA 1.0 kinetic PCR molecular system (kPCR) for the quantitation of HIV-1 plasma viral load. J Clin Virol. 2009;44:297-301. [ Links ]
18. Wagner C, Fleury H, Lin C, Canchola J, Despres N, Swiatkowski P, et al. Method comparison between the VERSANTÒ HIV-1 RNA 1.0 Assay (kPCR) and COBASÒ AmpliPrep/COBASÒ TaqManÒ HIV-1 test: 15th Annual International Symposium on HIV and Emerging Infectious Diseases (ISHEID). 28-30 May, 2008, Toulon, France. [ Links ]
19. Yan CS, Hanafia I, Kelleher AD, Carr AD, Amin J, McNallya LP, et al. Lack of correlation between three commercial platforms for the evaluation of human immunodeficiency virus type 1 (HIV-1) viral load at the clinically critical lower limit of quantification. J ClinVirol. 2010;49:249-53. [ Links ]
20. Letter to the Editor Increased frequency of viral loads above 10000 HIV-1 RNA copies/ml measured by Roche Cobas TaqMan assay in comparison with Cobas Amplicor assay J Clin Virol 48 (2010) 75-76. [ Links ]
21. Bland JM, Altman DG. Statistical methods for assessing agreement between two methods of clinical measurement. Lancet. 1986;i:307-10. [ Links ]














