Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Infectio
Print version ISSN 0123-9392
Infect. vol.17 no.1 Bogotá Jan./Mar. 2013
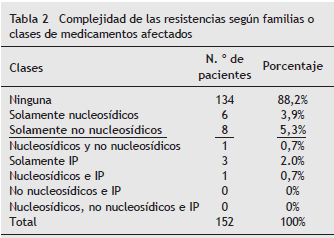
ORIGINAL Resistencia transmitida del virus de la inmunodeficiencia humana en pacientes sin exposición previa a tratamiento antirretroviral, Cali, Colombia, 2010 Pablo Galindo-Orregoa,b,*, Héctor F. Mueses-Marín a, Jaime Galindo-Quintero ay Jorge L. Martínez-Cajas a,c a Grupo de Investigación Educación y Salud en VIH/SIDA de la Corporación de Lucha Contra el Sida, Cali, Colombia b Residente Medicina Interna, Universidad de la Sabana, Bogotá, Colombia c Profesor asistente de Medicina, División de Enfermedades Infecciosas, Queen´s University, Kingston, ON, Canadá Recibido el 15 de junio de 2012; aceptado el 3 de julio de 2013 Resumen Introducción: En Colombia, existe poca información publicada sobre farmacorresistencia transmitida en el virus de inmunodeficiencia humana (VIH), y actualmente, las pruebas genotípicas de resistencia no son recomendadas por las guías colombianas para pacientes nunca expuestos ( naïve ) a terapia antirretroviral (TAR). Se condujo un estudio para determinar la frecuencia de resistencias transmitidas en pacientes naïve a TAR, quienes fueron atendidos en una clínica especializada en VIH/síndrome de inmunodeficiencia adquirida en Cali, Colombia. Metodología: Se realizó un estudio transversal en 152 pacientes adultos elegibles, con infección confirmada por VIH, naïve a TAR, con pruebas genotípicas de resistencia disponibles, y que accedieron a participar. El período de reclutamiento fue de 2008 a 2010. Las mutaciones de resistencias incluidas en el análisis fueron las definidas por la Organización Mundial de la Salud 2009 e International AIDS Society-USA 2010. Adicionalmente, se recolectó información sociodemográfica y condiciones relacionadas con el VIH. Resultados: La edad promedio fue 32 ± 10,2 años, 76% fueron hombres. La frecuencia de resistencia primaria fue de 6,6% (según la lista de Bennett-Organización Mundial de la Salud 2009), pero se encontró algún nivel de resistencia hasta en un 11,8% de los casos (al considerar mutaciones de la lista International AIDS Society-USA 2010). Las mutaciones más comunes fueron K103N/S (2%), F77L (2%) y M46L (2%). Mutaciones a los inhibidores no nucleosídicos de transcriptasa reversa fueron encontradas en 5,3%, mutaciones a los inhibidores no nucleosídicos de transcriptasa reversa en 3,9% y mutaciones a inhibidor de proteasa en 2% de las secuencias. El único factor relacionado con la resistencia primaria fue la duración de la infección por VIH. Conclusiones: La frecuencia de resistencia transmitida es similar a la encontrada en estudios previos en Colombia y en otros países con amplio uso de antirretrovirales, y está por encima del umbral sobre el cual sería costo-efectivo incluir el estudio genotípico de resistencias como test de rutina antes de la iniciación de la TAR, especialmente en pacientes con infección por VIH de menos de un año de duración. © 2013 ACIN. Publicado por Elsevier España, S.L. Todos los derechos reservados. PALABRAS CLAVE VIH; Resistencia; Mutación; Genotipificación; Colombia Transmitted HIV Resistance in ART-Naïve Patients in Cali, Colombia, 2010 Abstract Introduction: In Colombia, little has been published on HIV-transmitted drug resistance, and genotype resistance testing (GART) is not recommended for antiretroviral therapy (ART)-Naïve patients, according to Colombian HIV guidelines. We conducted a study to determine the frequency of HIV-transmitted drug resistance from a sample of ART-Naïve patients attending an HIV clinic in Cali, Colombia. Methodology: A cross-sectional study was carried out on 152 eligible adult patients with confirmed HIV infection who were ART-Naïve, had HIV GART results, and who agreed to participate. The recruitment period was from 2008 to 2010. Resistance mutations included in the analysis are those defined by the WHO- 2009 and IAS-USA, 2010. Additional data was collected, including socio-demographic characteristics and HIV-related conditions. Results: The mean age was 32 ±10.2 years; 76% were men. Frequency of transmitted drug resistance was 6.6%, but some level of resistance was found in up to 11.8% of total cases (if IAS-USA 2010 mutations were also included). The most common mutations were K103N/S (2%), F77L (2%) and M46L (2%). NNRTI mutations were found in 5.3%, NRTI mutations in 3.9% and PI mutations in 2% of the sequences. The only factor associated with primary resistance was the duration of HIV infection. © 2013 ACIN. Published by Elsevier España, S.L. All rights reserved. KEYWORDS: HIV; Resistance; Mutation; Genotyping; Colombia Introducción A la fecha, el virus de la inmunodeficiencia humana (VIH-1) ha infectado a 33 millones de personas en todo el mundo 1. En Colombia, la prevalencia de infección por el VIH se estima en alrededor del 0,6%, afectando aproximadamente a 170.000 personas 2. La introducción de las drogas antirretrovirales (ARV) ha influido en el declive de la morbilidad y la mortalidad debidas al VIH/síndrome de inmunodeficiencia adquirida (SIDA) 3 , y la infección por VIH se ha convertido en una enfermedad crónica que necesita terapia/tratamiento antirretroviral (TAR) supresor de por vida. A pesar de esto, el VIH es capaz de adquirir resistencia a cualquiera de los ARV y esto puede afectar negativamente a la respuesta al tratamiento. Asimismo, los virus resistentes a los fármacos también pueden transmitirse de persona a persona 4,5. En el ámbito mundial, la resistencia del VIH a los medicamentos se considera un problema creciente y en este sentido la Organización Mundial de la Salud (OMS) recomienda la vigilancia de la farmacorresistencia del VIH como un componente de los programas de TAR 6. Las pruebas de detección de resistencia a los ARV se usan actualmente para asistir en la selección de la TAR. Estas pruebas ofrecen los beneficios clínicos de aumentar la probabilidad de supresión viral máxima y así reducir la morbilidad de los pacientes tratados para la infección crónica por VIH. Es así como, en la actualidad, la mayoría de las guías para el uso de ARV en Norteamérica y Europa recomiendan el uso de las pruebas de resistencia antes de iniciar TAR 4,7,8. Los factores más importantes que facilitan la aparición y acumulación de mutaciones del VIH a los ARV son las características biológicas propias del VIH sumadas principalmente a la supresión viral parcial e incompleta por adherencia subóptima a la TAR en algunos pacientes. Diferentes estudios sugieren que el riesgo de que se transmita un virus resistente al menos a un medicamento ARV oscila en el rango de entre 7 y 21%, con un 3 a 5% de riesgo de transmisión de resistencias a más de una clase de medicamentos 9,10. En este mismo aspecto, un estudio reciente estimó que la prevalencia de resistencias transmitidas por zonas del mundo oscila entre 4 y 13% (América del Norte 12,9%, Europa 10,9%, América Latina 6,3%, África 4,7% y Asia 4,2%) 11. En Colombia, un estudio transversal en pacientes naïve reportó 5,8% de mutaciones de resistencia, siendo más comunes la K103N (4,9%) y la M184V (2,9%), y notó que un conteo de linfocitos T CD4 < 200 células/mm 3 y estado clínico C (según la clasificación de los centros para el control y la prevención de enfermedades de 1993) se asociaron con la resistencia primaria 12. En Colombia, sin embargo, no se ha encontrado evidencia de otros estudios que describan una caracterización sociodemográfica y clínica en este tipo de población. En Colombia, el uso de drogas ARV antes de 1996 es difícil de definir pues no hay datos oficiales a ese respecto. En 1997, el sistema de seguridad social de medicamentos incluyó la zidovudina, la lamivudina, el indinavir y el ritonavir en la lista de medicamentos para el tratamiento de la infección por VIH. En 2002, se introdujeron el abacavir, el efavirenz y el lopinavir/ritonavir. En 2004, siguieron el saquinavir, el fosamprenavir y el atazanavir 13. Más tarde, en 2011, se introdujo el tenofovir dentro del Plan Obligatorio de Salud. Otros ARV han estado disponibles en Colombia, como por ejemplo el raltegravir, el maraviroc y la etravirina, pero su uso está altamente restringido, ya que estos no están cubiertos por el Plan Obligatorio de Salud. Para el año 2011, el ONUSIDA reportó para Colombia una cobertura de tratamiento de entre 35 y 50% para personas con infección VIH con conteo de células T-CD4 < 350. En Colombia hay pocos datos de patrones de uso de ARV e históricamente el esquema de tratamiento inicial más utilizado en los últimos 20 años fue la combinación de lamivudina/ zidovudina, la cual se asoció en los primeros años con un inhibidor de proteasa (IP), que usualmente fue indinavir o ritonavir 13,14. Posteriormente, y debido a sus frecuentes efectos colaterales, estos IP fueron gradualmente reemplazados por un inhibidor no nucleosídico de transcriptasa reversa NNRTI, en inglés Non-nucleoside reverse transcriptase inhibitors ), usualmente nevirapina o efavirenz, por un inhibidor nucleosídico de transcriptasa reversa (NRTI, en inglés Nucleoside Reverse Transcriptase Inhibitor ) (abacavir) o por otros IP mejor tolerados como nelfinavir o lopinavir/ritonavir, todos ellos casi invariablemente acompañando la combinación lamivudina/zidovudina 14,15. En la Corporación de Lucha ocontra el Sida (CLS), Cali, el 77% de pacientes toman una combinación de 2 NRTI más 1 NNRTI, y un 19% de pacientes toman 2 NRTI más 1 IP potenciado con ritonavir. Muy pocos pacientes toman otras combinaciones de medicamentos que incluyen inhibidores de entrada viral, NNRTI de segunda generación o inhibidores de integrasa (datos de CLS no publicados). No se conocen otros estudios locales en Cali sobre el acceso a TAR en los pacientes con infección por VIH. Las guías colombianas de manejo de pacientes VIH/SIDA recomiendan pruebas genotípicas de resistencia (PGR) únicamente en pacientes con más de una falla terapéutica a los ARV. Por otro lado, el alto costo del estudio genotípico en un país de recursos intermedios como Colombia hace necesaria la generación de mejor y más actualizada evidencia para establecer la necesidad y pertinencia de dichas pruebas previas a la iniciación de la primera combinación de ARV. Esto ayudaría a actualizar las recomendaciones sobre el uso de estudios genotípicos de resistencia en pacientes no expuestos a ARV que viven con VIH/SIDA en países con recursos como el nuestro. Por ende, este estudio pretendió determinar la frecuencia e la farmacorresistencia transmitida en una muestra de pacientes sin exposición previa ( naïve) a TAR, y obtener la identificación de posibles factores asociados a la presencia de dichas resistencias. Métodos Criterios de inclusión y recolección de datos Se llevó a cabo un estudio descriptivo de corte transversal que incluyó a todos los pacientes adultos mayores de 18 años con infección confirmada por el VIH (resultado reactivo por serología tipo inmuno-ensayo enzimático de tercera generación y test Western Blot confirmatorio), naïve a TAR, con PGR previo al inicio de la TAR, consentimiento informado de uso anónimo de los datos de la historia clínica y que se encontraban en el programa de atención integral de la CLS, en Cali, Colombia, entre los años 2008 y 2010. La población objeto de estudio corresponde a personas con VIH/SIDA, procedentes de Cali y de otros municipios del Valle del Cauca, no expuestos previamente a TAR, que son remitidos a la CLS para su ingreso a la atención integral especializada ambulatoria y TAR. La ausencia de exposición a medicamentos ARV se basó en indagación a los pacientes y verificación de historia de exposición previa a medicamentos con las instituciones referentes. Se excluyeron pacientes con información relevante incompleta o sin información del estudio genotípico de resistencia, así como pacientes con estudios genotípicos cuyo resultado fue no tipificable o incompletamente tipificable para la determinación de mutaciones de resistencia relevantes. La muestra inicial fue de 156 pacientes elegibles, de los cuales 4 fueron excluidos por pobre calidad de las secuencias (genotipos no tipificables o con tipificación incompleta). La información relacionada con las características generales sociodemográficas y marcadores clínicos relacionados con el VIH se obtuvo de los datos registrados en las historias clínicas de los pacientes y se ingresaron en un formato de recolección de datos. Pruebas genotípicas de resistencia Las muestras de sangre para el estudio genotípico fueron tomadas por el laboratorio clínico de la Cruz Roja Colombiana Seccional Valle en el punto de toma de muestras de la CLS, bajo los mismos estándares para todas las muestras; una vez preparadas, dichas muestras se remitieron para su secuenciación y obtención de resultados al laboratorio central de referencia de la CLS, el cual usa alternativamente los sistemas TRUGENE ® HIV-1 y ViroSeq TM HIV-1 para las PGR a los ARV por secuenciación de ácidos nucléicos de los genes de la transcriptasa reversa (TR) y la proteasa (PR) del VIH-1. Para la genotipificación, el paciente debió tener carga viral detectable y superior a 1.000 copias/mL en el momento del examen. La carga viral fue medida por ensayo PCR en tiempo real de la transcriptasa inversa. Tanto las PGR como la carga viral se efectuaron en el laboratorio central de referencia de la CLS, el Centro de Análisis Molecular, Bogotá, Colombia. Análisis de las mutaciones de resistencia Las mutaciones asociadas a resistencia a los ARV se definieron de acuerdo con la clasificación de la OMS 2009 16 , y la IAS-USA 2010 17. Para determinar la presencia de resistencia y su complejidad, se aplicó el algoritmo de HIVdb Stanford y se consideraron como afectados todos aquellos medicamentos que presentaran desde cualquier nivel de reducción de la susceptibilidad del virus (correspondiente a 10 o más puntos totales según el algoritmo de Stanford, desde "potencial bajo nivel de resistencia"). El tamaño final de la muestra fue de 152 pacientes, para el cual, asumiendo una frecuencia esperada de resistencias mínima del 6% (basado en estudio previo en Colombia 12) y a un nivel de confianza del 95%, se estimó un margen de error del 3,8%. La base de datos y los análisis estadísticos se llevaron a cabo en STATA, versión 9. Para describir las características generales de los participantes, así como frecuencias de mutaciones y resistencias, se generaron tablas de frecuencias. Posteriormente, la variable dependiente del estudio (presencia de mutaciones que confieren resistencias) se relacionó mediante análisis bivariado con las características generales sociodemográficas, antecedentes y marcadores clínicos relacionados con el VIH, para lo cual se usaron tablas de contingencia y test chi-cuadrado o corrección exacta de Fisher según fuera el caso. Revisión por comité de ética El presente estudio fue aprobado por el Comité de Ética para Investigación en Humanos de la CLS. Un consentimiento informado escrito de uso anónimo de datos de la historia clínica fue requerido para el ingreso de los participantes en el estudio. Resultados Características de los pacientes incluidos Sociodemográficas Edad promedio en el momento del estudio genotípico 32 ± 10,2 años (rango 18-67 años). La mayoría, hombres (76%). Más de la mitad residían en Cali (61%), la mayoría (52%) en estratos socioeconómicos bajos (0, 1 y 2) y medio (3) (28%), principalmente eran mestizos (82%), y gran parte habían completado estudios de secundaria o superiores (81%). El 68% no convivían en pareja (solteros [55%], separados o viudos [13%]), y el 32% convivían en pareja (casados, unión libre). El 67% con algún tipo de empleo, y principalmente estaban afiliados al régimen contributivo del sistema de aseguramiento en salud (86%). Hábitos Un poco más de la mitad (54%) reportaron haber tenido algún consumo de licor en el año anterior en el momento del genotipo, una cuarta parte consumían cigarrillos, y un 9% reportaron consumo de sustancias psicoactivas. Comportamientos sexuales En cuanto al uso del condón, el 18,5% reportó que lo usaban siempre; el 49% eran hombres que tienen sexo con hombres, y el resto eran mujeres (24%) u hombres heterosexuales (27%). Antecedentes patológicos El 40% presentó antecedentes de otras enfermedades de transmisión sexual diferentes al VIH. El 35% de los pacientes manifestó que su pareja actual era VIH+ y de estos el 51% reportó que su pareja estaba en tratamiento, principalmente con esquemas de primera línea (2 NRTI + 1 NNRTI). El 13% reportó hospitalizaciones relacionadas con el VIH, previas al momento de ingreso en el programa institucional de la CLS, y el 24% se encontraban con enfermedad avanzada al diagnóstico de la infección por VIH. Un 81% de los pacientes tenían menos de un año de diagnóstico de infección por VIH en el momento de hacerse la PGR, pero en el 61% del total se estimó un tiempo probable mayor de un año desde la infección retroviral aguda hasta el momento de hacerse la PGR. La mayoría (67%) iniciaron con una carga viral superior a 10.000 copias/mL tanto en el momento del diagnóstico de infección por VIH como en el de tomarse la PGR. Asimismo, alrededor del 80% tenían conteo de células CD4 > 200 células/mm 3 , tanto en el momento del diagnóstico como al hacerse la PGR; sin embargo, en cuanto a la razón CD4/CD8, gran parte (72%) se encontraba con valores < 0,5, pero cerca del 80% no habían presentado infección oportunista alguna relacionada con el VIH/SIDA. De esta población, en el 65% no se encontró antecedente o actividad actual de otras comorbilidades diferentes a las relacionadas con el VIH en el momento del examen genotípico. Mutaciones encontradas Tomando en cuenta exclusivamente la lista de mutaciones de la OMS 2009 16, se encontraron una o más de dichas mutaciones en 10 pacientes (6,6%; intervalo de confianza 95%; 2,6-10,6%), la mayor parte de las cuales afectó a la susceptibilidad del virus a los análogos no nucleosídicos inhibidores de la TR (tabla 1). Además, otros 8 pacientes adicionales (5,2%) portaban alguna de las siguientes mutaciones: Q58E, E44D, T69N, V108I, I62V, todas ellas consideradas mutaciones de resistencia por la lista de IAS-USA y en la Base de Datos de VIH de Stanford (Estados Unidos). Esto implica que el porcentaje de resistencia transmitida podría alcanzar hasta el 11,8%. Dentro de estas 18 personas, 7 pacientes presentaron 2 importantes mutaciones incluidas en la lista de IAS-USA 2010, pero no en la lista OMS 2009: V108I (4 pacientes) y V179D (3 pacientes), las cuales por sí solas afectaron a la susceptibilidad a los NNRTI. Estas 2 mutaciones no son consideradas polimorfismos según nuestra exploración de La base de datos de VIH de la Universidad de Stanford (más del 1% de frecuencia en genotipos salvajes de VIH subtipo B). Uno o más polimorfismos u otras mutaciones no consideradas relevantes para conferir por sí solas algún nivel de resistencia en pacientes naïve se observaron en 74 pacientes del estudio (48,7%), y la mayor frecuencia de las mismas se presentó en aquellas relacionadas con los IP y con los NRTI. Las más frecuentes fueron: V118I (23%) de los NRTI; L63P (10,5%), L10I (9,2%), A71T (9,2%), I62V (7,9%), I93L (7,9%) y V77I (7,2%) para los IP. Prevalencias de resistencias a antirretrovirales (según mutaciones encontradas y analizadas en base de datos de virus de inmunodeficiencia humana de Stanford) La frecuencia de algún nivel de resistencia del virus (potencial bajo/bajo/intermedio/alto) o ausencia de susceptibilidad total a uno o más medicamentos ARV fue 11,8% (18/152) en los pacientes del estudio (intervalo de confianza 95%; 6,6-17,0%) al incluir las mutaciones del IAS-USA 2010. Esto difiere del 6,6% de frecuencia de resistencia, que es lo que se estima si se usa solamente la lista según OMS 2009. La familia de medicamentos ARV que se encontró más frecuentemente afectada por algún nivel de resistencia del virus fue la correspondiente a los análogos no nucleosídicos inhibidores de la TR (NNRTI, 5,3%), seguida por los análogos nucleosídicos inhibidores de la misma transcriptasa (NRTI, 3,9%). La afectación de más de una familia de ARV fue mucho más baja (0-1,4%) (tabla 2).
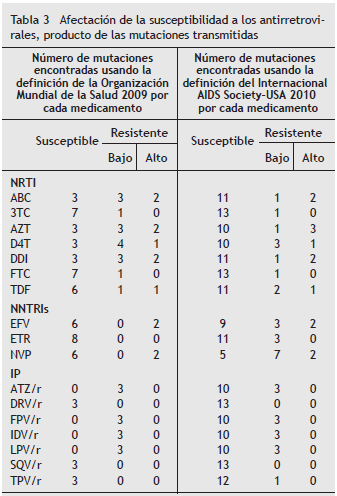
Los ARV, individualmente, se ven afectados de manera diferente. Los ARV más afectados por la resistencia transmitida son los NNRTI efavirenz y nevirapina, y los NRTI abacavir, zidovudina y didanosina, para los cuales hubo resistencia de alto nivel; estos, seguidos por los NRTI estavudina y tenofovir y los IP atazanavir, fosamprenavir, indinavir y lopinavir, solo afectados con bajo nivel de resistencia (tabla 3).
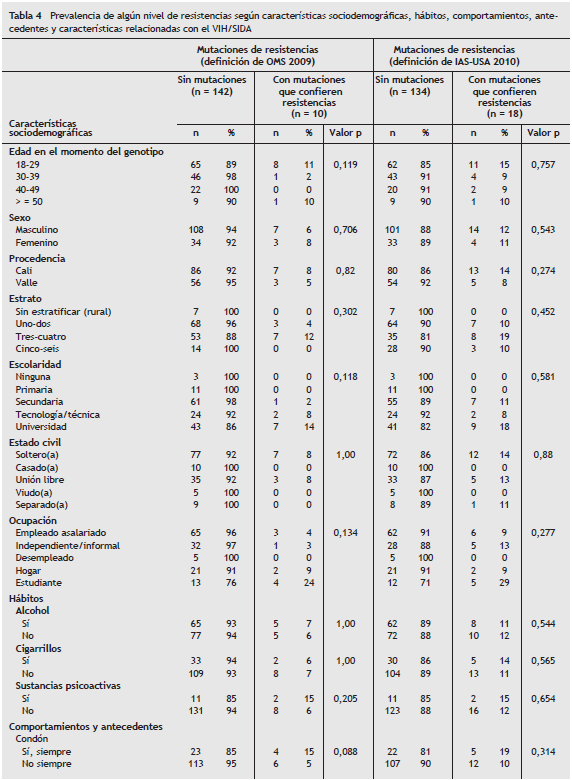
Prevalencia de mutaciones de resistencias a antirretrovirales según características sociodemográficas, hábitos, comportamientos, antecedentes y características relacionadas con el VIH/SIDA
En la tabla 4 se destaca la distribución de la prevalencia de algún nivel de resistencia según características sociodemográficas, hábitos, comportamientos, antecedentes y características relacionadas con el VIH/SIDA, encontrando diferencias significativas (p < 0,05) solamente con el tiempo probable desde la infección retroviral aguda hasta el momento de la realización de la PGR. En el mismo sentido, el análisis bivariado reveló una asociación cercana a la significancia estadística entre presencia de mutaciones de resistencia y una carga viral en el momento del genotipo de 1.000 a 10.000 copias.
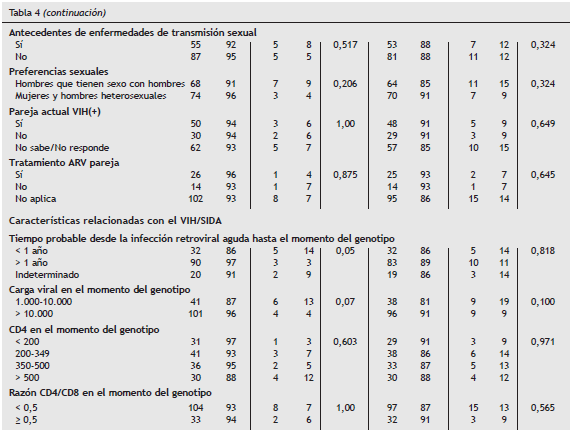
En nuestro estudio, dada la baja frecuencia absoluta de pacientes con mutaciones de resistencias (n = 10 o n = 18), no se logró correr un análisis multivariado debido al bajo poder estadístico para encontrar relaciones con la categoría presencia de mutaciones.
Discusión
El presente estudio se llevó a cabo en una población de pacientes VIH+ bajo atención integral especializada ambulatoria de la CLS en la ciudad de Cali, Colombia, en quienes no había historia previa de exposición alguna a ARV. Nuestros hallazgos tienen implicaciones respecto a la necesidad de realizar estudios genotípicos en pacientes naïve , a la necesidad de la vigilancia de resistencia del VIH a los ARV y a factores relacionados con la transmisión de VIH farmacorresistente en Colombia.
Los participantes del estudio, en su mayoría correspondieron a una población de adultos jóvenes, con gran predominio de hombres; principalmente diagnosticados de manera reciente, y en su mayoría sin complicaciones asociadas a enfermedad avanzada por el VIH. En general, y en cuanto a las características sociodemográficas, hábitos y antecedentes, esta población es similar al universo de personas infectadas por el VIH que acuden por primera vez a programas de atención integral como el de la CLS (comunicaciones institucionales internas).
Bennett et al. han definido una lista de mutaciones de resistencia en VIH que es, a la fecha, la mejor aproximación a las mutaciones de resistencia transmitida que se deben vigilar (lista OMS 2009) 16. Esta incluye 93 mutaciones de resistencia no polimórficas cuya frecuencia en virus salvajes es de 0,5% o menos. De esta manera, excluye mutaciones que ocurren de manera natural en virus de diferentes subtipos o mutaciones polimórficas que pueden acompañar a mutaciones no polimórficas inducidas por exposición a drogas ARV. Por ejemplo, los polimorfismos 36I y 93L de la proteasa viral que a pesar de aparecer en listas de mutaciones de resistencia preparadas por comités expertos (por ejemplo, IAS-USA, Base de Datos de VIH de Stanford), no son siempre inducidas por exposición a drogas, sino que son también frecuentes en virus salvajes de subtipos no B del VIH-1, y también acompañan con frecuencia a otras mutaciones mayores en virus expuestos a IP.
De acuerdo con la lista de mutaciones de la OMS 2009, se encontraron una o más de dichas mutaciones en 10 pacientes, la mayor parte de las cuales afectó a la susceptibilidad del virus a los análogos nucleosídicos inhibidores de la TR: la encontrada con más frecuencia fue la F77L, seguida por la M41L, la K70R, la L210W y la T215Y; de manera similar, llama la atención el hallazgo de mutaciones relacionadas con los NNRTI, la K103N en 2 pacientes y la K103S en 1 paciente, lo mismo que la relacionada con los IP M46L en 3 pacientes, todas las cuales también parecen haber perdurado en estos pacientes durante largos períodos de tiempo después de ocurrida su transmisión.
La consideración de otras mutaciones que por sí solas pueden conferir algún nivel de afectación de la susceptibilidad del virus a los ARV, aun cuando no pertenezcan a la lista de la OMS 2009 pero sí a la de IAS-USA 2010, también es importante. Al incluir todas aquellas que estando presentes pueden afectar a la efectividad de los medicamentos, se encontró que dentro del total de pacientes en 18/152 (11,8%) hubo mutaciones que ocurren casi exclusivamente después de exposición a ARV (no son polimorfismos). Por otra parte, estudios previos reconocen que la estimación de la resistencia transmitida varía de acuerdo con el set de mutaciones que se utilicen para definir las mutaciones de resistencia 16, lo que sugiere que la resistencia transmitida podría medirse dentro de un rango, en lugar de usarse un número absoluto con límites entre un parámetro más estricto y uno menos estricto, que es lo que hemos escogido hacer en nuestro estudio. Debe tenerse en cuenta que no es posible descartar completamente que otras mutaciones o polimorfismos infrecuentes en virus salvajes no sean inducidos por la presión de la TAR y que estos sean más propensos a ser transmitidos, resultando así en resistencia transmitida, pero que no se detectaría por definición usando la lista OMS 2009. Por ejemplo, el caso del polimorfismo 36I de la proteasa, que siendo infrecuente en el subtipo B salvaje (15%), se vuelve muy frecuente en el mismo subtipo B (34%) con mutaciones de resistencia a los IP y también, por otra parte, es un polimorfismo muy habitual en subtipos de VIH no B (Stanford HIV Database HIV Seq Program, consultado el 5 de marzo de 2013). De este modo, la lista de la OMS 2009 podría estar subestimando la transmisión de mutaciones secundarias y polimorfismos que favorecen la resistencia aun cuando estas pudiesen estar inicialmente inducidas por la TAR en los sujetos transmisores. Sin embargo, para la determinación de la tendencia de la prevalencia a través del tiempo y la comparación entre países, la lista OMS 2009 ofrece un estándar muy robusto.
La frecuencia hallada de mutaciones transmitidas relevantes para la resistencia del virus a los ARV (según la lista OMS 2009), en pacientes naïve (6,6%), luce similar a la encontrada en otro estudio llevado a cabo en Colombia durante 2007- 2008 (5,8%) 12, aunque no es posible saber si las mutaciones incluidas en tal estudio difieren de las usadas por nosotros pues, desafortunadamente, tal investigación no presentó cómo se definieron. Sin embargo, la prevalencia podría ser mayor en nuestro estudio (11,8%) si se toman en cuenta las mutaciones en lista por la IAS-USA, y se acercaría a las reportadas en estudios de América del Norte, Brasil y Europa, en los cuales se ha sugerido que el riesgo de transmisión de un virus con resistencia a al menos un medicamento ARV oscila entre 7 y 21% 9-11. La afectación de más de una familia de ARV (multirresistencia de clase) encontrada en el presente >estudio (1,4%) fue mucho más baja que en América del Norte (donde ha sido cercana al 6%), pero parecida a la correspondiente en Europa (< 2%) y Brasil 18,19.
La prevalencia de mutaciones de resistencia, aun si se sigue la definición estricta de la OMS 2009, fue de 6,6%, un nivel por encima de la prevalencia para la cual se ha demostrado costo-efectividad de la PGR realizada antes de iniciar la TAR en países de altos ingresos 20,21. El uso de las PGR en pacientes naïve se ha recomendado en las guías de manejo de VIH más influyentes en Norteamérica y Europa con base en la costo-efectividad probada para las PGR cuando la prevalencia de farmacorresistencia del VIH en los pacientes naïve está sobre el 4% 20. Desafortunadamente, a la fecha, no existen estudios publicados que examinen la costo-efectividad de la PGR en el contexto colombiano. Tales estudios se requieren para evaluar la idoneidad de su uso en el medio colombiano en pacientes naïve . Por ahora, la evidencia existente apoya su uso más que rechazarlo.
Un estudio previo en Colombia 12 , realizado en pacientes naïve , reportó como mutaciones más comunes la K103N (4,9%) y la M184V (2,9%), aun cuando el tiempo promedio transcurrido desde el diagnóstico de la infección por el VIH hasta el momento del genotipo fue sustancialmente mayor (alrededor de 6 años) que en el presente estudio. Nuestra investigación encontró una frecuencia de mutaciones K103N/S en un 2%, pero no halló la mutación M184V. Es de notar que la mutación M184V es una de las que más rápidamente se archiva o desaparece cuando el tratamiento ARV no está presente, tanto en pacientes con exposición a ARV como en pacientes naïve , lo que ha sido documentado en varios estudios previos. Por ejemplo, el estudio CASCADE 22 encontró solamente 3 casos de M184V y 1 mutación M184I en 45 casos de resistencia transmitida. Tal hallazgo en nuestro estudio es también consistente con el lapso relativamente prolongado del tiempo transcurrido entre la infección retroviral aguda y el momento de la PGR en nuestros participantes. Por otro lado, el estudio colombiano previo 12 advierte sobre que pudo haber pacientes con transmisión sumamente reciente del virus en tal estudio, lo cual fue improbable en el nuestro. Así pues, la ausencia de la mutación M184V en las PGRs probablemente se debió a que la secuenciación de ARN de población completa simplemente no pudo detectar poblaciones minoritarias de M184V, a que dicha mutación se habría ya revertido y quedado "archivada" en el genoma del huésped o a que sencillamente no se transmitió de forma eficiente.
Varios estudios han comparado la prevalencia de resistencias transmitidas entre los individuos recientemente infectados y aquellos con infección crónica de más larga evolución, siendo mayor la prevalencia para el primer grupo 23,24. En nuestro estudio, se encontró asociación estadística significativa entre la presencia de mutaciones de resistencia y la duración de la infección retroviral < 1 año, lo cual es consistente con estudios previos que indican que las mutaciones de resistencia transmitida tienden a revertirse con el tiempo 25,26. Las otras variables exploradas no presentaron asociación estadísticamente significativa, pero se encontró una relación cercana al límite de significancia con la carga viral baja (1.000 a 10.000 copias/mL). La carga viral baja podría explicarse por un efecto deletéreo de algunas de las mutaciones de resistencia sobre la capacidad de replicación viral, previamente descrito 27.
Es muy probable que una proporción importante de los virus resistentes en la muestra estudiada se hayan transmitido de personas que experimentaban falla virológica al tratamiento, ya que a la fecha existen ensayos clínicos 28 que confirman que el riesgo de transmisión del VIH es extremadamente bajo en caso de supresión viral total. También se sabe que el factor proximal más claramente asociado con la aparición de resistencia en el VIH y de falla virológica en pacientes que toman TAR es la adherencia subóptima al tratamiento 29. Así que es concebible asumir que los transmisores de virus resistentes son en su mayoría personas que cumplen este requisito. Nuestros hallazgos sugieren que los factores que puedan estar afectando a la adherencia a la TAR en los pacientes tratados deben examinarse con atención, incluyendo condiciones propias y/o socioeconómicas de los pacientes y del sistema de salud. No obstante, es importante también enfatizar que hasta un 38% de los eventos de transmisión de VIH ocurren en el período de infección temprana 30, razón por la cual debe reforzarse la detección por los médicos de atención primaria de casos sugestivos de infección por VIH reciente, incluyendo el síndrome retroviral agudo.
Nuestro estudio tiene varias limitaciones que tratamos de minimizar en lo posible durante la ejecución del mismo. Primero, la muestra no es probabilística, lo cual le resta representatividad; sin embargo, los participantes son similares en sus características sociodemográficas a la mayoría de pacientes con VIH en Cali y Colombia. Segundo, como ocurre en todos los estudios de este tipo, que a pesar de nuestro mejor esfuerzo, existe la posibilidad de que algunos participantes hayan sido erróneamente clasificados como ARV naïve . Tercero, debido a la falta de disponibilidad de archivos electrónicos de las secuencias de nucleótidos, los genotipos no pudieron ser reanalizados para determinar subtipos de VIH; sin embargo, en Colombia el subtipo B es fuertemente predominante y es muy probable que la mayoría de los casos representaran tal subtipo en nuestra investigación.
Conclusiones
Nuestro estudio concluye que la frecuencia de resistencia transmitida en esta muestra de pacientes naïve a TAR de Cali y el Valle del Cauca en el suroccidente de Colombia es mayor que el umbral de costo-efectividad para la realización de las PGR, y que su realización sistemática en todos los pacientes naïve debe ser considerada en una próxima revisión de las guías colombianas de VIH, posiblemente con énfasis en su recomendación para pacientes cuya infección retroviral aguda tenga alta probabilidad de haber ocurrido en el último año previo al momento de llevar a cabo la prueba genotípica de resistencia.
Agradecimientos
A la CLS por la financiación total del proyecto; a los colaboradores, en particular a Juan Fernando Agudelo, de la CLS, a Patricia Olaya, del CAM-Bogotá, al Dr. Carlos Granados, docente de la Universidad de la Sabana, al Dr. Francisco Javier Gutiérrez, docente de la Universidad de Antioquia, a la Dra. Beatriz E. Alvarado, docente de Queen´s University, al Canadian HIV Clinical Trials Network de los Institutos Canadienses de Investigación en Salud por apoyar la preparación de este manuscrito, así como a los pacientes participantes que permitieron el uso anónimo de la información contenida en sus historias clínicas institucionales.
* Autor para correspondencia. Correo electrónico: centroinvestigaciones@cls.org.co (P. Galindo-Orrego).0123-9392/$ - see front matter © 2013 ACIN. Publicado por Elsevier España, S.L. Todos los derechos reservados.
Bibliografía
1. Joint United Nations Programme on HIV/AIDS. Status of the Global HIV Epidemic. 2008 Report on the global AIDS Epidemic. Geneva: UNAIDS; 2008. consultado 8 Feb 2012. Disponible en: http://www.unaids.org/en/dataanalysis/epidemiology/2008reportontheglobalaidsepidemic/ [ Links ]
2. Joint United Nations Programme on HIV/AIDS/World Health Organization/ United Nations Children´s Fund. Epidemiological Fact Sheets on HIV and AIDS. Core Data on Epidemiology and Response Colombia. Ginebra: UNAIDS/OMS/UNICEF; 2008. consultado 2 Abr 2012. Disponible en: http://www.who.int/globalatlas/predefinedReports/EFS2008/full/EFS2008_CO.pdf [ Links ]
3. Palella FJ, Delaney KM, Moorman AC, Loveless MO, Fuhrer J, Satten GA, et al. Declining morbidity and mortality among patients with advanced human immunodeficiency virus infection. HIV Outpatient Study Investigators. N Engl J Med. 1998;338:853-60. [ Links ]
4. Panel on Antiretroviral Guidelines for Adults and Adolescents. Guidelines for the use of antiretroviral agents in HIV-1-infected adults and adolescents. Department of Health and Human Services. consultado 2 Abr 2012. Disponible en: http://aidsinfo.nih.gov/ContentFiles/AdultandAdolescentGL.pdf [ Links ]
5. Masquelier B, Lemoigne E, Pellegrin I, Douard D, Sandler B, Fleury HJ. Primary infection with zidovudine-resistant HIV. N Engl J Med. 1993;329:1123-4. [ Links ]
6. Jordan MR, Bennett DE, Bertagnolio S, Gilks CF, Sutherland D. World Health Organization surveys to monitor HIV drug resistance prevention and associated factors in sentinel antiretroviral treatment sites. Antivir Ther. 2008;13(Suppl 2):15-23. [ Links ]
7. Panel de expertos de Gesida y Plan Nacional sobre el SIDA. Documento de consenso de Gesida/Plan Nacional sobre el SIDA respecto al TAR en adultos infectados por el virus de la inmunodefi- ciencia humana. Ministerio de Sanidad, Política Social e Igualdad, España. consultado 28 Mar 2012. Disponible en: http://www.gesida.seimc.org/pcientifica/fuentes/DcyRc/gedcyrc2011-Documentoconsenso-TAR-adulto-verordenador.pdf [ Links ]
8. Europa AIDS Clinical Society. Guías Clínicas. Tratamiento y seguimiento de adultos infectados por el VIH en Europa. Versión 5-4. EACS; 2011. consultado 28 Mar 2012. Disponible en: http://www.europeanaidsclinicalsociety.org/images/stories/EACS-Pdf/EACSGuidelines-Spanish-5-4.pdf [ Links ]
9. Little SJ, Holte S, Routy JP, Daar ES, Markowitz M, Collier AC, et al. Antiretroviral-drug resistance among patients recently infected with HIV. N Engl J Med. 2002;347:385-94. [ Links ]
10. Wheeler WH, Ziebell RA, Zabina H, Pieniazek D, Prejean J, Bodnar UR, et al. Prevalence of transmitted drug resistance associated mutations and HIV-1 subtypes in new HIV-1 diagnoses, U.S.-2006. AIDS. 2010;24:1203-12. [ Links ]
11. Frentz D, Boucher CA, van de Vijver DA. Temporal Changes in the Epidemiology of Transmission of Drug-Resistant HIV-1 across the World, AIDS Rev. 2012;14:17-27. [ Links ]
12. Díaz-Granados CA, Mantilla M, Lenis W. Antiretroviral drug resistance in HIV-infected patients in Colombia. Int J Infect Dis. 2010;14:e298-303. [ Links ]
13. Gómez SM, Olaya P, Díaz FJ. Resistencia a los medicamentos antirretrovirales en pacientes que reciben tratamiento para VIHSIDA en Colombia. Infectio. 2010;14:248-56. [ Links ]
14. Díaz-Granados CA, Silva A, Bermúdez A, Roncancio D, DiRuggiero P, Mantilla M. Rate and predictors of optimal virologic response to antirretroviral therapy in Colombia. Int J Infect Dis. 2007;11:531-5. [ Links ]
15. Machado JE, Alzate JA. Patrones de prescripción de antirretrovirales en 997 pacientes colombianos. Biomédica. 2008;28:78-86. [ Links ]
16. Bennett DE, Camacho RJ, Otelea D, Kuritzkes DR, Fleury H, Kiuchi M, et al. Drug Resistance Mutations for Surveillance of Transmitted HIV-1 Drug-Resistance: 2009 Update. PLoS One. 2009;4:e4724. [ Links ]
17. Johnson VA, Brun-Vézinet F, Clotet B, Günthard HF, Kuritzkes DR, Pillay D, et al.Update of the Drug Resistance Mutations in HIV-1: December 2010.Top HIV Med. 2010;18:156-63. [ Links ]
18. Rodrigues R, Scherer LC, Oliveira CM, Franco HM, Sperhacke RD, Ferreira JL, et al. Low prevalence of primary antiretroviral resistance mutations and predominance of HIV-1 clade C at polymerase gene in newly diagnosed individuals from south Brazil. Virus Res. 2006;116:201-7. [ Links ]
19. Brindeiro RM, Diaz RS, Sabino EC, Morgado MG, Pires IL, Brigido L, et al. Brazilian Network for HIV Drug Resistance Surveillance (HIV-BResNet): a survey of chronically infected individuals. AIDS. 2003;17:1063-9. [ Links ]
20. Weinstein MC, Goldie SJ, Losina E, Cohen CJ, Baxter JD, Zhang H, et al. Use of Genotypic Resistance Testing To Guide HIV Therapy: Clinical Impact and Cost-Effectiveness. Ann Intern Med. 2001;134:440-50. [ Links ]
21. Sax PE, Islam R, Walensky RP, Losina E, Weinstein MC, Goldie SJ, et al. Should resistance testing be performed for treatment-naive HIV-infected patients? A cost-effectiveness analysis. Clin Infect Dis. 2005;41:1316-23. [ Links ]
22. Masquelier B, Bhaskaran K, Pillay D, Gifford R, Balestre E, Jørgensen LB, et al; CASCADE Collaboration. Prevalence of transmitted HIV-1 drug resistance and the role of resistance algorithms: data from seroconverters in the CASCADE collaboration from 1987 to 2003. J Acquir Immune Defic Syndr. 2005;40:505-11. [ Links ]
23. Violin M, Forbici F, Cozzi-Lepri A, Velleca R, Bertoli A, Riva C, et al. Primary HIV-1 resistance in recently and chronically infected individuals of the Italian Cohort Naive for Antiretrovirals. J Biol Regul Homeost Agents. 2002;16:37-43. [ Links ]
24. Wensing AM, van de Vijver DA, Angarano G, Asjö B, Balotta C, Boeri E, et al. Prevalence of drug-resistant HIV-1 variants in untreated individuals in Europe: implications for clinical management. J Infect Dis. 2005;192:958-66. [ Links ]
25. Pao D, Andrady U, Clarke J, Dean G, Drake S, Fisher M, et al. Long-term persistence of primary genotypic resistance after HIV-1 seroconversion. J Acquir Immune Defic Syndr. 2004;37:1570-3. [ Links ]
26. Little SJ, Frost SD, Wong JK, Smith DM, Pond SL, Ignacio CC, et al. Persistence of transmitted drug resistance among subjects with primary human immunodeficiency virus infection. J Virol. 2008;82:5510-8. [ Links ]
27. Dykes C, Demeter LM. Clinical significance of human immunodeficiency virus type 1 replication fitness. Clin Microbiol Rev. 2007;20:550-78. [ Links ]
28. Cohen MS, Chen YQ, McCauley M, Gamble T, Hosseinipour MC, Kumarasamy N, et al. Prevention of HIV-1 Infection with Early Antiretroviral Therapy. N Engl J Med. 2011;365:493-505. [ Links ]
29. Bangsberg DR, Kroetz DL, Deeks SG. Adherence-resistance relationships to combination HIV antiretroviral therapy. Curr HIV/AIDS Rep. 2007;4:65-72. [ Links ]
30. Powers KA, Ghani AC, Miller WC, Hoffman IF, Pettifor AE, Kamanga G, et al. The role of acute and early HIV infection in the spread of HIV and implications for transmission prevention strategies in Lilongwe, Malawi: a modelling study. Lancet. 2011;378:256-68. [ Links ]













