Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Infectio
Print version ISSN 0123-9392
Infect. vol.17 no.3 Bogotá July/Sept. 2013
ORIGINAL
Infecciones del tracto urinario bajo en adultos y embarazadas: consenso para el manejo empírico
E. Martinez a, J. Osorio b , J. Delgado c , G.E. Esparza d , G. Motoa e , V.M. Blanco e , C.A. Hernandez e , A. Agudelo f , L.J. Aluma g , C.A. Betancurt h , W. Ospina i , J.C. Camargo j , H. Canaval c,g, C. Castañeda k , A. Correa e , E. De La Cadena e , A. Gomez l , J. Gomez m , C.L. Rico n , L. Matta o , Y.A. Medina p , H. Mendoza q , L.A. Mendoza g , C. Pallares b , H. Perez r , S. Valderrama s , M. Villabon t y M.V. Villegase,*
a Asociación Colombiana de Infectología, Capítulo Suroccidente, Colombia
b Hospital Universitario Departamental de Neiva-Hernando Moncaleano Perdomo, Neiva, Huila, Colombia
c Hospital Universitario del Valle-Evaristo García, Cali, Valle del Cauca, Colombia
d Proasecal SAS, Bogotá, Colombia
e Centro Internacional de Entrenamiento e Investigaciones Médica (CIDEIM), Cali, Colombia
f Clínica Materno Infantil Los Farallones, Cali, Valle del Cauca, Colombia
g Centro Médico Imbanaco, Cali, Valle del Cauca, Colombia
h Clínica SOMA, Medellín, Colombia
i Hospital General de Medellín, Hospital San Vicente de Paúl, Clínica León XIII, Medellín, Colombia
j Hospital San José, Bogotá, Colombia
k Clínica Crecer, Cartagena, Colombia
l Hospital Militar Central, Universidad Militar Nueva Granada, Bogotá, Colombia
m Hospital San Vicente de Paúl, Medellín, Colombia
n Fundación Santa Fe de Bogotá, Bogotá, Colombia
o Corporación Clínica Comfenalco Unilibre, Cali, Colombia
p Profamilia, Bogotá, Colombia
q Hospital Central de la Policía, Bogotá, Colombia
r Hospital de Sogamoso, Sogamoso, Boyacá, Colombia
s Hospital Universitario San Ignacio, Pontificia Universidad Javeriana-Grupo de Investigación en Enfermedades Infecciosas, Bogotá, Colombia
t Clínica de los Nogales, Clínica Juan N. Corpas, Bogotá, Colombia
Recibido el 30 de septiembre de 2013; aceptado el 10 de noviembre de 2013
Resumen
Introducción: La infección no complicada del tracto urinario bajo y la bacteriuria asintomática son causas frecuentes de consulta médica ambulatoria y en el servicio de urgencias en Colombia y el mundo. La falta de pautas y consenso para el manejo, así como la emergencia de resistencia a las múltiples opciones terapéuticas disponibles en los uropatógenos provenientes de la comunidad, hacen necesario elaborar unas recomendaciones que orienten al clínico sobre el abordaje óptimo de estas entidades.
Objetivo: Definir un consenso sobre el manejo empírico de la bacteriuria asintomática y la infección del tracto urinario (ITU) bajo en adultos y mujeres embarazadas en Colombia.
Metodología: Se lleva a cabo una metodología de consenso con expertos en urología, infectología, medicina interna, ginecología y microbiología basada en la revisión de las referencias bibliográficas disponibles en los términos de búsqueda relacionados, haciendo énfasis en estudios locales.
Resultados: Se elaboró un algoritmo de manejo para el tratamiento empírico de la ITU baja no complicada en adultos con antisépticos urinarios como nitrofurantoína y fosfomicina trometamol como primera línea, con recomendaciones terapéuticas específicas para el tratamiento de la bacteriuria asintomática en mujeres embarazadas. Adicionalmente, se formuló un algoritmo de decisión para el procesamiento de cultivos de orina. La recurrencia o recaída frecuente justifica remisión a urología e infectología.
Conclusiones: Se generan recomendaciones prácticas de fácil implementación en el diagnóstico y manejo de la ITU bajo en adultos y embarazadas, y de los casos donde es necesario tratar la bacteriuria asintomática, con opciones terapéuticas efectivas y de espectro reducido.
© 2013 ACIN. Publicado por Elsevier España, S.L. Todos los derechos reservados.
PALABRAS CLAVE
Infección del tracto urinario; Cistitis; Bacteriuria asintomática; Embarazo; Tratamiento
Lower Urinary Tract Infections in Adults and Pregnant Women: A Consensus for Empirical Treatment
Abstract
Background: Uncomplicated infection of the lower urinary tract and asymptomatic bacteriuria are frequent causes of visits to outpatient clinics and emergency departments in Colombia and worldwide. The lack of guidelines and a consensus for their management, and the emergence of resistance of community-based uropathogens to the available therapeutic options, make it necessary to develop recommendations to guide clinicians on the optimal approach to these entities.
Objective: Define a consensus for the empiric management of asymptomatic bacteriuria and Urinary Tract Infection (UTI) in adults and pregnant women in Colombia.
Methods: We carried out a consensus methodology with experts in urology, infectious diseases, internal medicine, gynecology and clinical microbiology; based on reviewing the available literature on the related terms, and emphasizing local studies.
Results: We developed a management algorithm for the empirical treatment of uncomplicated lower UTI in adults with urinary antiseptics such as nitrofurantoin and fosfomycin trometamol as first line, with specific therapeutic recommendations for the treatment of asymptomatic bacteriuria in pregnant women. Additionally, we created a decision algorithm for processing urine cultures. Frequent recurrence or relapse justifies referral to urology and infectious disease professionals.
Conclusions: We generated straightforward and easy-to-implement recommendations for the diagnosis and management of UTI in adults and pregnant women, and in cases where it is necessary to treat asymptomatic bacteriuria, with effective therapeutic and narrow spectrum options.
© 2013 ACIN. Published by Elsevier España, S.L. All rights reserved
KEYWORDS:
Urinary tract infection; Cystitis; Asymptomatic bacteriuria; Pregnancy; Treatment
Introducción
Las infecciones sintomáticas del tracto urinario bajo en adultos pueden clasificarse como complicadas o no complicadas. Las primeras, que generalmente se asocian con pielonefritis y se manifiestan con fiebre, escalofríos o dolor en flancos 1, no son objeto de discusión de este consenso.
La ITU baja no complicada es un diagnóstico común en mujeres jóvenes, no embarazadas, sin comorbilidades, con función renal normal, inmunocompetentes y sin daño anatómico o manipulación de la vía urinaria. Se ha descrito que la mitad de las mujeres habrá reportado al menos un episodio de ITU a la edad de 32 años 2 , y que el 25% tendrá un episodio recurrente después de la primera infección 3 . La situación en hombres es diferente ya que la incidencia en adultos menores de 50 años es inferior al 1%, incrementándose considerablemente después de esa edad debido con frecuencia al aumento en el tamaño de la próstata o la instrumentación del tracto urinario. En mujeres embarazadas el panorama es un poco diferente, dado que las ITU son la complicación médica más frecuente en el embarazo, con una prevalencia de 7 a 10%. Además, un tratamiento inadecuado se asocia a un alto riesgo de padecer complicaciones maternas y fetales, que precisan de exámenes complementarios para su diagnóstico y terapia apropiada.
Entre los factores de riesgo descritos en la literatura se encuentran, entre otros, aumento en la frecuencia de actividad sexual en el último mes, un nuevo compañero sexual en los últimos 12 meses, uso de espermicidas, la inserción de catéteres de drenaje o de derivación sobre la vía urinaria posquirúrgicos y episodios previos de ITU 4,5,7,8. En adultos mayores, estos factores incluyen además la presencia de incontinencia urinaria, una pobre higiene del área genital o vivir en hogares de cuidado geriátrico 6 .
En la mayoría de los casos no se requieren pruebas diagnósticas adicionales y un ciclo corto de antibióticos es suficiente para controlar la infección; la tasa de complicaciones o falla terapéutica es baja si se escoge el antibiótico apropiado. El diagnóstico generalmente se establece cuando el paciente acude a consulta con al menos uno de los siguientes síntomas: disuria, polaquiuria, urgencia urinaria, dolor suprapúbico o hematuria. En el caso de las mujeres, la presencia de estos síntomas en ausencia de leucorrea o irritación vaginal aumenta la probabilidad de ITU baja 9 .
El tratamiento antimicrobiano apropiado contribuye no solo a las tasas altas de curación clínica y microbiológica sino también a prevenir episodios de reinfección 10. Factores como las tasas locales de resistencia en uropatógenos, el tiempo de excreción urinaria del medicamento, los efectos sobre la flora vaginal e intestinal, la seguridad y el costo se han descrito como condiciones a considerarse para seleccionar una terapia apropiada. Los tratamientos cortos han demostrado ser equivalentes en eficacia a los tratamientos convencionales, pero con un menor número de efectos adversos y costos más bajos 11 .
Los microorganismos causantes de ITU generalmente provienen de la flora entérica que coloniza el peritoneo y la uretra, siendo E. coli el microorganismo más prevalente, seguido por Klebsiella spp. , P. mirabilis, Enterococcus spp., y S. saprophyticus 12,13. Sin embargo, el aumento en la resistencia de estos uropatógenos frente a antibióticos de uso rutinario hace que la escogencia actual de un tratamiento empírico sea más difícil. Por esta razón, la sociedad americana de enfermedades infecciosas (IDSA) señala la necesidad de tener en cuenta el riesgo de selección de especies multidrogo resistentes cuando se quiera iniciar un tratamiento antibiótico 14 . IDSA, considerando las tasas locales de resistencia, ha sugerido usar umbrales para definir cuándo un agente no debería usarse para el tratamiento empírico: por ejemplo en el caso de las fluoroquinolonas estas no deberían exceder el 10% y para trimetoprim-sulfametoxazol no debe ser mayor al 20% 15.
En Colombia no se ha desarrollado pauta para el manejo de la ITU baja no complicada, por lo que se propuso como objetivo elaborar un consenso sobre el abordaje terapéutico empírico de la ITU baja no complicada.
Metodología
El Grupo para el estudio de la Resistencia Nosocomial en Colombia-CIDEIM, la Asociación Colombiana de Epidemiología Hospitalaria (ACEH) y la Red de Vigilancia de Eventos Nosocomiales del Valle (RENOVA) nombraron un comité conjunto para desarrollar un consenso para el manejo empírico de la ITU baja en adultos y en embarazadas. Se invitaron expertos nacionales de reconocida trayectoria en urología, gineco-obstetricia, medicina interna, infectología y microbiología clínica. Se llevó a cabo una revisión de la literatura a través de Medline, Science Direct, OVID, Hinari, y Fundación Cochrane, sobre ITU baja en adultos y embarazadas, cistitis, uso de antibióticos y resistencia bacteriana de uropatógenos. Los artículos más relevantes fueron enviados previamente a todos los integrantes del comité, se seleccionaron cuatro temas de consenso: ITU baja no complicada en adultos, bacteriuria asintomática, ITU baja en embarazadas y diagnóstico microbiológico en ITU, teniendo como referencia el consenso de la IDSA. Los temas fueron discutidos en dos sesiones plenarias por los participantes de la mesa distribuidos de acuerdo a cada especialidad. Se eligió un redactor por tema de consenso quien presentó los acuerdos por cada mesa y los distribuyó entre los integrantes. Una vez concluida la revisión de cada tema, un coordinador revisó, integró y realizó los ajustes necesarios de cada tema para componer un documento final, el cual fue entregado a cada miembro de los comités para ser revisado y aprobado. Este documento debe interpretarse como una guía práctica para el personal de salud y está basada en los niveles de evidencia de las revisiones realizadas.
Resultados
Infección del tracto urinario baja no complicada
Se define como ITU baja la presencia de síntomas urinarios como disuria, urgencia, polaquiuria y dolor suprapúbico, en ausencia de leucorrea, irritación vaginal, dolor lumbar, fiebre y compromiso sistémico. Según la disponibilidad en la institución, la rapidez en su reporte y la posibilidad de interpretación de los resultados por un médico, es recomendable realizar un uroanálisis o Gram de orina sin centrifugar en pacientes con sospecha de ITU buscando la presencia de leucocituria o prueba positiva de estearasa leucocitaria y de nitritos 16. No se deberá limitar o posponer innecesariamente el inicio del tratamiento en espera del resultado.
Una vez realizado el diagnóstico de ITU baja no complicada se recomienda como primera línea de manejo nitrofurantoína en un régimen de 5 a 7 días a dosis de 100 mg vía oral cada 6 horas, y para la presentación de macrocristales de nitrofurantoína monohidrato (Retard), el tratamiento se simplifica a dosis de 100 mg cada 12 horas, la cual ha mostrado tener una eficacia clínica entre el 84% y el 95% y una mejor tolerancia gastrointestinal. De igual forma, fosfomicina trometamol representa una excelente opción como primera línea de tratamiento, con la ventaja de administrarse en una dosis única de 3 g, con similar eficacia (91%), mínima resistencia in vitro y probablemente un efecto menor sobre la flora intestinal 17,18. Debe tenerse en cuenta que aunque fosfomicina no está incluida en el listado de medicamentos cubiertos por el Plan Obligatorio de Salud del país, si se incluye en las guías hospitalarias justificando su uso, podría utilizarse.
Debido a que en nuestro medio hay evidencia de un 20% o más de resistencia de uropatógenos frente a TMP-SMX y ciprofloxacina, no se recomienda usarlos en el tratamiento empírico de las ITU baja 19,20. Además, el uso de ciprofloxacina en microorganismos como E. coli , K. pneumoniae y P. aeruginosa añade un riesgo de selección de resistencia bacteriana a diferentes tipos de antibióticos por mecanismos como betalactamasas de espectro extendido (BLEE), carbapenemasas tipo KPC, activación de bombas de eflujo, cierre de porinas y mutaciones en el DNA, con posible selección de Clostridium difficile, entre otros 21.
Con respecto a la acidificación de la orina concomitante al manejo con nitrofurantoína, el grupo de expertos no encontró evidencia suficiente para sugerir esta conducta, por lo cual se deja a criterio clínico. Aunque las tasas de resistencia frente a nitrofurantoína o fosfomicina se mantienen bajas en nuestro medio, se sugiere hacer uso racional de estos antibióticos para no propiciar la emergencia de resistencia en el futuro.
Como alternativa a la primera línea en pacientes con intolerancia a los antisépticos urinarios o con alteración de la función renal se sugiere el uso de cefuroxime, 500 mg vía oral, dos veces al día durante 3 días. Existen otros antibióticos menos recomendables por presentar resistencia primaria o una farmacocinética inferior en orina, que se han usado en regímenes de 3 a 7 días, según los perfiles de resistencia regionales o de cada institución o cuando el reporte del urocultivo o antibiograma muestren el aislamiento susceptible a los mismos 22; entre estos están: cefalosporinas de primera generación, ampicilina sulbactam y amoxicilina clavulanato.
No se recomienda realizar uroanálisis o urocultivo de control una vez terminado el tratamiento. Este último se reserva solo para los casos en donde no se evidencie mejoría clínica 48 horas después de la administración correcta del tratamiento antimicrobiano o si los síntomas recurren en las siguientes dos semanas. Mientras se esperan los resultados del urocultivo puede iniciarse otro antibiótico de primera o segunda línea para el manejo empírico, asumiendo que el microorganismo es resistente al antimicrobiano usado durante el primer episodio.
El grupo de expertos del consenso considera que estas pautas de manejo deben aplicarse en mujeres con menos de tres episodios documentados de ITU baja no complicada durante el último año o dos episodios en los últimos seis meses, sin evidencia previa de anormalidades anatómicas o funcionales. De lo contrario, se recomienda valoración por urología e infectología. En el caso de los hombres, se recomienda tratar según las recomendaciones de esta guía y remitir al urólogo para valoración posterior (fig. 1).
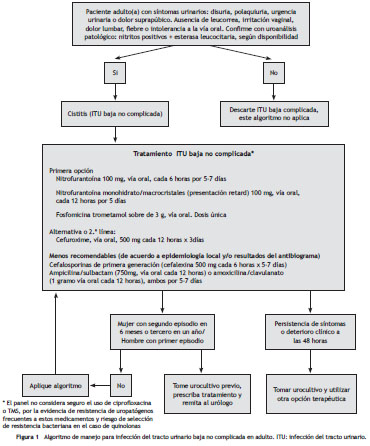
Conclusiones frente a la terapia antibiótica en infección del tracto urinario baja no complicada
Las anteriores recomendaciones están encaminadas a orientar el manejo empírico inicial de las infecciones urinarias bajas independientemente de las características del huésped como edad, sexo o presencia de factores potenciales asociados a resistencia. El grupo de expertos considera que tanto nitrofurantoína como fosfomicina son opciones terapéuticas satisfactorias para la mayoría de los episodios de ITU baja o cistitis; sin embargo, se recomienda evaluar en la historia clínica del paciente la exposición previa o repetida a estos antisépticos que pudiera comprometer su eficacia para el tratamiento del episodio actual. Las pautas emitidas permiten un abordaje sencillo y práctico en el manejo de la ITU baja no complicada.
Bacteriuria asintomática
La bacteriuria asintomática (BAS) se define como el recuento significativo de colonias bacterianas en muestras de orina, colectadas apropiadamente de pacientes sin signos o síntomas atribuibles a infecciones del tracto urinario 23 . Se entiende por un recuento de colonias significativo el aislamiento de una única especie con > 10 5 UFC/ml en una sola muestra para hombres, o dos muestras consecutivas en mujeres; para muestras recolectadas por catéter urinario, se requiere un recuento de > 10 2 UFC/ml de una sola especie 24. La presencia de piuria es insuficiente para el diagnóstico de bacteriuria 25-27.
La prevalencia de BAS varía de acuerdo al género, la edad, las intervenciones médicas y las comorbilidades. En adultos jóvenes tiene una prevalencia de 1-2% en hombres y de 1-9% en las mujeres 28, en quienes puede aumentar hasta 23,5% durante el embarazo 29. En mujeres con infección por VIH o alteraciones hematológicas no se ha reportado una prevalencia mayor de BAS respecto a las pacientes sin estas condiciones 30,31.
En el caso de diabetes mellitus (DM) controlada, las mujeres presentan una prevalencia de BAS mayor que la encontrada en hombres: 14,2% versus 2,3% 32, las cuales pueden ascender a 21% y 8% cuando hay evidencia de microalbuminuria 33. En pacientes > 65 años, independiente de las patologías asociadas, esta tendencia cambia, y la prevalencia reportada de BAS es del 30% en hombres y 10% en mujeres, aumentado en pacientes que residen en hogares de cuidado geriátrico: 55% y 40%, respectivamente 34. En pacientes llevados a artroplastia y hemiartroplastia de cadera, la prevalencia reportada de BAS es de 3,5% y de 16%, para cada una 35.
E. coli es el agente causal de al menos el 80% de las BAS en ambientes no hospitalarios. P. mirabilis, K. pneumoniae, Enterobacter spp . y P. aeruginosa también pueden ser aislados. Entre las bacterias Gram positivas, Enterococcus spp ., S. aureus y S. saprophyticus son los micro organismos más frecuentemente asociados a esta condición 28. La naturaleza clínica benigna de la BAS ha sido explicada, entre otras, por la ausencia de fenotipos adherentes al uroepitelio debido a que las E. coli causantes de BAS carecen de fimbrias funcionales; sin embargo, algunas variantes se adhieren al uroepitelio sin promover una respuesta pro-inflamatoria 36. La cepa 83972 de E. coli , frecuentemente aislada en las BAS, presenta características metabólicas adaptativas que le permiten establecerse en la vejiga humana a largo plazo 37.
Entre los factores de riesgo para el desarrollo de una BAS se encuentran la edad avanzada, el género femenino, la presencia de DM, hipertensión arterial, disminución de la función renal, antecedente de cirugía genitourinaria, urolitiasis, incontinencia urinaria y obesidad 38-40. En la mujer embarazada la combinación de cambios mecánicos, hormonales y fisiológicos contribuyen a cambios en el tracto urinario, impactando significativamente en la presencia BAS 41.
El tratamiento innecesario de la BAS en pacientes ambulatorios y hospitalarios es una práctica común 42, incluso aunque las guías actuales establecen que el significado clínico y manejo de la BAS favorecen claramente el tamizaje y tratamiento en casos específicos como en mujeres embarazadas y pacientes que serán sometidos a procedimientos genitourinarios invasivos 43; existe evidencia de que la mujer que presenta BAS en el primer trimestre del embarazo y no recibe el tratamiento antibiótico apropiado puede desarrollar complicaciones maternas o fetales como pielonefritis aguda, trabajo de parto prematuro o bajo peso al nacer 44. La presencia de BAS en otras poblaciones adultas diferentes a las mencionadas no ha demostrado un efecto perjudicial y, aunque se ha descrito que podría asociarse a un mayor riesgo de infección urinaria sintomática, el tratamiento de la BAS no disminuye este riesgo ni mejora otros desenlaces clínicos 45.
La evidencia actual para el tratamiento antibiótico de los pacientes con BAS que van a ser sometidos a procedimientos no urológicos aún es inconsistente; por ejemplo, para los reemplazos articulares de cadera la literatura actual admite el tratamiento antimicrobiano de los pacientes con evidencia de BAS en la evaluación pre operatoria, aunque otros autores han reportado que las infecciones asociadas al procedimiento quirúrgico no son causadas por el mismo agente etiológico identificado en el urocultivo. Para la cirugía de columna lumbar en mujeres mayores de 65 años con BAS y que requieran cateterismo Foley, se sugiere que el episodio de bacteriuria sea resuelto mediante tratamiento antimicrobiano antes del procedimiento quirúrgico 46. En pacientes que deban ser sometidos a cirugía cardiaca y tengan catéter urinario, el reemplazo del catéter y la administración de un ciclo corto de antibióticos contribuyen a la disminución de la carga bacteriana en orina; sin embargo, no se ha evaluado específicamente el impacto de este efecto en la incidencia de infecciones postoperatorias 47.
El régimen terapéutico en pacientes que serán sometidos a procedimientos urológicos aún no está bien establecido, la Sociedad Americana de Enfermedades Infecciosas en la guía de práctica clínica para el manejo de la bacteriuria asintomática del 2006 recomienda el inicio de la terapia la noche anterior o inmediatamente antes del procedimiento 24. Kutlu et al., en una serie de 39 pacientes sometidos a cirugía urológica, instauraron un régimen terapéutico con dosis única 30-60 minutos antes del procedimiento y una segunda dosis para los pacientes que continuaron con el catéter urinario, este régimen demostró igual eficacia que el tratamiento de larga duración en la prevención de bacteriemia 48. La cistoscopia flexible de fibra óptica sin biopsia conlleva un riesgo de infección similar a la colocación de un catéter urinario, por lo tanto en el primer caso no se recomienda la erradicación de la bacteriuria asintomática 49.
Conclusiones frente a la terapia antibiótica en bacteriuria asintomática
Este consenso de expertos recomienda, en el caso de pacientes que deban ser llevados a procedimientos quirúrgicos no urológicos programados de las especialidades de cardiología, neurocirugía y remplazos ortopédicos, realizar durante la fase pre-operatoria tamizaje de BAS mediante uroanálisis y urocultivo y, en caso de presentar un resultado positivo, administrar tratamiento dirigido y tomar cultivo de seguimiento. En el paciente de urgencias, solicitar uroanálisis y Gram de orina sin centrifugar y, en caso de cumplir con criterios de infección, dar tratamiento antimicrobiano con antiséptico urinario 50 (fig. 2).
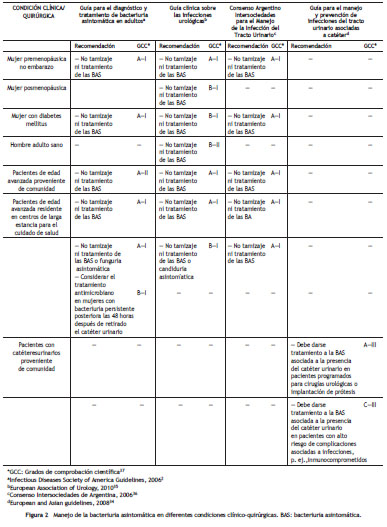
Infección urinaria y embarazo
La ITU durante el embarazo se define como el recuento de gérmenes patógenos por encima de 10 5 Unidades Formadoras de Colonias (UFC)/mL tomada por micción espontánea.
Se clasifica en infección urinaria baja, que puede ser asintomática (bacteriuria asintomática) o sintomática (cistitis), e infecciones altas (pielonefritis). La bacteriuria asintomática ocurre en 4-7% de las embarazadas, y en un 20-40% de los casos progresa a pielonefritis.
Efectos sobre el embarazo
La ITU durante el embarazo se asocia a un aumento de la incidencia de parto pretérmino, aumento del riesgo de infección fetal y de las membranas amnióticas, y procesos infecciosos maternos con compromiso metabólico sistémico sepsis, choque séptico, afectación hepática y pulmonar 51. Cuando el agente causal es el estreptococo del grupo B, se ha observado un mayor riesgo de ruptura prematura de membranas, parto pretérmino, sepsis neonatal, meningitis y neumonía neonatal.
La BAS se asocia a complicaciones como trabajo de parto pretérmino, bajo peso al nacer, restricción de crecimiento intrauterino, ruptura prematura de membranas y muerte neonatal 52,53.
Cuadro clínico
La bacteriuria asintomática se diagnostica por la realización rutinaria del cultivo de orina en todas las embarazadas.
La cistitis o infección urinaria baja cursa en general con síntomas que comprenden el síndrome vesical: disuria, polaquiuria, nicturia y tenesmo vesical. En pielonefritis es frecuente encontrar dolor lumbar, fiebre, dolor supra púbico, puño percusión lumbar positiva y en ocasiones síndrome vesical.
Factores de riesgo
Los factores de riesgo que predisponen a la infección urinaria y a la conversión de bacteriuria asintomática a pielonefritis corresponden a gestantes tardías, multiparidad, bajo nivel socioeconómico, antecedentes de infecciones urinarias, alteraciones estructurales y funcionales en la vía urinaria, rasgo drepanocítico y diabetes 54,55.
Etiología
La ITU en el embarazo es causada por bacterias provenientes de la flora perineal. Las enterobacterias E. coli, Klebsiella spp . y P. mirabilis se encuentran hasta en el 95% de los cultivos de orina. Otros agentes etiológicos correspon den a Gram positivos como S. saprophyticus, Enterococcus spp ., y el estreptococo del grupo B ( S. agalactiae ), M. genitalium , P. aeruginosa y en menor frecuencia G. vaginalis, y U. urealitycum 56.
Diagnóstico bacteriuria asintomática
En estas pacientes el urocultivo rutinario se puede realizar en cualquier momento de la gestación, preferiblemente a las 12-16 semanas de embarazo. No repetir si el resultado del mismo es negativo y no hay antecedentes o riesgos de infección urinaria; el cultivo de orina se repite en el tercer trimestre en pacientes con enfermedad renal, diabetes y antecedente de infección urinaria. Para el diagnóstico de BAS se requiere un recuento de colonias significativo (> 10 5 UFC/mL) en el cultivo de orina 57.
Diagnóstico de cistitis
Para el diagnóstico de cistitis es necesaria la presencia de síntomas urinarios localizados como polaquiuria, urgencia miccional, disuria y hematuria. En estas pacientes se debe realizar uroanálisis y urocultivo. Si el uroanálisis es patológico se sugiere iniciar tratamiento empírico y esperar el resultado del urocultivo y antibiograma para identificar el agente etiológico, conocer su perfil de sensibilidad y ajustar la terapia, si se requiere. Se considera un urocultivo positivo cuando el recuento de colonias es significativo (> 10 5 UFC/mL). Si el urocultivo es negativo, se sugiere realizar una nueva valoración clínica y, según los hallazgos, considerar el retiro de la terapia antibiótica previamente iniciada 58.
Si el cuadro clínico se asocia a síntomas urinarios sistémicos como fiebre, escalofrío, náuseas, vómito, dolor abdominal o lumbar, sintomatología de respuesta inflamatoria generalizada y sepsis, debe sospechar que la paciente curse con pielonefritis; para su diagnóstico se requiere la presencia de bacterias en el cultivo de orina (mayor de 100.000 UFC). Por el riesgo de morbilidad materna y fetal se indica hospitalización para manejo anteparto 59.
Interpretación de exámenes de laboratorio y discrepancias
Sedimento urinario: normal: menor de 10 leucocitos/mm 3 ; sospechoso: entre 10 y 50 leucocitos/mm 3 y anormal: mayor de 50 leucocitos/mm 3 .
Urocultivo: no significativo: < 10 4 UFC/mL; dudoso: entre 10 4 y 10 5 UFC/mL; significativo: >10 5 UFC/mL
Los errores de interpretación más frecuentes son:
Presencia de células bajas de descamación: indica mala recolección de la muestra.
Cultivo positivo con más de dos gérmenes: se considera en la mayoría de los casos contaminado, se deben evaluar factores de riesgo como sonda vesical a permanencia o infección intrahospitalaria.
Presencia de bacterias en el uroanálisis sin leucocituria: posible contaminación, se sugiere repetir la muestra del uroanálisis y realizar un urocultivo.
Leucocituria sin gérmenes: posible origen vaginal, descartar vaginitis y patologías asociadas.
Gram de orina sin centrifugar, se considera un método simple de evaluación, sin embargo no hay una técnica bien estandarizada y hay diferentes criterios para considerar la prueba positiva. Tiene utilidad en embarazadas para demostrar la presencia de al menos una bacteria en gestantes con infección urinaria sintomática 60. (Ver recomendaciones microbiológicas).
Tratamiento
El manejo se inicia de acuerdo a la sensibilidad para cada antibiótico, señalada por el antibiograma en el urocultivo y al espectro conocido de los antimicrobianos, la epidemiología local, además de la seguridad y eficacia clínica demostradas del medicamento (fig. 3).

En el caso de la BAS, el panel de expertos recomienda iniciar con un antiséptico urinario como nitrofurantoína o fosfomicina (tabla 1).

Para el tratamiento de la cistitis en el embarazo, se sugiere administrar:
1. Cefalexina 500 mg cada 6 horas durante 5-7 días o
2. Amoxicilina clavulánico: 500 mg/cada 8 horas durante 5-7 días.
3. Antisépticos urinarios:
Nitrofurantoína 100 mg cada 6 horas durante 7 días (excepto si se aisla M. morgannii , P. mirabilis spp., Providencia spp., y Serratia spp., por resistencia intrínseca) o Fosfomicina trometamol 3 g dosis única.
Si la cistitis es causada por S. agalactiae el tratamiento es diferente (tabla 2). Si este mismo microorganismo es aislado en el cultivo de orina con recuento menor 10 5 UFC/mL no hay recomendación para el tratamiento, y se sugiere terapia intraparto para prevención de la infección neonatal por estreptococo del grupo B 61.

Profilaxis de infección urinaria
Evitar cateterismos vesicales; búsqueda y tratamiento permanente de la bacteriuria asintomática.
Reinfección o recurrencia de la infección urinaria
Infección persistente: es toda infección que ocurre en las primeras semanas luego del tratamiento adecuado de la infección previa, documentándose el mismo germen causal.
Reinfección: infección documentada posterior a un tratamiento adecuado por un germen causal diferente.
Infección recurrente: infección que se presenta en un periodo corto posterior a una ITU adecuadamente tratada con urocultivo negativo posterior al tratamiento. La aparición de 3 infecciones urinarias en 12 meses se considera infección urinaria recurrente. La patogénesis implica reinfección o persistencia bacteriana.
Una reinfección recurrente corresponde a la presencia de infección urinaria por diferente microorganismo en más de dos semanas después del tratamiento y de un resultado de un urocultivo negativo; en la persistencia bacteriana, la misma bacteria puede cultivarse en la orina 2 semanas después de iniciar el tratamiento adecuado 62.
Estos casos se deberán tratar de acuerdo al resultado del urocultivo y su antibiograma y estas pacientes se benefician de profilaxis antibiótica.
Terapia supresora
Entre las indicaciones para terapia de supresión se encuentran: mujeres con bacteriuria persistente y no resolución de la ITU a pesar del uso de múltiples esquemas antibióticos. El objetivo es evitar la progresión a infección sintomática.
Esta terapia consiste en manejo médico con antibiótico orientado por antibiograma además de medicación antibiótica continua, terapia profiláctica supresora:
1. Nitrofurantoína (100 mg/día al acostarse).
2. Fosfomicina (3 g dosis cada 7-10 días) y
3. Cefalexina (250 mg/día), terapia durante toda la gestación y hasta 4 semanas posparto.
Complicaciones maternas y fetales
Entre las complicaciones maternas se describen: anemia, ruptura prematura de membranas, hipertensión, falla renal transitoria, fiebre posparto, síndrome de dificultad respiratoria del adulto y sepsis. La sepsis ocurre en el 15-20% de los casos de pielonefritis. Entre las complicaciones fetales (presentes en 6-50% en pacientes con pielonefritis) se han descrito: alta incidencia de parto pretérmino, corioamnionitis clínica o subclínica, infección y bacteremia neonatal.
Seguimiento
El cultivo de orina y la presentación o persistencia de los síntomas clínicos constituye la base del seguimiento.
Después de un diagnóstico de bacteriuria asintomática el urocultivo se debe realizar cada mes. En infección urinaria baja la paciente debe ser evaluada 10 días después de completar el tratamiento antibiótico. En recurrencias se debe dar un nuevo ciclo de tratamiento orientado por el urocultivo y considerar la terapia supresora. En presencia de urocultivos postratamiento con recuentos menores de 10.000 UFC se recomienda repetir el urocultivo.
Infección del tracto urinario baja: situaciones especiales en ginecología
No se considera indicada la búsqueda de la infección asintomática en las mujeres no embarazadas.
Prevención
Las pacientes con factores de riesgo deben recibir recomendaciones preventivas. Las recomendaciones preventivas comprenden: ingesta de líquidos de rutina 1 o 2 litros/ día, micción lo más pronto posible cuando se presenta la urgencia urinaria, evitar la contaminación de la uretra con materia fecal, limpieza suave genital diaria, evitar aceites o jabones perfumados y desodorantes vaginales, lubricación adecuada durante la relación sexual, evitar la contaminación después de la relación sexual anal, desocupar la vejiga antes y lo más pronto posible después de la relación sexual, uso de ropa interior en algodón poco ajustada para mantener la textura seca del área genital y urinaria, control de la glicemia en pacientes diabéticas. El consumo de vitamina C, aunque sigue siendo una recomendación en muchos escenarios, tiene una evidencia inconsistente 63.
Tratamiento
Infección urinaria baja en la posmenopausia
El estrógeno vaginal puede ser una medida de profilaxis eficaz para la infección urinaria en mujeres posmenopáusicas, sus efectos colaterales incluyen sensibilidad en las mamas, sangrado vaginal o manchado, flujo vaginal no fisiológico, irritación vaginal, ardor y prurito. El estrógeno vaginal también es recomendado para el tratamiento de la vaginitis atrófica.
La presentación del estrógeno vaginal (ovulo, crema, larga vs corta acción) se determina por la preferencia de la paciente. Se indican los estrógenos conjugados orales 0.625 mg cada día, o el estrógeno tópico que corresponde a 0.5 mg de crema de estriol por vía vaginal cada noche durante 2 semanas, a continuación, se puede aplicar dos veces a la semana durante 8 meses.
Si están disponibles, la flujometría urinaria y la evaluación del residuo posmiccional se consideran pruebas opcionales en las mujeres posmenopáusicas para excluir causas complicadas de infección urinaria.
Infección urinaria recurrente
Varios estudios han demostrado una incidencia muy baja de anormalidades anatómicas (0 a 15%) en cistoscopias realizadas en pacientes con infección urinaria recurrente, por lo tanto, no parece necesario realizar una cistoscopia en todas las mujeres que se presentan con infección urinaria no complicada recurrente.
Cuando la infección urinaria es recurrente, el cultivo de orina y el análisis de la sensibilidad antibiótica debe ser realizado al menos una vez en el paciente sintomático.
Profilaxis antibiótica en pacientes no embarazadas
La profilaxis con baja dosis de antibiótico de manera continua es efectiva para prevenir infecciones del tracto urinario inferior (tabla 3). La paciente debe entender la posibilidad de presentarse efectos colaterales comunes, especialmente reacciones cutáneas y gastrointestinales. Se desconoce el antibiótico profiláctico óptimo, por lo que la elección depende de los patrones de resistencia local y la susceptibilidad previa.
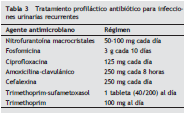
Diagnóstico microbiológico en infección del tracto urinario. Recomendaciones prácticas
El diagnóstico de ITU baja no complicada requiere una evaluación rigurosa de aspectos clínicos y microbiológicos. Las siguientes recomendaciones son una herramienta para la elaboración de Guías que faciliten un manejo apropiado de las muestras y una correcta interpretación clínica de los resultados.
1. Solicitud médica: se sugiere incluir en la solicitud, el método de recolección de muestra utilizado, uso previo o actual de antimicrobianos, embarazo, edad, características especiales (ej. vejiga neurogénica), etc.
2. Colección de muestras: para muestras de orina colectadas por micción espontánea, se recomienda lavado de genitales externos con agua y jabón, instruir a las mujeres para que separen los labios externos al iniciar la micción y en los hombres no circuncidados para que retraigan el prepucio. Recoger el chorro medio de la micción en un frasco estéril de boca ancha y cierre hermético. Para las muestras tomadas por cateterismo vesical, se recomienda asepsia rigurosa del meato urinario y descarte de los primeros mililitros de orina para evitar ITU iatrogénica. En los pacientes que tienen sonda vesical permanente (Foley), limpiar el puerto de colección y tomar por aspirado con jeringa. No se recomienda tomar de la bolsa colectora.
3. Transporte de muestras: transportar la muestra al laboratorio en el menor tiempo posible. Si no se consigue procesar antes de 1 hora, refrigerar a 4°C o utilizar tubos de transporte que incluyan conservantes para orina (ácido bórico). Procesar la muestra antes de 24 horas.
4. En la tabla 4 se muestran los métodos de tamizaje para el diagnóstico presuntivo de ITU. Recomendaciones para la siembra de muestras: utilizar los medios de cultivo apropiados que permitan el crecimiento de Gram positivos y Gram negativos. Por practicidad se recomiendan medios como agar CLED, agares cromogénicos, etc. Estos inhiben el fenómeno de Swarming de Proteus spp., y facilitan la identificación presuntiva del microorganismo y una fácil determinación de cultivos contaminados. Para el uso de agares cromogénicos se recomienda protegerlos de la luz directa, utilizar un método confirmatorio para la identificación y susceptibilidad antimicrobiana. Para el sembrado utilice asa bacteriológica calibrada a 0,01 mL para muestras espontáneas, y 0,001 mL para muestras por técnica invasiva. Realice siembra por rejilla de acuerdo a la técnica empleada por protocolo en su laboratorio. Incubar en aerobiosis por un periodo mínimo de 16 horas de incubación entre 35-37°C. No se requiere CO 2 suplementario 67,68.
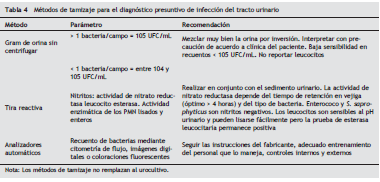
Nota: Las muestras de orina no deben sembrarse en botellas de hemocultivo automatizado en razón a los siguientes argumentos:
La composición de las botellas está diseñada para ser compatible con muestras de sangre únicamente.
Las cantidades de antibióticos en orina pueden ser hasta 1.000 veces superiores a las concentraciones séricas. Lo cual se traduce en una inhibición insuficiente por parte de los polímeros y resinas incluidos en las botellas.
El recuento de colonias sigue siendo el parámetro definitivo para el diagnóstico microbiológico de ITU. En la tabla 5 se sugieren estrategias para la realización de informes microbiológicos para ITU.

5. Si bien tradicionalmente el punto de corte para la determinación de urocultivos significativos ha sido 105 UFC/mL, se sugiere considerar las siguientes condiciones para valorar recuentos inferiores:
Punción suprapúbica: cualquier recuento es importante, pero evaluar si puede ser un contaminante de piel por técnica aséptica deficiente durante el procedimiento.
Mujer con síndrome miccional y leucocituria: recuentos ≥ 102 UFC/mL pueden ser importantes. Correlacionar con antecedentes clínicos y factores de riesgo.
Urocultivos en hombres: recuentos ? 103 UFC/mL sumado a síndrome miccional pueden tener importancia clínica.
Sugerencia para el laboratorio: en cultivos con crecimiento monomicrobiano y recuento por debajo de 105 UFC/mL, reportar al clínico el recuento de colonias obtenido con una identificación mínima para que se realice una correlación de este hallazgo con las características individuales del paciente. Ej. 103 UFC/mL de Enterobacteriaceae 69,71.
6. Antibiogramas para uropatógenos:
Aislamientos Gram negativos de comunidad, tamizar de primera línea con antibióticos orales: ampicilina/sulbactam, cefalexina (por medio de cefalotina como se recomienda por CLSI), nitrofurantoína, norfloxacina, fosfomicina y trimetoprim/ sulfa.
Aislamientos Gram negativos de pacientes hospitalizados o con resistencia intrínseca o adquirida a los antibióticos anteriores se sugiere tamizar con: ciprofloxacina, piperacilina/ tazobactam, ceftriaxona/cefotaxima, ceftazidima, cefepima, ertapenem, imipenem, doripenem, meropenem, amikacina y gentamicina. Incluir la prueba autómatica de BLEEs y realizar la prueba de Hodge modificada cuando se considere apropiado.
Aislamientos de enterococo, realizar tamizaje con ampicilina, ciprofloxacina, nitrofurantoína y fosfomicina (interpretar en E. faecalis únicamente). S. saprophyticus no requiere antibiograma porque responde bien a los antibióticos de primera línea mencionados anteriormente pero presenta resistencia intrínseca a fosfomicina.
Para S. agalactiae se sugiere realizar antibiograma cuando se presente alto riesgo de anafilaxia con betalactámicos (que constituyen el tratamiento de elección), incluir eritromicina y clindamicina, realizar D-test y de acuerdo a su resultado reportar al médico solo el dato de clindamicina.
Omitir del reporte a eritromicina por recomendación CLSI/ CDC 71 . En la tabla 6 se mencionan algunas consideraciones especiales de reporte por grupo de microorganismos.
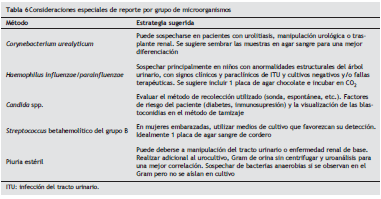
Situaciones especiales: para cefalosporinas orales, tamizar con cefalotina de acuerdo a recomendación vigente CLSI. Para cefazolina en el tratamiento de ITU, utilizar puntos de corte 2009. Solo reportar en E. coli , Klebsiella spp., y P. mirabilis . Para fosfomicina, utilizar únicamente método de disco difusión e interpretar solo para E. coli y E. faecalis de acuerdo a CLSI. Ignorar las colonias que se observan dentro de los halos de inhibición 70,71.
Conflicto de intereses
Este consenso fue realizado con la colaboración y patrocinio del Grupo Zambon. Sin embargo, dicho grupo no tuvo participación en la elaboración y no intervino en los contenidos del presente artículo.
Agradecimientos
Agradecemos al Dr. Rafael Cantón por su asesoría científica y aporte en la realización del consenso. Al Grupo Zambon por su colaboración y patrocinio.
* Autor para correspondencia.
Correo electrónico: mariavirginia.villegas@gmail.com (M.V. Villegas)
0123-9392/$ - see front matter © 2013 ACIN. Publicado por Elsevier España, S.L. Todos los derechos reservados.
Bibliografía
1. Ronald AR, Harding GK. Complicated urinary tract infections. Infect Dis Clin North Am. 1997;11(:583-92. [ Links ]
2. Foxman B, Brown P. Epidemiology of urinary tract infections: transmission and risk factors, incidence, and costs. Infect Dis Clin North Am. 2003;17:227-41. [ Links ]
3. Foxman B, Gillespie B, Koopman J, Zhang L, Palin K, Tallman P, et al. Risk factors for second urinary tract infection among college women. Am J Epidemiol. 2000;151:1194-205 [ Links ] Scholes D, Hooton TM, Roberts PL, Stapleton AE, Gupta K, Stamm WE. Risk Factors for recurrent urinary tract infection in young women. J Infect Dis. 2000;182:1177-82. [ Links ]
5. Strom BL, Collins M, West SL, Kreisberg J, Weller S. Sexual activity, contraceptive use, and other risk factors for symptomatic and asymptomatic bacteriuria. A case-control study. Ann Intern Med. 1987;107:816-23. [ Links ]
6. Nicolle LE. Urinary tract infection in long-term-care facility residents. Clin Infect Dis Off Publ Infect Dis Soc Am. 2000;31:757-61. [ Links ]
7. Fihn SD, Latham RH, Roberts P, Running K, Stamm WE. Association between diaphragm use and urinary tract infection. JAMA J Am Med Assoc. 1985;254:240-5. [ Links ]
8. Hooton TM, Scholes D, Hughes JP, Winter C, Roberts PL, Stapleton AE, et al. A prospective study of risk factors for symptomatic urinary tract infection in young women. N Engl J Med. 1996;335:468-74. [ Links ]
9. Bent S, Nallamothu BK, Simel DL, Fihn SD, Saint S. Does this woman have an acute uncomplicated urinary tract infection? JAMA J Am Med Assoc. 2002;287:2701-10. [ Links ]
10. Falagas ME, Kotsantis IK, Vouloumanou EK, Rafailidis PI. Antibiotics versus placebo in the treatment of women with uncomplicated cystitis: a meta-analysis of randomized controlled trials. J Infect. 2009;58:91-102. [ Links ]
11. Katchman EA, Milo G, Paul M, Christiaens T, Baerheim A, Leibovici L. Three-day vs longer duration of antibiotic treatment for cystitis in women: systematic review and meta-analysis. Am J Med. 2005;118:1196-207. [ Links ]
12. Faro S, Fenner DE. Urinary tract infections. Clin Obstet Gynecol. 1998;41:744-54. [ Links ]
13. Johnson JR, Stamm WE. Diagnosis and treatment of acute urinary tract infections. Infect Dis Clin North Am. 1987;1:773-91. [ Links ]
14. Gupta K, Hooton TM, Naber KG, Wullt B, Colgan R, Miller LG, et al. International clinical practice guidelines for the treatment of acute uncomplicated cystitis and pyelonephritis in women: A 2010 update by the Infectious Diseases Society of America and the European Society for Microbiology and Infectious Diseases. Clin Infect Dis Off Publ Infect Dis Soc Am. 2011;52:e103-20. [ Links ]
15. Gupta K, Stamm WE. Outcomes associated with trimethoprim/ sulphamethoxazole (TMP/SMX) therapy in TMP/SMX resistant community- acquired UTI. Int J Antimicrob Agents. 2002;19:554-6. [ Links ]
16. Hurlbut TA 3rd, Littenberg B. The diagnostic accuracy of rapid dipstick tests to predict urinary tract infection. Am J Clin Pathol. 1991;96:582-8. [ Links ]
17. Hooton TM. Uncomplicated urinary tract infection. N Engl J Med. 2012;366:1028-37. [ Links ]
18. Knothe H, Schäfer V, Sammann A, Shah PM. Influence of fosfomycin on the intestinal and pharyngeal flora of man. Infection. 1991;19:18-20. [ Links ]
19. Castro-Orozco R, Barreto-Maya A, Guzman-Alvarez H, Ortega- Quiroz R, Benitez-Peña L. Patrones de resistencia antimicrobiana en uropatógenos gramnegativos aislados de pacientes ambulatorios y hospitalizados Cartagena, 2005-2008. Rev Salud Publica (Bogota). 2010;12:1010-9. [ Links ]
20. Gomez C, Plata M, Sejnaui J, Rico C, Vanegas-Gonzales S. Resistencia de la E. coli en urocultivos de pacientes con sospecha de infección urinaria intra y extra-hospitalaria en la Fundación Santa Fe de Bogotá. Revista Urología Colombiana, 2009;18:53-8. [ Links ]
21. Bermejo J, Bencomo B, Arnesi N, Lesnaberes P, Borda N, Notario R. Alta correlación entre el consumo de ciprofloxacina y la prevalencia de K. pneumoniae productora de ß -lactamasas de espectro extendido. Rev Chil Infectología. 2006;23:316-20. [ Links ]
22. Kahlmeter G, ECO.SENS. An international survey of the antimicrobial susceptibility of pathogens from uncomplicated urinary tract infections: the ECO.SENS Project. J Antimicrob Chemother. 2003;51:69-76. [ Links ]
23. Rubin RH, Shapiro ED, Andriole VT, Davis RJ, Stamm WE. Evaluation of new anti-infective drugs for the treatment of urinary tract infection. Infectious Diseases Society of America and the Food and Drug Administration. Clin Infect Dis Off Publ Infect Dis Soc Am. 1992;15 Suppl 1:S216-27. [ Links ]
24. Nicolle LE, Bradley S, Colgan R, Rice JC, Schaeffer A, Hooton TM, et al. Infectious Diseases Society of America guidelines for the diagnosis and treatment of asymptomatic bacteriuria in adults. Clin Infect Dis Off Publ Infect Dis Soc Am. 2005;40:643-54. [ Links ]
25. Hooton TM, Scholes D, Stapleton AE, Roberts PL, Winter C, Gupta K, et al. A prospective study of asymptomatic bacteriuria in sexually active young women. N Engl J Med. 2000;343:992-7. [ Links ]
26. Zhanel GG, Nicolle LE, Harding GK. Prevalence of asymptomatic bacteriuria and associated host factors in women with diabetes mellitus. The Manitoba Diabetic Urinary Infection Study Group. Clin Infect Dis Off Publ Infect Dis Soc Am. 1995;21:316-22. [ Links ]
27. Bachman JW, Heise RH, Naessens JM, Timmerman MG. A study of various tests to detect asymptomatic urinary tract infections in an obstetric population. JAMA J Am Med Assoc. 1993;270:1971-4. [ Links ]
28. Ipe DS, Sundac L, Benjamin WH Jr, Moore KH, Ulett GC. Asymptomatic bacteriuria: prevalence rates of causal microorganisms, etiology of infection in different patient populations, and recent advances in molecular detection. FEMS Microbiol Lett. 2013;346:1-10. [ Links ]
29. Mokube MN, Atashili J, Halle-Ekane GE, Ikomey GM, Ndumbe PM. Bacteriuria amongst pregnant women in the Buea Health District, Cameroon: Prevalence, predictors, antibiotic susceptibility patterns and diagnosis. PloS One. 2013;8:e71086. [ Links ]
30. Awolude OA, Adesina OA, Oladokun A, Mutiu WB, Adewole IF. Asymptomatic bacteriuria among HIV positive pregnant women. Virulence. 2010;1:130-3. [ Links ]
31. Iwalokun BA, Iwalokun SO, Hodonu SO, Aina OA, Agomo PU. Evaluation of microalbuminuria in relation to asymptomatic bacteruria in Nigerian patients with sickle cell anemia. Saudi J Kidney Dis Transplant Off Publ Saudi Cent Organ Transplant Saudi Arab. 2012;23:1320-30. [ Links ]
32. Renko M, Tapanainen P, Tossavainen P, Pokka T, Uhari M. Metaanalysis of the significance of asymptomatic bacteriuria in diabetes. Diabetes Care. 2011;34:230-5. [ Links ]
33. Papazafiropoulou A, Daniil I, Sotiropoulos A, Balampani E, Kokolaki A, Bousboulas S, et al. Prevalence of asymptomatic bacteriuria in type 2 diabetic subjects with and without microalbuminuria. BMC Res Notes. 2010;3:169. [ Links ]
34. Matthews SJ, Lancaster JW. Urinary tract infections in the elderly population. Am J Geriatr Pharmacother. 2011;9:286-309. [ Links ]
35. Cordero-Ampuero J, González-Fernández E, Martínez-Vélez D, Esteban J. Are antibiotics necessary in hip arthroplasty with asymptomatic bacteriuria? Seeding risk with/without treatment. Clin Orthop. 2013 Feb 21. [ Links ]
36. Mabbett AN, Ulett GC, Watts RE, Tree JJ, Totsika M, Ong CY, et al. Virulence properties of asymptomatic bacteriuria E. coli. Int J Med Microbiol IJMM. 2009;299:53-63. [ Links ]
37. Vejborg RM, de Evgrafov MR, Phan MD, Totsika M, Schembri MA, Hancock V. Identification of genes important for growth of asymptomatic bacteriuria E. coli in urine. Infect Immun. 2012;80:3179-88. [ Links ]
38. Varli M, Guruz H, Aras S, Yalcin A, Atli T, Turgay M. Asymptomatic bacteriuria among the elderly living in the community: Prevalence, risk factors and characteristics. Eur Geriatr Med. 2012;3:87-91. [ Links ]
39. Chen SL, Jackson SL, Boyko EJ. Diabetes mellitus and urinary tract infection: epidemiology, pathogenesis and proposed studies in animal models. J Urol. 2009;182(6 Suppl):S51-6. [ Links ]
40. Matteucci E, Troilo A, Leonetti P, Giampietro O. Significant bacteriuria in outpatient diabetic and non-diabetic persons. Diabet Med J Br Diabet Assoc. 2007;24:1455-9. [ Links ]
41. Odigie J, Anugweje K. Asymptomatic bacteriuria in pregnancy in Port Harcourt. Asian Pac J Trop Med. 2010;3:580-3. [ Links ]
42. Chowdhury F, Sarkar K, Branche A, Kim J, Dwek P, Nangit A, et al. Preventing the inappropriate treatment of asymptomatic bacteriuria at a community teaching hospital. J Community Hosp Intern Med Perspect. 2012;2. doi:10.3402/jchimp.v2i2.17814. [ Links ]
43. Raz R. Asymptomatic bacteriuria. Clinical significance and management. Int J Antimicrob Agents. 2003;22 Suppl 2:45-7. [ Links ]
44. Jain V, Das V, Agarwal A, Pandey A. Asymptomatic bacteriuria & obstetric outcome following treatment in early versus late pregnancy in north Indian women. Indian J Med Res. 2013;137:753-8. [ Links ]
45. Nicolle LE. Asymptomatic bacteriuria: review and discussion of the IDSA guidelines. Int J Antimicrob Agents. 2006;28 Suppl 1:S42-8. [ Links ]
46. Lee SE, Kim KT, Park YS, Kim YB. Association between asymptomatic urinary tract infection and postoperative spine infection in elderly women : A retrospective analysis study. J Korean Neurosurg Soc. 2010;47:265-70. [ Links ]
47. Hatton KW, Flynn JD, Lallos C, Fahy BG. Integrating evidencebased medicine into the perioperative care of cardiac surgery patients. J Cardiothorac Vasc Anesth. 2011;25:335-46. [ Links ]
48. Sayin Kutlu S, Aybek Z, Tekin K, Okke D, Akalin S, Altintas S, et al. Is short course of antimicrobial therapy for asymptomatic bacteriuria before urologic surgical procedures sufficient? J Infect Dev Ctries. 2012;6:143-7. [ Links ]
49. Herr HW. Should antibiotics be given prior to outpatient cystoscopy? A plea to urologists to practice antibiotic stewardship. Eur Urol. 2013 Aug 30. doi:pii:S0302-2838(13)00906-8. 10.1016/j.eururo.2013.08.054. [ Links ]
50. Drekonja DM, Zarmbinski B, Johnson JR. Preoperative urine cultures at a veterans affairs medical center. JAMA Intern Med. 2013;173:71-2. [ Links ]
51. Cumitech 2c: laboratory diagnosis of urinary tract infections. [S.l.]: Amer Soc For; 2009. [ Links ]
52. Hantush Zadeh S, Khosravi D, Shahbazi F, Kaviani Jebeli Z, Ahmadi F, Shirazi M. Idiopathic urinary findings and fetal growth restriction in low risk pregnancy. Eur J Obstet Gynecol Reprod Biol. 2013;171:57-60. [ Links ]
53. Cunnington M, Kortsalioudaki C, Heath P. Genitourinary pathogens and preterm birth. Curr Opin Infect Dis. 2013;26:219-30. [ Links ]
54. Lumbiganon P, Laopaiboon M, Thinkhamrop J. Screening and treating asymptomatic bacteriuria in pregnancy. Curr Opin Obstet Gynecol. 2010;22:95-9. [ Links ]
55. Smaill F. Asymptomatic bacteriuria in pregnancy. Best Pract Res Clin Obstet Gynaecol. 2007;21:439-50. [ Links ]
56. Herráiz MA, Hernández A, Asenjo E, Herráiz I. [Urinary tract infection in pregnancy]. Enferm Infecc Microbiol Clin. 2005;23 Suppl 4:40-6. [ Links ]
57. Macejko AM, Schaeffer AJ. Asymptomatic bacteriuria and symptomatic urinary tract infections during pregnancy. Urol Clin North Am. 2007;34:35-42. [ Links ]
58. Vazquez JC, Abalos E. Treatments for symptomatic urinary tract infections during pregnancy. Cochrane Database Syst Rev. 2011;(1):CD002256. [ Links ]
59. Dattaray C, Mandal D, Shankar U, Bhattacharya P, Mandal S. Obstetric patients requiring high-dependency unit admission in a tertiary referral centre. Int J Crit Illn Inj Sci. 2013;3:31-5. [ Links ]
60. Alós Cortés JI, Andreu Domingo A, Arribas Mir L, Cabero Roura L, de Cueto López M, López Sastre J, et al. [Prevention of Neonatal Group B Sreptococcal Infection. Spanish Recommendations. Update 2012. SEIMC/SEGO/SEN/SEQ/SEMFYC Consensus Document]. Enferm Infecc Microbiol Clin. 2013;31:159-72. [ Links ]
61. Young JL, Soper DE. Urinalysis and urinary tract infection: update for clinicians. Infect Dis Obstet Gynecol. 2001;9:249-55. [ Links ]
62. Schneeberger C, Geerlings SE, Middleton P, Crowther CA. Interventions for preventing recurrent urinary tract infection during pregnancy. Cochrane Database Syst Rev. 2012;11:CD009279. [ Links ]
63. Krcmery S, Hromec J, Demesova D. Treatment of lower urinary tract infection in pregnancy. Int J Antimicrob Agents. 2001;17:279-82. [ Links ]
64. Ochoa-Brust GJ, Fernández AR, Villanueva-Ruiz GJ, Velasco R, Trujillo-Hernández B, Vásquez C. Daily intake of 100 mg ascorbic acid as urinary tract infection prophylactic agent during pregnancy. Acta Obstet Gynecol Scand. 2007;86:783-7. [ Links ]
65. Pigrau-Serrallach C. [Recurrent urinary tract infections]. Enferm Infecc Microbiol Clin. 2005;23 Suppl 4:28-39. [ Links ]
66. Baron EJ, Miller JM, Weinstein MP, Richter SS, Gilligan PH, Thomson RB Jr, et al. A guide to utilization of the microbiology laboratory for diagnosis of infectious diseases: 2013 recommendations by the Infectious Diseases Society of America (IDSA) and the American Society for Microbiology (ASM)(a). Clin Infect Dis Off Publ Infect Dis Soc Am. 2013;57:e22-e121. [ Links ]
67. Anacleto FE, Resontoc LP, Padilla GH. Bedside diagnosis of outpatient childhood urinary tract infection using three-media dipslide culture test. Pediatr Nephrol Berl Ger. 2009;24:1539-43. [ Links ]
68. Kubik MJ, McCarter YS. Controversies in the diagnosis of urinary tract infections. Clin Microbiol Newsl. 2012;34:185-91. [ Links ]
69. Lepe-Jimenez J, Coira-Nieto A, Cacho J, Cañavate C, Andreu-Domingo A. Diagnóstico microbiológico de las infecciones del tracto urinario. Procedimientos en Microbiología Clínica. SEIMIC; 2010. [ Links ]
70. Cockerill FR. Performance standards for antimicrobial susceptibility testing: twenty-third informational supplement ; M100 - S23. Wayne, PA: CLSI; 2013. [ Links ]
71. CLSI. 2010. Performance standards for antimicrobial susceptibility testing. twentieth informational supplement. Report No.: CLSI document M100-S20. Clinical and Laboratory Standards Institute, Wayne, PA. [ Links ]













