Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Infectio
Print version ISSN 0123-9392
Infect. vol.19 no.3 Bogotá Sept./Dec. 2015
https://doi.org/10.1016/j.infect.2015.02.002
ORIGINAL
http://dx.doi.org/10.1016/j.infect.2015.02.002
Factores de riesgo asociados a complicaciones por Bordetella pertussis en la Fundación Hospital de la Misericordia, 2009-2013
María del Pilar Montilla Velásquez a, * , Germán Camacho Moreno a, Sandra Liliana Romero b y Karen Gómez a
a Departamento de Pediatría, Universidad Nacional de Colombia-Fundación Hospital de la Misericordia, Bogotá D.C, Colombia
b Comité de Infecciones, Fundación Hospital de la Misericordia, Bogotá D.C, Colombia
Recibido el 16 de diciembre de 2014; aceptado el 3 de febrero de 2015
Disponible en Internet el 10 de abril de 2015
Resumen
Objetivo: Caracterizar factores de riesgo asociados a complicaciones en los pacientes con tosferina en 2009-2013.
Materiales y métodos: Estudio de casos y controles. Identificación de factores de riesgo asociados a complicaciones en pacientes con Bordetella pertussis , confirmados con reacción en cadena de la polimerasa.
Resultados: Se caracterizó a 96 pacientes. Un total de 76% eran menores de 6 meses, media de 4,56 ± 6,8 meses. El 58,3% eran niños y el 41,5%, niñas. Un 51% tuvo alguna complicación. Al 58% se les hospitalizó en cuidado crítico. Un 9,4% tuvo sepsis y el 14,6% requirió ventilación asistida. Un 4,2% fallecieron. La media de estancia en cuidado crítico fue de 8,75 días ( ± 85) y hospitalaria de 13,92 días ( ± 12,81). Se identificaron los siguientes factores de riesgo asociados a complicación: noción de contagio (OR: 2,20), ausencia de vacunación (OR: 3,31). Clínica: cianosis (OR: 4,07), deshidratación (OR: 2,72), taquicardia (OR: 2,64), taquipnea (OR: 3,94), desaturación (OR: 3,34). Paraclínica: coinfección bacteriana (OR: 7,66), linfocitosis (OR: 3,18), trombocitosis (OR: 3,038).
Conclusión: Los antecedentes, clínica y paraclínicos pueden definir pacientes con infección por Bordetella pertussis en riesgo de complicaciones e ingreso en cuidado crítico.
PALABRAS CLAVE
Tosferina; Factores de riesgo; Complicaciones; Reacción en cadena de la polimerasa
© 2014 ACIN. Publicado por Elsevier España, S.L.U. Este es un artículo Open Access bajo la licencia CC BY-NC-ND ( http://creativecommons.org/licenses/by-nc-nd/4.0/ ).
Risk factors associated with complications of Bordetella pertussis at the Fundacion Hospital de la Misericordia, 2009-2013
Abstract
Objective: To characterize the risk factors associated with complications in patients infected with Bordetella pertussis , 2009-2013.
Material and methods: Case-control study. Identification of risk factors associated with complications in patients with Bordetella pertussis , confirmed by polymerase chain reaction.
Results: A total of 96 patients were characterized. 76% were younger than 6 months, mean 4.56 ± 6.8 months; there were 58.3% boys and 41.5% girls. A total of 51% had complications. Some 58% were hospitalized in critical care. Sepsis occurred in 9.4% patients, and 14.6% required assisted ventilation. A total of 4.2% died. The mean critical care stay was 8.75 days ( ± 85) and the mean hospital stay was 13.92 ± 12.81 days. The following risk factors associated with complications were identified: notion of contagion (OR: 2.20), no vaccination (OR: 3.31). Clinical: (OR: 4.07) cyanosis, dehydration (OR: 2.72), tachycardia (OR: 2.64), tachypnea (OR: 3.94), desaturation (OR: 3.34). Paraclinical: Bacterial co-infection (OR: 7.66), lymphocytosis (OR: 3.18), thrombocytosis (OR: 3.038).
Conclusion: Background, clinical and paraclinical factors can identify patients with B. pertussis infection at risk for complications and admission to the critical care unit.
KEYWORDS
Whooping cough; Risk factors; Complications; Polymerase chain Reaction
© 2014 ACIN. Published by Elsevier España, S.L.U. This is an open access article under the CC BY-NC-ND license ( http://creativecommons.org/licenses/by-nc-nd/4.0/ ).
0123-9392/© 2014 ACIN. Publicado por Elsevier España, S.L.U. Este es un artículo Open Access bajo la licencia CC BY-NC-ND ( http://creativecommons.org/licenses/by-nc-nd/4.0/ ).
Introducción
La tosferina es una enfermedad infectocontagiosa prevenible, causada por la bacteria Bordetella pertussis (B. pertussis). Causa gran morbimortalidad y es generadora de importantes costos al sistema de salud. Su incidencia ha aumentado recientemente, con desenlaces fatales, en los últimos años, en lactantes y neonatos, siendo la letalidad reportada en Colombia de casi 3 casos por cada 100 niños 1 .
Para efectos de este estudio, el evento se definió según los criterios del Instituto Nacional de Salud 2 (INS):
« Menor de 3 meses: toda infección respiratoria aguda, acompañada al menos de uno de los siguientes síntomas: tos en accesos, estridor, apnea, cianosis o vómito después de toser.
De 3 meses a 12 años: toda infección respiratoria con tos de más de una semana de duración acompañada de uno o más de los siguientes síntomas: tos paroxística, estridor o vómito después de la tos, sin otra causa aparente. O niños con tos paroxística intensa acompañada de estridor de cualquier tiempo de evolución.
Mayores de 12 años: toda infección respiratoria acompañada de tos prolongada de más de 2 semanas de duración y presencia o no de paroxismos, expectoración y vómito. »
El periodo de incubación es de 7 a 10 días y cursa con 3 fases de expresión clínica, siendo en la fase espasmódica fácilmente transmisible, con una tasa de ataque de hasta el 90% en personas no inmunes en contacto con el enfermo 2,3 .
La enfermedad causa múltiples complicaciones: neumonía, otitis media, sepsis, convulsiones, encefalopatía, desnutrición, deshidratación, hemorragia subconjuntival, epistaxis, edema facial, neumotórax, hematomas subdurales, hernias, prolapso rectal, incontinencia urinaria y fracturas costales 4 . El ingreso a cuidado crítico e inicio de ventilación mecánica es frecuente en menores de 3 meses y se debe a insuficiencia respiratoria secundaria a apnea y a neumonía bacteriana 5 .
En los neonatos y lactantes con vacunación incompleta (menos de 3 dosis), puede ser muy grave, siendo mortal en el 1% de los casos 6 . La complicación más frecuente es neumonía (6-15%), falla ventilatoria, hiperleucocitosis e hipertensión pulmonar 7 .
Aunque los factores de riesgo para enfermedad grave han sido definidos, el curso clínico de los niños que requieren cuidado intensivo no está descrito completamente.
La caracterización y evaluación de los factores de riesgo asociados a complicaciones e ingreso a cuidado crítico de esta enfermedad en la Fundación Hospital de la Misericordia (HOMI) está indocumentado.
Metodología
Estudio realizado en HOMI, en pacientes hospitalizados con diagnóstico confirmado por PCR con infección con B. pertussis , durante el periodo de 2009-2013. El diseño empleado fue de casos y controles y se identificaron los factores de riesgo asociados a complicaciones. Los casos y controles se aparearon por sexo.
Para definir los casos y los controles e ingresar al estudio, ambos grupos debían cumplir con la definición de caso confirmado por laboratorio del INS: « Caso probable confirmado por el laboratorio mediante cultivo, PCR o IFD con resultado positivo » 2 . En este caso todos los pacientes tuvieron PCR para Bordetella positivo, y se definieron así:
- Caso: paciente con alguna complicación definida como apnea, bradicardia, neumonía, desaturación repetida, falla ventilatoria, convulsión, encefalopatía, choque, paro cardiorrespiratorio, y definición de caso confirmado del INS 2 .
- Control: paciente hospitalizado en cualquier dependencia de la institución, sin complicaciones definidas en el punto anterior, que cumpla con la definición de caso confirmado del INS 2 .
La unidad de análisis fue la ficha de vigilancia epidemiológica con registro de confirmación de la enfermedad por PCR y las historias clínicas de los pacientes durante su hospitalización.
El cálculo de la muestra se basó en el estudio titulado Pertussis requiring intensive care 8 , para el cálculo de un OR de 5,26 (1,48 a 12,85) para linfocitosis con los siguientes parámetros: proporción de casos expuestos: 78%, proporción de controles expuestos: 33%, número de controles por caso: uno, y una confianza del 95,0%. Al analizar a todos los pacientes diagnosticados durante los años de estudio, se obtuvo una potencia de 95,5%.
Se realizó un análisis descriptivo univariado y bivariado. Las variables se agruparon según la presencia o no de complicación y se analizaron a través de la prueba chi cuadrado. Se realizó el cálculo de OR de cada una de las variables dicotómicas para evaluar su asociación a complicaciones. Se efectuó un análisis multivariado para eliminar factores de confusión. El proyecto fue evaluado y aprobado por el Comité de Ética e Investigación de HOMI.
Resultados
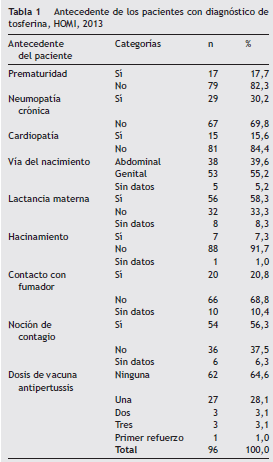
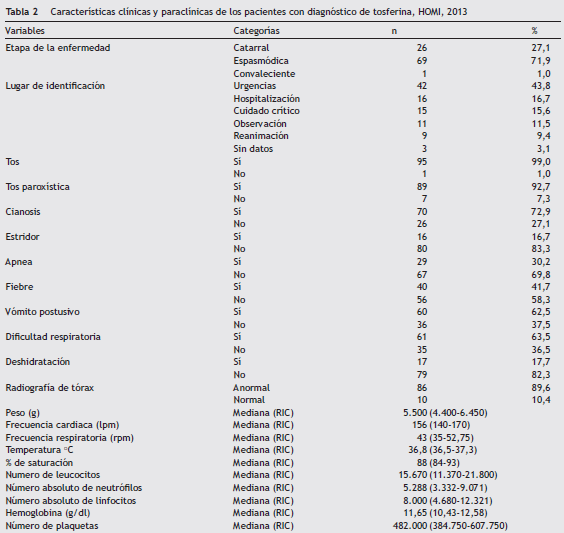
Se analizaron 96 historias de los niños que cumplieron con los criterios de inclusión. El 76% tuvo una edad menor a 6 meses, con una media de 4,56 meses ( ± 6,8 meses), y un rango entre 1,2 y 52,8 meses. El 58,3% de los casos fueron niños y el 41,5% fueron niñas. Dentro de los antecedentes hubo mayor frecuencia de prematuridad y cardiopatía ( tabla 1 ). Se observó, además, que más de la mitad de los pacientes no tuvo vacunación contra B. pertussis ( tabla 1 ). Se caracterizaron las variables clínicas y paraclínicas. La identificación de los casos fue mayor en urgencias y en la fase espasmódica de la enfermedad ( tabla 2 ).
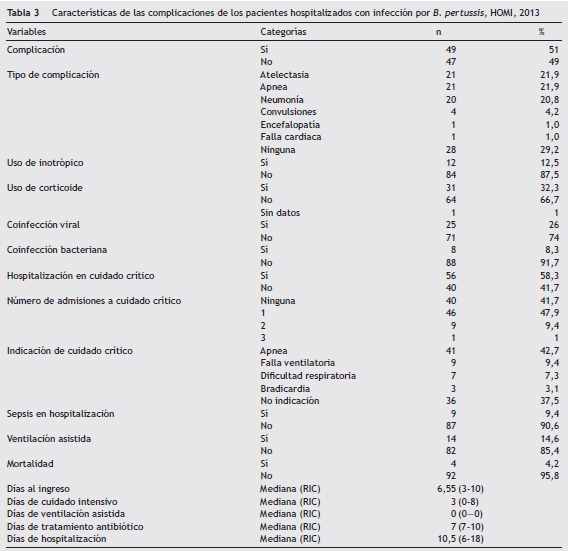
El 51% de los casos tuvo algún evento que complicó su evolución ( tabla 3 ). Las más frecuentes fueron atelectasia (21,9%), apnea (21,9%) y neumonía (20,8%). El 26% tuvo coinfección viral y el 8% coinfección bacteriana. Esta última, definida como hemocultivo positivo durante su hospitalización. El 58% de los pacientes requirió hospitalización en cuidado crítico: 42% por apnea, 9,4% por sepsis y el 14,6% por ventilación asistida. El 4,2% de los pacientes fallecieron. El promedio de estancia en cuidado crítico fue de 8,75 días ( ± 85) con un rango de entre 0 y 44 días.
En la tabla 4 se observa la distribución de las variables estudiadas según casos y controles. Los siguientes factores de riesgo se asociaron a complicación: edad menor a 2 meses con un OR de 3,31 (IC 95%: 1,232-8,939; p = 0,015) y edad menor a 4 meses (OR: 4,061; IC 95%: 1,43-11,501; p = 0,006).
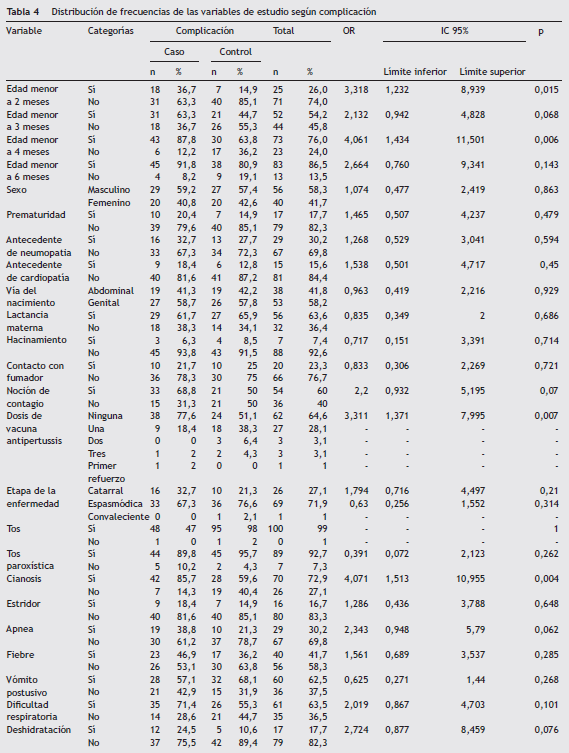
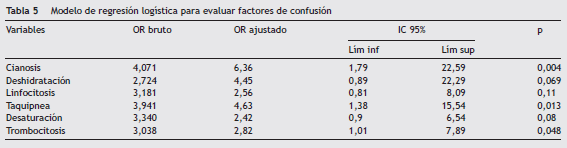
Antecedentes: Noción de contagio positivo según anamnesis, con un OR de 2,20 (IC 95%: 0,93-5,19; p = 0,07), no estadísticamente significativa y ausencia de vacunación antipertussis (OR: 3,31; IC 95%: 1,37-7,99; p = 0,007). Clínica: cianosis (OR: 4,07; IC 95%: 1,51-10,95; p = 0,004), deshidratación (OR: 2,72; IC 95%: 0,877-8,459; p = 0,076), taquicardia (OR: 2,645; IC 95%: 1,004-6,967; p = 0,045), taquipnea (OR: 3,941; IC 95%: 1,472-10,548; p = 0,005) y desaturación (OR: 3,340; IC 95%: 1,440-7,751; p = 0,004), Paraclínica: coinfección bacteriana (OR: 7,667; IC 95%: 0,905-64,943; p = 0,059), linfocitosis (OR: 3,18; IC 95%: 1,219-8,300; p = 0,015), trombocitosis (OR: 3,038; IC 95%: 1,283-7,196; p= 0,01). El análisis de regresión logística de los factores de riesgo ajustados fueron cianosis, taquipnea y trombocitosis ( tabla 5 ).
Discusión
La tosferina es una enfermedad reemergente que, según la Organización Mundial de la Salud, muestra un aumento progresivo en la mortalidad infantil, en países en vía de desarrollo, ocupando el quinto puesto entre las causas de muerte prevenibles con la vacunación 9,10.
La identificación de los factores asociados a complicación es una forma de dirigir el esfuerzo y los recursos objetivamente. Al analizar los pacientes estudiados, el perfil de paciente infectado con B. pertussis es un lactante menor, masculino, con noción de contagio positivo, sin vacunación previa. Estos 2 últimos factores son riesgo para complicación. Se ha descrito que la vacunación requiere un mínimo de 2 dosis para ser eficaz; por tanto, son los lactantes de menos de 4 meses los de mayor riesgo 3 . La vacunación protege contra las formas graves en los neonatos y lactantes menores, a partir de la administración de la primera dosis 11 .
En Colombia la enfermedad se presenta con mayor frecuencia en la población menor de 5 años, con afectación predominante en menores de un año 12 . En este estudio el riesgo de complicación fue mayor en menores de 2 y 4 meses. En la literatura, se han descrito factores de riesgo asociados a mortalidad, entre los que se encuentran: edad menor a un año, vacunación ausente o incompleta, neumonía, taquicardia sinusal inexplicada y convulsiones 13 .
En este estudio la presencia de atelectasias, apnea, neumonía, convulsiones, encefalopatía y falla cardiaca constituyeron las complicaciones más frecuentes.
El diagnóstico de la mayoría de los pacientes se identificó en el servicio de urgencias, en la fase espasmódica de la enfermedad, reconocidos por la definición de caso 2 . Casi todos tuvieron tos cianosante y emetizante y, dentro de los síntomas más relevantes, apnea y dificultad respiratoria, dada por taquicardia, taquipnea, y desaturación. Estos últimos fueron factores asociados a complicación.
La presencia de linfocitosis y trombocitosis en el hemograma se asoció a complicación, al igual que la coinfección bacteriana en el primer hemocultivo. La linfocitosis se ha descrito como parte de la tosferina maligna y un factor de riesgo para complicación 7 . La trombocitosis se describe en este estudio, por primera vez, como factor de riesgo.
Dentro de la evolución de los pacientes complicados, se encuentra el requerimiento de inotrópicos, hospitalización en cuidado crítico y ventilación mecánica asistida. En la literatura se encuentra que casi la mitad de los pacientes hospitalizados por infección por Bordetella pueden tener riesgo de hospitalización en cuidado crítico 8. La necesidad de ingreso en unidades de cuidados intensivos y de ventilación mecánica es más frecuente en menores de 3 meses y se debe a insuficiencia respiratoria secundaria a apnea y a la neumonía bacteriana secundaria 5.
Aunque en este estudio pocos pacientes fallecieron, la letalidad reportada de 4,6% es muy elevada, con cifras por encima del reporte nacional: 2,97% (30 muertes por tosferina/ 1.010 confirmados) en 8 entidades territoriales 12 y otros estudios de la literatura que reportan cifras entre 1 y 2% 13 . Esta diferencia puede ser secundaria a la naturaleza de la institución, dado que es un centro de referencia a nivel nacional en pediatría y muchos de los casos ingresados habrían sido manejados en otros hospitales previamente, probablemente con diagnóstico y manejo tardíos. En la literatura se reporta que los casos fatales se presentan en pacientes menores de un año de edad y casi el 100% se presenta en menores de 6 meses, por lo que los síntomas característicos de la enfermedad no son típicos de este grupo etario, siendo diagnosticados tardíamente 14 .
El promedio de estancia en cuidado crítico fue de aproximadamente una semana, con más de 10 días de estancia hospitalaria, que generan un impacto financiero en el sistema de salud, las instituciones prestadoras de servicios y la familia 15 .
Este estudio tiene una potencia moderada, dada la fuente secundaria de los datos. Es necesario realizar estudios prospectivos para confirmar las conclusiones aquí planteadas y ampliar otras variables, como los marcadores inflamatorios.
Este trabajo se realizó en una institución que aporta aproximadamente el 25% de los casos confirmados en la ciudad de Bogotá. Dado que es una institución de referencia, los datos pueden, y sus conclusiones deben, ser extrapolados solamente en instituciones con características similares a la referencia.
La implementación de estos datos es viable a través de la prevención, dado que con el conocimiento de grupos etarios perjudicados y su estado de inmunización para tosferina se pueden implementar acciones de vacunación precoz o inicio de un esquema acelerado con acortamiento de los intervalos y vacunación a las madres en los casos de brote. Por otra parte, los factores de riesgo detectados en la consulta inicial de urgencias o atención primaria son posibles predictores de complicación, por lo que la atención prioritaria puede reducir consecuencias graves.
Conclusión
Los factores de riesgo para complicaciones como ausencia de vacunación antipertussis, cianosis, taquipnea, desaturación, linfocitosis y trombocitosis son guía para identificar tempranamente a los pacientes potencialmente críticos e intervenir de manera más apropiada, objetiva y eficiente antes de su deterioro clínico.
Responsabilidades éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datos.
Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informado.
Los autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Agradecimientos
A la Universidad Nacional de Colombia y a la Fundación Hospital de la Misericordia por su apoyo en el desarrollo de esta investigación.
* Autor para correspondencia: Carrera 7 N 43-33 Apto. 207 Torres del Fonce. Cel: +3168023504. Correo electrónico: mpmontillav@unal.edu.co (M.d.P. Montilla Velásquez).
Bibliografía
1. Instituto Nacional de Salud. Boletín Epidemiológico Semanal. Semana epidemiológica N 52 de 2012 [Internet]. 2012 [consultado 13 Feb 2014]. Disponible en: http://www.ins.gov.co/boletin-epidemiologico/Boletn%20Epidemiolgico/2012%20Boletin%20epidemiologico Semana%2052.pdf [ Links ]
2. Equipo Inmunoprevenibles, Subdirección de Prevención Vigilancia y Control en Salud Pública, Intituto Nacional de Salud. Protocolo de vigilancia en Salud publica. Tosferina [Internet]. 2014 [consultado 9 Feb 2014]. Disponible en: http://www.ins.gov.co/lineas-de-accion/Subdireccion-Vigilancia/sivigila/Protocolos%20SIVIGILA/PRO%20Tos%20ferina.pdf [ Links ]
3. Olivares Ortiz J, Bueno Campaña M. Tos ferina: revisión clínica a propósito de un caso. Pediatría Aten Primaria. 2011;13(52):575-84. [ Links ]
4. Sawal M, Cohen M, Irazuzta JE, Kumar R, Kirton C, Brundler M-A, et al. Fulminant pertussis: A multi-center study with new insights into the clinico-pathological mechanisms. Pediatr Pulmonol. 2009;44(10):970-80. [ Links ]
5. Kliegman RM, Stanton BMD, Schor NF, Geme JS, Behrman RE. Tos ferina ( Bordetella pertussis y B. parapertussis ). Capítulo 18. En: Nelson: Tratado de pediatría. ExpertConsult acceso WEB en español. España: Elsevier-Saunders; 2013, 908-911 [consultado 13 Feb 2014] [ Links ].
6. Heininger U, Klich K, Stehr K, Cherry JD. Clinical findings in Bordetella pertussis infections: Results of a prospective multicenter surveillance study. Pediatrics. 1997;100(6):E10. [ Links ]
7. Donoso A, Arriagada D, Cruces P, Díaz F. Coqueluche grave: estado del arte. Rev Chil Infectol. 2012;29:290-306. [ Links ]
8. Surridge J, Segedin ER, Grant CC. Pertussis requiring intensive care. Arch Dis Child. 2007;92(11):970-5. [ Links ]
9. World Health Organization. Pertussis [Internet]. WHO [consultado 9 Feb 2014]. Disponible en: http://www.who.int/immunization/topics/pertussis/en/index.html [ Links ]
10. Organización Panamericana de la Salud. Alerta epidemiológica tos ferina (Coqueluche). 2012 [consultado 13 Feb 2014]. Disponible en: http://www.paho.org/hq/index.php?option=comdocman&task=doc view&gid=17052&Itemid [ Links ]
11. Briand V, Bonmarin I, Lévy-Bruhl D. Study of the risk factors for severe childhood pertussis based on hospital surveillance data. Vaccine. 2007;25(41):7224-32. [ Links ]
12. Instituto Nacional de Salud. Boletín Epidemiológico Semanal. Semana epidemiológica N 52 de 2011 [Internet]. 2011 [consultado 13 Feb 2014]. Disponible en: http://www.ins.gov.co/boletin-epidemiologico/Boletn%20Epidemiolgico/2011%20Boletin%20epidemiologico Semana%2052.pdf [ Links ]
13. Mikelova LK, Halperin SA, Scheifele D, Smith B, Ford-Jones E, Vaudry W, et al. Predictors of death in infants hospitalized with pertussis: A case-control study of 16 pertussis deaths in Canada. J Pediatr. 2003;143(5):576-81. [ Links ]
14. Donoso FA, Wegner AA, León BJ, Ramírez A. Coqueluche en niños menores de 6 meses de vida. Rev Chil Pediatría. 2001;72(4):334-339. [ Links ]
15. O´Brien JA, Caro JJ. Hospitalization for pertussis: Profiles and case costs by age. BMC Infect Dis. 2005;5:57. [ Links ]













