Introducción
En la actualidad, la mayoría de sociedades científicas recomiendan el inicio de tratamiento antirretriviral (TAR) en todos los pacientes con infección VIH, incluyendo los que tienen más de 500 linfocitos CD4/.1-4
Con los tratamientos actualmente disponibles se consigue la reducción de la carga viral (CV) por debajo de los límites de detección en los pacientes naive en las primeras 12-24 semanas en la mayoría de pacientes.5-6Aunque la supresión prolongada de la CV es uno de los objetivos en todas las guías, surgen discrepancias en el concepto de fracaso virológico (FV). La mayoría de ellas2-4coinciden en la definición de FV como dos determinaciones consecutivas de CV>50 copias/ml, a las 24 semanas del inicio del TAR, mientras que la DHHS1 lo define como la imposibilidad de conseguir o mantener una replicación viral por debajo de 200 copias/ml. También se considera FV si, tras conseguir la supresión virológica en la semana 24, vuelve a hacerse detectable en dos determinaciones consecutivas.
Las estrategias para conseguir el objetivo terapéutico pasan por la adecuada selección del régimen inicial, la realización de un test de mutaciones de resistencia (MR) previo y conseguir una buena adherencia. Otros factores que se consideran predictores de éxito son la viremia basal pre-tratamiento baja y un recuento inicial de CD4 por encima de 200 cel/μl.1,3,5,6
El objetivo principal de este trabajo es determinar la tasa de FV a 24 y 48 semanas en vida real en los pacientes atendidos en un hospital de tercer nivel. Como objetivos secundarios se pretende analizar las características de la población atendida, el TAR de inicio utilizado, los motivos que propiciaron el cambio del mismo y la relación entre el resultado obtenido y los diferentes predictores de éxito descritos en la bibliografía.
Estudio retrospectivo de 3 años de duración realizado en un hospital de tercer nivel. Se seleccionaron pacientes adultos VIH naive que iniciaron TAR entre enero de 2012 y diciembre de 2014. Se excluyeron aquellos pacientes que iniciaron tratamiento con indicación de profilaxis post-exposición y embarazo. El tiempo de seguimiento fue de 48 semanas.
Se registraron datos demográficos (edad, sexo, nacionalidad y nivel de estudios), datos clínicos (mecanismo de transmisión, estadio clínico), datos de laboratorio (CV y CD4 al inicio del TAR y realización de un test de MR previo) y TAR elegido (fármacos elegidos, familia y si se trata de un único comprimido al día (STR)). Como CV y CD4 basal, se recogió el dato de la visita de inicio de tratamiento o, en caso de no aparecer, el más próximo retrospectivamente al inicio del TAR.
Se registraron la CV y los CD4 correspondientes a las visitas de las semanas 24 y 48 de tratamiento, considerando un margen de tiempo de hasta 4 semanas más (semana 28 y semana 52). A partir de ese dato se determinó el éxito o fracaso del tratamiento a las 24 y 48 semanas mediante dos análisis, entendiendo FV como:
• CV>50 copias/ml a las 24 o 48 semanas del inicio del TAR (que no haya llegado a hacerse indetectable en ningún momento o que, tras conseguir la supresión virológica, vuelva a hacerse detectable en dos determinaciones consecutivas. (definición de las guías GESIDA, EACS,IAS2-4)
• la imposibilidad de conseguir o mantener una replicación viral por debajo de 200 copias/ml (Guías DHHS1).
Se registraron los problemas de medicación surgidos tras las 48 semanas: TAR no preferente por las diferentes guías1-4, no realización de estudio de MR previo al inicio del TAR, seguimiento y adherencia. La atención y seguimiento de los pacientes se realiza mediante un equipo de médicos internistas especializados en enfermedades infecciosas y VIH, una enfermera y un servicio de farmacia que cuenta con farmacéutico especialista en farmacia hospitalaria y personal de enfermería. Se consideró que había habido un buen seguimiento cuando el porcentaje de visitas médicas a las que asistió el paciente superó el 80% de las programadas ese año. La adherencia se consideró como adecuada cuando superó el 90%. El registro de adherencia de nuestro centro se basa en la frecuencia con la que acude el paciente a recoger la medicación al servicio de farmacia, y se registra en aquellas dispensaciones que preceden a una visita médica. Se calcula la adherencia de los últimos 4 meses como el porcentaje de la diferencia entre los días teóricos para los que se le ha dispensado medicación (120 días) y los comprimidos sobrantes que dice tener el paciente y/o los días transcurridos entre la fecha calculada de finalización teórica de la medicación (en función de la previsión del programa de dispensación) respecto al día en la que el paciente acude a recoger de nuevo la medicación. El valor de adherencia para cada paciente se determina en base al valor medio de los registros de adherencia recogidos durante todo el tiempo de seguimiento.
Se registraron los cambios de TAR realizados durante el primer año y el motivo del cambio. Se registraron los mismos datos del segundo TAR que del primero (fármacos elegidos, tipo de TAR y si era STR).
Se estudiaron los motivos de todas las pérdidas de seguimiento o ausencia de datos a las 48 semanas, así como las posibles causas de FV en pacientes con más de >200 copias/ ml a la semana 48.
Se realizó un análisis univariante y multivariante de los factores predictores de FV, teniendo en cuenta aquellos pacientes que disponían de datos de CV a las 48 semanas, tanto para la definición de FV con CV>50 copias/ml como para la de CV>200 copias/ml. Se relacionó fracaso con viremia basal alta (>100.000 copias/ml), recuento inicial de linfocitos CD4 (<200 cel/μl), realización de estudio de MR previo, TAR recomendado por las guías científicas1-4, tipo de TAR empleado (según la clasificación de la familia del tercer fármaco), utilización de STR, adherencia >90% y correcto seguimiento. Se utilizaron medidas de "odds radio" considerando como estadísticamente significativo una p<0,05 con un intervalo de confianza (IC) del 95%. Todos los datos analizados fueron obtenidos a partir de pacientes que habían firmado el onsentimiento informado correspondiente a la Cohorte Multicéntrica de Personas Adultas con Infección VIH (PISCIS)
Resultados
Datos generales demográficos, clínicos y de tratamiento:
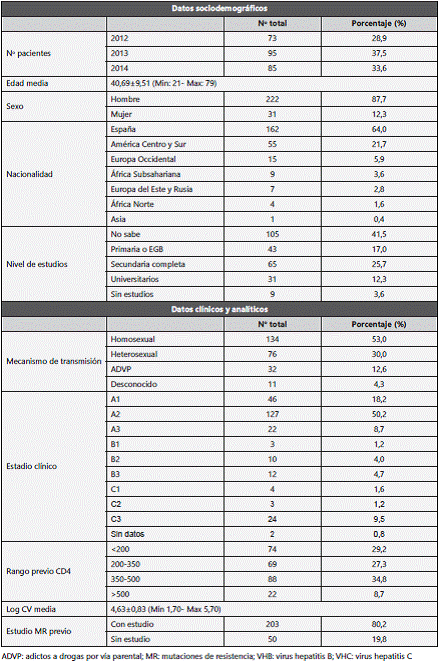
Se incluyeron 253 pacientes. Los datos sociodemográficos, clínicos y analíticos aparecen reflejados en la tabla 1.
Tres pacientes con CV indetectable a la semana 24 estaban detectables a la 48 (2 de ellos con CV>200 copias/ml, uno por abandono y otro por mala adherencia).
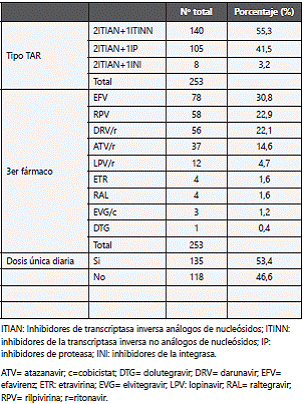
Respecto al TAR elegido, la combinación mayoritaria fue la de 2 inhibidores de la transcriptasa inversa análogos de nucleósidos (ITIAN)+1 inhibidor de la transcriptasa inversa no análogo de nucleósido (ITINN), seguida de 2 ITIAN+1 inhibidor de la proteasa (IP) y por último la de 2 ITIAN+1INI. (Tabla 2)
La combinaciones de ITIAN fueron mayoritariamente emtricitabina (FTC)+tenofovir (TDF) o abacavir (ABC)+lamivudina (3TC), excepto en 4 pacientes que comenzaron con zidovudina (ZDV) en combinación con 3TC.
En cuanto al tercer fármaco, efavirenz (EFV) y rilpivirina (RPV) formó
parte de la terapia antiviral en más del 50% de los pacientes.
Éxito y fracaso virológico:
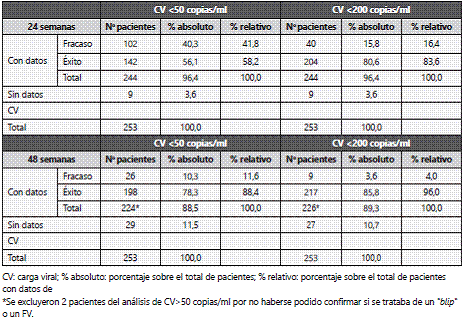
Se evaluaron los datos analíticosde 244 (96,4%) pacientes a las 24 semanas y de 226 (89,3%) a las 48 semanas para determinar el éxito o FV. Los resultados aparecen detallados en la tabla 3.
El análisis de los pacientes con datos de CV disponible a las 24 semanas muestra que el 58,2% de los pacientes estaban indetectables, aunque el 83,6% tenían la CV por debajo de 200 copias/ml. Este porcentaje se incrementa a un 88,4% y un 96,0% respectivamente a las 48 semanas.
De los 27 pacientes sin datos analíticos a las 48 semanas, en 10 casos fue por cambio de residencia, 8 por pérdida de control de visita médica, 5 porque no se hicieron la analítica, 2 porque en la analítica faltaba la CV, 1 por abandono y 1 por éxitus. De los 9 pacientes que fracasaron con CV>200 copias/ ml, en 6 casos fue por abandono, 2 por mala adherencia y 1 por pérdida de control.
Cambios de TAR inicial:
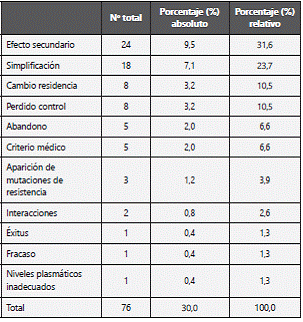
A 76 pacientes (30,0%) se les cambió el TAR inicial. La mediana de tiempo hasta el cambio fue de 157 días. La principal causa fue la aparición de efectos secundarios (31,6%) seguida de la simplificación del tratamiento (23,7%). Los motivos de cambio y los efectos secundarios registrados aparecen detallados en las tabla 4 y tabla 5.
57 de estos pacientes iniciaron un segundo TAR: 27 con una combinación de 2ITIAN+1ITINN, 23 con 2ITIAN+1IP, 5 con 2ITIAN+1INI, 1 con un IP en monoterapia y 1 con biterapia de IP+INI. A 24 de estos pacientes (42,1%) se les instauró un régimen STR.
A 9 de los 57 pacientes se les retiró la segunda combinación de TAR durante el primer año de seguimiento, 2 por abandono, 2 por cambio de residencia, 2 por fracaso, 1 por simplificación, 1 por estudio de resistencias y 1 por pérdida de control.
En cuanto a los problemas relacionados con la medicación, se registraron 2 pacientes con RPV+FTC+TDF que iniciaron con CV ligeramente superior a 100.000 copias (uno estuvo indetectable tanto a la semana 24 como 48 y el otro a las 48); 17 pacientes iniciaron con regímenes que incluían LPV/r, ZDV o ETR, fármacos no incluidos en las guías como opciones preferentes de inicio (dos de ellos estaban detectables en la semana 48 pero con CV<200 copias/ml); en 50 pacientes (19,8%) no se realizó el estudio de MR previo; 202 (79,8%) de los pacientes tuvieron buen seguimiento y en 181 (93,8%) de los 193 pacientes en los que se determinó la adherencia, esta fue considerada adecuada (> 90%).
Análisis de datos:
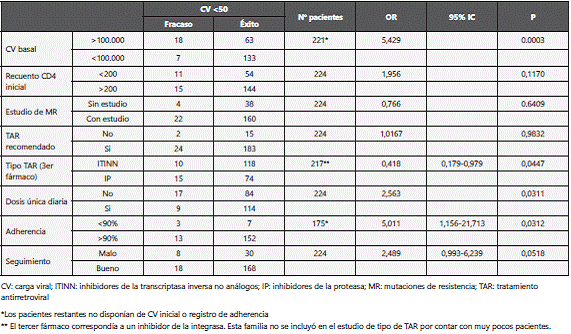
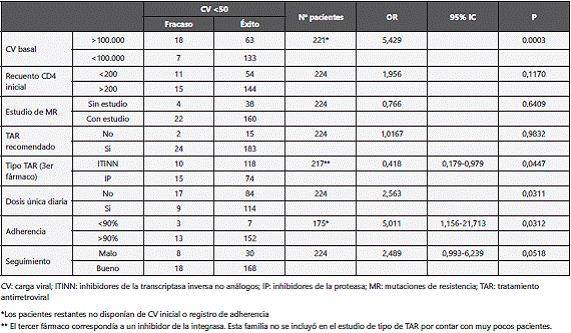
El análisis univariante realizado (tabla 6) mostró una relación estadísticamente significativa entre viremia basal elevada (>100.000 copias/ml) o mala adherencia (<90%) y un mayor riesgo de FV (CV>50 copias/ml) al tratamiento en la semana 48. En el análisis del tipo de TAR, sólo se tuvo en cuenta el grupo de ITINN e IP, ya que el número de pacientes con INI era muy bajo (8 pacientes). Se asociaron los regímenes basados en IPs con un mayor riesgo de fracaso (CV>50 copias/ ml), al igual que los regímenes no STR, los cuales correspondían en su mayoría con terapias basadas en IPs.
El resto de variables no mostraron una asociación significativa con la probabilidad de éxito o fracaso. Tampoco mostraron asociaciones estadísticamente significativas con la probabilidad de fracaso las diferentes variables en el análisis de FV con CV>200 copias/ml, a excepción del mal seguimiento, que se asoció con mayor probabilidad de fracaso (OR=6,97; IC95% 1,778-27,319; p=0,0053).
En el análisis multivariante se relacionó con una mayor probabilidad de FV (CV>50 copias/ml) al tratamiento en la semana 48 la CV basal elevada (>100.000 copias/ml) (OR=8,596; IC95% 2,315-31,917; p<0,001) y con una menor probabilidad la correcta adherencia >90% (OR=0,215; IC95% 0,043-1,077; p=0,062). No se encontraron diferencias estadísticamente significativas con el resto de variables.
Discusión
Los datos demográficos y clínicos de nuestra población naive que inicia TAR se asemejan a los del último informe de "Vigilancia epidemiológica del VIH y SIDA en España" del Ministerio de Sanidad, Servicios Sociales e Igualdad7 de 2015, donde se muestra que, de los 3.366 nuevos casos diagnosticados de VIH en 2014, el 84,7% eran hombres, la mediana de edad fue de 35 años, el 32,1% eran personas originarias de otros países y la transmisión en hombres que tienen sexo con otros hombres (HSH) fue la más frecuente (53,9%). La proporción de diagnósticos tardíos (<350 CD4/mm3) fue del 46,2%, mientras que en nuestro estudio fue del 56,5%.
A las 24 semanas de tratamiento menos del 60% de nuestros pacientes habían conseguido CV indetectable. A las 48 semanas los datos mejoran considerablemente, con un 11,6% de FV con CV>50 copias/ml, y un 4,0% de pacientes con más de 200 copias/ml. Estos datos son acordes con la tasa de FV habitual que aparece reflejada en las guías GESIDA-PNS3 (4- 12% a las 48 semanas).
Otros estudios publicados encuentran que entre un 5%8 y un 13%9 de los pacientes cambian el TAR inicial por fracaso del mismo. Es importante la definición de FV empleada en cada estudio, así como el año o la técnica de PCR VIH que se ha realizado, aspecto que no siempre viene claramente definido. En el estudio de Jarrin et al.9 únicamente aparece fallo/resistencia al tratamiento, sin especificar claramente qué consideran como fracaso, y en el de Keita et al.8 se define fracaso del tratamiento no sólo a la imposibilidad de conseguir CV indetectable o al repunte de la misma, sino también a la aparición clínica de los síntomas de progresión de la enfermedad o la ausencia de aumento en el recuento de CD4 a pesar de la terapia TAR.
Existe controversia sobre la importancia de cargas virales sostenidas entre 50 y 199 copias/ml en el posterior FV y desarrollo de MR. Un estudio que analizó 18 cohortes europeas y norteamericanas con 17.902 pacientes10 encontró que la CV entre 50 y 199 copias/ml estaba débilmente asociada con el FV, lo que apoya las directrices americanas que lo definen como una CV confirmada por encima de 200 copias/ml.
Otra cohorte suiza de 9.972 pacientes,11 tras 11 años de seguimiento,
relacionó la CV>200 copias/ml como predictor de FV, no siendo así en CV detectables inferiores a esa cifra.
Otro estudio de 2.374 pacientes12, encontró más probabilidad de FV en pacientes con CV entre 50 y 199 copias/ml sólo en pacientes pretratados, no siendo así en los pacientes naive. Ni el tipo de TAR ni la duración acumulada de CVs bajas se asociaron a mayor FV. En una cohorte de Montreal tras 12 años de seguimiento13, encuentran que todas las categorías de pacientes con CVs bajas persistentes entre 50 y 999 copias/ ml se asociaron con un mayor riesgo de FV.
En estos estudios también vemos las diferencias entre definiciones de FV, siendo definido como "dos cargas virales consecutivas de por lo menos 500 Lde TAR"10,como "una carga viral de ARN de VIH de >1000 copias/ ml"13, o como"una CV>400 copias/ml"11.
También es importante señalar que en la práctica clínica es difícil tener datos analíticos en las semanas generalmente evaluadas en los ensayos clínicos 24, 48, 96 y 192 y hacer un seguimiento tan estricto. La definición de éxito terapéutico como CV<50 copias/ml a las 24 semanas es un dato probablemente muy exigente que no conseguimos alcanzar en el 42% de los pacientes. En el caso de ampliar el margen de tiempo para alcanzar éxito terapéutico a un seguimiento de hasta las 48 semanas, el porcentaje aumenta considerablemente (88%), llegando a superar al que aparece mencionado en las Guías GESIDA-PNS3 del 75% a las 48 semanas. Tan sólo 9 pacientes tenían CV>200 copias/ml a las 48 semanas, todos ellos por abandono o mala adherencia o seguimiento. Con esto podemos decir que todos los pacientes que tuvieron buena adherencia y seguimiento tuvieron éxito en el tratamiento.
En cuanto a los problemas relacionados con la medicación detectados, hay que considerar que las pautas preferentes han ido cambiando en estos últimos tres años, como es el caso de lopinavir/ritonavir que fue considerado como pauta preferente hasta 2013.14 Aunque en este estudio la elección de un TAR no recomendado no se asoció con una mayor probabilidad de FV, existen datos que relacionan el uso de pautas no recomendadas con una menor respuesta virológica y una mayor mortalidad.15
Respecto a los cambios de tratamiento, el motivo de retirada mayoritario fue el de efectos secundarios (31,6%), seguido de simplificación del tratamiento (23,7%). Cambios de residencia, pérdidas de control y abandonos suman el 27,6%. Estos datos son acordes con los publicados sobre la cohorte CoRIS9 de 2008 a 2010, donde se indica que la causa más frecuente de cambio de TAR es la toxicidad (40%), seguida de la simplificación (14%) y el fracaso/resistencia al tratamiento (13%).
La encuesta realizada en España por Pedrol et al.16 en 349 pacientes con VIH en 19 hospitales para caracterizar los motivos de cambio del TAR también obtuvo que la causa más frecuente del cambio fue la simplificación (37%), seguida de la toxicidad (30%) y el fracaso terapéutico (21%). En otro estudio español,17 de 603 pacientes naive que iniciaron TAR la mediana de tiempo en el mismo TAR fue de 17,5 meses. El TAR se había interrumpido en el 36% de los pacientes en el primer año de seguimiento, siendo la toxicidad la causa principal del cambio de terapia (25%), seguida de la simplificación (19%), y el FV (15%).
Dentro de las discontinuaciones de tratamiento provocadas por efectos adversos, Prosperi et al.18 relacionaron la edad avanzada, el estadío clínico C de la CDC, el sexo femenino y el grupo de riesgo homo y bisexual con una mayor probabilidad de sufrir efectos adversos al TAR.
En cuanto a los factores relacionados con el éxito o fracaso del tratamiento, la adherencia >90% se mantiene como factor predictor de éxito clave en todos los análisis, seguido de la baja CV basal al inicio del tratamiento.
También se encontraron diferencias entre tipo de TAR y régimen STR, siendo los ITINN y los STR predictores de éxito, pero hay que señalar que estos datos pueden depender más del tipo de paciente que del tratamiento en sí, ya que los IPs, por su elevada barrera genética, clásicamente se han empleado en pacientes con resistencias acumuladas o en los que se prevé una mala adherencia. También son el único grupo de fármacos que no cuentan con STR.
La principal limitación de este estudio es que, al ser retrospectivo, carece de datos de registro de reacciones adversas que no propiciaron cambios de tratamiento, pero que puede que afectaran a la calidad de vida o la adherencia de los pacientes.
Otra limitación es que el registro de adherencia no es completo en todos los pacientes. Hay que señalar que en nuestro centro el registro de adherencia se implantó en el 2012, por lque hay pacientes en los que pudo no registrarse por no estar aún implantado, y otros en los que seguramente no se hizo por fallo humano o porque el paciente tenía medicación y no cudió a la farmacia en la dispensación previa programada.
Este estudio ha permitido conocer la tasa de FV en vida real en nuestro centro con los fármacos disponibles hasta 2014, así como confirmar la importancia de predictores de éxito ya descritos. La incorporación de nuevos fármacos al arsenal terapéutico puede suponer una mejora de resultados en un futuro próximo.