Introducción
La emergencia de enterobacterias resistentes a los carbapenémicos (ERC) es un problema de salud pública a nivel mundial, con un alto impacto tanto en la morbimortalidad de los pacientes como en el incremento de los costos en la atención relacionados con estancias hospitalarias prolongadas y uso de antibióticos de amplio espectro1, 2. La detección y diferenciación de las ERC productoras de carbapenemasas (EPC) facilita la implementación de precauciones de contacto y permite un abordaje terapéutico adecuado3.
Con el propósito de detectar las ERC y optimizar el uso de los carbapenémicos a través de estudios farmacocinéticos y farmacodinámicos (PK/PD), el Instituto de Estándares Clínicos y de laboratorio (CLSI por sus siglas en inglés ) disminuyó los puntos de corte en 2010, y recomendó realizar pruebas fenotípicas confirmatorias como el test de Hodge modificado (THM) para el control de la diseminación de las carbapenemasas. En el año 2015, la versión M100-S25 de los estándares para pruebas de susceptibilidad, incorporaron el test bioquí mico Carba NP para la detección de carbapenemasas, siendo la primera vez que se recomienda su aplicación además de Enterobacteriacea en no fermentadores como Pseudomonas aeruginosa y Acinetobacter spp.4. Los métodos de detección basados en el uso de discos con inhibidores como ácido fenilborónico (APB) presentan sensibilidad y especificidad cercanas al 100% en la detección de carbapenemasas clase A de Ambler 5, grupo funcional 2b. Sin embargo, se han reportado resultados falsos positivos con cepas productoras de betalactamasa tipo AmpC como Enterobacter spp y Serratia spp. A pesar de que la reacción en cadena de la polimerasa (PCR) sigue siendo la metodología más sensible y específica para la determinación de este tipo de enzimas, su acceso a los la boratorios de rutina no se encuentra masificado debido a los costos y el entrenamiento requerido para su implementación.
Recientemente Zwaluw y col. (2015) y Melano R. y col. (2016), han reportado buenos resultados al evaluar un nuevo método de inactivación de carbapenémico (MIC*) como alternativa costo efectiva para la detección de carbapenemasas en EPC 6,7 al compararlo con métodos colorimétricos y la PCR. Este método está basado en la capacidad de la enzima carbapenemasa de hidrolizar la concentración de 10µg de Meropenem (MEM) contenida en un sensidisco de papel de filtro mediante la elución del mismo en agua destilada estéril. En el presente estudio se pretende evaluar al MIC* en EPC tipo KPC frente a técnicas como el APB, THM y la PCR.
Metodología
Aislados clínicos: Se tomaron 179 aislados procedentes de muestras clínicas de diferentes instituciones de salud y que se encuentran dentro del sistema de vigilancia de resistencia bacteriana del Ecuador. 88 cepas entre K. pneumoniae, K. oxytoca, E.coli, S. marcescens, C. freundii con CMI ≤ 1 µg/mL para imipenem (IMI) y meropenem (MER) y negativas para el gen blaKPC por PCR y 91 cepas de las mismas especies con CMI ≥4 µg/mL para imipenem (IMI) y meropenem (MER) y positivas para blaKPC por reacción en cadena de la polimerasa. (Tabla 1) Todas las cepas fueron debidamente caracterizadas mediante el Vitek2 compact® (BioMerieux Inc.).
Tabla 1 Comparación de pruebas moleculares y fenotípicas en ERC-PC tipo KPC.
| Especie | N | CMI ug/mL | blaKPC | THM + N %) | APB + N (% ) | MIC* + N (%) | |
|---|---|---|---|---|---|---|---|
| Susceptible | MEM | IMI | |||||
| Klebsiella pneumoniae | 63 | ≤ 1 | ≤1 | - | 2/63 (3) | 3/63 (5) | 0/63 |
| Klebsiella oxytoca | 2 | ≤1 | ≤1 | - | 0/2 | 2/2 | 0/2 |
| Escherichia coli | 14 | ≤1 | ≤1 | - | 0/14 | 0/14 | 0/14 |
| Serratia marcescens | 8 | ≤1 | ≤1 | - | 1/8 | 0/8 | 0/8 |
| Citrobacter freundii | 1 | ≤1 | ≤1 | - | 0/1 | 0/1 | 0/1 |
| Resistente | MEM | IMI | |||||
| Klebsiella pneumoniae | 64 | ≥4 | ≥4 | + | 64/64 | 64/64 | 64/64 |
| Klebsiella oxytoca | 6 | ≥4 | ≥4 | + | 6/6 | 6/6 | 6/6 |
| Escherichia coli | 13 | ≥4 | ≥4 | + | 12/13 (93) | 13/13 | 13/13 |
| Serratia marcescens | 7 | ≥4 | ≥4 | + | 6/7 (93) | 7/7 | 7/7 |
| Citrobacter freundii | 1 | ≥4 | ≥4 | + | 1/1 | 1/1 | 1/1 |
APB: ácido fenilborónico, CMI Concentración mínima inhibitoria. MIC*: método de Inactivación de carbapenémicos THM: Test de Hodge modificado
Pruebas moleculares: En todas las cepas sensibles y resistentes a los carbapenémicos se buscó la amplificación del gen blaKPC por medio de una PCR múltiplex siguiendo los protocolos previamente reportados por Poirel y col. 8 e implementados en el sistema de vigilancia de resistencia antimicrobiana del Ecuador.
Ensayos de susceptibilidad y pruebas fenotípicas: Todas las cepas fueron sometidas a Concentración Mínima Inhibitoria (CMI) por microdilución a los carbapenémicos tomando como referencia normas CLSI 2016 utilizando Vitek2 (BioMe- rieux Inc.). Discos de IMI 10ug (Oxoid) fueron utilizados para todas las pruebas fenotípicas realizados agar Mueller Hinton (Oxoid). Para el test de Hodge modificado (THM) se siguió el protocolo recomendado por el CLSI M100S-26th. Para la prueba de la sinergia de carbapenémicos con ácido 3- aminofenilborónico (APB), se aproximaron a una distancia de 20-mm los discos de Imipenem (IMI) y de papel filtro sin antibiótico impregnados con 300µg de (APB) (Sigma, Chemicals) siguiendo las recomendaciones de Pasterán y col5.
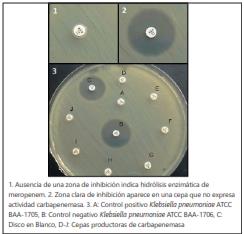
Método de inactivación de los carbapenémicos (MIC*).- Se siguió el protocolo descrito por Zwalow y col. 2015. Con un asa de 10 µL se tomó el aislado previamente cultivado en agar Mueller-Hinton e incubadas durante 24 horas a 35°C y se resuspendió en 400 µL agua destilada estéril; de forma inmediata se sumergió un disco de Meropenem (MEM) 10µg (Oxoid®) dentro de la suspensión y se incubó durante 2 horas a 35°C. Luego se retiró el disco con pinza estéril para ser colocado sobre una placa de agar Mueller-Hinton previamente sembrada de forma masiva con la cepa E.coli ATCC 25922 a una turbidez de 0,5 McFarland. Se utilizaron Klebsiella pneumoniae ATCC BAA-1705 y Klebsiella pneumoniae ATCC BAA- 1706 como controles positivo y negativo respectivamente. Se incubó a 35°C durante 6 horas. La interpretación se basó en la presencia (negativo para carbapenemasas) o ausencia de halo de inhibición (positivo para carbapenemasas)
Resultados
El 100% de los aislamientos incluidos en el estudio, tuvieron una relación directa entre la presencia o ausencia del gen blaKPC con las pruebas de susceptibilidad a los carbapené icos. Los resultados del THM mostraron falsos positivos, K. pneumoniae (n=2) y S. marcescens (n=1), y falsos negativos E. coli (n=1) y S. marcescens (n=1). Resultados similares fueron encontrados con el APB y no se observaron resultados falsos positivos o negativos en el MIC* en EPC (Tabla 1). El MIC* demostró una concordancia kappa de 1 con las pruebas moleculares y con sensibilidad - especificidad que supera el 99% (Tabla 1 y tabla 2).
Tabla 2 Rendimiento de las pruebas fenotípicas en ERC-PC tipo KPC
| THM | APB | MIC* | |
|---|---|---|---|
| Sensibilidad | 98% | >99% | >99% |
| Especificidad | 97% | 94% | >99% |
| VPP | 97% | 95% | >99% |
| VPN | 98% | >99% | >99% |
APB: ácido fenilborónico, MIC*: método de inactivación de carbapenémicos, THM Test de Hodge modificado, VPP: Valor predictivo positivo, VPN: valor predictivo negativo.
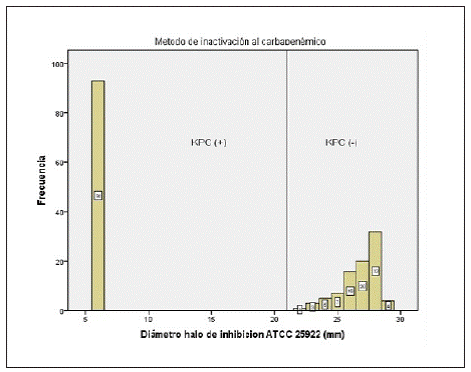
El punto de corte utilizado (>19mm) para interpretar una prueba como positiva o negativa fue capaz de separar 100% las ERC-PC blaKPC (+) de aquellas blaKPC (-), se notó ausencia de halo en todas las cepas blaKPC (+) (Figura 1 y Figura 2 )
Discusión
Enterobacterias productoras de carbapenemasas y en especial aquellas que producen carbapenemasas tipo KPC son cada vez más frecuentes en muchos países a nivel mundial9,10. El hallazgo de un paciente con infecciones producidas por EPC reduce las opciones terapéuticas y promueve el inicio de combinaciones de antibióticos, algunos de alta toxicidad y la aplicación de medidas de prevención y contención, por lo cual su sospecha y confirmación son fundamentales para reducir la mortalidad y la expansión de estos microorganismos12.
La descripción del MIC* por Zwaluw y col. (2015) para la detección de carabapenemasas en bacilos gram negativos, ha despertado mucho interés por la serie de ventajas que presenta, como reactivos de fácil disponibilidad en laboratorios de baja complejidad, su bajo costo y su alta reproducibilidad6. En nuestro estudio se demostró un factor adicional en EPC tipo KPC, que fue la alta concordancia entre el MIC* y la PCR, esta última considerada como el “gold standard”, pero que presenta inconvenientes como su costo elevado, la necesidad de equipos y re- activos de difícil acceso especialmente en los laboratorios asistenciales de países en vías de desarrollo11. La sospecha de EPC se realiza en las pruebas de susceptibilidad rutinarias, observan- do la CMI a los carbapanémicos por encima de los puntos de corte establecidos por CLSI o los puntos de corte epidemiológicos establecidos por EUCAST, junto con la presencia de multi o inclusive pan resistencia a los antibióticos. De forma inmediata es necesaria la intervención mediante medidas de contención epidemiológica y sumando evidencia que se trate de una carbapenemasa13. Para la confirmación de que han demostrado ser muy útiles en la detección de serín - carbapemasas, sin embargo en nuestro estudio como en otros reportes, la presencia de resultados falsos positivos producidos por la presencia de balactamasas de espectro extendido (BLEE) o cefalosporinasas tipo AmpC con impermeabilidad continúan siendo un inconveniente16,17,5. Por su parte el MIC*, en nuestro estudio no se demostró este tipo de resultados, presentando una sensibilidad y especificidad muy cercana al 100% para detectar carbapenemasas blaKPC en enterobacterias. Ensayos colorimétricos como el Carba NP, ya sea de cultivo puro 18 o directamente de hemocultivos19 han demostrado buenos resultados con sensibilidad superior al 90% y recomendados en enterobacterias, Pseudomonas aeruginosa y Acinetobacter spp. Sin embargo también presentan varias dificultades como la detección de carbapenemasas tipo OXA-48 20 junto con su accesibilidad al método y los costos en ciertos países en vías de desarrollo.
La interpretación de los resultados del MIC* es un tema pendiente por resolver, se demostró que el 100% de las EPC blaKPC (+) no presentaban halo de inhibición, mientras que las cepas blaKPC (-) presentan halos superiores a los 20mm, resultados que concuerdan con los reportados por Tijet 2016; no se evidenciaron resultados entre 6-20mm, sin embargo de ocurrir este evento se recomienda el uso de otra técnica disponible.
En conclusión, el test MIC* es una técnica que puede reemplazar al THM y APB empleados para determinar la presencia de carbapenemasas tipo KPC en EPC, por su bajo costo, disponibilidad de reactivo y su rendimiento frente a pruebas moleculares.