Introducción
La infección de vías urinarias (IVU) es una de las enfermedades más prevalentes en la práctica clínica, encontrándose tanto en pacientes hospitalizados como ambulatorios de todo el mundo1,2. Es la segunda enfermedad infecciosa más frecuente después de las respiratorias y es la causa de infección bacteriana más común en mujeres3.
Se ha descrito que la mayoría de las IVU son causadas por miembros de la familia Enterobacteriaceae, principalmente Escherichia coli en el 69-90% de los casos, seguido de Klebsiella spp, Staphylococcus saprophyticus y Proteus. Algunos estudios refieren que la resistencia de las bacterias aisladas supera el 20% para trimetoprim/sulfametoxazol y cefalosporinas de primera generación y el 50% para amoxicilina2,3-6.
La epidemiología de las bacterias resistentes a los antibióticos varía entre tipos de infección, y algunas condiciones de uso regionales que deben ser bien documentadas6,7. También se han identificado factores asociados con la resistencia a los antibióticos usados en IVU; para ciprofloxacina han sido reportados anomalías del tracto urinario, la edad mayor de 65 años, cateterismo urinario y el tratamiento previo con fluoroquinolonas como factores asociados a resistencia por parte de E. Coli8. En la región no se han identificado factores asociados a la resistencia de antibióticos.
El uso empírico de los antibióticos de manera inadecuada en el tratamiento de las IVUs puede facilitar el desarrollo de resistencia a los agentes antimicrobianos, lo cual plantea un gran reto para los clínicos y para los investigadores, ya que los datos sobre la prevalencia de uropatógenos y la sensibilidad a los antimicrobianos varían entre centros de atención y ciudades y deben ser identificados para cada hospital7,9-11. Es por esto que se buscó determinar los principales agentes etiológicos y la frecuencia de resistencia a los antibióticos por parte de los microorganismos aislados en urocultivos y antibiogramas de pacientes a los que previamente se había diagnosticado IVU.
Metodología
Se realizó un estudio descriptivo de corte transversal sobre los principales agentes etiológicos, el perfil de sensibilidad y resistencia a los antibióticos utilizados en los pacientes con diagnóstico de IVUs del Hospital San Pedro y San Pablo de la Virginia, Risaralda, en el periodo de estudio comprendido entre el 1 de abril de 2014 y 31 de marzo de 2015.
Se realizaron dos tipos de análisis:
1. Identificación de los urocultivos, de los fármacos evaluados para sensibilidad y resistencia en el antibiograma. Se identificaron las bacterias aisladas en la totalidad de urocultivos procesados y los resultados de los antibiogramas en el laboratorio clínico y microbiológico del hospital durante todo el periodo de estudio. Dichos urocultivos fueron procesados mediante la técnica manual de chromagar orientador del proveedor Beckton Dickinson Diagnostics (BD) con asa calibrada, incubación a 37ºC por 24 horas y se incluyeron en el análisis aquellos con más de 100.000 Unidades Formadoras de Colonias por mililitro (UFC). Además, se evaluaron todos los cultivos que tuvieron su correspondiente antibiograma basados en el método manual de la difusión de disco Kirby-Bauer mediante el uso de sensidiscos Beckton Dickinson Diagnostics (BD) BBL™ Sensi-Disc™ para definir la sensibilidad y resistencia a los antibióticos bajo los parámetros de Clinical and Laboratory Standards Institute (CLSI).
2. Se realizó un muestreo aleatorio simple con la población total de pacientes con diagnósticos de IVU durante el periodo de estudio, (proporción esperada de tratamiento efectivo del 65%, error permisible del 5,0% e intervalo de confianza del 95%). A partir de las historias clínicas, previo consentimiento por parte del hospital, se construyó una base de datos con variables sociodemográficas (sexo, edad, raza, tipo de afiliación al Sistema General de Seguridad Social en Salud [SGSSS]), clínicas (tratamiento ambulatorio/hospitalario, Clasificación de las IVUs según lo consignado y definido por el médico tratante: infección de vías urinarias bajas, pielonefritis, infección vías urinarias complicada, infección vías urinarias en embarazadas), comorbilidad/factores de riesgo (sexo, diabetes, riñón único, insuficiencia renal, urolitiasis, inmunodeficiencias, alteración anatómica en vías urinarias, sonda vesical permanente) y la comedicación dispensada (antiplaquetarios, antiinflamatorios, antidiabéticos, hipolipemiantes, antiulcerosos, inmunosupresores y corticoides).
Se incluyeron los antibióticos usados para el manejo de la IVU: nombre del medicamento, dosis, vía de administración, días de administración; se incluyó como prescripción adecuada todos aquellos antibióticos aceptados como manejo de primera o segunda línea según lo consignan las recomendaciones de las guías Infectious Diseases Society of America (IDSA), las guías europeas sobre el manejo de infección de vías urinarias, y las guías de tratamiento de infecciones del tracto urinario bajo en adultos y embarazadas en Colombia2,11; se aceptó como manejo inadecuado la ausencia de prescripción de un antibiótico a pesar de haber definido diagnóstico de IVU, y también aquellos pacientes en quienes no se utilizaron los antibióticos recomendados para el manejo empírico de primera o segunda línea según las guías de práctica clínica referidas.
Para el análisis de los datos, se utilizó el paquete estadístico SPSS Statistics, versión 22.0 (IBM, EE. UU.) para Windows. Se empleó estadística descriptiva como promedio, desviación estándar, valores mínimos y máximos para variables continuas y porcentajes para variables categóricas. Se realizaron las pruebas de la t de Student o ANOVA para la comparación de variables cuantitativas y de la X 2 para las categóricas.
Se aplicaron modelos de regresión logística binaria usando como variable dependiente el uso adecuado o no del antibiótico para IVU y como variables independientes aquellas que se asociaron de manera estadísticamente significativa en los análisis bivariados. Se determinó como nivel de significancia estadística una p<0,05.
El protocolo fue sometido a aprobación por el Comité de Bioética de la Universidad Tecnológica de Pereira en la categoría de “investigación sin riesgo”, según la resolución No. 8430 de 1993 del Ministerio de Salud de Colombia, que establece las normas científicas, técnicas y administrativas para la investigación en salud.
Resultados
De un total de 2418 pacientes que presentaron IVU durante el periodo de estudio, se realizaron 1563 urocultivos, de los cuales 409 presentaron algún crecimiento de uropatógenos, y de estos, 329 (21,0%) mostraron crecimiento mayor a 100.000 UFC.
Análisis de sensibilidad y resistencia
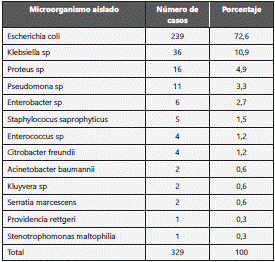
Los microorganismos más frecuentemente aislados fueron en primer lugar Escherichia coli, seguido de Klebsiella sp y Proteus sp como puede observase en la tabla 1.
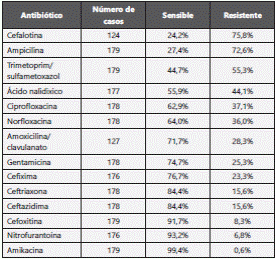
Con respecto a los antibióticos analizados en los antibiogramas, sobre el perfil de susceptibilidad de E. coli mostró mayor frecuencia de sensibilidad para amikacina, nitrofurantoina y cefoxitina como se muestra en la tabla 2; por otro lado, se halló un perfil de resistencia con mayor frecuencia para cefalotina, ampicilina y trimetoprim/sulfametoxazol.
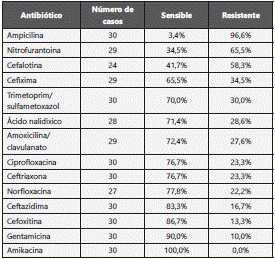
En el análisis de Klebsiella sp se observó un mayor porcentaje de sensibilidad para amikacina, seguido de gentamicina, cefoxitina y ceftazidima. En cuanto a la resistencia, los que presentaron mayor proporción fueron ampicilina, seguido de nitrofurantoina y cefalotina como puede observarse en la tabla 3.
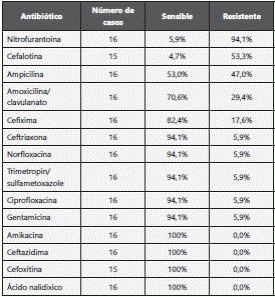
En la tabla 4 se puede observar que la mayor sensibilidad para Proteus sp está dada para amikacina, ceftazidima, cefoxitina, ácido nalidixico. En cuanto a la resistencia, a los fármacos que más se presentó fueron nitrofurantoina, cefalotina y ampicilina.
Análisis de pacientes
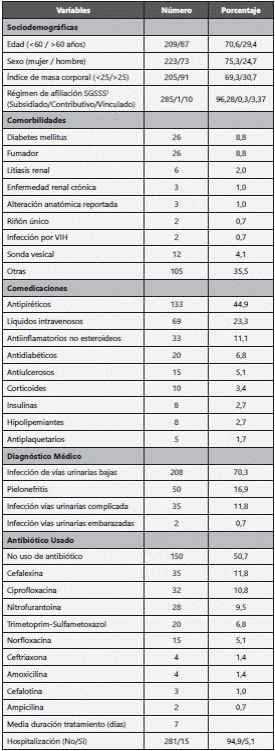
Las variables clínicas, farmacológicas y sociodemográficas de los 296 pacientes seleccionados aleatoriamente se incluyen en la tabla 5. Las IVUs fueron más frecuentes entre mujeres, menores de 60 años, con una edad media de 42,0±24,0 años. La IVU baja fue el diagnóstico médico más frecuente seguido de la pielonefritis.
Las condiciones coexistentes más comunes fueron diabetes mellitus, urolitiasis y la presencia de sonda vesical; mientras que entre las comedicaciones más frecuentemente prescritas estaban los antipiréticos y antiinflamatorios no esteroideos (AINEs) (tabla 5).
Análisis de la prescripción de antibióticos
El antibiótico inicial más formulado fue cefalexina en 35 casos (11,8%), seguido de la ciprofloxacina (n=32, 10,8%). A 150 pacientes (50,7%) no se les prescribió ningún antibiótico. El 4,4% de los pacientes recibieron antibióticos por más de 10 días y solo se hallaron 72 pacientes (24,32%) que presentaban tratamiento adecuado (tabla 5).
Análisis multivariado
La regresión logística mostró que el uso de antiulcerosos (OR: 4,28; IC95%: 1,070-17,153; p=0,04) se asoció de manera estadísticamente significativa con una mayor probabilidad de que se eligiera inadecuadamente el antibiótico, mientras que el uso concomitante de líquidos endovenosos (OR: 0,12; IC95%: 0,047-0,307; p<0,001) se asoció con menor probabilidad de que el antibiótico elegido fuera incorrecto.
Discusión
El presente estudio permitió identificar los principales agentes etiológicos y el perfil de resistencia a los antibióticos de estos microorganismos aislados por urocultivo en pacientes diagnosticados con IVU en la Virginia, Risaralda, entre los años 2014 y 2015. Se analizó un importante número de pacientes con este diagnóstico que lo hace comparable con lo reportado por otros autores en diferentes poblaciones13-17.
Respecto a los agentes etiológicos aislados, el patógeno más frecuentemente encontrado fue E. coli seguido por Klebsiella sp, lo cual es similar a los hallazgos de múltiples estudios tanto locales como internacionales3,14,15,17-19. Proteus sp fue hallado en el tercer lugar de frecuencia, y este varía entre el segundo a quinto agente causal más común3,12,14,20,21. En algunos estudios se ha presentado un aumento de los casos de IVUs por Pseudomonas sp, la cual es más frecuente cuando al paciente le han colocado una sonda vesical o cuando recibió algún antibiótico profiláctico previo19, sin embargo, no es considerado como un patógeno frecuente, como sí lo son Corynebacterium urealyticum encontrado en pacientes con IVU asociada a urolitiasis, manipulación de la vía urinaria o trasplante renal y S. aureus que puede estar asociado a bacteriemia o absceso renal20-23.
Cabe destacar la presencia de Acinetobacter baumanii en dos casos. Se ha reportado alta resistencia antibiótica para este bacilo gram negativo en pacientes con diagnóstico de IVU secundaria a uso de sonda vesical internados en unidades de cuidados intensivos24.
Con respecto a los patrones de sensibilidad y resistencia de los diferentes uropatógenos a los antimicrobianos de uso común para el tratamiento de la IVU, se encontró que E. coli presenta resistencia superior al 30% para trimetoprim/ sulfametoxazol, cefalotina, ciprofloxacina, norfloxacina y ampicilina. Diferentes investigaciones muestran una creciente alta resistencia bacteriana a trimetoprim/sulfametoxazol a pesar de que se recomienda su uso exclusivamente después de tener acceso a un antibiograma que demuestre sensibilidad12,23,25-28. En este estudio, el 42,9% de los pacientes recibió al menos uno de los antibióticos mencionados. Además, comparado con el estudio realizado en Pereira, Risaralda, se presentó una mayor resistencia para cefalotina, trimetoprim/ sulfametoxazol y ampicilina por parte de E. coli, evidencia clara de la importancia de caracterizar los microorganismos causantes de IVU en cada población3.
Se han encontrado para ciprofloxacina resistencias elevadas tanto en el presente estudio como en estudios internacionales (37,1% vs; 56,0% en Lima, Perú, 41.9% en Medellín- Colombia; 70,4% también en Perú, 11% en Chile y 28,1% en Pereira-Colombia)3,27,29-31; este aumento estaría asociado a un mayor uso del antibiótico sin prescripción médica o, a su formulación inadecuada3,12,31.
Se debe tener en cuenta que el 50,7% de los pacientes no recibieron tratamiento antibiótico a pesar de contar con el diagnóstico clínico de IVU, lo cual es contrario a lo recomendado por las guías de práctica clínica2,12. Para el diagnóstico de las infecciones no se requieren pruebas adicionales a una anamnesis dirigida y en caso de ser necesario (2 síntomas de IVU o menos) se solicitará gram de orina sin centrifugar, o tirillas reactivas para nitritos y esterasas leucocitarias para guiar el diagnóstico e iniciar el tratamiento inmediato de forma empírica. Un manejo apropiado contribuye a la curación clínica y microbiológica, a prevenir la reinfección y evitar complicaciones mayores32.
Adicionalmente en este estudio se halló una asociación entre el empleo inadecuado del antibiótico con el uso concomitante de antiulcerosos, fármacos frecuentemente prescritos de forma inapropiada, en indicaciones diferentes a las aprobadas y sin reportes que indiquen beneficios en el tratamiento de infección de vías urinarias33. Diversos estudios han encontrado asociación entre el uso de IBPs y el desarrollo de neumonía adquirida en la comunidad y las infecciones intrahospitalarias por Clostridium difficile, esto relacionado con una disminución de la acides gástrica, reduciendo así una barrera innata para las bacterias34,35. También se ha reportado una asociación entre IBPs y eventos clínicos adversos, donde las IVUs se han reportado como uno de los más frecuentes, pudiendo ser un factor asociado a resistencia bacteriana en esta patología, siendo un interesante tópico para futuras investigaciones36. Además, se ha reportado que los pacientes con uso de IBPs tienen frecuentemente asociadas características de salud que los predisponen a algunas condiciones médicas adversas, por lo que el uso generalizado e incorrecto de los IBP podría ser un factor de confusión36.
Entre las limitaciones del trabajo se debe tener en cuenta que los pacientes objeto de estudio fueron adultos de un hospital de primer nivel y en su mayoría pertenecientes al régimen subsidiado del SGSSS, por lo que se puede extrapolar a poblaciones con características similares. Tampoco se conocen las razones de la elección los antibióticos formulados por parte de los médicos o de la no selección de ninguno en aquellos casos en los que no se prescribieron. Este estudio no permite definir si se omitieron factores de riesgo previos importantes a la hora de definir el manejo por parte del médico como los son el uso de antibióticos días antes, la manipulación de la vía urinaria, si se trataba de recurrencias, si había uso de medicamentos inmunosupresores, si se trataba del primer episodio o no de IVU, entre otros, debido a que la información se obtuvo de los registros de las historias clínicas y se limita a lo consignado por el médico tratante.
En el análisis de sensibilidad y resistencia se encontró que algunos antibiogramas no analizaron siempre los mismos antibióticos, por lo cual en esos casos no estaban presentes el mismo número de pruebas para un antibiótico; solo se incluyeron para este análisis los antibiogramas que fueron reportados completamente. Se desconoce cómo se tomaron las muestras de orina (micción espontanea, sondaje o punción suprapúbica), ya que se acudió directamente a los análisis de las mismas, por este motivo solo se tuvieron en cuenta los urocultivos con crecimiento mayor a 100.000 UFC, pudiendo quedar por fuera pacientes con muestras tomadas por sonda o punción suprapúbica en que un menor crecimiento bacteriano en el urocultivo sería significativo.
Se debe continuar la identificación de los patógenos etiológicos que causan infección del tracto urinario y, posteriormente, la susceptibilidad a los antibióticos para ayudar a los médicos en la determinación de la opción más apropiada del tratamiento antimicrobiano empírico. También se deben desarrollar trabajos que evalúen y comparen la resistencia reportada a los antibióticos en los urocultivos y la respuesta clínica de los mismos en los pacientes en los cuales se usaron a pesar de encontrar resistencia, pues se describen diferencias entre esta y la respuesta clínica, como en el caso del trimetoprim/sulfametoxazol donde se reportan tasas de curación microbiológica en pacientes con cepas sensibles en 86% y con cepas resistentes en 42%32.
En conclusión, en este trabajo encontramos que en los pacientes atendidos en este hospital se halló una resistencia bacteriana superior al 20% a aminopenicilinas, trimetoprim/ sulfametoxazol, cefalosporinas de primera generación y quinolonas, especialmente a ciprofloxacina por parte de E. coli y Klebsiella sp; lo que sugiere la importancia de identificar y caracterizar los microorganismos y los perfiles de sensibilidad a los antimicrobianos en cada población y hospital para definir con mejor criterio cuales deben ser los antibióticos que se deban elegir en la primera línea del manejo empírico. A un importante número de pacientes no se les inicio tratamiento antibiótico a pesar de haber realizado diagnóstico clínico de IVU lo que puede llevar a complicaciones secundarias a esta infección, situación que obliga a emprender programas de actualización y capacitación al personal médico.