Introducción
La paracoccidioidomicosis (PCM) es una enfermedad tropical desatendida que constituye la micosis sistemática más importante de América Latina. La mayor prevalencia se encuentra en Brasil con 30 casos por millón de habitantes seguido de Venezuela, Ecuador, Argentina y Colombia1,2. La infección es causada por el hongo dimórfico térmico del complejo Paracoccidioides3,4, afecta principalmente a hombres agricultores durante los años más productivos de su vida, de manera que, además del impacto clínico por la afectación de pulmones, mucosas, piel, ganglios linfáticos, bazo, glándulas suprarrenales e incluso sistema nervioso central; la enfermedad acarrea altos costos sociales, económicos y constituye un grave problema de salud pública en la región5,6.
Lo anterior pone de manifiesto la necesidad de un diagnóstico correcto para estimar la prevalencia en poblaciones de riesgo y brindar tratamiento oportuno7. En este orden de ideas, las pruebas inmunológicas se han empleado como una buena alternativa porque en adición al diagnóstico diagnóstico, permiten dar cuenta de la monitorización de la evolución y la respuesta al tratamiento8, además pueden ser más simples y menos costosas que las moleculares, lo que facilitaría su implementación. Entre las principales pruebas inmunológicas se encuentran la inmunodifusión en gel de agar (ID), inmunofluorescencia indirecta, pruebas de ELISA, inmunotransferencia y Western Blot2,9-14. En estas pruebas existe una importante variabilidad con respecto a la obtención del antígeno y las preparaciones antigénicas que van desde mezcla de antígenos crudos, parcialmente purificados y purificados como la gp4315, lo que podría tener implicaciones en el desempeño diagnóstico, particularmente en la especificidad por la reactividad cruzada con otros microorganismos16.
Por otro lado, estudios previos han descrito alta heterogeneidad en parámetros de validez diagnóstica, así para la ID los datos de sensibilidad oscilan entre el 65% y 100% utilizando filtrados de cultivos y Ag 7, en la contrainmunoelectroforesis la sensibilidad varía entre 77% a 97% con una especificidad de 95%15,16, mientras para la ELISA se ha reportado una sensibilidad entre 95% y 100% y una especificidad de 88% y 93,4% utilizando filtrados de antígenos y gp43 respectivamente17. Lo expuesto evidencia alta diversidad de pruebas de inmunodiagnóstico, heterogeneidad en los resultados de validez diagnóstica, reportes parciales de la utilidad diagnóstica en la medida que los estudios previos no incluye parámetros de gran relevancia para orientar la toma de decisiones como las razones de verosimilitud o área bajo la curva, a lo que se suman posibles problemas de potencia estadística en algunos estudios con bajo número de pacientes18 o sujetos sin la infección.
Por lo anterior, el objetivo de este estudio es evaluar la validez diagnóstica de las pruebas inmunológicas en la infección por Paracoccidioides, a partir de un metaanálisis de la literatura publicada entre 1972-2017.
Material y método
Protocolo de búsqueda y selección de los estudios según las fases de la guía PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-Analyses)19
Identificación: Se realizó una búsqueda de artículos por especificidad con términos DeCS (Descriptores en Ciencias de la Salud) y por sensibilidad con términos no incluidos en te sauros y en buscadores abiertos como google, en las bases de datos PubMed, Sciencedirect, Scielo, Scopus, Ovid, Ebsco y Google scholar. En la búsqueda se utilizaron los términos paracoccidioides AND sensitivity, paracoccidioides AND specificity, paracoccidioides AND diagnosis, paracoccidioides AND validity, paracoccidioides AND predictive value. Adicional a lo anterior se escribieron a algunos autores para identificar artículos no disponibles en las bases de datos consultadas. Se realizó la búsqueda en Lilacs, sin hallar resultados adicionales a los identificados en Scielo.
Algunas estrategias de búsqueda en PubMed fueron ((Paracoccidiodes [Title/Abstract]) AND sensitivity [Title/Abstract]); en OVID (Paracoccidiodes and specificity).ab.; en ScienceDirect TITLE-ABSTR-KEY (Paracoccidiodes AND diagnosis) y en Scielo (ab:(Paracoccidiodes)) AND (ab:(validity)).
Tamización: Se incluyeron estudios con los términos de búsqueda en título, resumen y/o palabras clave, sin restringir temporalidad, publicados en inglés, portugués y español, que fuesen artículos originales, realizados en humanos y que su objetivo fuese evaluar pruebas diagnósticas para la infección por Paracoccidioides. De manera retrospectiva no se aplicaron restricciones, la publicación más antigua data de la década de los 1970 y de manera prospectiva la última aplicación del protocolo de búsqueda y selección de estudios se realizó en diciembre del 2017.
Elección: Se excluyeron los estudios que evaluaran pruebas moleculares, detección de antígenos o pruebas imagenológicas, que tuviesen la información incompleta, y que no fue posible obtener en texto completo pese al envío de mensajes a los autores.
Inclusión: Los artículos que cumplieron con los criterios anteriores se incluyeron para la síntesis cualitativa de las variables: título, autores, año de publicación, revista, lugar de procedencia de los pacientes incluidos, número de pacientes, sexo, prueba evaluada, muestra biológica, tipo de antígeno o antígenos utilizados, verdaderos positivos (personas infectadas con la prueba evaluada positiva), falsos positivos (personas sin la infección positivos en la prueba), falsos negativos (infectado con prueba negativa) y verdaderos negativos (sanos con prueba negativa).
Reproducibilidad y evaluación de la calidad metodológica
El protocolo de búsqueda y selección de los artículos, así como la extracción de las variables del estudio, se realizaron por dos revisores de manera independiente para garantizar la reproducibilidad de estos dos procedimientos. Para la eliminación de duplicados se exportaron los títulos de los artículos obtenidos al programa Zotero 5.0 (Corporation for Digital Scholarship Viena)®; al finalizar esta etapa se inició el proceso de clasificación de las investigaciones mediante la lectura de los resúmenes. Se extrajo la información de manera independiente por parte de los investigadores con el fin de garantizar la reproducibilidad de la extracción de las variables del estudio. La evaluación de la calidad metodológica se hizo con la aplicación de la guía QUADAS (Quality Assessment of Diagnostic Accuracy Studies)20.
Análisis de la información
Para cada una de las pruebas se evaluó la validez a través de los parámetros de sensibilidad, especificidad, razón de verosimilitud positiva, razón de verosimilitud negativa, razón de odds (OR) diagnóstica y el área bajo la curva ROC, todos con sus respectivos intervalos de confianza del 95%. Para la interpretación de los parámetros, se consideraron resultados satisfactorios para el diagnóstico de la infección por Paracoccidioides (o adecuada discriminación de sanos e infectados) una razón de verosimilitud negativa <0,3, razón de verosimilitud positiva >4,0, área bajo la curva ROC >0,85 y la OR diagnóstica mayor que 10.
La información fue analizada en el software Meta-DiSc (The meta-analysis of studies of evaluations of diagnostic and screeningtests) con un nivel de significación de 0,05. Este software calcula la prueba Chi-cuadrado, Tau2 y la prueba de inconsistencia (I2) para el análisis de la heterogeneidad de los parámetros de sensibilidad, especificidad, razones de verosimilitud, OR diagnóstica y el área bajo la curva ROC, los cuales son estimados como una medida combinada usando un modelo de efectos aleatorios. Para el análisis de sensibilidad del metanálisis se estima el porcentaje de peso de cada estudio en la medida global de las razones de verosimilitud, con el fin de asegurar que ningún estudio presenta un mayor efecto sobre la medida combinada.
Se realizó meta-regresión o análisis de subgrupos, según el tipo de antígeno usado y la calidad metodológica de los estudios.
Resultados
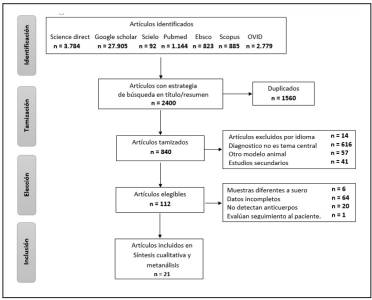
En la aplicación de las diferentes estrategias de búsqueda y fuentes de información se identificaron 2.400 artículos con los términos de búsqueda en el título, resumen y/o palabras clave, se tamizaron 840 artículos de los cuales se eliminaron 728 por no cumplir los criterios de inclusión. De los artículos elegibles se excluyeron seis por tratarse de muestras de esputo, líquido cefalorraquídeo, orina y lavado broncoalveolar, 64 por no reportar los datos para el cálculo de los verdaderos positivos, falsos positivos, verdaderos negativos y falsos negativos, 12 publicaciones que evaluaban pruebas moleculares, tres artículos para la detección de antígenos y cinco estudios sobre otros métodos diagnósticos (Figura 1).
Los artículos incluidos fueron publicados entre los años 1972 y 2017 donde se evaluaba la detección de anticuerpos para antígenos de P. brasilensis y P. lutzii en suero, 13 estudios evaluaron más de una prueba y las pruebas analizadas incluyen inmunodifusión, western blot, ELISA, aglutinación en látex, entre otras. Los sujetos de estudio provenían principalmente de países como Brasil y Colombia, los estudios incluyeron diferentes tamaños de muestra que oscilaron entre 42 y 551, en total se incluyeron 6.156 individuos, 1.404 sanos, 2.415 con otras infecciones y 2.337 con infección por Paracoccidioides, 92,7% fueron hombres (Tabla 1).
Tabla 1 Descripción de los estudios con base en el año de publicación, país, prueba y sujetos evaluados.
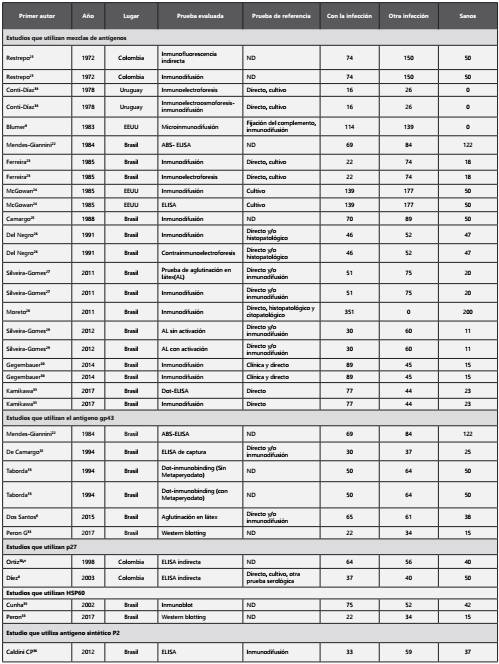
*Se calcula la validez diagnóstica para la forma aguda, crónica y residual
Se identificaron 22 estudios que evaluaron la precisión diagnóstica de las pruebas utilizando una mezcla de antígenos. La mayoría de estos estudios aplicaron la técnica de inmunodifusión. Se identificaron siete estudios que reportan una sensibilidad del 100%, la menor fue reportada por Gegembauer (2014) con 59% (IC95% 33 - 82)30. En alusión a la especificidad, en 12 investigaciones fue del 100%, la menor fue reportada por el estudio de Silveira-Gomes (2012) con 79%29. La mayoría de las reacciones cruzadas al usar los exoantígenos de P. brasilensis se presentan para pacientes con aspergilosis e histoplasmosis.
Seis autores evaluaron la detección de anticuerpos para la glicoproteína purificada gp 43, todos en pacientes de Brasil. Se obtuvo una sensibilidad del 100% en las pruebas de Dot inmunobinding con y sin la utilización de mataperyodato de sodio (Taborda)13, seguido de 98,4% reportado para la prueba de inmunoensayo con partículas de látex (Dos santos)8. La sensibilidad más baja fue reportada por Peron et al para la prueba de western blotting con 91%, por su parte la mayor especificidad fue reportada para la metodología de Dot inmunobinding con metaperyodato de sodio 100% (Taborda)13 y la más baja fue reportada para el test de látex 94% (Dos santos)8.
En los estudios realizados en Colombia la mejor sensibilidad se obtuvo en el estudio de Díez con 92% (IC95% 78-96) (8) y la menor en el de Ortíz con 73% (IC95% 61-84)34. En alusión a la especificidad, la mejor se encontró en el estudio de Ortiz con 90% (IC95% 55-100)34. La proteína HSP60 fue otro de los antígenos evaluados; sin embargo, su desempeño no alcanzó el 80% en ninguno de los parámetros (Perón 2017)33.
En general, los estudios presentaron un nivel medio o satisfactorio de calidad, aunque los criterios relacionados con la descripción del estándar fueron deficiente (Figura 2). Vale precisar que la mayoría de estudios (n=19) no realizaron una selección aleatoria de los participantes y la mayoría, al reclutar sujetos en centros asistenciales, seguían la lógica de la investigación basada en casos y controles. También se debe aclarar que el criterio QUADAS “interpretación de la prueba evaluada sin conocimiento de la referencia” no fue posible evaluarlo dado que en la metodología no se explicitan la forma de procesar las muestras (los investigadores si conocían el resultado del estándar, pero no explicitan si hubo cegamiento o independencia de quienes procesaron la evaluada).
En el metanálisis global se encontró heterogeneidad en todos los parámetros evaluados (Valor p Chi cuadrado <0,05). La medida combinada en el modelo de efectos aleatorios para la sensibilidad fue de 92,2% (IC 95% 91,1 - 93,2), la especificidad de 95,1% (IC 95% 94,3 - 95,8) y el área bajo la curva de 0,99 (Figura 3). En adición, el metanálisis de efectos aleatorios para los demás parámetros de la evaluación diagnóstica, estimó una razón de verosimilitud positiva de 24,7 (IC 95% 14,2 - 42,9), la razón de verosimilitud negativa de 0,08 (IC 95% 0,05 - 0,12) y la OR diagnóstica de 495,9 (202,1 - 1216,6).
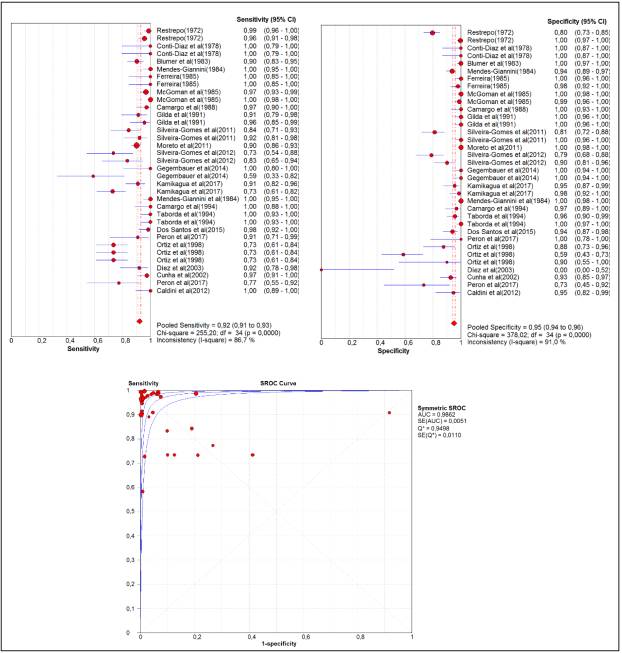
Figura 3 Metanálisis de la sensibilidad, especificidad y áreaba bajo la curva ROC para el total de pruebas inmunológicas en la infección por Paracoccidioides
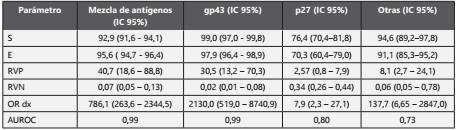
En la Tabla 2 se compara la validez diagnóstica según los antígenos evaluados. Los estudios que utilizan mezclas de antígenos y los que utilizan gp43 evidenciaron resultados satisfactorios en todos los parámetros con diferencias significativas en la sensibilidad y especificidad; por su parte, en la combinación de estudios que utilizaron el antígeno p27 no se hallaron resultados aceptables en ninguno de los parámetros. Al excluir del metanálisis las publicaciones con menor calidad metodológica sólo disminuye la sensibilidad en las pruebas que utilizan mezcla de antígenos a 88,9% (86,8 - 90,8); en los demás parámetros, al igual que en los estudios que utilizan gp43, no se hallaron diferencias estadísticamente significativas.
Discusión
La literatura relacionada con el inmunodiagnóstico de la Infección por Paracoccidioides es extensa y diversa. En este metanálisis se identificaron 21 estudios publicados entre los años 1972 al 2017, realizados en su mayoría en pacientes de Colombia y Brasil, con predominio de la infección en hombres. Este hallazgo coincide con la literatura descrita en la medida que la PCM es endémica en Colombia y Brasil, este último concentra alrededor del 80%de los casos reportados en el mundo37,38. Con respecto al sexo, los datos coinciden con estudios previos que han descrito que la proporción de la infección en hombres respecto a las mujeres varía desde 5,4:1 hasta 11,7:138 lo que apoya la hipótesis del factor protector de las hormonas femeninas en la infección por Paracoccidioides sp39-41.
Este estudio puso de manifesto que para el diagnóstico serológico de PCM se han empleado diferentes preparaciones antigénicas que incluyen pool de antígenos, antígenos purificados o recombinantes gp43, p27, proteína de choque térmico HSP60 y el antígeno sintético P2. En alusión a la glicoproteína de 43 kda (gp43), se encontró que los test que la utilizaron reportaron los valores más altos en todos los parámetros de validez diagnóstica. Una explicación a estos resultados se encuentra en que la gp43 es la proteína más predominante e inmunogénica de P. brasiliensis, lo que se ve reflejado en los altos niveles de anticuerpos anti-gp 43 en pacientes que presentan la forma grave de la enfermedad42. De hecho, el 100% de los pacientes con PMC mostraron resultados positivos cuando fueron evaluados con el ensayo de Dotinmunobinding13. Sin embargo, algunos autores enfatizan que no se recomienda el uso de una única preparación de antígeno en las pruebas serológicas convencionales, ya que se han encontrado bajas concentraciones de esta glucoproteína en filtrados del cultivo de cepas de P. lutzii; así como variaciones en su producción entre aislados pertenecientes a la misma especie42. Sumado a ello, la complejidad técnica para su purificación, así como los costos asociados16 hacen que sea preferible la utilización de un pool de antígenos.
En coherencia con lo anterior, en este estudio la mayoría de investigaciones utilizaron mezclas antigénicas en las pruebas serológicas como derivados de la pared celular, citoplasmáticos y filtrados de cultivo43. Al respecto, algunos investigadores sostienen que existen múltiples dificultades en la estandarización para obtener mezclas de antígenos, puesto que ellos varían en calidad dependiendo del aislado del hongo, la fase morfológica, las condiciones de cultivo, el tiempo de inoculación, la técnica empleada, el uso de múltiples subcultivos17 y además, afectan la especificidad por la presencia de antígenos compartidos con otros hongos44. No obstante, este estudio puso en evidencia que a pesar de la variabilidad en los parámetros descritos, todos los criterios de validez diagnóstica que utilizaron mezclas de antígenos fueron satisfactorios y muy próximos a los que utilizaron el antígeno específico gp43. En este sentido, estudios posteriores deberían evaluar la costo-efectividad en la utilización de ambas técnicas.
Por otro lado, con el fin de estandarizar la obtención del antígeno y mejorar el serodiagnóstico de la PCM se ha propuesto la identificación de antígenos específicos alternos a la gp43 como la P27, HSP60 y el antígeno sintético P2. En alusión a la proteína p27 en este estudio no se encontraron resultados satisfactorios en la medida combinada de ninguno de los parámetros de validez diagnóstica evaluados. Ortiz et al reportaron una especificidad del 87,5%, la cual disminuye al comparar la reactividad con sueros heterólogos a 58,7%; así como una sensibilidad del 73,4%, sugiriendo que la proteína p27 puede representar un sólo epítope y por lo tanto ser reconocido sólo por algunos pacientes con PCM34. Por otro lado, la HSP60 pertenece a la familia de proteínas de choque térmico (HSP) y es altamente inmunogénica, sin embargo su desempeño en los estudios incluidos varió significativamente pese a la utilización de la misma técnica (Western blotting ), Cunha et al., indica una sensibilidad de 97,3% y especificidad de 92,5%35, mientras que Perón et al reporta 77,3% de sensibilidad y 73% de especificidad con evidencia de reacciones cruzadas en pacientes con histoplasmosis, probablemente originado por la homología de la proteína con HSP presente en Histoplasma capsulatum y en sujetos sanos por la presencia de anticuerpo anti-HSP33.
El antígeno que tuvo el mejor desempeño fue el péptido sintético P2 con una sensibilidad del 100% y una especificidad del 94,6% por ELISA, este estudio realizado por Pistelli et al afirma que el antígeno presenta características de mimotopo a gp7536 la cual es una proteína de superficie con actividad fosfatasa bien caracterizada45. Una de las ventajas de este péptido es que puede ser modificado para mejorar el reconocimiento y disminuir las reacciones cruzadas con sueros de otras micosis, convirtiéndose en una prometedora alternativa de estandarización serológica para esta micosis, además que es una estrategia más barata, simple y reproducible, en comparación con la purificación de proteínas36.
Entre las técnicas incluidas en este estudio se encuentran la inmunodifusión, inmunoelectroforesis, Dot-inmunobinding, Western blotting, Inmunoblot, ELISA y pruebas de aglutinación en látex. Durante años la inmunodifusión ha sido la prueba serológica de elección para el diagnóstico de pacientes con Infección por Paracoccidioides; no obstante, es una técnica engorrosa que requiere mucho tiempo para su ejecución31. Algunos laboratorios sugieren que la inmunoelectroforesis podría implementarse como prueba de rutina para la tamización de la PCM en pacientes con sospecha clínica debido a la rapidez con la que se pueden obtener los resultados; no obstante, otros autores argumentan que el tiempo es prácticamente el mismo que en la inmunodifusión; además que en la inmunoelectroforesis es necesario un buffer de agarosa y una fuente de poder, condiciones que no siempre están disponibles en zonas endémicas de países subdesarrollados16. En este contexto, la ELISA se ha convertido en una técnica popular para la identificación de anticuerpos de manera que puede aplicarse en la práctica clínica habitual o en investigación, esta técnica ha sido ampliamente aceptada como una prueba rápida, versátil, simple de realizar y económica, que utiliza reactivos de larga duración que pueden ser almacenados fácilmente, además, que se pueden determinar diferentes clases de inmunoglobulinas permitiendo así una evaluación más precisa de la respuesta inmune humoral16,31.
En alusión a la calidad metodológica de las evaluaciones diagnósticas se encontró alto riesgo de sesgo en el dominio de selección de los pacientes, el cual se dio a expensas de la no inclusión de una muestra aleatoria o consecutiva, lo que podría derivar en un sesgo de espectro clínico. Si bien este tipo de sesgos afecta en mayor medida la validez externa que a los parámetros de precisión diagnóstica; la aplicabilidad o extrapolación de los resultados de estudios individuales será limitada debido a las posibles diferencias en el espectro de pacientes, lo cual hace referencia no sólo al estadio de la enfermedad sino también a las características demográficas y a la presencia de comorbilidades. En este sentido, el metanálisis, al resumir la información de estudios desarrollados en diferentes contextos, podría mejorar la validez externa o extrapolación de resultados a diferentes lugares, aunque el nivel de evidencia que se genera depende de la calidad de los estudios originales, en este caso, comprometida porque algunos estudios son básicamente de casos y controles valida dos con muestras históricas de pacientes con paracoccidiodomicosis (en algunos casos con patología) y en otras con muestras históricas de pacientes presumidos (no es claro como se hizo el diagnóstico de la enfermedad) lo que sobreestima seriamente la sensibilidad46. Evaluaciones diagnósticas posteriores deberían incluir un mejor espectro clínico y una descripción detallada de la población incluida20.
Entre las principales limitaciones de esta investigación se encuentra la dificultad para acceder a algunas publicaciones, ya que cerca de 30 estudios no se pudieron recuperar a pesar de escribirles a los autores. Además, no fue posible hacer un análisis por subgrupos debido a la escasa información reportada para variables clínicas como la presencia de inmunosupresión, la presentación aguda, crónica o residual, el tipo de lesión y el agente causal.
Pese a las limitaciones descritas este estudio permite concluir que las pruebas inmunológicas disponibles para el diagnóstico serológico de la infección por Paracoccidioides generan resultados satisfactorios en todos los parámetros de validez diagnóstica, con excepción de los que utilizan como antígeno p27. Sumado a ello, no se encontraron diferencias clínicamente importantes en los índices de validez diagnóstica de los estudios que utilizaron pool de antígenos o la proteína específica gp43. Sin embargo, el nivel de evidencia es bajo debido a la calidad metodológica de los estudios incluidos.