Introducción
La ventriculitis es una forma grave de presentación de infección del sistema nervioso central, que a menudo requiere largos periodos de antibióticos endovenosos. Los criterios para inicio de terapia intraventricular son relacionados al fracaso terapéutico luego de haber utilizado drogas por vía endovenosa1 .
La terapia intraventricular ha sido utilizada con éxito. Entre los antibióticos utilizados por vía intraventricular se citan principalmente vancomicina y colistina 2-4.
Las dosis recomendadas de tigeciclina en pediatría no están muy bien establecidas, ya que se han reportado fracasos de tratamiento con dosis de 2,5 mg/k/día, aunque se citan dosis mayores de hasta 6 mg/k/dia 5,6. Por otro lado, su penetración en sistema nervioso central no es óptima. El aumento de la dosis no asegura el éxito en el tratamiento de las infecciones del SNC6,7).
Reportamos aquí el uso de tigeciclina intraventricular en seis casos de ventriculitis ocasionada por Enterococcus faecium, resistente a vancomicina(EVR) y a otros antibióticos. Presentacion de casos Se presentan seis casos de ventriculitis causada por Entecococcus faecium, resistente a vancomicina. Todos ellos con antecedente de procedimiento neuroquirúrgico previo a la infección en más de una oportunidad, uso de antibióticos de amplio espectro y colonización rectal por EVR.
Presentación de casos
Se presentan seis casos de ventriculitis causada por Entecococcus faecium, resistente a vancomicina. Todos ellos con antecedente de procedimiento neuroquirúrgico previo a la infección en más de una oportunidad, uso de antibióticos de amplio espectro y colonización rectal por EVR.
Todos ellos con secuelas neurológicas importantes. No se detectó tabiques en el espacio ventricular en la Tomografía Computarizada Cerebral en ningún paciente.
El diagnostico de ventriculitis se estableció según criterios de Lozier y cultivo positivo en todos los casos8 .
El Enterococcus faecium aislado fue sensible a cloranfenicol, linezolid y quinupristin-dalfopristin y tigeciclina en diversos porcentajes. (Tabla 1) Los criterios de sensibilidad y resistencia de los gérmenes se establecio según criterios del Clinical and Laboratory Standards Institute (CLSI). De estas opciones terapéuticas, la única que se encuentra disponible en nuestros centros asistenciales es la tigeclina.
Tabla 1 Sensibilidad del Enterococcus faecium. Puntos de corte establecidos por Clinical and Laboratory Standards Institute (CLSI). N= 6
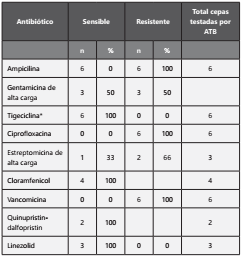
ATB: antibióticos
*corte <0,25
El primer caso detectado fue tratado al inicio con tigeciclina EV a 2,5 mg/kp/dia en dos dosis y la dosis intraventricular fue de 2,5 mg/dia. Este fue el único caso que presentó recaida a los ocho días de finalizado el primer ciclo de tratamiento, razón por la cual se incrementò la dosis del antibiótico a 4 mg/kp/dia por via EV y a 4 mg/dia por via intraventricular, dosis que se mantuvieron para la recaida del caso número uno y los cinco siguientes casos. Todos fueron tratados con tigeciclina por vía endovenosa a 4 mg/k/día en dos dosis y ante la persistencia del crecimiento bacteriano en liquido ventricular, a pesar de la terapia endovenosa se decidió el inicio de la terapia intraventricular previo consentimiento informado a los padres, con tigeciclina a 4 mg/día, repetidos cada 24 horas.
Protocolo de aplicación de tigeciclina
Se reconstituyó la tigeciclina liofilizada con cloruro de sodio (0,9%), de manera a obtener una concentración de 10 mg del antibiótico por cada centímetro cubico de la solución. De esta mezcla, se tomó 4 mgr a ser diluidos en 2,5 cc de líquido cefalorraquídeo (LCR) del mismo paciente, tomado a través del catéter de derivación ventricular externo (VDE). Una vez que la mezcla del antibiótico y LCR se realizara, se procedió a la instilación intraventricularde la misma, cerrando la VDE por espacio de una hora.
El inicio de la terapia intraventricular se decidió en base a consentimiento de los padres y cultivos persistentemente positivos para EVR en LCR a pesar de terapia EV. Las muestras de LCR se tomaron cada 48 a 72 horas para los cultivos pertinentes.
Todos ellos mejoraron y presentaron criterios citoquímicos de curación en el LCR. El tratamiento con tigeciclina intraventricular se prolongó por cinco a siete días más luego de la obtención del primer cultivo de LCR negativo. Sólo un caso presentó recaída con crecimiento del germen luego de ocho días de terminado el primer ciclo de tratamiento, por lo que se procedió a reinicio de la terapia endovenosa e intraventricular, con lo cual se logró la curación en forma rápida.
Los datos de los pacientes pueden observarse en la tabla 2.-
Tabla 2 Características de los pacientes que recibieron tigeciclina intraventricular
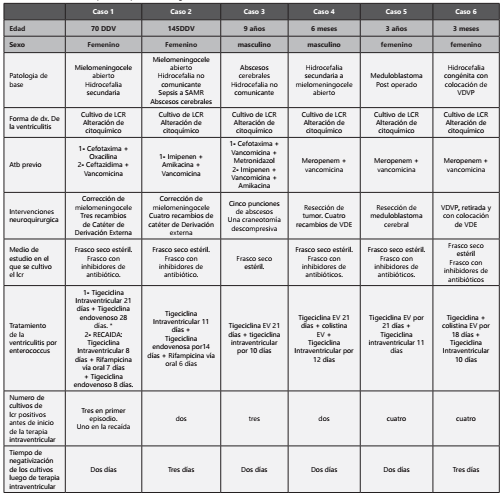
d: día VDE: válvula de derivación externa
*caso inical en el que se utilizó 2,5 mg intraventricular en el primer episodio., subiendo a 4 mg/día para tratamiento de la recaída.
Luego de la terapia, no se detectó empeoramiento de los pacientes con respecto a su estado neurológico basal. No encontramos efectos o eventos neurológicos atribuibles a la terapia intraventricular tales como empeoramiento del estado de alerta, convulsiones o focalizaciones.
Discusion
La tigeciclina es un antibiótico bacteriostático de amplio espectro, del grupo de las glicilciclinas. Ha sido aprobado para uso en adultos, pero su utilización en pediatría aún se encuentra restringida9 .
Tiene pasaje deficiente a través de la barrera hematoencefálica, lo que podría dificultar la esterilización del LCR cuando se administra sólo por vía endovenosa.
Ha sido utilizada por diversos expertos, en casos de gérmenes multirresistentes, sobre todo en casos de bacteriemias 6,7.
Los cálculos de las dosis para vía endovenosa para pacientes pediátricos se reportan de 2,5 mg/k/día, pero existen reportes diversos acerca de la dosis correcta, yendo de 2 a 6,5 mg/ kp/día10.
Existen reportes de uso de tigeciclina intraventricular utilizada a diferentes dosis; asi, algunos autores iniciaron con 2 mg intraventricular; pero se vieron obligados a doblar la dosis ante fracaso del tratamiento en el día 10 de terapia. Con dosis de 4 mg, se logró la cura11.
Otros autores presentan casos de uso de este antibiótico bajo dos modalidades distintas: dosis intraventricular simple (similar a la utilizada en nuestros casos) y la infusión ventricular continua. En ambos casos la utilizan a 4 mg en una o dos dosis12.
Independientemente de la dosis o modalidad utilizada para administrar la tigeciclina intraventricular, todos los autores mantienen la terapia EV, en conjunto con la intraventricular.
En nuestra casuística, utilizamos dosis de 4 mg/k/día EV solo por via EV en el primer caso. Aun con esta dosis, hubo fracaso en la esterilización del LCR, por lo que se planteó el uso de tigeciclina intraventricular de forma compasiva.
A la terapia endovenosa, se agregó la terapia intraventricular a dosis de 4 mg/día, en forma concomitante en todos los casos. La duración del tratamiento fue variable, retirándose el tratamiento Intraventricular cinco días después del primer G.C. Samudio-Domínguez, et al cultivo de LCR negativo. La terapia EV se mantuvo 21 días en promedio. En el primero de los casos se presentó recaída, por lo que se tuvo que repetir el tratamiento.
Hemos observado que la esterilización del LCR de nuestros pacientes se produjo más rápido que lo reportado por Long y colaboradores, los cuales presentan de 21 a 23 días de terapia antes de obtener cultivos negativos en el LCR en casos de ventriculitis por acinetobacter. No podemos saber si la esterilización más rápida podría deberse a una mayor efectividad del antibiótico cuando se administra toda la dosis una sola vez al día o a la respuesta del germen al antibiótico Se debe hacer un esfuerzo para medir los niveles de la droga y correlacionarlos con la esterilización del LCR. Lastimosamente, nosotros no contamos con la tecnología adecuada para poder realizarlo.
Si bien se citan efectos adversos hematológico y pancreático en la literatura13, no los presentaron ninguno de nuestros pacientes. Desafortunadamente no pudo realizarse la medición de la droga ni en sangre ni en LCR, lo cual habría sido fundamental para conocer la dosis optima que permita la esterilización del LCR.
Las dosis de tigeciclina en niños debería revisarse, ya que la misma es importante para asegurar la curación14.
Estos casos se suman a otros, en los cuales de uso exitoso de tigeciclina intraventricular fue exitoso15,16.
En conclusión, la tigeciclina intraventricular puede ser una opción de tratamiento exitoso en pacientes y lugares que no poseen otra alternativa terapéutica. Recomendamos que la terapia intraventricular sea acompañada de la terapia endovenosa y seguimiento estricto de los cultivos de LCR, a fin de retirar el antibiótico a la brevedad posible. La presencia de efectos adversos, debe ser monitorizada y, cuando sea factible, las dosis del antibiótico en LCR deben ser medidas a fin de establecer las dosis más adecuadas para el tratamiento.














