Introducción
Los avances tecnológicos en salud han logrado el aumento de la supervivencia de las personas que viven con el virus de la inmunodeficiencia humana (VIH) (PVV). Tanto es así que estudios recientes han encontrado una probabilidad de su pervivencia en PVV con tratamiento antirretroviral (TAR) del 96% durante el primer año después del diagnóstico y hasta del 88% a los 15 años1. De hecho, algunos estudios explo ran los riesgos de morir por enfermedades cardiovasculares, la enfermedad pulmonar obstructiva crónica y los cánceres, dado los largos tiempos de supervivencia de esta población2. Diferente a lo que ocurría hacia finales de 1985 en EE. UU., cuando se reportó que el 83% falleció durante el primer año y la tasa estimada de supervivencia al tercer año era del 11%3.
Estudios más recientes, realizados en China encontraron un tiempo medio de supervivencia de los casos de VIH/sida ma yor de 16 años entre 1997 y 20184 con un mayor riesgo de muerte al aumentar la edad, al detectar la enfermedad du rante el ingreso hospitalario en fase sida y no recibir TAR3. En relación con las personas con el síndrome de inmunode ficiencia adquirida (sida), se ha estimado que la probabilidad de supervivencia a ocho años desde el inicio del sida es del 78% en quienes reciben TAR. En contraste, la supervivencia a 6 años en pacientes con sida sin TAR es del 26%; conclu yendo así que más de la mitad de las PVV que reciben TAR sobrevivieron más de 10 años desde el inicio del sida y más de la mitad de las PVV que no reciben tratamiento mueren dentro de los dos años posteriores al inicio del sida1.
Entre los factores descritos en la literatura que afectan la supervivencia de las PVV están: sexo masculino, edad > 40 años, estadio clínico avanzado5, bajo índice de masa corpo ral6, el no uso temprano de la TAR7, el diagnóstico tardío de la enfermedad8 y la presencia de enfermedades oportunistas como la tuberculosis9. En cuanto a los resultados de labo ratorio también se han descrito variables pronóstico para mortalidad como: el bajo recuento de células T CD4+, la baja albúmina sérica, el recuento alto de glóbulos blancos, el por centaje elevado de neutrófilos y la anemia10.
En Colombia, la Cuenta de Alto Costo (CAC) (organismo téc nico no gubernamental que promueve la gestión de riesgos, la generación de resultados en salud y la gestión de cono cimiento de las enfermedades de alto costo) ha realizado seguimiento de los pacientes con VIH, gracias a la normati vidad vigente del país que obliga a las Empresas Administra doras de Planes de Beneficios de salud (EAPB) al reporte de todos los casos con VIH11. Estas entidades son las encargadas de la gestión de riesgo de los afiliados independiente si la afiliación es pagada por el trabajador y empleador (régimen contributivo), si es financiada con otros recursos (subsidiado) o si proviene de entidades que tienen su propio financia miento (universidades, fuerzas militares, policía nacional, me dicina prepagada y direcciones territoriales de salud). En un primer acercamiento a los análisis de supervivencia, la CAC encontró en una cohorte de 60 mil pacientes seguida duran te siete años una menor supervivencia en las PVV afiliadas al régimen subsidiado, estar en estadio sida y no recibir TAR12. Este artículo tiene como fin describir la supervivencia a siete años y los principales factores asociados a esta en las PVV que fueron atendidas en el sistema de salud colombiano y reportadas a la CAC entre el 1 de febrero de 2011 al 31 de enero de 2018.
Métodos
Población de estudio
Personas atendidas dentro del marco del Sistema General de Seguridad Social en Salud (SGSSS) diagnosticadas con VIH entre el 1 de febrero de 2011 al 31 de enero de 2018 y que fueron reportadas a la CAC en cumplimiento de la obligato riedad de este reporte13,14 por parte de las entidades encar gadas de la gestión del riesgo.
Variables
La variable principal es el tiempo de supervivencia o de censu ra de los pacientes, medida en años y estuvo delimitado por un primer evento el cual correspondió a la fecha de diagnóstico de infección por VIH y por un segundo evento definido como la fecha de muerte. La confirmación diagnóstica fue realizada según el algoritmo de la Guía de Práctica Clínica (GPC) basada en la evidencia científica para la atención de la infección por VIH/sida en adolescentes (con 13 años de edad o más) (15 y va lidada con los soportes de los laboratorios clínicos o el reporte en la historia clínica de la confirmación diagnóstica.
Se definió como censura a la derecha las pérdidas del se guimiento debido al abandono de la atención, muerte por causas externas o por finalización del seguimiento sin la ocurrencia del evento muerte. Los pacientes no censurados fueron quienes presentaron muerte por sida o por otra pato logía no definitoria de sida.
Covariables
Se seleccionaron de acuerdo con el marco conceptual de la investigación. Estas fueron medidas al momento del diag nóstico de VIH: sexo, edad, régimen de afiliación, región de residencia, conteo de linfocitos T CD4+, diagnóstico tem prano (definido como los pacientes diagnosticados con lin focitos T CD4+ ≥500 células/μL) y estadio clínico según el sistema de clasificación de los CDC 2008 16. También se midieron las variables: ultima carga viral para VIH, tiempo entre la fecha de diagnóstico y fecha de inicio de la primera TAR, presencia de enfermedades oportunistas definitorias de sida y comorbilidades durante el periodo de estudio.
Fuentes de datos
Los datos fueron tomados a partir de historias clínicas de personas con diagnóstico de VIH reportados a la CAC entre el 1 de febrero de 2011 al 31 de enero de 2018. La informa ción contiene datos sobre la población afiliada a cualquie ra de los regímenes según la ley 100 de 199317 o pacientes no afiliados al sistema de salud pero que son atendidos por las Secretarias de Salud de Colombia. Este proceso de re porte estandarizado de variables es obligatorio y se realiza mediante la Resolución 4725 de 201114 y la Resolución 783 del 201213, declaradas por el Ministerio de Salud y Protección Social de Colombia. Dicha información fue ingresada a un sistema de validación estandarizada que revisó la coherencia entre variables; posteriormente, los datos fueron auditados contrastándolos con los soportes de historia clínica y resulta dos de laboratorio remitidos a la CAC. En aquellos casos don de no coincidió lo reportado contra lo soportado, se realizó la corrección en la base de datos según la fuente primaria.
Descripción estadística de la población de estudio
Las variables categorizadas fueron presentadas en valores absolutos y relativos.
Análisis de supervivencia
Se realizó la descripción de la información marginal y por categorías de las variables de la muestra de supervivencia. Se aplicó el método de Kaplan-Meier para estimar la proba bilidad de supervivencia para diferentes periodos de tiempo a partir de la fecha de diagnóstico. También se evaluaron las funciones de riesgo, las gráficas de doble logaritmo comple mentario y se realizó la prueba de hipótesis log-rank para comparar la supervivencia entre las categorías de estudio.
Se ajustó un modelo de supervivencia paramétrico flexible de Royston Parmar, con una distribución de base modelada por una función del log-tiempo restringida por splines cúbicos18, debido a que, el modelo de Cox no cumplía con el supuesto de riesgos proporcionales, esto fue probado mediante el uso de los residuos de Schoenfeld y de Schoenfeld escalados. Para determinar la complejidad adecuada del número de nodos para caracterizar la función de base se realizaron pruebas de sensibi lidad variando el número de nodos internos de 1 a 8 y se evaluó mediante el criterio de información de Akaike (AIC) para deter minar el ajuste óptimo18. El modelo seleccionado fue un modelo con 3 nodos internos (4 grados de libertad). Se presentaron los resultados en una escala de Hazard ratios (HR) para facilitar la interpretación de los efectos de las covariables.
Se consideró significancia estadística a un valor de p menor que 0,05. Se utilizó STATA 13 (Stata Corporation, College Sta tion, TX, USA) para todos los análisis estadísticos.
Consideraciones éticas
En Colombia, la legislación permite a la CAC utilizar datos clí nicos sobre enfermedades de alto costo, reportados por las aseguradoras de salud, para auditar y generar información confiable. No se hizo ninguna intervención ni modificación in tencionada de variables biológicas, fisiológicas, sicológicas o sociales de los individuos participantes, por lo cual el estudio se clasificó como investigación sin riesgo según lo establecido en la Resolución 8430 de 1993 del Ministerio de Salud de la República de Colombia. Por lo anterior, no se requirió con sentimiento informado o aprobación ética. La CAC, tiene la responsabilidad de velar por la protección de los datos perso nales y clínicos de acuerdo con lo establecido en el artículo 15 de la Constitución Política de Colombia de 1991 desarrollado en la Ley estatutaria 1581 de 2012 “por el cual se dictan dis posiciones generales para la protección de datos personales”.
Resultados
Descripción estadística
Se obtuvo información en 64 907 PVV. De estos, 76,6% co rrespondieron al sexo masculino. El grupo de edad con ma yor número de casos fue entre los 25 a 49 años (60,6%). La mayor proporción de población pertenecía al régimen con tributivo. La región colombiana que reportó mayor número de casos fue la Central con el 27,0% de los casos (tabla 1).
Tabla 1 Características sociodemográficas y clínicas de la población de estudio
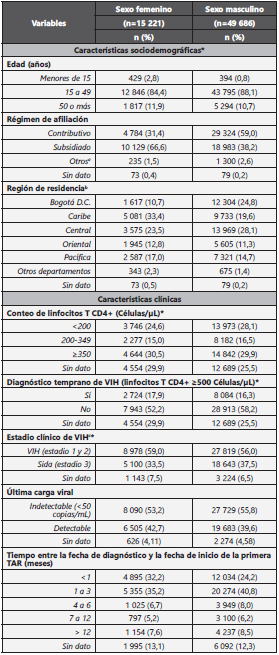
a. Incluye: régimen especial, régimen de excepción y no asegurado.
b. División acorde al producto interno bruto definido por el Departamento Administrativo Nacional de Estadística para el año 2017(19). Las divisiones son: Región Caribe: Atlántico, Bolívar, Cesar, Córdoba, Sucre, Magdalena, La Guajira. Región Central: Caldas, Risaralda, Quindío, Tolima, Huila, Caquetá, Antioquia. Región Oriental: Norte de Santander, Santander, Boyacá, Cundinamarca, Meta. Región Pacífica: Chocó, Cauca, Nariño, Valle. Otros departamentos: Amazonas, Arauca, Casanare, Guainía, Guaviare, Putumayo, San Andrés, Vaupés, Vichada.
c. Clasificación estadio de VIH CDC 2008
* Estas variables fueron medidas al momento del diagnóstico.
Entre las variables clínicas, solo el 16,7% del total de PVV tu vieron un diagnóstico temprano de la enfermedad. Adicio nalmente, se evidenció que, del total de pacientes con una clasificación de estadio al momento del diagnóstico, el 39,2% se encontraron en etapa de sida. Con respecto a la última carga viral (CV), el 55,2% de los pacientes se encontraban con cargas virales indetectables (<50 copias/mL).
Con relación al tiempo entre la fecha de diagnóstico y la fe cha de inicio de la primera TAR, se evidenció que el tiempo de mayor frecuencia fue menos de 1 a 3 meses (65,6%). La tabla 1 muestra la distribución de las características sociode mográficas y clínicas en hombres y en mujeres.
Las enfermedades oportunistas definitorias de sida que se presentaron con mayor frecuencia en el total de PVV duran te el periodo de estudio fueron la tuberculosis y la caquexia asociada a VIH con el 9,3% y 17,1%, respectivamente. Las co morbilidades más frecuentes fueron: la dislipidemia (14,2%), la anemia (8,5%) y otras enfermedades de transmisión sexual (15,5%) (tabla 2).
Análisis de supervivencia
Aproximadamente, entre las personas incluidas en la cohor te, el tiempo de seguimiento fue de mínimo 1 día y máximo 7 años. El 50% de los individuos tuvo seguimiento hasta por 2,7 años y el promedio (3,0 años) estuvo ligeramente por en cima de la mediana. La mortalidad ocurrió en 2 940 casos (4,6%), de los cuales 1 766 fueron muertes por sida (1,9%), 589 casos fallecieron por otra patología no definitoria de sida (0,9%) y 1 174 casos por causa externa (1,8%). La estimación de la supervivencia global (SG) a 7 años fue de 94,8% (IC 95%: 94,5-95,2).
Al analizar las curvas de Kaplan-Meier por categorías de las variables, la supervivencia a lo largo del tiempo de segui miento fue mayor en los menores de 15 años, pero fue dismi nuyendo a medida que aumentaban los rangos en los grupos de edad. El régimen subsidiado tuvo menor supervivencia (91,8%; IC 95%: 91,0-92,5), al igual que las personas que fue ron diagnosticadas en etapa sida (91,2%; IC 95%: 90,5-91,9) (figura 1).
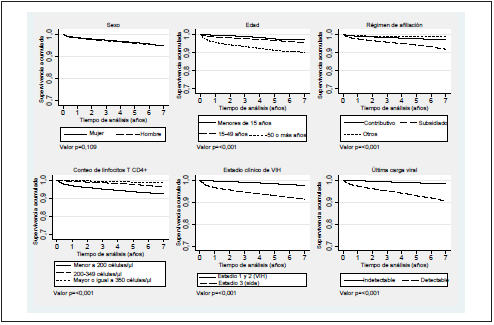
Figura 1 Curvas de supervivencia de Kaplan-Meier de variables sociodemográficas y clínicas en las PVV
Las PVV con conteo de linfocitos T CD4+ mayor de 350 cé lulas/μL tuvieron una supervivencia de 98,6% (IC 95%: 98,1- 98,9) mientras que en los de menos de 200 células/μL fue de 92,2% (IC 95%: 91,4-93,0). La supervivencia fue mayor en los pacientes con conteo de linfocitos T CD4+ mayores o iguales a 350 células/μL, pero fue menor a medida que disminuyeron los valores del conteo (figura 1).
El grupo que presentó la última carga viral indetectable tuvo una probabilidad de supervivencia a los 7 años de 98,3% (IC 95%: 98,0-98,6) mientras que en los detectable fue menor (90,4%; IC 95%: 89,4- 91,3).
La prueba de hipótesis de log-rank realizada a las caracte rísticas sociodemográficas y clínicas (listadas en la tabla 1), evidenció diferencias estadísticamente significativas entre las categorías de las variables excepto entre hombres y mujeres (p=0,1). En la figura 1 se presentan las curvas de superviven cia de Kaplan-Meier, junto con los resultados de la prueba de hipótesis de log-rank para las variables sociodemográficas y clínicas incluidas en el modelo de supervivencia realizado.
Modelo de supervivencia paramétrico flexible
Los resultados en la tabla 3 reflejan el modelo final ajustado por las variables detectadas como estadísticamente signifi cativas mediante la prueba Log-rank y las variables clínica mente relevantes encontradas en la literatura. Al ajustar por las variables incluidas en el modelo, el riesgo de muerte fue mayor en las personas de sexo masculino comparadas con las de sexo femenino (Valor p=0,010). También se observaron diferencias estadísticamente significativas en la superviven cia en las personas de 50 años o más a comparación de los menores de 15 años. El riesgo de muerte también se pre sentó mayor en las personas con un régimen de afiliación al sistema de salud subsidiado con respecto al contributivo. Igualmente, en pacientes con diagnóstico de sida a compara ción con VIH. Llama la atención el alto riesgo que representa la última medición de carga viral detectable a comparación con las personas que presentan una carga viral indetectable (valor p<0,001). Finalmente, en los pacientes con conteo de linfocitos T CD4+ menores a 200 y entre 200 a 349 células/ μL, se presentó un mayor riesgo de muerte a comparación de los pacientes con un conteo mayor o igual a 350 células/ μL (valor p<0,001).
Tabla 3 Modelo de supervivencia paramétrico flexible, ajustado con 3 nodos internos y 4 grados de libertad
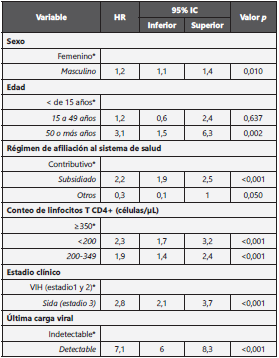
HR: Hazard ratio. IC: intervalo de confianza. *Categoría de referencia. A excepción de la última carga viral, las variables incluidas en el modelo fueron medidas al momento del diagnóstico de VIH.
Discusión
El VIH es una enfermedad que según la literatura, menos del 7% de las PVV se pueden comportar como no progresores a largo plazo y controladores de élite, manteniendo un recuento alto de células CD4 (≥500 células/mm3) y una carga viral baja o indetectable por un largo tiempo20. Por lo tanto, un gran porcentaje de PVV tienen un deterioro de su sistema inmu nológico facilitando la aparición de enfermedades definitorias de sida y por ende un mayor riesgo de mortalidad. Este estu dio es el primer análisis publicado que describe la probabili dad de supervivencia de las personas que viven con VIH que han sido reportadas a la Cuenta de Alto Costo y son atendidos en el sistema de salud colombiano; así como los factores de riesgo que están relacionados con una mayor mortalidad.
En el presente estudio, el sexo no tuvo un efecto significa tivo sobre el riesgo de muerte en el modelo sin ajustar; no obstante, al ajustarse se encontró que el sexo masculino pre senta un mayor riesgo de mortalidad. En países como Brasil7 e Irán21 se ha demostrado que las PVV de sexo masculino tienen un mayor riesgo de muerte, lo cual puede estar ex plicado por diferencias genéticas22 y condiciones sociocul turales como una mayor percepción de cuidado y adherencia de las mujeres a los programas de salud; y una búsqueda más temprana de los servicios de salud en las mujeres, es pecialmente por la oferta de la prueba diagnóstica durante el embarazo23. Por otro lado, el régimen subsidiado mostró un HR dos veces mayor que el contributivo, lo que podría ser una aproximación de las brechas de desigualdad en las po blaciones, así también lo muestra un estudio en Reino Unido el cual describe que las desventajas socioeconómicas están fuertemente asociadas con peores resultados en salud aún en un entorno con atención médica universal24.
En cuanto a la edad, nuestros resultados también son consis tentes con la literatura que muestra una menor probabilidad de sobrevivir a edades más avanzadas 25. Por ejemplo, un metanálisis26 realizado con PVV antes del TAR, identificaron la edad ≥45 años como un factor explicativo de la mortalidad tanto en pacientes con VIH-1 y VIH-2, concluyendo que la edad avanzada está asociada con la progresión clínica espe cialmente en aquellos que no han recibido TAR, por lo cual es importante el diagnóstico temprano y el inicio del trata miento27. Otro estudio4 realizado a través de un modelo de regresión de riesgos proporcionales de Cox mostró que los pacientes con más de 51 años tienen un HR de 1,90 (1,35- 2,68) comparado con las PVV ≤25 años.
El diagnóstico de la infección por el VIH es prioritario, pues es la entrada de los pacientes a la cascada del continuo de la atención para VIH y un indicador clave para el monitoreo de las estrategias en salud pública28 es así que nuestro estu dio mostró que el diagnóstico temprano de VIH (linfocitos T CD4+ ≥500 células/μL) mejora la supervivencia, información similar a otros estudios20. Este hallazgo debe permitir el fortalecimiento de acciones que minimicen las barreras para el diagnóstico temprano como la optimización del uso de diversas herramientas de diagnóstico aumentando el acceso a la prueba28.
El conteo bajo de linfocitos T CD4+ también ha documentado una relación inversamente proporcional entre el estado inmunológico y la mortalidad; un estudio en España mostró que por cada incremento de 50 linfocitos T CD4+ en el momento del diagnóstico, el riesgo de muerte disminuyó en un 83% (IC 95%: 82,0-84,0)29. Resultados recientes también evidencian que las PVV con recuentos de CD4 más bajos se relacionaban con mayor riesgo de mortalidad y morbilidad. Países como Perú, por ejemplo, mostraron una sobrevida de 68% a 8 años de seguimiento en PVV con menos de 100 células/mL, mostrando que la mortalidad va reduciéndose conforme incrementa el recuento de CD421.
Por otra parte, nuestro estudio también mostró que las personas en estadio sida (estadio 3) presentaron una menor supervivencia comparada con las PVV en estadio clínico VIH (estadio 1 y 2); los estudios también respaldan este hallazgo, encontrando por ejemplo que en un estudio en Puerto Rico30 la probabilidad de supervivencia a 6 años fue menor en el grupo de estadio sida (0,57; IC 95%: 0,55-0,60, p<0,001) en comparación con las personas en estadio de VIH (0,87; IC 95%: 0,09-0,72). Un metanálisis que incluyo 57 estudios también concluyó que la mayoría de los pacientes que reciben TAR sobrevivirán más de 10 años después de la aparición del sida, mientras que la mayoría de los pacientes que no reciben TAR mueren dentro de los 2 años siguientes a la etapa final de la enfermedad1 . La detectabilidad de la carga viral, en el transcurso del segui miento también evidenció mayor riesgo de mortalidad, infor mación congruente con un estudio31 que mostró que tener una alta carga viral alcanzaba un HR de 1,17 (IC 95%: 1,07- 1,48) para mortalidad. El seguimiento de la carga viral ha sido considerado un mejor predictor de muerte en PVV compara do con el recuento de linfocitos T CD4+, pues los pacientes tardan más en alcanzar un recuento de células CD4 normal y menos tiempo en alcanzar una carga viral indetectable.
Fortalezas y debilidades
Las fortalezas de nuestro estudio se traducen en la veracidad de la información, pues son datos que provienen de un regis tro nacional que surten un proceso de auditoría estandariza do para garantizar la validez de los datos, así como la obliga toriedad en el registro, que hace que un gran porcentaje de las PVV sean reportadas, por ser atendidos en el sistema de salud (Alrededor del 96% de la población colombiana se en cuentra afiliada al SGSSS32) mejorando la validez externa de los hallazgos y limitando el sesgo de selección. Por otro lado, al ser un registro anual se pudo hacer la trazabilidad histórica del seguimiento del paciente. No obstante, es un registro pa sivo que cuenta con sus propias limitaciones.
Existieron limitaciones que están relacionadas con el alto porcentaje de registros faltantes especialmente en las vari ables de enfermedades oportunistas definitorias de sida y comorbilidad, pues en el proceso de auditoria no pudieron ser verificables, lo que condiciona la descripción estadística (tabla 2) solo a la población con la información reportada y verificada. Este dato no reportado pudo ser por omisión, por sesgo de recuerdo o falta de soportes en el momento de validar el dato. Tampoco pudo ser incluida la variable re lacionada con el tipo de esquema usado al inicio de la TAR, dado que en un gran porcentaje de casos solo se validó uno o dos medicamentos cuando los esquemas están conforma dos con más de dos medicamentos. Por lo anterior, el análisis múltiple realizado está sujeto al sesgo de confusión residu al dado por la imposibilidad de ajustar por estas variables. Además, no se pudieron describir los diagnósticos especí ficos de muerte de la población dado que el registro solo captura la causa de muerte agrupada como: muerte por VIH/ sida, por otra patología no definitoria de Sida y muerte por causa externa, lo cual impide realizar un análisis por causa específica de muerte.
Conclusiones
Nuestro estudio describió que un diagnóstico temprano y un tratamiento oportuno puede cambiar el curso de la en fermedad en términos de supervivencia. Además estimó que la probabilidad de la supervivencia de las PVV aumenta en quienes al ser diagnosticados se encuentran en edades jóvenes, presenten un recuento mayor o igual a 350 células/ μL de linfocitos T CD4+, mantengan una carga viral inde tectable y no se encuentren en etapa sida. Estos hallazgos pueden orientar las acciones en el fortalecimiento de estrate gias y reorientación de los recursos en actividades dirigidas a la detección oportuna de los casos, a la tamización del VIH especialmente en menores de 50 años y a la integración in mediata de las PVV a los programas de VIH para garantizar el manejo adecuado de la enfermedad y el inicio temprano de la terapia antirretroviral. Por otro lado, se sugiere evaluar las debilidades en la gestión de la población masculina y en el régimen de salud subsidiado que limitan la supervivencia de estas subpoblaciones. Futuros estudios pueden ir encamina dos a la exploración de posibles interacciones entre las vari ables de estudio, así como el análisis de nuevas variables que puedan determinar la supervivencia en las PVV.