Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista de Salud Pública
Print version ISSN 0124-0064
Rev. salud pública vol.14 no.4 Bogotá July/Aug. 2012
Facultad de Ciencias Farmacéuticas, Universidad de Cartagena.Colombia. lfrancoo@unicartagena.edu.co, gmatizm@unicartagena.edu.co, indirabpb@hotmail.com
RESUMEN
Objetivo Determinar la equivalencia biofarmacéutica de marcas comerciales de Ciprofloxacino 500 mg disponibles en el mercado colombiano.
Métodos Se tomaron 12 productos comerciales de Ciprofloxacino tabletas 500 mg, adquiridos en droguerías y farmacias de cuatro de las principales ciudades del país, a los cuales se les realizaron los siguientes ensayos: Identificación del principio activo por HPLC, contenido de ingrediente activo, uniformidad de dosificación, pruebas de desintegración y disolución; además se compararon los perfiles de disolución de los productos frente a uno tomado como referencia. Los resultados se analizaron a fin de establecer diferencias estadísticamente significativas y posible intercambiabilidad entre los productos evaluados.
Resultados El análisis comparativo de los productos, permitió evidenciar marcadas diferencias en cuanto a la liberación in vitro del principio activo, con uno de los productos incumpliendo este importante parámetro de calidad. Todos los productos evaluados cumplen con las especificaciones oficiales de identificación y valoración del principio activo, uniformidad de dosificación y tiempo de desintegración. En cuanto a la cinética de disolución se encontraron diferencias entre las formulaciones, con productos de deficiente Eficiencia de Disolución (ED) y que a pesar de cumplir con la especificación a Q30, se disuelven muy lentamente.
Conclusiones Once productos cumplen con todas las especificaciones establecidas en la USP-33/NF28. Los resultados de este trabajo constituyen un valioso aporte para en un futuro cercano y en función de las políticas nacionales, poder establecer bioequivalencia entre estos productos.
Palabras Clave: Ciprofloxacino, biofarmacéutica, bioequivalencia, equivalencia genérica, disolución, cinética, control de calidad (fuente: MeSH, NLM).
ABSTRACT
Objective Determining the biopharmaceutical equivalency of 500 mg ciprofloxacin tablets available on the Colombian market (i.e. comparing different trademarks).
Methods Twelve commercial 500 mg ciprofloxacin tablets were obtained from drugstores and pharmacies in Colombia’s four major cities. They were submitted to the following assays: HPLC identification of active ingredients, active ingredient content, dose uniformity, disintegration and dissolution tests and comparing the products’ dissolution profiles to that of the innovator. The results were analyzed to establish statistically significant differences and possible inter-changeability between the products being tested.
Results Comparative analysis of the products revealed marked differences regarding in vitro release of the active principle (one product failing this important quality parameter). All the products tested here complied with the official specifications for identifying and assaying the active principle, dosage unit uniformity and the disintegration test. Regarding dissolution kinetics, differences were found between formulations as some products had poor dissolution efficiency (DE) and dissolved very slowly despite complying with the Q30specification.
Conclusions 11 products complied with USP33-NF28specifications (guidelines on specifications for impurities in antibiotics). This work has made a valuable contribution towards establishing these products’ bioequivalence in the near future regarding national policy.
Key Words: Ciprofloxacin, bio-pharmaceutics, bioequivalence, generic equivalency, dissolution, kinetics, quality control (source: MeSH, NLM).
La Organización Mundial de la Salud considera la accesibilidad a fármacos esenciales como uno de los problemas de salud pública de mayor importancia, especialmente en países con economías en desarrollo. Los fármacos esenciales son definidos como aquellos que satisfacen las necesidades de atención en salud de la mayoría de la población, los cuales deben estar disponibles en todo momento en las cantidades y formas farmacéuticas requeridas (1). En Colombia, la demanda de tales medicamentos la cubren el producto innovador y otros, que se pueden encontrar en el mercado con denominación genérica y/o marcas registradas; dos formas diferentes de alcanzar el objetivo de participar del mercado de una determinada molécula activa.
El costo de un tratamiento con medicamentos genéricos suele ser inferior respecto al que utiliza otros productos que contienen el mismo principio activo y en la misma forma farmacéutica, pero con denominaciones comerciales diferentes (2,3). Sin embargo, la introducción de medicamentos genéricos inicialmente estuvo acompañada de problemas de calidad, falsificaciones, adulteraciones, productos con bajas concentraciones o pobres disoluciones del principio activo, que podían afectar la efectividad del tratamiento (4). Esta situación comenzó a subsanarse cuando el legislador estableció la obligatoriedad del cumplimiento de las denominadas Buenas Prácticas de Manufactura (5); con lo cual, los laboratorios se dieron a la tarea de trabajar con elevados estándares de calidad; no obstante, la desconfianza ante productos diferentes al innovador subyace en la conciencia de médicos y pacientes. Para poder aclarar esta diferencia entre medicamentos innovadores y genéricos, se ha postulado que todos los medicamentos fabricados por competidores, debieran demostrar bioequivalencia para asegurar que su eficacia es comparable al original (6), pero al ser estos estudios tan costosos, la siguiente mejor opción son los ensayos analíticos biofarmacéuticoso ensayos de equivalencia farmacéutica in vitro, la cual se demuestra comprobando que los productos cumplen en forma similar con los parámetros de identidad, potencia, uniformidad de dosis, ensayo de disolución y perfiles de disolución, de acuerdo a especificaciones estable-cidas por una normatividad, en este caso las farmacopeas oficiales (7-9).
El ciprofloxacino es una quinolona sintética de segunda generación y agente bactericida de amplio espectro, frecuentemente prescrito a nivel hospitalario y ambulatorio para el manejo de infecciones microbiológicas de leves a persistentes (10,11). Químicamente es el ácido 1-ciclopropil-6-fluoro-1,4-dihidro-4-oxo-7-(1-piperazinil)-3-quinolincarboxílico, y ha sido clasificado por diversos autores como fármaco en clase II, III y IV dentro del Sistema de Clasificación Biofarmacéutica BCS (12,13). En el Instituto Nacional de Vigilancia de Medicamentos y Alimentos de Colombia (INVIMA), se encuentran alrededor de 47 Registros Sanitarios para tabletas de 500 mg de Ciprofloxacino(14), los cuales suponen materias primas, formulaciones, procesos de manufactura y políticas de precios diferentes de acuerdo al laboratorio fabricante, ofreciendo numerosas posibilidades de elección. Lo que resulta inquietante, tanto para el comprador institucional como para el particular, es tener que elegir entre un producto u otro aproximadamente 47 veces más costoso, sin tener elementos de juicio reales, pues en el mercado, a la fecha se encuentran productos con valores que oscilan entre $370 pesos colombianos/tableta y $17 500/tableta (3).
La pregunta obligada es: ¿Existe algún elemento de calidad involucrado que justifique tales diferencias? En este sentido, el presente trabajo evalúa una muestra de 12 productos de Ciprofloxacino clorhidrato tabletas de 500 mg, disponibles en el mercado colombiano, en cuanto a su identidad, potencia, uniformidad de dosis, tiempo de desintegración, disolución a punto final y perfiles de disolución, a fin de evidenciar o no homogeneidad en estos parámetros de calidad que permita plantear equivalencia farmacéutica.
Tabletas de Ciprofloxacino clorhidrato de 500 mg, correspondientes a 12 productos disponibles en el mercado farmacéutico colombiano, fueron adquiridos en farmacias y droguerías de las ciudades de Bogotá, Cali, Barranquilla y Cartagena. Los estudios se realizaron sobre 3 lotes de cada formulación, todos dentro del periodo de vida útil y se codificaron por marca con letras mayúsculas de la A hasta la L, siendo C el medicamento tomado como referencia.
Todos los ensayos fueron realizados siguiendo los métodos descritos en la USP-33/NF28 (15) previa validación de algunos parámetros. Las comparaciones se realizaron frente a un estándar de referencia secundario valorado con el estándar primario de Ciprofloxacino Clorhidrato USP Lote: 10C265.
Identificación y valoración del principio activo
Se pesaron y pulverizaron 10 tabletas de cada lote, disolviendo cuantitativamente con la fase móvil, correspondiente a una mezcla de acetonitrilo-ácido fosfórico 0,025 M (13:87) y ajustada a pH 3,0 ± 0.1; hasta obtener una solución con una concentración de aproximadamente 50 ppm, la cual fue filtrada a través de membrana PVDF(0.45 µm), e inyectada en el equipo de HPLC (LaChrom Elite®, Merck-Hitachi),equipado con detector de arreglo de diodos, bajo condiciones isocráticas, utilizando columna Chromolith® C-18 (150x5 mm), flujo 1.5 mL/min. La identificación y cuantificación se realizó a 278 nm, comparando frente a una curva de calibración preparada con el estándar a concentraciones de 20-80 ppm. Se prepararon tres muestras de valoración por cada lote.
Uniformidad de dosificación
Se realizó de acuerdo a lo indicado en el método de variación de peso establecido en el capítulo <905>USP-33 (15), sobre 10 tabletas/lote pesadas individualmente en balanza analítica (OhausAdventurer), calculan-do el porcentaje de ciprofloxacino en cada unidad, utilizando los valores obtenidos en la valoración, de acuerdo a la siguiente expresión:

Donde: Xi = Ciprofloxacino/unidad
Wi = Peso/unidad
A = Contenido de Ciprofloxacino obtenido en valoración
WÌ
= Peso promedio
Posteriormente se calculó el valor de aceptación (AV) definido en la USP-33. Se cumplen los requisitos de uniformidad de dosificación si el AV de las primeras 10 unidades analizadas es menor o igual a 15 %; en caso de que el AV sea mayor de 15 %, será necesario analizar 20 unidades adicionales.
Ensayo de desintegración
Se colocó una tableta en cada uno de los 6 tubos del equipo de desintegración (Vanderkamp 10-911-71c), utilizando agua desionizada como líquido de inmersión a 37°C±2,0°C, determinándose finalmente el tiempo promedio de desintegración para cada producto (15).
Velocidad de disolución
Se realizó sobre 6 unidades/lote, en un equipo de disolución Varian-705-DS, utilizando el aparato 2, agitación de 50 rpm, y como medio 900 mL de ácido clorhídrico 0,01N, a 37,0±0,5°C. 30 minutos después de iniciado el ensayo, se tomó una muestra filtrada de cada vaso (PVDF 0.45 µm). La cuantificación se realizó en un espectrofotómetro UV/Vis Shimadzu-1700, a 276 nm, empleando una curva de calibración construida con el estándar disuelto en el medio de disolución. La USP-33especifica que no menos del 85 % de lo declarado en el marbete (S1:Q80+5 %) se debe disolver en 30 minutos. Para productos que no cumplan primer criterio, el ensayo se repite sobre 6 unidades adicionales para evaluar el segundo criterio (S2: promedio de 12 unidades ≥Q y ninguna unidad <Q-15 %), si este no se alcanza, será necesario evaluar un tercer criterio S3 con doce unidades más (15).
Perfil de disolución
Los perfiles de disolución se construyeron bajo las mismas condiciones experimentales que la prueba de disolución, con la diferencia de que los muestreos se realizaron a los 2,4,8,10,20,30 y 45 minutos de iniciado el ensayo, reponiendo el volumen extraído inmediatamente con medio fresco equilibrado a 37,0±0,5°C.Se construyeron curvas de concentración vs tiempo para describirla liberación del fármaco de los comprimidos por cada lote y producto. Pese a que este parámetro como tal no es una prueba farmacopeica oficial, la FDA recomienda enfáticamente su utilización (16), dada la información que aporta, fundamental para hacer comparaciones; destacándose el valor de área bajo la curva (ABC), eficiencia de la disolución (ED) y factor de similitud (f2). El ABC es un valor adimensional, que construido de forma idéntica para cada producto en análisis, permite hacer inferencias de su comportamiento de disolución y compararlo con otros lotes o productos. El ABC fue calculada mediante la regla trapezoidal utilizando el software GraphPadPrism® versión 4.0. La eficiencia de la disolución (ED), caracteriza la liberación del fármaco, en este trabajo se definió como la razón entre el área bajo la curva de disolución hasta 45 minutos y el área total de un rectángulo que describe el 100 % de disolución a ese tiempo (17,18). El factor de similitud compara y determina numéricamente qué tan parecidos son dos perfiles de disolución entre sí. Es una medida de la similitud del porcentaje de disolución entre ambas curvas, se calculó a partir de la siguiente ecuación (8,9,19,20):
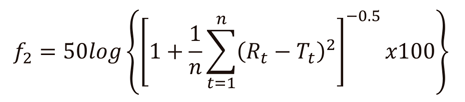
Donde: n = número de puntos experimentales
Rt = % de fármaco disuelto a cada tiempo de la referencia
Tt = % de fármaco disuelto a cada tiempo del producto
Este factor toma valores de 100 cuando los perfiles son idénticos y tenderá a cero a medida que se hacen más disímiles. La FDA sugiere que dos perfiles de disolución se consideran similares si 100≥f2≥50. Unf2≥50, refleja diferencias menores al 10 %, f2≥65, indica que las diferencias se reducen al 5 %, y cuando f2≥83 las diferencias se hacen incluso menores al 2 % (21).
Análisis de datos
Los resultados correspondientes a tres ensayos independientes fueron expresados como el promedio ±ESM y analizados mediante pruebas t frente a un valor de referencia y análisis de varianza de una vía (ANOVA), seguido de Dunnet o Tukeypost hoc para comparaciones múltiples. Valores de P<0,05 fueron considerados significativos.
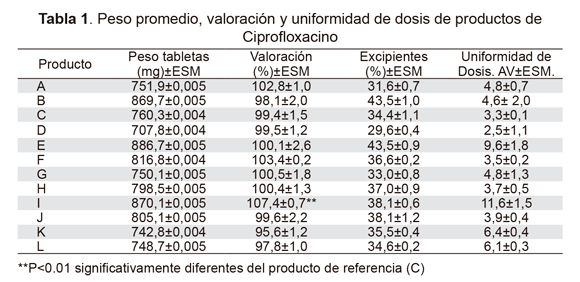
En la Tabla 1 se presentan los resultados obtenidos en los ensayos de valoración, uniformidad de dosificación y peso promedio, en todos los casos, los datos satisfacen las especificaciones farmacopeicas; con valores entre 95,6-107,4 % para el contenido de ingrediente activo, lo cual se ajusta correctamente a los limites de 90,0-110,0 %, y valores de aceptación (AV) entre 2,5-11,6 %, inferiores al 15 % establecido en la USP-33. El ensayo de peso promedio mostró que los productos distribuyen los 500 mg de ciprofloxacino en tabletas que oscilan entre 707,0-886,0 mg. Para la identificación del principio activo se compararon los cromatogramas obtenidos en el ensayo de valoración, evidenciándose total correspondencia en los tiempos de retención de las muestras y el estándar de referencia.
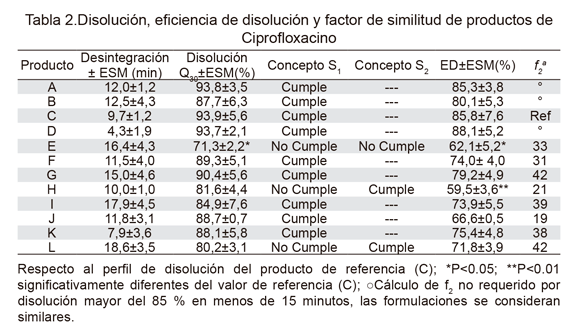
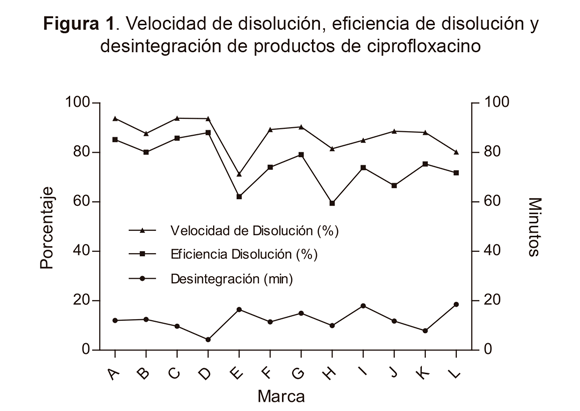
En la Tabla 2 se presentan los tiempos de desintegración, porcentajes de disolución, eficiencia de la disolución y el factor de similitud de los productos evaluados. Con respecto al tiempo de desintegración, los productos oscilaron entre 4,3-18,6 min, presentando el de referencia un tiempo de 9,7 min, lo cual no es indicativo de diferencias en la calidad de los productos dado que este ensayo no es exigido por la USP-33 para las tabletas de ciprofloxacino. Los resultados de la prueba de disolución revelan que 9 de las 12 marcas evaluadas, incluyendo el producto de referencia, cumplen con el criterio de disolución en S1, 2 de ellas alcanzan la condición en S2 (H y L), y el producto E nosupera S2, e incluso incumple una condición de S3, por lo que no se evaluó en tercer criterio. En relación a la eficiencia de disolución, los productos A, B, C y D presentaron valores similares, superiores al 80 % y estadísticamente comparables al de una disolución ideal del 100 %, por lo que se consideran biofarmacéuticamente equivalentes, mientras que el resto de los productos exhibieron baja ED con valores entre 59-79 %. El factor de similitud calculado para los productos indica que las formulaciones A, B y D tienen un comportamiento similar al producto de referencia (C), mientras que los restantes presentan diferencias superiores al 15 % con la referencia. En la Figura 1 se presenta el comportamiento promedio de los productos, observándose los tiempos de desintegración más altos para las marcas E, I y L, las que consecuentemente presentaron bajos valores de disolución. Por su parte el producto D refleja el mejor comportamiento con el menor tiempo de desintegración (4.3 min) y la mayor eficiencia de disolución (88 %).
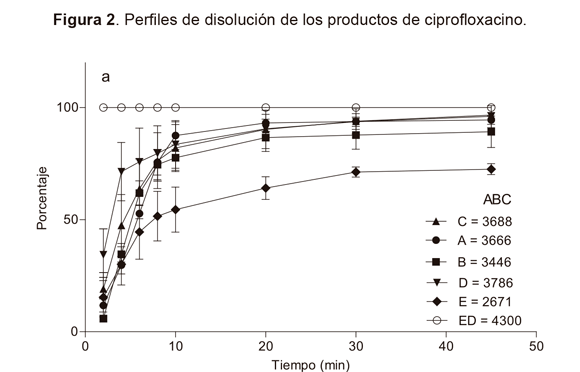
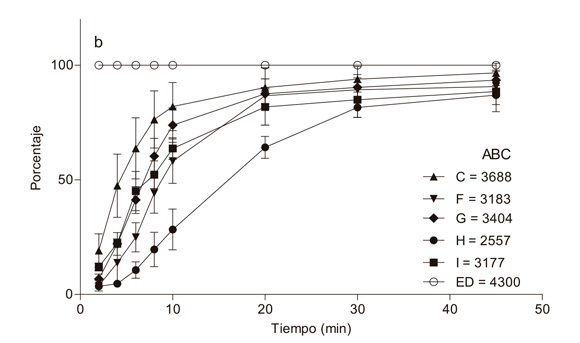
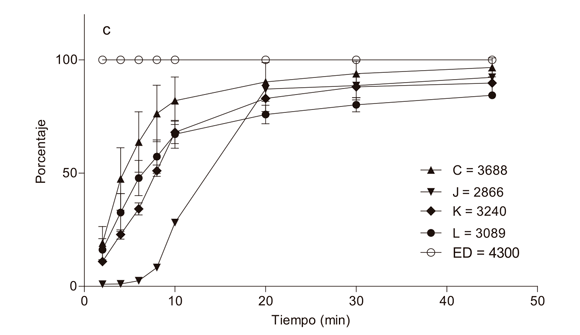
Los perfiles de disolución de los productos evaluados comparándolos con el de referencia se presentan en la figura 2, se observan comportamientos de disolución similares para la mayoría de los productos, liberando aproximadamente el 50 % del principio activo a los 10 minutos y más del 75 % a los 20 minutos, con excepción de los productos E (Figura 3a), H (Figura 3b) y J (Figura 3c) este ultimo mostrando una disolución lenta al inicio pero que posteriormente alcanza a cumplir con el requisito farmacopeico a Q30.
Los comprimidos son formas farmacéuticas sólidas, en las que para alcanzar un balance ideal requieren de la correcta aplicación de las artes y ciencias farmacéuticas. En estos sistemas de entrega del fármaco, a las considerables ventajas de uniformidad de dosis, facilidad de transporte, estabilidad química y economía de escala, se contraponen una menor liberación, disolución y biodisponibilidad presentes en una fórmula desbalanceada (22).
Respecto al contenido de principio activo, en este estudio no se encontraron diferencias significativas entre las marcas evaluadas y todos los lotes analizados cumplen con las especificaciones establecidas en la USP-33/NF28 para tabletas de ciprofloxacino. Igualmente, en el ensayo de uniformidad de dosificación por el método de variación de peso, se cumplieron los criterios farmacopeicos, y dado que ésta prueba es un indicador de la distribución homogénea del principio activo, se puede afirmar que todas las marcas presentan una adecuada y uniforme incorporación del ciprofloxacino durante su fabricación. Es notable la homogeneidad en el peso de las tabletas en todas las marcas, lo que permite entrever la calidad y uniformidad durante su proceso de fabricación.
Estudios de ciprofloxacino realizados en otros países, han mostrado resultados tanto favorables como desfavorables en cuanto al control de calidad físico-químico de los medicamentos genéricos (6,19,23-27).Uno de los análisis más discutidos en estos estudios, se refiere a los resultados de las pruebas de desintegración, en donde como en nuestro caso se presentan marcas con menores tiempos de desintegración (D y K) que el de referencia (C), y otras con tiempos de desintegración más prolongados, esto último afecta necesariamente la disolución y eficacia terapéutica del medicamento, ya que el principio activo se disuelve de manera acelerada solo cuando se han disgregado completamente los gránulos que dieron origen al comprimido, hecho especialmente crítico en formas farmacéuticas de liberación inmediata (24,27,28-30).
En este estudio, de manera similar a lo reportado por otros autores, se evidencia que aunque los productos evaluados cumplen con las especificaciones de valoración, sus disoluciones no son igualmente eficientes, lo que se puede atribuir a las diferencias en las formulaciones y/o procesos de manufactura del laboratorio fabricante. Además, una vez comprimido el producto, este puede sufrir cambios fisicoquímicos ya sea en la forma cristalina del fármaco o excipientes a formas menos solubles, esto asociado a una inestabilidad física del medicamento que el fabricante debe detectar en sus estudios de estabilidad y corregir para la renovación del registro sanitario (24,31).
El Sistema de Clasificación Biofarmacéutico (BCS), fue introducido para definir la correlación entre solubilidad, velocidad de disolución, y permeabilidad intestinal con la biodisponibilidad de los fármacos y de esta manera reducir los estudios de bioequivalencia con todas sus implicaciones éticas y económicas, favoreciendo la ejecución de pruebas in vitro específicas a fin de establecer bioequivalencia en productos orales de liberación inmediata de acción sistémica. Según esta clasificación, existen cuatro categorías (32): I (alta solubilidad y alta permeabilidad); II (baja solubilidad y alta permeabilidad); III (alta solubilidad y baja permeabilidad) y IV (baja solubilidad y baja permeabilidad). Para las categorías I y II, se esperan correlaciones importantes entre las pruebas in vitro e in vivo, para la clase III bajas o ausentes correlaciones, y para la clase IV, no se esperan correlaciones (33). Ciprofloxacino está clasificado entre las categorías II/IV.
Los perfiles de disolución realizados a los 12 productos de ciprofloxacino, mostraron marcadas diferencias entre ellos, lo que indica falta de homogeneidad en cuanto a la liberación in vitro del fármaco. Sólo tres de las formulaciones (A, B y D) pueden ser consideradas similares al producto de referencia (C) de acuerdo al factor de similitud f2 y biofarmacéuticamente equivalentes en función de la eficiencia de disolución (ED), sin embargo deben evaluarse en medios de disolución más biorelevantes para poder establecer con certeza la intercambiabilidad entre las marcas (23,34). Las formulaciones de los productos G, I, K y L son similares entre sí (f2≈40) y presentan diferencias hasta del 15 % entre sus perfiles y el producto de referencia. Los productos más disímiles con el de referencia resultaron ser E, F,H y J, con diferencias que van hasta el 40 % (35). Esta falta de homogeneidad entre los productos de ciprofloxacino tabletas también ha sido evidenciada en otros países latinoamericanos (19,24), mientras que estudios realizados en Europa, África y Asia han demostrado homogeneidad, bioequivalencia e incluso intercambiabilidad entre genéricos de ciprofloxacino tabletas con su respectivo innovador (26,30). La información recopilada en este trabajo no es suficiente para establecer si dos marcas de ciprofloxacino son o no intercambiables; esto sólo puede asegurarse mediante estudios de biodisponibilidad realizados para cada producto.
En conclusión, de los doce productos evaluados, once incluyendo la referencia cumplen con todas las especificaciones establecidas en la USP-33/NF28, siendo equivalentes farmacéuticos; sin embargo un análisis detallado del comportamiento cinético in vitro de la disolución muestra diferencias entre las formulaciones, lo que sugiere que su comportamiento in vivo podría también ser diferente. Posteriores estudios son requeridos para demostrar o no intercambiabilidad entre los productos de ciprofloxacino tabletas de 500 mg en el mercado colombiano. Este trabajo constituye un valioso aporte para en un futuro cercano y en función de las políticas nacionales, poder establecer bioequivalencia entre estos productos.
Agradecimientos: A la Universidad de Cartagena por la financiación de este estudio (Código Proyecto: 010-2009).
Conflicto de intereses: Ninguno
1. Chan M. The pharmaceutical scene in 2008â2009. Essential Medicines. Biennial Report. World Health Organization. 2010. [ Links ]
2. Palma-Aguirre JA. ¿Es lo mismo un original que una copia? Revista Médica IMSS. 2005;43(4):277-9. [ Links ]
3. Ministerio de Salud y Protección Social. [Internet]. Listado precios promedio y unidades en la cadena de comercialización de medicamentos.Circular 2 de 2012 Enero-Septiembre 2012. Disponible en:http://www.sispro.gov.co/.Consultado el 5 de julio de 2012. [ Links ]
4. Exebio LM. Aspectos éticos de los estudios de biodisponibilidad y bioequivalencia de productos farmacéuticos contenidos en las legislaciones de América Latina. Acta bioethica. 2004;10(2):247-259. [ Links ]
5. Congreso de la República de Colombia. Programa de Fortalecimiento Legislativo. Acceso a Medicamentos Esenciales y de Alto Costo. [Internet]. Disponible en:http://www.med-informatica.com/OBSERVAMED/Propiedad_intelectual/AccesoMedEsencialesYaltocosto.pdf. Consultado el 9 de julio de 2012. [ Links ]
6. Adegbolagun O, Olalade O, Osumah S. Comparative evaluation of the biopharmaceutical and chemical equivalence of some commercially available brands of ciprofloxacin hydrochloride tablets. Tropical Journal of Pharmaceutical Research. 2007;6(3):737-45. [ Links ]
7. Ruiz E, Rubini A, Mandel JS, Volonté M. Equivalencia farmacéutica de comprimidos conteniendo Naproxeno 500 mg. Latin American Journal of Pharmacy. 2007;26(4):530-5. [ Links ]
8. Food and Drug Administration. Formas posológicas orales sólidas de liberación inmediata. Cambios de escala y posteriores a la aprobación: documentación química de fabricación y controles de pruebas de disolución in vitro y bioequivalencia in vivo.[Internet].Disponible en:http://www.fda.gov/Drugs/GuidanceComplianceRegulatoryInformation/Guidances/ucm202142.htm.Consultado el 26 de octubre de 2011. [ Links ]
9. Food and Drug Administration.Guía para la Industria:Pruebas de disolución de formas de dosificación oral sólidas de liberación inmediata.[Internet].Disponible en: http://www.fda.gov/ Drugs/GuidanceComplianceRegulatoryInformation/Guidances/ucm200707.htm. Consultado el 26 de octubre de 2011. [ Links ]
10. Davis R, Markham A, Balfour J. Ciprofloxacin. An updated review of its pharmacology, therapeutic efficacy and tolerability. Drugs. 1996;51(6):1019-1074. [ Links ]
11. Schaeffer AJ. The expanding role of fluoroquinolones. The American journal of medicine. 2002;113(1):45-54. [ Links ]
12. Breda SA, Jimenez-Kairuz AF, Manzo RH, Olivera ME. Solubility behavior and biopharmaceutical classification of novel high-solubility ciprofloxacin and norfloxacin pharmaceutical derivatives. International journal of pharmaceutics. 2009;371(1-2):106-13. [ Links ]
13. Cook J, Addicks W, Wu YH. Application of the biopharmaceutical classification system in clinical drug development-an industrial view. The AAPS Journal. 2008;10(2):306-10. [ Links ]
14. INVIMA. Consulta de Registros Sanitarios para principio activo Ciprofloxacino. [Internet]. Disponible en: http://web.invima.gov.co/portal/faces/index.jsp?id=11464. Consultado el 22 de septiembre de 2011. [ Links ]
15. United States Pharmacopeia 33 and National Formulary 28. Pharmacopeial Forum On line 35(4). 2010. [ Links ]
16. Food and Drug Administration. U.S. Department of Health & Human Services. FDA U.S. Estudios de biodisponibilidad y bioequivalencia para productos farmacéuticos administrados oralmente-consideraciones generales. Guía para la industria. [Internet].Disponible en: http://www.fda.gov/Drugs/GuidanceComplianceRegulatoryInformation/Guidances/ucm201469.htm. Consultado el 10 de octubre de 2011. [ Links ]
17. Khan K. The concept of dissolution efficiency. Journal of pharmacy and pharmacology. 1975;27(1):48-9. [ Links ]
18. Cutrignelli A, Lopedota A, Trapani A, Boghetich G, Franco M, Denora N, et al. Relationship between dissolution efficiency of Oxazepam/carrier blends and drug and carrier molecular descriptors using multivariate regression analysis. International journal of pharmaceutics. 2008;358(1):60-8. [ Links ]
19. Brevedan M, Varillas M, González V, Pizzorno M. Evaluación de la equivalencia farmacéutica de comprimidos de ciprofloxacino del mercado argentino. Latin American Journal of Pharmacy. 2009;28(5):768-74. [ Links ]
20. Volonte MG, Sanchez L, Pasquale ME, Gaviria M. Equivalencia Farmacéutica de Comprimidos conteniendo 150 mg de Ranitidina. Acta Farmacéutica Bonaerense. 2007;25(3):393-400. [ Links ]
21. Food and Drug Administration. Guía para la Industria:Exención de los estudios de biodisponibilidad y bioequivalencia in vivo para formas posológicas orales sólidas de liberación inmediata en base a un sistema de clasificación de biofarmacéuticas. [Internet].Disponible en:http://www.fda.gov/Drugs/GuidanceComplianceRegulatoryInformation/Guidances/ucm201453.htm. Consultado el 6 de octubre de 2011. [ Links ]
22. Banker GS, Rhodes CT. Modern Pharmaceutics: Basic Principles and Systems, Fourt Edition, New York, Taylor & Francis; 2002. [ Links ]
23. Kyriacos SB, Boukarim C, Safi W, Mroueh M, Maroun A, Ghada E, et al. In vitro testing of ciprofloxacin formulations and preliminary study on BCS biowaiver. Journal of Food and Drug Analysis. 2009;17(2):78-84. [ Links ]
24. Martínez ME, Camacho IA, Gracia YA, Gracia SL. Evaluación in-vitro de doce marcas de comprimidos de ciprofloxacino que se comercializan en el mercado mexicano. Rev Mexicana de Ciencias Farmacéuticas. 2010;(4):43-9. [ Links ]
25. Trefi S, Gilard V, Malet-Martino M, Martino R. Generic ciprofloxacin tablets contain the stated amount of drug and different impurity profiles: A 19F, 1H and DOSY NMR analysis. Journal of Pharmaceutical and Biomedical Analysis. 2007;44(3):743-54. [ Links ]
26. Oishi TS, Haque MA, Dewan I, Islam SMA. Comparative in vitro dissolution study of some ciprofloxacin generic tablets under biowaiver conditions by RP-HPLC. 2011; 2(12): 3129-3135. [ Links ]
27. Mu'az J, Gazali L, Sadiq G, Tom G. Comparative in vitro evaluation of the pharmaceutical and chemical equivalence of multi-source generic ciprofloxacin hydrochloride tablets around Maiduguri metropolitan area. Nigerian Journal of Pharmaceutical Sciences. 2009;8(2). [ Links ]
28. Aulton ME. Farmacia: La ciencia del diseño de las formas farmacéuticas. Madrid.Editorial Elsevier. 2004. [ Links ]
29. Ngwuluka N, Lawal K, Olorunfemi P, Ochekpe N. Post-market in vitro bioequivalence study of six brands of ciprofloxacin tablets/caplets in Jos, Nigeria. Scientific Research and Essay. 2009;4(4):298-305. [ Links ]
30. Nayak A, Pal D. Comparative in vitro bioequivalence analysis of some ciprofloxacin HCl generic tablets. International Journal of Pharmaceutical Sciences and Research. 2010;1:1-7. [ Links ]
31. Fathy M, Hassan M, Mohamed F. Differential scanning calorimetry to investigate the compatibility of ciprofloxacin hydrochloride with excipients. Pharmazie. 2002;57(12):825-8. [ Links ]
32. Amidon GL, Lennernäs H, Shah VP, Crison JR. A theoretical basis for a biopharmaceutic drug classification: the correlation of in vitro drug product dissolution and in vivo bioavailability. Pharmaceutical research. 1995;12(3):413-20. [ Links ]
33. Gupta E, Barends D, Yamashita E, Lentz K, Harmsze A, Shah V, et al. Review of global regulations concerning biowaivers for immediate release solid oral dosage forms. European journal of pharmaceutical sciences. 2006;29(3):315-24. [ Links ]
34. Olivera M, Manzo R, Junginger H, Midha K, Shah V, Stavchansky S, et al. Biowaiver monographs for immediate release solid oral dosage forms: Ciprofloxacin hydrochloride. Journal of pharmaceutical sciences. 2011;100(1):22-33. [ Links ]
35. Frutos G, Ocaña J. Técnicas de remuestreo en la comparación de curvas de disolución de fármacos. Anales de la Real Academia Nacional de Farmacia.2011;77(2):1-19. [ Links ]













