Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista de Salud Pública
Print version ISSN 0124-0064
Rev. salud pública vol.16 no.6 Bogotá Nov./Dec. 2014
https://doi.org/10.15446/rsap.v16n6.31466
Artículo/Investigación
Evaluación de la capacidad acumuladora de mercurio del ají (Capsicum annuum)
Evaluation of the mercury accumulating capacity of pepper (Capsicum annuum)
Híver M. Pérez-Vargas1, Jhon V. Vidal-Durango2 y José L. Marrugo-Negrete3
1 Universidad de Sucre, Sincelejo, Colombia. hmpv84@yahoo.es
2 Corporación Universitaria del Caribe (CECAR). Sincelejo, Colombia. johnvidavi@yahoo.com
3 Universidad de Córdoba. Montería, Colombia. jlmarrugon@yahoo.com
Recibido 2 Agosto 2013/Enviado para Modificación 10 Junio 2014/Aceptado 12 Agosto 2014
RESUMEN
Objetivo Evaluar la capacidad acumuladora de mercurio por parte la planta de ají (Capsicum annuum), en suelos contaminados procedentes del corregimiento Mina Santa Cruz, Sur de Bolívar, Colombia, con el propósito de establecer el riesgo para la salud de la población consumidora.
Materiales y Métodos Se tomaron muestras de tejidos (raíces, tallos y hojas) de plantas de C. annuum sembradas en dos suelos contaminados con mercurio y un suelo control, durante sus primeros cinco meses de crecimiento para determinar mercurio total mediante la técnica de espectrofotometría de absorción atómica por vapor frio. Se determinó mercurio total en muestras de frutos de ají consumido en Mina Santa Cruz.
Resultados Las concentraciones medias de mercurio total en raíces fueron mayores en comparación con tallos y hojas. Los niveles de mercurio en suelos y el tiempo influyeron en la acumulación en tejidos. Las concentraciones de mercurio en frutos de C. annuum fueron bajas en relación a la ingesta tolerable semanal dispuesta por la OMS.
Conclusión Los porcentajes de translocación de mercurio a las partes aéreas de la planta fueron bajos tanto en el suelo control como en los suelos contaminados. A pesar de los bajos niveles de mercurio en este alimento se debe disminuir al máximo el consumo de alimentos contaminados con dicho metal.
Palabras Clave: Mercurio, minería, oro, alimentos, espectrofotometría (fuente: DeCS, BIREME).
ABSTRACT
Objective To assess the mercury accumulating capacity in contaminated soils from the community of Mina Santa Cruz, in the south of the department of Bolívar, Colombia, of the pepper plant (Capsicum annuum), in order to establish the risk to the health of the consuming population.
Materials and Methods Samples were taken from tissues (roots, stems, and leaves) of pepper plants grown in two soils contaminated with mercury and a control soil during the first five months of growth to determine total mercury through cold vapor atomic absorption spectrometry. Total mercury was determined in the samples of pepper plant fruits consumed in Mina Santa Cruz.
Results The mean concentrations of total mercury in the roots were higher than in stems and leaves. Accumulation in tissues was influenced by mercury levels in soil and the growth time of the plants. Mercury concentrations in fruits of pepper plant were lower than tolerable weekly intake provided by WHO.
Conclusion Percent of translocation of mercury to aerial parts of the plant were low in both control and contaminated soils. Despite low levels of mercury in this food, it is necessary to minimize the consumption of food contaminated with this metal.
Key Words: Mercury, mining, gold, foods, spectrophotometry (source: MeSH, NLM).
El mercurio es considerado un contaminante global y está relacionado con diversos efectos sobre la salud humana, puede llegar a los diferentes compartimientos ambientales a través de fuentes naturales y antropogénicas, siendo la minería aurífera la fuente principal de emisión en países en vía de desarrollo. Todas las formas conocidas de este metal pesado han sido establecidas como tóxicas, incluso la exposición a concentraciones elevadas puede causar la muerte (1). Tanto en su forma elemental, como en especies orgánicas e inorgánicas, los compuestos mercuriales son persistentes y bioacumulativos; por lo tanto de gran riesgo para la salud humana y la calidad ambiental, puesto que son acumulados en las plantas, ingresando así a la cadena trófica, pasando a los animales y finalmente al hombre (2).
La exposición al mercurio puede ocurrir a través del consumo de alimentos (productos vegetales, animales domésticos o peces), la ingesta de agua y la respiración de aire contaminados, siendo el consumo de pescado la principal vía de ingreso de este tóxico al organismo (3). Los compuestos organomercuriales son fácilmente absorbidos y potencialmente neurotóxicos, cerca del 90 % del metilmercurio es absorbido por la sangre a través del tracto gastrointestinal; a diferencia de las sales inorgánicas (10 %) y del mercurio elemental (0,1 %) (4). Los efectos más documentados en la salud humana relacionados con contaminación por mercurio incluyen inflamaciones severas en la piel, déficit en el desarrollo neurológico, daños en la memoria visual, atención y velocidad en las respuestas auditivas y psicomotoras (5). El metilmercurio ha sido asociado principalmente con afecciones en el cerebelo y teratogénesis; su peligro radica en la capacidad de ser acumulado en el cerebelo y la corteza cerebral, donde es fuertemente enlazado a las proteínas a través de los grupos sulfhidrilos, ejerciendo su toxicidad mediante la generación de especies reactivas de oxígeno, que actúan sobre proteínas blanco, por ejemplo las citoquinas (6). De igual forma, tiene la capacidad para atravesar la barrera placentaria en forma de un conjugado de mercurio-cisteína a través del sistema de transporte activo para aminoácidos neutros, lo que ocasiona un gran riesgo para el feto, y en consecuencia puede producir problemas en los recién nacidos (7).
En los países en vía de desarrollo como Brasil, Colombia, Ecuador y Bolivia, la minería aurífera artesanal es un factor de gran importancia, debido a que genera cantidades de residuos de mercurio directamente liberadas al ambiente, y más aún porque es practicada sin tener en cuenta recomendaciones de seguridad y control de emisiones establecidas para esta actividad económica (8). La extracción de oro con mercurio consiste de cuatro etapas principales: amalgamación, separación de la parte mineral de la amalgama, quema de la amalgama mercurio-oro y purificación del oro; durante el desarrollo de dichos procesos se produce el derramamiento directo de grandes cantidades de mercurio a suelos, ríos y cuerpos de agua como ciénagas y lagunas (9, 10).
En Colombia, una de las zonas de mayor explotación aurífera se encuentra ubicada entre el norte de Antioquia y sur de Bolívar, donde existían alrededor de 12 400 minas de explotación en el año 2002, y ya en ese entonces se emitían al ambiente entre 80 y 100 toneladas de mercurio por año (11). El sitio de muestreo de los suelos contaminados en este estudio fue el corregimiento Mina Santa Cruz, municipio Barranco de Loba, distrito minero de San Martin de Loba; donde los yacimientos de los cerros Buena Seña y Santa Cruz se consideran los más representativos de la región. Esta es una zona de explotación aurífera en la que se vierten grandes cantidades de mercurio a las corrientes de agua, suelos y atmosfera mediante el proceso de amalgamación mercurio-oro, y la quema de la misma, proceso en el que el mercurio es volatilizado para regresar posteriormente a la geósfera mediante las lluvias, lo que puede contribuir a la contaminación de suelos aledaños a las zonas de explotación minera.
El punto de partida de este estudio se fundamenta en la proliferación de variedad de especies vegetales que se han adaptado a las condiciones de estrés, generadas por la presencia de mercurio en suelos de Mina Santa Cruz. El ají es cultivado y consumido por los pobladores locales, y comercializado a las poblaciones cercanas, lo que puede constituirse en un riesgo en la salud de los habitantes de la región. Sin embargo, no se conocen reportes de concentraciones de mercurio total en este producto, por lo que el objetivo principal de este estudio fue evaluar la capacidad acumuladora de mercurio por parte de las plantas de ají, que crece en suelos contaminados procedentes de Mina Santa Cruz, con el propósito de establecer el riesgo en la salud de la población consumidora.
METODOLOGÍA
Sitio de estudio y muestreo de suelos
Se tomaron dos muestras de suelo provenientes del Corregimiento Mina Santa Cruz: la primera fue tomada en un sitio donde se presume menor contaminación, en la zona boscosa donde hay mayor vegetación (8º 42’ 42,4” Norte; 74º 17’ 53,5” Occidente); la segunda muestra se tomó en un sitio donde se presume mayor contaminación, cerca de las corrientes de amalgamación (8º 42’ 42,9’’ Norte; 74º 42’ 15,8’’ Occidente). El suelo control fue tomado en la ciudad de Sincelejo (09º 19’ 01,27” Norte; 75 º 23’ 16,47” Occidente). Todas las muestras se obtuvieron desde la capa superficial hasta una profundidad no superior de 30 cm (12).
Diseño experimental
Se trabajó sobre un diseño factorial que tuvo como variable respuesta la concentración de mercurio total (HgT) en tejidos; y como factores, el grado de contaminación del suelo (tres niveles: suelo control, menos contaminado y más contaminado) y el tiempo de crecimiento de la planta (observación durante 5 meses de crecimiento). El número de repeticiones por combinación de niveles de factores fue de 9, muestreándose en total 45 plántulas de ají distribuidas aleatoriamente en cada uno de los suelos.
Siembra de plántulas y toma de muestras
Se hicieron germinar cerca de 500 semillas, de las cuales se seleccionaron 150 plántulas con características morfológicas similares para ser distribuidas en los suelos control, más contaminado y menos contaminado. Cada una de las plántulas fue sembrada en 1 Kg de suelo contenido en una bolsa de polietileno para siembra en invernadero. Todas las plantas se regaron dos veces al día con agua de grifo a tres cuartos de su capacidad de campo según metodología usada por Chen en 2004 (13).
Posteriormente se recolectaron muestras de raíces, tallos y hojas con intervalos de un mes, hasta completar 5 meses de crecimiento. Las muestras fueron secadas al aire libre por 3 días, luego llevadas a una estufa a 60° C por 3 horas; y empacadas en bolsas de polietileno de cierre hermético para ser conservadas hasta la realización del análisis de mercurio total. Finalmente, se colectaron muestras del ají cultivado y consumido en Mina Santa Cruz, con el propósito de conocer los niveles de este producto en el corregimiento en estudio.
Análisis del laboratorio para suelos y tejidos vegetales
Las muestras de suelo fueron homogenizadas y caracterizadas mediante análisis de pH, porcentaje de materia orgánica y concentración de mercurio total y biodisponible (soluble en agua, intercambiable y unida a carbonatos). El mercurio en suelos fue determinado por el método de absorción atómica con vapor frío adaptado de Sadiq (14) y USEPA (15); y en el caso de las muestras vegetales, por la misma técnica, con el procedimiento de digestión y análisis de Sadiq y USEPA (16).
Los análisis se realizaron por duplicado en un espectrofotómetro de absorción atómica Thermo Electron S-series (provisto de una celda con ventanas de cuarzo). Los resultados se reportan en ng Hg/g peso seco. Para mercurio biodisponible la extracción se realizó usando la técnica BCR-SES, cuyas condiciones de reacción fueron: 20 ml de ácido acético (CH3COOH), a 25º C durante 16 horas, cada análisis se realizó con n=3 repeticiones.
Análisis de datos
Los datos de concentración de HgT en suelos, raíces, tallos, hojas y frutos se presentan como media +/- error estándar. Para el análisis estadístico se aplicaron pruebas de normalidad (Kolmogorov-Smirnov) y homogeneidad de varianza de Bartlett, en algunos casos fue necesario transformar los datos para poder hacer las comparaciones respectivas. La influencia de los factores sobre la variable respuesta se evaluó mediante una Anova Factorial, y la comparación entre niveles de factor se realizó mediante Anova en una vía y prueba de múltiples rangos, mediante el método de diferencia mínima significativa (LSD) de Fisher, lo que fue posible gracias al programa estadístico Statgraphics Centurion XV.
RESULTADOS
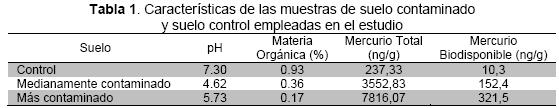
Caracterización de Suelos: Los suelos provenientes de Mina Santa Cruz presentaron bajos niveles de materia orgánica en comparación con el Suelo Control. Los niveles de pH fueron menores para los suelos contaminados, mientras que el Suelo Control presentó pH cercano a neutro. Las concentraciones de mercurio biodisponible (HgB) fueron mayores en los suelos con mayor concentración de HgT. Estos resultados se presentan en la Tabla 1.
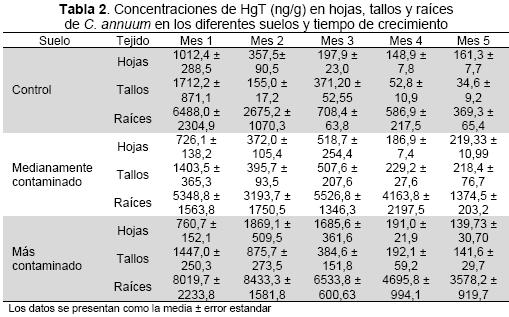
Mercurio total en plantas de Capsicum annum. La Tabla 2 muestra las concentraciones de HgT en tejidos de las plantas sembradas en los diferentes suelos, durante los 5 meses de crecimiento. El análisis de varianza factorial demostró la influencia del tiempo de crecimiento (P=0,0001) y del nivel de mercurio en suelo (P=0,0014) sobre la variable respuesta. Se observa que los niveles de mercurio fueron altos al inicio de crecimiento, y al final fueron menores en todos los casos; asimismo, las concentraciones en raíces fueron más altas en la mayoría de los casos en relación a los niveles de HgT en suelo, aunque no siempre ocurrió de esta forma en el caso de tallos y hojas.
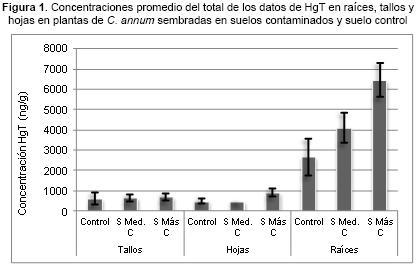
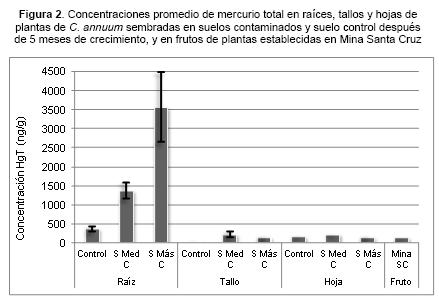
Las niveles de HgT más altos fueron observados en raíces, mientras que la acumulación en tallos y hojas fue similar; esto se corroboró al promediar el total de datos de concentraciones (Figura 1).
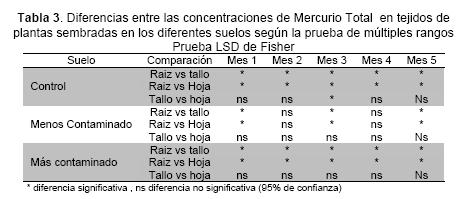
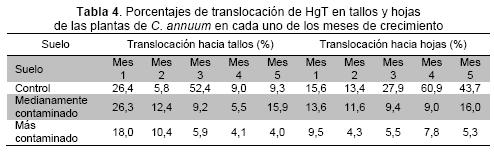
Al realizar el análisis teniendo en cuenta el tiempo de crecimiento, se presentaron diferencias estadísticamente significativas al comparar las concentraciones en raíces con relación a tallos y hojas (Tabla 3). Los porcentajes de translocación de HgT hacia las partes aéreas de la planta (tallos y hojas) en la mayoría de los casos no superaron el 26 % (Tabla 4).
La concentración media de HgT en frutos de plantas de ají establecidas en Mina Santa Cruz fue de 129,4±16,05 ng/g, estos valores fueron comparados con las concentraciones de mercurio total en hojas, tallos y raíces de las plantas sembradas en los suelos contaminados para el último mes, dado que este es el tiempo más cercano al periodo de fructificación de las plantas de esta especie, observándose similitud respecto de tallos y hojas (Figura 2).
DISCUSIÓN
Tanto en los suelos contaminados como en el suelo control, se presentaron niveles bajos de materia orgánica (categorizados por el laboratorio de suelos y agua de la Universidad de Sucre como suelos con contenido ínfimo o valor muy bajo). El pH de ambos suelos contaminados estuvo por debajo de los valores medios (5,8 a 7,2); lo cual puede deberse a que los yacimientos en los municipios de San Martin de Loba y Barranco de Loba son de tipo filoniano, constituidos por cuarzo, pirita, esfalerita, galena y sulfosales de plata, y oro libre o asociado con sulfuros (17).
Los niveles de mercurio en suelos provenientes de Mina Santa Cruz fueron mayores para el denominado Suelo Más Contaminado, y similares para el Suelo Menos Contaminado determinados por Vidal en 2010, cuyas concentraciones fueron 6907,8 y 3132,5 ng/g de HgT respectivamente. El porcentaje de materia orgánica para el Suelo Más Contaminado y Menos Contaminado fue menor a los reportados en el mismo estudio (3,2 % y 1,03 % respectivamente) (18).
El suelo más contaminado presentó una concentración de HgT por encima de lo estipulado por Devlin (2006) (19), quien reporta valores promedio entre 3 a 4600 ng/g; lo que indica el impacto que ha tenido el suelo debido a la actividad minera artesanal en esta zona. Para el Suelo Más Contaminado, el valor de HgT está por encima de los niveles empleados en estudios reconocidos de fitorremediación como el de Moreno en 2005, quien trabajó con suelos contaminados en un rango de 1 300 a 4 500 ng/g en la mina de Tailings, Nueva Zelanda (20).
El análisis de varianza para establecer la influencia de los factores en la acumulación de HgT demostró la incidencia del tiempo de crecimiento (valor p=0.0001) y de la concentración de HgT en suelos (valor p=0.0016), en la acumulación del metal en tejidos de C. annuum; asimismo, se presentaron diferencias estadísticamente significativas en la acumulación de HgT en las diferentes partes de la planta (valor p<0,0001). Tanto en el Suelo Control como en los suelos contaminados, los valores más altos de acumulación de HgT en raíces concuerdan con estudios en otras especies de plantas, como el realizado por Sierra en 2008, quien reporta mayor retención de HgT en raíces de Solanum melongena (1,262 ± 0,122 mg/kg) respecto a los tallos (0,394 ± 0,072 mg/kg), luego de la etapa de florescencia (21).
Las altas concentraciones de HgT en raíces de plantas sembradas en los suelos contaminados no implican un aumento proporcional en las cantidades translocadas hacia tallos y hojas en las respectivas plantas. Este comportamiento puede interpretarse como un mecanismo de evasión del contaminante, puesto que el porcentaje de translocación de HgT más alto en tallos de plantas sembradas en suelos contaminados fue de 26,3 %, a diferencia de los resultados obtenidos en el suelo control, donde en tallos se presentaron porcentajes de translocación de hasta el 52,4 % y de 60,9 % en hojas, aunque las bajas concentraciones en este suelo no implican que dichos porcentajes signifiquen altas concentraciones de HgT en dichos tejidos.
La acumulación de mercurio en las plantas ha sido estudiada en una variedad de especies, entre las que encontramos el Guisante (Pisum sativum L.) y la hierba buena (Menta), reportándose que las raíces acumulan una mayor cantidad de mercurio que las hojas (22); lo que algunos autores indican como un mecanismo de defensa tóxica, destacándose que cerca del 80 % del metal se adhiere a las paredes celulares, haciendo de la raíz una barrera que limita el paso del metal hacia las partes aéreas de la planta (23). Algunos autores atribuyen este proceso al papel de las fitoquelatinas, moléculas de naturaleza peptídica, que poseen aminoácidos azufrados a los el mercurio se une con facilidad, disminuyéndose así su translocación hacia tallos y hojas (24).
En cuanto a las concentraciones de HgT en frutos de C. annum proveniente de Mina Santa Cruz, aunque estas fueron bajas, se debe tener en cuenta que la USEPA (2005) cataloga al mercurio como uno de los elementos más peligrosos, aún en pequeñas cantidades (25). Asimismo, Posada en 2006 reporta que la exposición a mercurio antes del nacimiento y durante la infancia está asociada a retraso mental, parálisis cerebral, sordera y ceguera; e incluso, en dosis pequeñas, puede afectar el desarrollo del niño, puesto que causa déficit de atención y problemas de aprendizaje, mientras que en adultos puede afectar la fertilidad y la regulación de la presión arterial, causar pérdida de la memoria y la visión, temblor y entumecimiento de los dedos de manos y pies (26). Por otra parte, la IARC ha clasificado a los compuestos organomerculiales como pertenecientes al Grupo 2B; es decir, tiene efectos cancerígenos comprobados en animales de experimentación y posibles en seres humanos (29-31); razón por la que el tema del consumo de alimentos contaminados con mercurio debe ser abordado con la mayor atención posible.
En 1993, la OMS fijó una ingesta tolerable semanal de 0,3 mg de HgT y de 0,2 mg de metilmercurio (32). Teniendo en cuenta las concentraciones de presentadas en frutos de ají colectados en Mina Santa Cruz (129,475 ng/g), un consumo promedio de 250 gramos semanalmente aportaría 32,35 µg de mercurio a la dieta, valores que podrían catalogarse como bajos al comparar con la ingesta semanal permitida; sin embargo, Díaz en 2002, menciona que los niveles de este metal fluctúan en concentraciones bajas (entre 5 y 75 ng/g) en una gran variedad de alimentos no habitualmente expuestos a contaminación (33), valores que están por debajo de los encontrados en frutos de Capsicum annuum consumidos por los habitantes de esta población. Sumado a esto se debe considerar el consumo alimentos que pueden estar aportando cantidades similares o mayores de mercurio a la ingesta diaria, especialmente el caso del pescado, que es reconocido mundialmente como la principal fuente de ingestión de mercurio (34).
Teniendo en cuenta lo anterior, se debe mencionar que en el corregimiento Mina Santa Cruz, la dieta de los habitantes esta constituida principalmente por alimentos procedentes de municipios cercanos, así como plantas cultivadas en estos mismos suelos (yuca, ñame, plátano, ají, árboles frutales), y animales domésticos criados para consumo (gallinas, patos, cerdos); lo que puede potenciar la problemática de salud en esta población. Como antecedente de la contaminación por mercurio en el sur de Bolívar, Oliveros en 1995 reporta la correlación positiva entre el número de días que los individuos consumen pescado durante un mes y la concentración de mercurio en cabello (35). Por esta razón, se hace necesario determinar concentraciones de HgT en otros alimentos que hacen parte de la dieta diaria en los habitantes del corregimiento Mina Santa Cruz, con el propósito de dimensionar la magnitud de la problemática que se puede estar presentando a causa del consumo de alimentos contaminados por este metal.
Los niveles de mercurio fueron mayores en raíces, lo que significa que Capsicum annuum es una especie que limita la translocación de mercurio total a sus partes aéreas (tallos, hojas y frutos), por lo tanto las concentraciones de HgT en frutos fueron bajas respecto a las raíces; sin embargo, las concentraciones de mercurio en alimentos deben ser mínimas, debido a su alto potencial neurotóxico, por lo que lo ideal es que los niveles de este contaminante en alimentos sean cero.
Para dimensionar la problemática de contaminación por mercurio en Mina Santa Cruz, se hace necesario estudiar las concentraciones del metal en una mayor cantidad de alimentos, y especialmente evaluar niveles de metilmercurio, que es la especie más tóxica al ser humano •
Agradecimientos: Al equipo técnico del laboratorio de Toxicología y Gestión Ambiental de la Universidad de Córdoba por su colaboración y asistencia en los momentos requeridos, a los habitantes del corregimiento Mina Santa Cruz por su hospitalidad y colaboración en el momento de las visitas, y al Departamento Administrativo de Ciencia, Tecnología e Innovación (Colciencias), por el apoyo económico que aportó mediante el proyecto “Remoción de mercurio en suelos por plantas que crecen en sitios contaminados por el metal en el norte de Colombia (Mina El Alacrán en el departamento de Córdoba y Mina Santa Cruz en el departamento de Bolívar)”, financiado por dicha entidad mediante convocatoria 475 de 2009.
REFERENCIAS
1. Clarkson T, Magos L, Myers G. The Toxicology of Mercury - Current Exposures and Clinical Manifestations. The New England Journal of Medicine. 2003; 349: 1731-1737. [ Links ]
2. Islam E, Yang X, He L, Mahmood Q. Assessing potential dietary toxicity of heavy metals in selected vegetables and food crops. Journal of Zhejiang University. 2007; 8(1): 1-13. [ Links ]
3. Gustin M, Taylor G, Leonard T. High Levels of Mercury Contamination in Multiple Media of the Carson River Drainage Basin of Nevada: Implications for Risk Assessment. Environmental Health Perspectives. 1994; 102(9): 772-778. [ Links ]
4. Goldman L, Shannon M. The Committee on Environmental Health. Technical Report. Mercury in the environment: Implications for pediatricians. Pediatrics. 2001; 108(1):197-205. [ Links ]
5. Ozuah P. Folk use of elemental mercury: a potential hazard for children? Journal of National Medical Association. 2001; 93(9): 320-322. [ Links ]
6. Aschner M, Syversen T, Souza D, Rocha J, Farina M. Involvement of glutamate and reactive oxygen species in methylmercury neurotoxicity. Braz J Med Biol Res. 2007; 40: 285-291. [ Links ]
7. Bocayuva L, Magalhães, V, Malm O, de Oliveira E. Performance on neurological development tests by riverine children with moderate mercury exposure in Amazonia, Brazil. Cadernos de Saúde Pública. 2005; 21(4): 1160-1167. [ Links ]
8. Hinton J, Veiga M, Beinhoff C. Women, mercury and artisanal gold mining: Risk communication and mitigation. J Phys IV France. 2003; 107: 617-620. [ Links ]
9. UPME. Producción más limpia en la minería del oro en Colombia: mercurio, cianuro y otras sustancias. Unidad de Planeación Minero Energética, Ministerio de Minas y Energía. Bogotá, 2007. [ Links ]
10. Olivero J, Johnson B. El lado gris de la minería del oro: La contaminación con mercurio en el norte de Colombia. Editorial Universitaria. Colombia. 2002. [ Links ]
11. UPME (Unidad de Planeación Minera Energética). Estadísticas minero energéticas. Edición No. 13. Bogotá, 2001. [ Links ]
12. Smolinska B, Cedzynska K. EDTA and urease effects on Hg accumulation by Lepidium sativum. Chemosphere. 2007; 69: 1388-1395. [ Links ]
13. Chen C, Qu L, Li B, Xing L, Jia G, Wang T, et al. Increased Oxidative DNA Damage, as Assessed by Urinary 8-Hydroxy-2-Deoxyguanosine Concentrations, and Serum Redox Status in Persons Exposed to Mercury. Clinical Chemistry. 2005; 51(4): 759-767. [ Links ]
14. Sadiq M, Zaidi T, Al-Mohana M. Sample Weight and Digestion Temperature as Critical Factors in Mercury Determination in Fish. Bulletin of Environmental Contamination and Toxicology. 1991; 47: 335-341. [ Links ]
15. USEPA. Method 7471B for determination of mercury in solid or semisolid waste. U.S. Environmental protection Agency. Cincinnati. Ohio. 1998. [ Links ]
16. USEPA. Methods for the determination of mercury in environmental samples. U.S. Environmental protection Agency. Cincinnati. Ohio. 1994. [ Links ]
17. UPME. Distritos mineros: exportaciones e infraestructura de transporte. Unidad de Planeación Minero Energética, Ministerio de Minas y Energía. Bogotá, 2005. [ Links ]
18. Vidal J, Marrugo J, Jaramillo B, Pérez L. Remediación de suelos contaminados con mercurio utilizando guarumo (Cecropia peltata). Ingeniería y desarrollo. 2010; 27: 113-129. [ Links ]
19. Devlin E. Acute toxicity, uptake and histopathology of aqueous methyl mercury to fathead minnow embryos. Ecotoxicology. 2006; 15: 97-110. [ Links ]
20. Moreno F, Anderson C, Stewart R, Robinson B. Mercury volatilisation and phytoextraction from base-metal mine tailings. Environmental Pollution. 2005; 136 (2): 341-352. [ Links ]
21. Sierra M, Millán R, Esteban E. Potential use of Solanum melongena in agricultural areas with high mercury background concentrations. Food and Chemical Toxicology. 2008; 46: 2143-2149. [ Links ]
22. Beauford W, Barber J, Barringer A. Uptake and distribution of Hg within higher plants. Physiol. Plant. 1977; 39: 261-265. [ Links ]
23. Wang Y, Greger M. Clonal Differences in Mercury Tolerance, Accumulation, and Distribution in Willow. J. Environ. Qual. 2004; 33:1779-1785. [ Links ]
24. Cobbett C. Phytochelatins and Their Roles in Heavy Metal Detoxification. Plant Physiology. 2000; (123): 825-832. [ Links ]
25. USEPA. Guidelines for Carcinogen Risk Assessment. U.S. Environmental protection Agency. Washington, DC. 2005. [ Links ]
26. Posada M, Arroyave M. Efectos del mercurio sobre algunas plantas acuáticas tropicales. Revista EIA. 2006; 6: 57-67. [ Links ]
27. Ortega J, Ferris J, López J, Marco, A, García J, Cánovas A, et al. Hospitales Sostenibles (II). Mercurio: exposición pediátrica. Efectos adversos en la salud humana y medidas preventivas. Rev Esp Pediatr. 2003; 59(3): 274-291. [ Links ]
28. Ronchetti R, Zuurbier M, Jesenak M, Koppe JE, et al. Children health and mercury exposure. Acta Paediatr Suppl. 2006; 95(453): 36-44. [ Links ]
29. Holmes P, James K, Levy L. Is low level environmental mercury exposure of concern to human health?. Sci Total Environ. 2010; 408(2): 171-182. [ Links ]
30. WHO, IARC. Overall evaluations of carcinogenetics: An updating of IARC monographs. Ginebra, Suiza; 1987 (Suppl. 7): Pág.100. [ Links ]
31. Boffeta P, Merler E, Vainio H. Carcinogenicity of mercury and mercury compounds. Scand J Work Environ Health. 1993; 19: 1-7. [ Links ]
32. WHO. Evaluation of certain additives and contaminants: Forty-first report of the joint FAO/WHO Expert Committee on Food Additives. WHO Technical Report Series 837, Geneva, Switzerland. 1993. [ Links ]
33. Díaz O, García M. Avances en toxicología de contaminantes químicos en alimentos. Universidad de Santiago de Chile y Ministerio de Salud Pública de Cuba. Santiago, Chile. 2002. [ Links ]
34. Marcano V, Tronconis A. Evaluación del contenido de mercurio en el pescado expendido en la ciudad de Mérida, Venezuela. Rev Ecol Lat Am. 2001; 8(2)15-24 [ Links ]
35. Olivero J, Mendoza C, Mestre J. Mercurio en cabello de diferentes grupos ocupacionales en una zona de minería aurífera en el Norte de Colombia. Rev. Saude publica. 1995; 29(5): 376-379. [ Links ]