Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista de Salud Pública
Print version ISSN 0124-0064
Rev. salud pública vol.18 no.2 Bogotá Mar./Apr. 2016
https://doi.org/10.15446/rsap.v18n2.31692
Doi: http://dx.doi.org/10.15446/rsap.v18n2.31692
Artículos Investigación
Estimación de años de vida ajustados por discapacidad según subtipo de ataque cerebrovascular isquémico agudo
Estimating disability-adjusted life-years for subtypes of acute ischemic stroke
Octavio Martínez-Betancur1, Patricia Quintero-Cusguen2 y Liliana Mayor-Agredo
1 Departamento de Medicina Interna. Facultad de Medicina. Universidad Nacional de Colombia. Bogotá. Colombia. omartinez@unal.edu.co
2 Unidad de Neurología. Hospital Universitario de La Samaritana. Bogotá. Colombia. patquincus@gmail.com; limayor@hotmail.com
Recibido 7 Agosto 2013/Enviado para Modificación 19 Julio 2014/Aceptado 3 Noviembre 2015
RESUMEN
Objetivo Probar la hipótesis que los años de vida ajustados por discapacidad (AVAD) estimados al egreso hospitalario para cada paciente con ataque cerebrovascular (ACV) isquémico agudo, sin terapia de reperfusión, no difieren entre los subtipos etiológicos.
Material y Métodos En el Hospital Universitario de la Samaritana de Bogotá, se seleccionaron para ingreso y seguimiento hasta el egreso, las historias de pacientes con diagnóstico de primer evento de ACV isquémico. El subtipo de ACV isquémico agudo se clasificó mediante los criterios establecidos por el Trial of Org 10172 in Acute Stroke Treatment (TOAST). Se estimaron los AVAD individuales de cada paciente con ACV isquémico agudo al egreso. La prueba de Kruskal Wallis se empleó para establecer diferencias de AVAD entre los cinco subtipos de ACV isquémico agudo.
Resultados De 39 pacientes con ACV isquémico agudo, se clasificaron 17 (43,6 %) de etiología aterosclerótica, 10 (25,6 %) con ACVs lacunares, 6 (15,4 %) cardioembólicos y 6 (15,4 %) pacientes sin etiología clara. El total de AVAD aportados por los pacientes con ACV isquémico agudo, fue 316,9 años, sin diferencias estadísticamente significativas entre los subtipos de isquemia. Al egreso hospitalario, un paciente sobreviviente de un ACV isquémico agudo pierde en promedio de 8,12 años de vida óptima libre de discapacidad.
Conclusión Los resultados no conclusivos se atribuyen a la concurrencia de procesos disímiles del cuidado clínico y a las distribuciones de factores de riesgo, comorbilidades y complicaciones de los pacientes.
Palabras Clave: Accidente cerebrovascular, años de vida perdidos por discapacidad (fuente: DeCS, BIREME).
ABSTRACT
Objective To test the hypothesis that DALYs, estimated individually for each patient with acute ischemic stroke upon hospital discharge, without reperfusion therapy, are not different between the different subtypes of ischemic stroke.
Patients and Methods In the Hospital Universitario de la Samaritana in Bogotá, the health records of patients diagnosed with their first acute ischemic stroke event from admission and monitoring to discharge were selected. The subtype of acute ischemic stroke was classified according to the criteria established by the Trial of Org 10172 in Acute Stroke Treatment (TOAST). DALYs were estimated for each patient with acute ischemic stroke at hospital discharge. To establish differences of DALYs among the five acute ischemic stroke subtypes (TOAST), the Kruskal Wallis test was used.
Results Of the 39 cases of acute ischemic stroke, 17 (43.6 %) were classified as artherosclerosis, 10 (25.6 %) as lacunar events, 6 (15.4 %) as cardioembolic attacks, and another 6 (15.4 %) cases with unclear etiology. At hospital discharge, the estimated total DALYs provided by patients with acute ischemic stroke was 316.9 years, without statistically significant differences between the subtypes of ischemic stroke. At hospital discharge, the average of optimal years free of disability lost by a patient surviving an acute ischemic stroke was 8.12.
Conclusion Non conclusive results are attributed to the concurrence of dissimilar acute clinical care processes and to the risk factors distributions, comorbidities and patient complications.
Key Words: Stroke, disability-adjusted life years (source: MeSH, NLM).
Con base en los planteamientos del Banco Mundial en el año 1993 sobre la necesidad de orientar la intervención gubernamental en salud para obtener el mayor rendimiento posible de los fondos invertidos, y la posibilidad de medir la eficacia de las intervenciones médicas en función de lo que cuesta ganar Años de Vida Ajustados por Discapacidad (AVAD), se dio el primer paso en el avance hacia el entendimiento del impacto poblacional en salud de las morbilidades crónicas, más allá de los simples estimativos de mortalidad (1). Un AVAD (DALYs por sus siglas en inglés) puede pensarse como un año perdido de vida saludable, y la carga de enfermedad de una población como una medida de la brecha existente entre el estado de salud de la población y una situación ideal en la cual cada persona viva libre de enfermedad y discapacidad hasta la vejez (2).
El tiempo es la métrica de los AVAD. Permite combinar los años de vida perdidos por una muerte prematura con la disminución de la capacidad de desarrollo humano durante los años restantes de vida de un paciente como consecuencia de una enfermedad, representando así una medida relativa de funcionalidad (3). En el mundo, el ataque cerebrovascular (ACV) se asocia con 43,7 millones anuales de AVAD perdidos, lo que representa aproximadamente 3,2 % de la totalidad global de AVAD perdidos. Además, entre las personas de todas las edades, el ACV ocupa mundialmente la séptima causa de pérdidas de AVAD, y entre toda la población adulta, la cuarta causa de pérdida de AVAD, precedida por HIV/SIDA, desórdenes depresivos unipolares y enfermedad isquémica cardíaca (3).
Los AVAD asociados a una condición clínica específica, expresan años de vida perdidos por muerte prematura (YLL), y años vividos con una discapacidad (YLD) de severidad y duración determinadas (4,5). Hasta el advenimiento reciente de metodologías para el cálculo de los AVAD a pacientes individuales, dichas medidas se aplicaban para el análisis de datos a nivel poblacional (6-9). Recientemente, se dispone de una técnica para derivar los AVAD perdidos de pacientes individuales con ACV isquémico agudo a partir de la edad, sexo y nivel de discapacidad medido por la escala modificada de Rankin (mRS) (10-13).
El tratamiento agudo del ACV isquémico tiene el cometido de minimizar la extensión de infarto resultante de la oclusión de una arteria determinada, con miras a atenuar la severidad de la discapacidad, pero, aparte de las medidas de soporte general como mantenimiento de las funciones pulmonar y cardiovascular, balance hidroelectrolítico y nutricional adecuados, y prevención de complicaciones sistémicas, la mayoría de tratamientos usados, en particular las terapias reológicas/antitrombóticas, no cuentan con beneficios probados sobre el desenlace funcional de los pacientes (14-16). Esta práctica corriente está basada en variaciones de los mecanismos fisiopatológicos involucrados en la clasificación etiológica o subtipos de ACV isquémico agudo, de tal manera que, ante cada nuevo paciente con déficit neurológico focal agudo que sugiera el diagnóstico, los recursos clínicos y tecnológicos hospitalarios se dirigen a determinar la etiología del ACV isquémico para decidir el manejo (17). Por otra parte, en la mayoría de los sitios donde la terapia trombolítica ha sido implementada en un contexto de cuidado neurológico especializado, menos de 5 % de todos los pacientes con ACV la reciben, pues entre la mitad a un tercio de todos ellos no son considerados candidatos para tratamiento por la tardanza en la prestación del cuidado (18,19).
El objetivo primario del presente trabajo es probar la hipótesis que los AVAD estimados individualmente al egreso hospitalario de cada paciente con ACV isquémico agudo, sin terapia de reperfusión, no difieren entre las diferentes categorías de clasificación etiológica según las cuales se decide el manejo de los pacientes. El objetivo secundario es la estimación de diferentes métricas de carga de enfermedad específica de ACV isquémico agudo, al egreso hospitalario sin terapia de reperfusión, entre las cuales se cuentan: estimación de la letalidad de la enfermedad, porcentual y en YLL; estimación de YLL que en promedio aporta cada paciente individualmente y cada subtipo etiológico; estimación de YLD que en promedio aporta cada paciente y cada subtipo etiológico; estimación de los AVAD totales, y número promedio de AVAD con que contribuye cada paciente y cada subgrupo etiológico a la carga de enfermedad.
MATERIAL Y MÉTODOS
Se analizó una cohorte histórica en el Hospital Universitario de la Samaritana de Bogotá, hospital de tercer nivel de asistencia en salud de referencia para el Departamento de Cundinamarca - Colombia, entre mayo de 2010 y junio de 2011. Se seleccionaron todas las historias clínicas de pacientes hospitalizados con diagnóstico de ACV, excluyendo los diagnósticos de ACV hemorrágico, ataque isquémico transitorio (AIT), enfermedad multinfarto cerebral y ACV a repetición. Sólo se consideraron para ingreso y seguimiento de la evolución clínica hasta el egreso, los diagnósticos de primer evento de ACV isquémico.
La extracción de datos de los registros en papel de las historias clínicas se realizó por duplicado con un intervalo de 20 días, por parte de un único evaluador y recolector de información, especialista clínico en neurología quien en su momento participó en el diagnóstico, tratamiento y seguimiento hospitalarios de los pacientes, enmascarado respecto a los objetivos del estudio. Se empleó un instrumento de recolección de información previamente validado en términos de apariencia y contenido. No se evaluó acuerdo intra revisor/extractor de los datos para las variables consideradas en el estudio.
La clasificación del subtipo de ACV isquémico agudo se realizó mediante los criterios del Trial of Org 10172 in Acute Stroke Treatment (TOAST) (17). La clasificación TOAST de los cinco subtipos se ACV isquémico agudo fue realizada de manera independiente por dos investigadores, y se estimó el acuerdo interevaluadores con el coeficiente Kappa, mediante el programa estadístico Epidat versión 3.1. Los desacuerdos entre evaluadores fueron resueltos por consenso para cada caso.
Para estimar los AVAD individuales de cada paciente con ACV isquémico agudo al egreso hospitalario, se sumaron los YLL más los YLD obtenidos mediante las siguientes fórmulas (10-13):
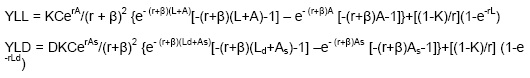
K = 1. Factor modulador de la ponderación de la edad.
β = 0,04. Parámetro para la función ponderadora de la edad.
r = 0,03. Tasa de descuento para los años de vida por preferencia temporal.
C = 0,1658
A: Edad del paciente al momento de la muerte. Cuando el paciente fallece (mRS = 6) se toma la edad al momento del ACV. Si el paciente es superviviente con discapacidad, se emplea la sumatoria de la edad al momento del ACV más la expectativa de vida con discapacidad para edad y sexo (Ld).
L: Expectativa de vida de la población general a la edad A.
D: Ponderación ajustada de la severidad de la discapacidad para cada uno de los niveles ordinales de de la mRS, realizadas por un panel de expertos internacionales con base en los lineamientos del World Health Organization Global Burden of Disease Project (20, 21). Específicamente para pacientes con secuelas funcionales derivadas de ACV isquémico agudo, las ponderaciones ajustadas de la severidad de la discapacidad a emplear en el cálculo de los AVAD, correspondientes a los niveles de mRS de 0 a 6 son, en su orden, 0, 0,053, 0,228, 0,353, 0,691, 0,998 y 1 (20).
As: Edad del paciente al momento del ACV isquémico agudo.
Ld: Duración del estado de discapacidad. Equivalente a la expectativa de vida de un paciente superviviente con un determinado grado de discapacidad (mRS) por ACV isquémico agudo desde la edad As.
La medición de la discapacidad residual (dimensión funcional de secuela de ACV isquémico agudo) al egreso mediante la mRS (22-30), fue realizada por un único investigador especializado en neurología. Sin terapia de reperfusión vascular, este estudio considera terminado el proceso de cuidado agudo de los pacientes tras el egreso hospitalario y asume la invariabilidad del nivel de discapacidad residual durante la supervivencia del paciente tras el egreso hospitalario, independientemente de si se realizaron o no programas de rehabilitación (5).
Para estimar la expectativa de vida de cada paciente superviviente de un ACV isquémico agudo a partir de la edad (As), se realizaron tablas de vida de supervivientes por edad, sexo y nivel de discapacidad según la mRS. Para generar las tasas de mortalidad específicas por edad y sexo para los supervivientes de ACV (31,32), se tomaron las razones de peligro (hazard ratio) para mortalidad, ya derivadas en un estudio previo para cada nivel de la mRS en relación con la población general (33). Las tasas específicas de mortalidad de población general por edad y sexo fueron las del departamento de Cundinamarca, Colombia, para los años 2010 a 2015 según el DANE (34). Las tablas de supervivencia y los cálculos de los AVAD fueron realizados en Microsoft Office Excel 2007.
Para la descripción estadística de los datos se emplearon medidas de resumen en relación con el tipo de variable analizada, y para el análisis exploratorio de datos se emplearon pruebas no paramétricas, considerando un valor Alpha de dos colas de 0,05 sin corrección para pruebas múltiples. Todos los análisis estadísticos se realizaron mediante el paquete SPSS versión 18.
RESULTADOS
De 152 pacientes con ACV, se excluyeron 35 con etiología hemorrágica y 78 pacientes con diagnósticos de AIT, enfermedad multinfarto cerebral y ACVs a repetición. Se analizaron 39 pacientes con ACV isquémico agudo, y se clasificaron según criterios TOAST como de etiología aterosclerótica de vasos carotídeos/grandes vasos intracraneanos 17 (43,6 %) pacientes, 10 (25,6 %) con ACVs lacunares, 6 (15,4 %) ataques cardioembólicos y 6 (15,4 %) pacientes en quienes no fue posible esclarecer la etiología. No se diagnosticaron casos asociados con hipercoagulabilidad, vasculitis, infección o tumor. El coeficiente Kappa de acuerdo entre evaluadores en la clasificación de los subtipos TOAST de ACV isquémico agudo, fue 0,680 (IC 95 %, 0,503 a 0,858). Los desacuerdos se presentaron en la clasificación de 9 casos.
La mayor frecuencia de casos de ACV isquémico agudo se presentó en hombres (79,5 %), con una relación hombre: mujer de 3,9: 1. Las medianas de la edad de presentación del evento isquémico fueron 71 años (rango intercuartílico, 62 a 82) para la totalidad de los pacientes, 73 años en mujeres y 71 años en hombres (U Mann-Whitney 115,5; valor p=0,772). En las mujeres, no obstante, la edad tuvo un CV mayor que en los hombres (0,382 vs. 0,172), con el 25 % de la distribución de la edad por debajo de 42 años en mujeres y 62 años en hombres.
La mediana del tiempo al egreso hospitalario fue 8 días (rango intercuartílico, 4 a 15). La letalidad intrahospitalaria del ACV isquémico agudo (mRS 6) fue 15,4 %, en total 35,10 YLL, en promedio 5,85 años perdidos por cada muerte prematura durante el evento agudo. Todos los supervivientes al egreso tuvieron algún grado de discapacidad funcional (mRS 1 a 5), con una distribución unimodal de discapacidad moderadamente severa (mRS 4) en 16 pacientes (41 %).
Las diferencias de la edad entre los subtipos etiológicos de ACV isquémico no fueron significativas estadísticamente (X23gl 4,414; valor p=0,220), como
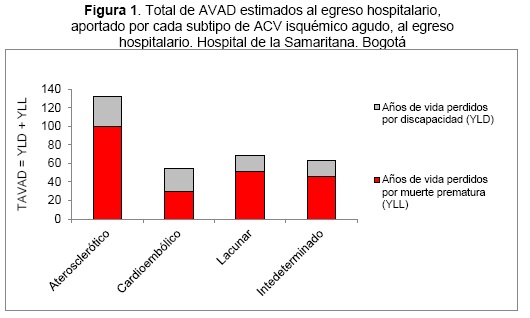
tampoco tuvieron significación estadística las diferencias de la severidad del estado funcional al egreso (mRS) con el subtipo etiológico (X23gl 1,811; valor p=0,629). Al egreso hospitalario, la estimación del total de AVAD aportados por los pacientes con evento agudo de ACV isquémico, fue 316,9 años, sin diferencias significativas estadísticamente entre los subtipos de isquemia (X23gl 4,507; valor p=0,212) (Figura 1).
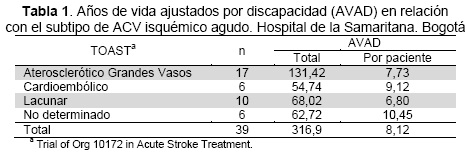
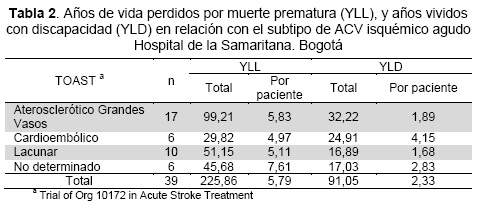
En promedio, cada paciente aportó 8,2 AVAD a la carga de ACV isquémico agudo, y la Tabla 1 muestra el promedio de AVAD aportado por cada subtipo etiológico de enfermedad. La Tabla 2 muestra las estimaciones de los YLL y YLD que, en promedio, aportaron cada paciente y cada subtipo etiológico a la carga de ACV isquémico agudo.
DISCUSIÓN
De la clasificación del subtipo de ACV isquémico agudo han dependido, tanto en diseños de ensayos clínicos como en estudios observacionales, el manejo agudo, el pronóstico y las estrategias a largo plazo para prevenir recurrencias, con fundamento en presunciones de heterogeneidad de los mecanismos subyacentes de injuria isquémica entre los subtipos (17,35-38). En el presente estudio, el acuerdo alcanzado entre observadores para la clasificación TOAST, no se aleja de lo informado en estudios epidemiológicos observacionales (37,38), aunque con mayor precisión del coeficiente Kappa estimado. Los desacuerdos más frecuentes se presentaron entre la categoría de aterosclerosis de grandes vasos y los eventos de causa no determinada. El diagnóstico de ACV de causa no determinada es difícil. En ocasiones, el médico se ve tentado a mejorar las definiciones de los subtipos con intuiciones derivadas de su propia experiencia clínica, bien porque cuenta con evaluación incompleta, porque toda la evaluación completa es negativa, o porque tiene dos o más potenciales etiologías identificadas de ACV isquémico agudo (39).
En los estudios de base hospitalaria, la frecuencia de ACV isquémico por subtipos etiológicos, puede no reflejar las causas relevantes de la enfermedad puesto que no todos los pacientes son ingresados a centros hospitalarios de tercer nivel de atención. Por su parte, en los estudios de base poblacional, las incidencias de los diferentes subtipos de ACV isquémico difieren en relación con la heterogeneidad de las distribuciones poblacionales de los factores de riesgo y comorbilidades, lo que supone diversidad del trasfondo clínico para cada subtipo de evento isquémico según la población estudiada (40). En general, los estudios de base poblacional en países occidentales clasifican los eventos isquémicos con mayor frecuencia como cardioembólicos, seguidos de los aterotrombóticos, a diferencia del Japón, donde priman los infartos lacunares seguidos de los aterotrombóticos y cardioembólicos (41-45). La distribución de frecuencia de los subtipos etiológicos clasificados en este estudio, difiere tanto de los resultados de estudios de base poblacional como de estudio observacionales de base hospitalaria, lo que sugiere posiblemente un trasfondo de mayor carga aterosclerótica en los pacientes analizados.
La mortalidad hospitalaria durante el evento agudo de ACV isquémico se relaciona con la edad del paciente y las comorbilidades, pero está determinada por las complicaciones desarrolladas durante la hospitalización. Por otra parte, los pacientes con ACV de mayor severidad son los que tienen mayor riesgo de complicaciones, y la mayor estancia hospitalaria es un factor de riesgo independiente para el desarrollo de complicaciones. Se estima que si se pudiera prevenir la totalidad de las complicaciones médicas y neurológicas de los pacientes con ACV isquémico, la tasa global de mortalidad intrahospitalaria en tales pacientes se reduciría en cerca de 54 % (45-48). La estancia hospitalaria en el presente estudio no se aleja de lo informado por Ingeman (48), cuya mediana de estancia fue 13 días. La tasa global de mortalidad intrahospitalaria del presente informe tampoco se aparta de lo registrado en otros estudios de base hospitalaria (45-48), tasas que van de 4,9 % a 10,1 %. Conocer que cada paciente muerto durante el curso agudo de un primer episodio de ACV isquémico ha perdido 5,85 años de vida, posibilita un entendimiento más comprensivo del efecto que sobre la mortalidad hospitalaria de tales pacientes ejerce la sumatoria de factores de riesgo, comorbilidades y complicaciones.
Al egreso hospitalario, un paciente sobreviviente de un ACV isquémico agudo se ve privado en promedio de 8,12 años de vida óptima libre de discapacidad. Los resultados no conclusivos se atribuyen a la concurrencia de procesos disímiles del cuidado clínico y a las distribuciones de factores de riesgo, comorbilidades y complicaciones de los pacientes. El verdadero valor de la investigación de resultados, a diferencia de los estudios de eficacia, es contar con poblaciones ampliamente heterogéneas que permitan valorar los resultados tal como se dan en la práctica clínica cotidiana. Esto lleva a considerar que, dado el tipo de estudio realizado, es de esperar heterogeneidad de variables sociodemográficas y clínicas que puedan influenciar los resultados independientemente de los procesos de cuidado clínico e interactuando con ellos •
REFERENCIAS
1. Banco Mundial. Informe sobre el desarrollo mundial 1993. Invertir en salud. Washington, D.C.: Banco Mundial; 1993. [ Links ]
2. Dua T, Garrido M, Mathers C, Saxena S. Global burden of neurological disorders: estimates and projections. En: Campanini B (Editora). Neurological disorders: Public Health Challenges. Ginebra: Banco Mundial; 2006. p. 27 - 39. [ Links ]
3. Mukherjee D, Patil CG. Epidemiology and the global burden of stroke. World Neurosurg. 2011; 76: S85 - S90. [ Links ]
4. Seuc AH, Domínguez E, Díaz O. Introducción a los DALYs. Rev Cubana Hig & Epidemiol. 2000; 38: 92 - 101. [ Links ]
5. Essink-Bok ML, Bonsel GJ. How to derive disability weights. En: Murray CJL, Salomon JA, Mathers CD, Lopez AD. Summary measures of population Health. Concepts, ethics, measurement and applications. Ginebra: World Health Organization; 2002. p. 449-465. [ Links ]
6. Murray CJL. Quantifying the burden of disease: the technical basis for disability-adjusted life years. Bull World Health Org. 1994; 72: 429-445. [ Links ]
7. Murray CJL, Lopez AD. Quantifying disability: data, methods and results. Bull World Health Org. 1994; 72: 481-494. [ Links ]
8. Mont D. Measuring health and disability. Lancet. 2007; 369: 1658-1663. [ Links ]
9. Jelsma J, de Weerdt W, de Cock P. Disability adjusted life years (DALYs) and rehabilitation. Disabil & Rehabil. 2002; 24: 7: 378-382. [ Links ]
10. Hong KS. Disability-adjusted life years analysis: implications for stroke research. J Clin Neurol. 2011; 7: 109-114. [ Links ]
11. Hong KS, Kim J, Cho YJ, SEo SY, Hwang SI, Kim SC, et al. Burden o ischemic stroke in Korea: analysis of disability-adjusted life years lost. J Clin Neurol. 2011; 7: 77-84. [ Links ]
12. Hong HS, Saver JL, Kang DW, Bae HJ, Yu KH, Koo J, et al. Years of optimum health lost due to complications after acute ischemic stroke. Disability-adjusted life-years analysis. Stroke. 2010; 41: 1758-1765. [ Links ]
13. Hong HS, Ali LK, Selco SL, Fonarow GC, Saver JL. Weighting components of composite end points in clinical trials. An approach using disability-adjusted life-years. Stroke. 2011; 42: 1722-1729. [ Links ]
14. Kidwell CS, Liebeskind DS, Starkman S, Saver JL. Trends in acute ischemic stroke trials through the 20th century. Stroke. 2001; 32: 1349-1359. [ Links ]
15. Langhorne P, Sandercock P, Prasad K. Evidence-based practice for stroke. Lancet Neurol. 2009; 8: 308-309. [ Links ]
16. Hacke W, Kaste M, Bluhmki E, Brozman M, Dávalos A, Guidetti Donata, et al For the ECASS Investigators. Thrombolysis with alteplase 3 to 4.5 hours after acute ischemic stroke. N Engl J Med. 2008; 359: 1317-1329. [ Links ]
17. Adams Jr HP, Bendixen BH, Kappelle J, Biller J, Love BB, Gordon DL, et al. Classification of subtype of acute ischemic stroke. Definitions for use in a multicenter clinical trial. Stroke. 1993; 24: 35-41. [ Links ]
18. Bogousslavsky J, Liu M, Moncayo J, Norrving B, Tsiskaride A, Yamagushi t, et al. Stroke. En: Campanini B (Editora). Neurological disorders: Public Health Challenges. Ginebra: Banco Mundial; 2006. p. 151-163. [ Links ]
19. Lavados PM, Hennis AJM, Fernandes JF, Medina MT, Legetic B, Sacks C, et al. Stroke epidemiology, prevention, and management strategies at a regional level: Latin America and the Caribbean. Lancet Neurol. 2007; 6: 362-372. [ Links ]
20. Hong KS, Saver JL. Quantifying the value of stroke disability outcomes. WHO Global Burden of Disease Project disability weights for each level of the modified Rankin scale. Stroke. 2009; 40: 3828-3833. [ Links ]
21. Barendregt JJ. Disability-adjusted life years (DALYs) and disability-adjusted life expectancy (DALE). En: Robine JM, Jagger C, Mathers CD, Crimmins EM, Suzman RM. Determining health expectancies. Sussex: Wiley; 2003. p. 247-261. [ Links ]
22. de Haan R, Limburg M, Bossuyt P, van der Meulen J, Aaronson N. The clinical meaning of Rankin 'handicap´ grades after stroke. Stroke. 1995; 26: 2027-2030. [ Links ]
23. Saver JL. Optimal end points for acute stroke therapy trials. Best ways to measure treatment effects of drugs and devices. Stroke. 2011; 42: 2356-2362. [ Links ]
24. Banks JL, Marotta CA. Outcomes validity and reliability of the modified Rankin scale: implications for stroke clinical trials. A Literature review and synthesis. Stroke. 2007; 28: 1091-1096. [ Links ]
25. New PW, Buchbinder R. Critical appraisal and review of the Rankin scale and its derivatives. Neuroepidemiology. 2006; 26: 4-15. [ Links ]
26. Duncan PM, Jorgensen HS, Wade DT. Outcome measures in acute stroke trials. A systematic review and some recommendations to improve practice. Stroke. 2000; 31: 1429-1438. [ Links ]
27. Roberts L, Counsell C. Assessment of clinical outcomes in acute stroke trials. Stroke. 1998; 29: 986-991. [ Links ]
28. Sulter G, Steen C, de Keyser J. Use of the Barthel index and modified Rankin scale in acute stroke trials. Stroke. 1999; 30: 1538-1541. [ Links ]
29. Dromerick AW, Edwards DF, Diringer MN. Sensitivity to changes in disability after stroke: a comparison of four scales useful in clinical trials. J Rehabil Res Dev. 2003; 40: 1-8. [ Links ]
30. Duncan PW, Lai SM, Keinhley J. Defining post-stroke recovery: implications for design and interpretation of drug trials. Neuropharmacology. 2000; 39: 835-841. [ Links ]
31. Vázquez E, Camaño F, Silvi J, Roca A. La tabla de vida: una técnica para resumir la mortalidad y la sobrevivencia. Boletín Epidemiol/OPS. 2003; 24: 6-10. [ Links ]
32. Seuc A, Domínguez E. Introducción al cáculo de esperanza de vida ajustada por diacapacidad. Rev Cubana Hig Epidemiol. 2002; 40: 95-102. [ Links ]
33. Hong KS, Saver JL. Years of disability-adjusted life gained as a result of thrombolytic therapy for acute ischemic stroke. Stroke. 2010; 41: 471-477. [ Links ]
34. DANE. Proyecciones de población 2005-2020. Colombia. Tablas abreviadas de mortalidad nacionales y departamentales 1985 - 2020. Bogotá. 2007. [Internet]. Disponible en: http://www.dane.gov.co/files/investigaciones/poblacion/proyepobla06_20/8Tablasvida1985_2020.pdf/. Consultado 6 de enero de 2010. [ Links ]
35. Adams Jr HP, Woolson RF, Clarke WR, Davis PH, Bendixen BH, Love BB, et al. Design of the Trial of Org 10172 in Acute Stroke Treatment (TOAST). Control Clin Trials. 1997; 18: 358-377. [ Links ]
36. Wilterdink JL, Bendixen B, Adams Jr HP, Woolson RF, Clarke WR, Hansen MD, for the TOAST Investigators. Effect of prior Aspirin use in stroke severity in the Trial of Org 10172 in Acute Stroke Treatment (TOAST). Stroke. 2001; 32: 2836-2840. [ Links ]
37. Maden KP, Karanjia PN, Adams Jr HP, Clarke WR, and the TOAST Investigators. Accuracy of initial stroke subtype diagnosis in the TOAST study. Neurology. 1995; 45: 1975-1979. [ Links ]
38. Kolominsky-Rabas PL, Weber M, Gellefer O, Neundoerfer B, Heuschmann PU. Epidemiology of ischemic stroke subtypes according to TOAST criteria. Incidence, recurrence, and long-term survival in ischemic stroke subtypes: a population-based study. Stroke. 2001; 32: 2735-2740. [ Links ]
39. Gordon DL, Bendixen BH, Adams HP, Clarke W, Kappelle LJ, Woolson RF, and the TOAST Investigators. Interphysician agreement in the diagnosis of subtypes of acute ischemic stroke: implications for clinical trials. Neurology. 1993; 43: 1021-1027. [ Links ]
40. Schulz UGR, Rothwell PM. Differences in vascular risk factors between etiological subtypes of ischemic stroke. Importance of population-based studies. Stroke. 2003; 34: 2050-2059. [ Links ]
41. Grau AJ, Weimar C, Buggle F, Heinrich A, Goertler M, Neumaer S, et al. Risk factors, outcome, and treatment in subtypes of ischemic stroke. The German Stroke Data Bank. Stroke. 2001; 32: 2559-2566. [ Links ]
42. Petty GW, Brown RD, Whisnant JP, Sicks JRD, O´Fallon WM, Wiebers DO. Ischemic stroke subtypes. A population-based study of incidence and risk factors. Stroke. 1999; 30: 2513-2516. [ Links ]
43. Tanizaki Y, Kiyohara Y, Kato I, Iwamoto H, Nakayama K, Shinohara N, et al. Incidence and risk factors for subtypes of cerebral infarction in a general population. The Hysayama study. Stroke. 2000; 31: 2616-2622. [ Links ]
44. Hajat C, Heuschmann PU, Coshall C, Padayachee S, Chambers J, Rudd AG, et al. Incidence of aetiological subtypes of stroke in a multi-ethnic population based study: the South London Stroke Register. J Nuerol Neurosurg Psychiatry. 2011; 82: 527-533. [ Links ]
45. Heuschmann PU, Kolominsky-Rabas PL, Misselwits B, Hermanek P, Leffmann C, Janzen RWC, et al, for The German Stroke Registers Study Group. Predictors of in-hospital mortality and attributable risks of death after ischemic stroke. Arch Intern Med. 2004; 164: 1761-1768. [ Links ]
46. Tuttolomondo A, Pedone C, Pinto A, DiRaimondo D, Fernandez P, DiSciacca R, et al. Predictors of outcome in acute ischemic cerebrovascular síndromes: the GIFA study. Int J Cardiol. 2008; 125: 391-396. [ Links ]
47. Bae HJ, Yoon DS, Lee J, Kim BK, Koo JS, Kwon O, et al. In-hospital medical complications and long term mortality after ischemic stroke. Stroke. 2005; 36: 2441-2445. [ Links ]
48. Ingeman A, Andersen G, Hundborg HH, Svendsen ML, Johnsen SP. In-hospital medical complications, length of stay, and mortality among stroke unit patients. Stroke. 2011; 42: 3214-3218. [ Links ]