Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista de Salud Pública
Print version ISSN 0124-0064
Rev. salud pública vol.18 no.3 Bogotá May/June 2016
https://doi.org/10.15446/rsap.v18n3.44078
Doi: http://dx.doi.org/10.15446/rsap.v18n3.44078
Artículos Investigación
Análisis filogenético de secuencias suramericanas del gen ns1 del serotipo dengue-2, relacionadas con sangrado clínico severo
Phylogenetic analysis of South American sequences of the nonstructural protein-1 (ns1) of dengue serotype 2 associated with severe clinical bleeding
Raimundo Castro-Orozco1, Lyda R. Castro-García2 y Doris E. Gómez-Camargo3
1 Universidad de San Buenaventura. Cartagena de Indias, Colombia. raimundo_castro_orozco@hotmail.com
2 Universidad del Magdalena. Santa Marta, Colombia. lydaraquelcastro@hotmail.com
3 Universidad de Cartagena. Cartagena de Indias, Colombia. degomez@hotmail.com
Recibido 20 Junio 2014/Enviado para Modificación 16 Noviembre 2015/Aceptado 22 Febrero 2016
RESUMEN
Objetivo Comparar secuencias de nucleótidos y de aminoácidos de la proteína no estructural 1-NS1 de cepas DENV-2, aisladas de pacientes febriles de diferentes países suramericanos, que cursaron cuadros clínicos con severidad o sin ella.
Materiales y Métodos El análisis filogenético fue realizado a partir de 28 secuencias moleculares completas (1 056 pb) del gen NS1 del serotipo DENV-2. Se realizó un análisis filogenético bayesiano utilizando el software MrBayes v.3.2.0, con el modelo SYM+G y un análisis filogenético con el método Neighbor-Joining con el modelo Jukes-Cantor. Además, las secuencias de aminoácidos fueron alineadas y comparadas entre sí, mediante el programa Clustal W incluido en el software MEGA v. 5.2.
Resultados En las secuencias de aminoácidos asociadas a sangrado, la sustitución más frecuente fue isoleucina→ treonina, en la posición 93. Estas secuencias presentaron un mayor porcentaje (94,6 %) de homología de aminoácidos de la proteína NS1 en comparación con el porcentaje de homología (74 %) de los aislamientos DENV-2 no asociados a sangrado. Se identificaron cinco clados que agrupan la mayoría de las secuencias analizadas (19/24; 79,2 %) con valores de probabilidad posterior mayores o iguales al 58 %. Siete (87,5 %) secuencias asociadas a sangrado se relacionan filogenéticamente dentro de los clados 4 y 5, con valores de probabilidad posterior del 58 % y 97 %, respectivamente.
Conclusión No se encontraron características filogenéticas ni tampoco diferencias entre las secuencias de aminoácidos de la proteína NS1-DENV-2 estudiadas, que pudieran ser relacionadas, de manera directa, con la severidad de la enfermedad.
Palabras Clave: Virus del Dengue, dengue grave, filogenia, homología de secuencia, América del Sur (fuente: DeCS, BIREME).
ABSTRACT
Objective The objective of this in silico study was to compare nucleotide and amino acids DENV-2-NS1 sequences isolated from febrile patients, with and without disease severity, from different South American countries.
Matherials and Methods A bayesian MCMC phylogenetic analysis was carried out using 28 complete sequences of the gene NS1 of the DENV-2 serotype (1 056 bp), using MrBayes v.3.2.0 software, with the model SYM+G (2.5 million generations). We also carried out a phylogenetic analysis with Neighbor-Joining method (Jukes-Cantor model). In addition, the amino acids sequences were aligned and compared with each other, using Clustal W included in MEGA v.5.2 software.
Results In the amino acids sequences associated with bleeding, the most frequent substitution was isoleucine → threonine at posicion 93. These sequences showed a high percentage (94.6 %) of amino acid homology in comparison with the percentage of amino acids homology (74 %) of DENV-2 isolates not associated with bleeding. Five clades were identified that group the vast majority of the DENV-2-NS1 sequences analyzed (19/24; 79.2 %) with posterior probability values greater than or equal to 58 %. Seven sequences (87.5 %) associated with bleeding were phylogenetically related within clades 4 and 5, the posterior probability values were 58 % and 97 %, respectively.
Conclusion Neither phylogenetic characteristics nor differences between amino acids of the DENV-2-NS1 sequences studied were found that could be associated directly with severity of the disease.
Key Words: Dengue virus, severe dengue, phylogeny, sequence homology, ns1 protein, dengue virus type 2, South America (source: MeSH, NLM).
La emergencia del dengue como problema de salud pública, en los países tropicales y subtropicales, se evidencia en las cifras de morbilidad reportadas, las cuales indican que son más de 50 millones de infecciones por año en aproximadamente 100 países (1,2).
Durante la última década se ha observado un incremento significativo de reportes de casos en casi todos los países del continente americano, excepto Uruguay y Chile porque aun no existe evidencia de transmisión indígena en estos dos territorios del cono sur (3).
En cuanto al mecanismo de contagio, participan mosquitos del género Aedes, principalmente A. aegypti para América y A. albopictus en Ásia (3-5) como vectores eficientes del virus dengue. Este miembro de la familia Flaviviridae, posee un genoma constituido por una monocadena de ARN con polaridad positiva, de 9 500 a 12 500 nucleótidos, que codifica para tres proteínas estructurales (proteína de cápside, C; de membrana, M y de envoltura, E) y siete proteínas no estructurales (NS1, NS2a, NS2b, NS3, NS4a, NS4b y NS5). Además, se reconocen cuatro serotipos (DENV-1/-4), filogenéticamente diferentes, con diversos genotipos para cada uno de ellos (1,6).
Aunque se ha demostrado que la introducción o reintroducción de serotipos o genotipos del virus dengue resulta en un incremento en el número de casos graves en la población afectada (7,8), existen evidencias que muestran al DENV-2 como el serotipo más virulento y con una mayor tasa de replicación (9-11) y la asociación entre los genotipos de origen asiáticos con una mayor severidad en los cuadros clínicos (12-14).
De acuerdo con esto, se ha intentado identificar diferencias genéticas asociadas con la severidad clínica de las infecciones por virus dengue, mediante el análisis filogenético de secuencias genomicas virales. Sin embargo, los estudios que han comparado secuencias de genes E y NS1 de cepas DENV-2 asiáticas no han identificado sitios específicos asociados con la severidad de la enfermedad febril (14-19). No se tiene conocimiento de este tipo de comparaciones utilizando secuencias genomicas de aislamientos suramericanos.
A pesar de esta aparente ausencia de asociación, existe evidencia que sugiere la participación de ciertas proteínas no estructurales en la patogenia de la infección por virus dengue. Como es el caso de la glicoproteína NS1 presente en todos los miembros de la familia Flaviviridae (19,20,21). Se ha demostrado que la antigenemia NS1 parece ser significativamente más alta en pacientes que desarrollan cuadros más severos de dengue, lo cual permite sugerir que la secreción de NS1 puede ser un evento patogénico importante en la infección por virus dengue (22,23).
En coherencia con lo anterior, en un estudio reciente se reporta que la proteína NS1 recombinante tiene un efecto inhibidor, dosis dependiente, sobre la activación de la protrombina, reflejándose en una prolongación en el tiempo parcial de tromboplastina activada, lo cual implica a NS1 en la perdida plasmática de una manera independiente de anticuerpos (24).
Por todo lo anterior, el objetivo del presente estudio in silico fue comparar secuencias de nucleótidos y de aminoácidos de la proteína no estructural 1-NS1 de cepas DENV-2 aisladas de pacientes febriles de diferentes países suramericanos, que cursaron cuadros clínicos con severidad o sin ella. La información clínica de estos pacientes fue obtenida de NIAID Virus Pathogen Database and Analysis Resource-ViPR (25), disponible en el sitio web http://www.viprbcr.org.
MATERIALES Y MÉTODOS
Este estudio in silico fue realizado a partir de 24 secuencias moleculares completas (1 056 pb) del gen NS1 del serotipo DENV-2 y una secuencia externa NS1-DENV-4, obtenidas de NIAID Virus Pathogen Database and Analysis Resource-ViPR (25), disponible en el sitio web http://www.viprbcr.org. Adicionalmente, se utilizaron secuencias representativas de tres genotipos del DENV-2 (América-Ásia, América y Ásia-2), disponibles en GenBank ( http://www.ncbi.nlm.nbi.gov/genbank/GenbankSearch.html).
Con las secuencias de nucleótidos obtenidas se realizó un alineamiento múltiple de secuencias utilizando el programa MAFFT, disponible en el sitio web http://www.ebi.ac.uk/Tools/msa/mafft/.
Con el fin de optimizar los parámetros para la construcción del árbol filogenético se utilizó el software JModeltest0.0.1 (26), identificándose al Symmetrical Model plus gamma, SYM+G, como el modelo con el mejor ajuste a los datos.
Se realizó un análisis filogenético bayesiano MCMC utilizando el software MrBayes v.3.2.0 (27), con el modelo SYM+G, utilizando los parámetros por defecto. Se permitió correr el algoritmo por 2 500 000 generaciones, con una frecuencia de muestreo cada 1 000 generaciones, hasta que la desviación estándar promedio de las frecuencias fuera inferior a 0,01. Se descartó el 25 % de los árboles como burnin y con los árboles remanentes se calcularon las distancias evolutivas del árbol consenso. Adicional a esto, se realizó un análisis filogenético mediante el método de Neighbor-Joining con el modelo Jukes-Cantor. Los arboles filogenéticos generados fueron visualizados con el programa TreeView (28).
Posteriormente, se realizó la transformación de las secuencias de nucleótidos en secuencias de aminoácidos usando el programa Bioedit 7.0.9 (29,30). Luego de su alineación, mediante el programa Crustal W incluido en el software MEGA v. 5.2 (30,31), las secuencias de aminoácidos fueron comparadas entre sí, para poder establecer las posiciones donde se presentaron sustituciones.
RESULTADOS
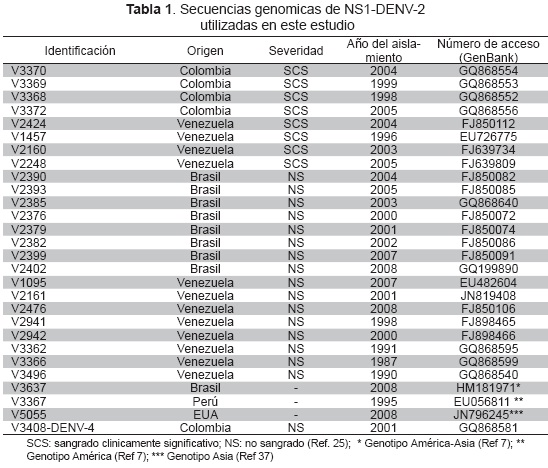
Las características epidemiológicas y los números de acceso al GenBank de las 28 secuencias genomicas de la proteina no estructural 1 del DENV-2 estudiadas, se presentan en la Tabla 1.
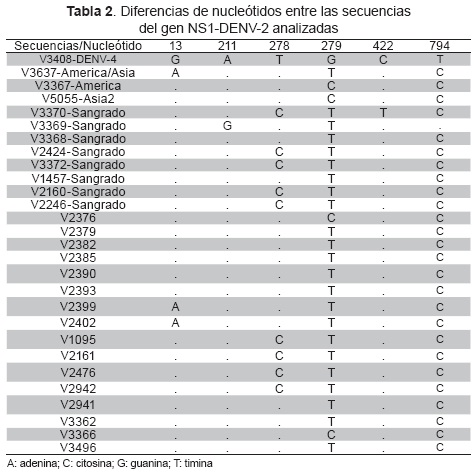
A partir de las secuencias de nucleótidos alineadas en el programa Bioedit, se lograron identificar 99 polimorfismos de un solo nucleótido, SNPs, de los cuales solo seis representaron cambios en la estructura primaria de la proteína NS1 del serotipo DENV-2 (Tabla 2). Estos cambios se presentaron en el 75 % (6/8) de los aislamientos DENV-2 asociados a sangrado clínicamente significativo, siendo la sustitución más frecuente isoleucina treonina, en la posición 93.
Solo dos aislamientos DENV-2 asociados a sangrado, ambos de origen colombiano, V3369 y V3370, presentaron más de un cambio en la secuencia de aminoácidos de la proteína NS1: aa71 isoleucina → valina / aa265 alanina → valina y aa93 isoleucina → treonina / aa141 alanina → valina, respectivamente.
Entre las ocho cepas DENV-2 asociadas a sangrado existe, en promedio, un 94,6 % de homología de aminoácidos en la proteína NS1, en cambio, los aislamientos no asociados presentaron, aproximadamente, un 74 % de homología.
En la topología obtenida por inferencia bayesiana (Figura 1) no se observan politomias, parafilas ni tampoco grupos monofileticos en términos de país de origen, en cambio, se identifican cinco clados que agrupan la gran mayoría de las secuencias del gen NS1 del DENV-2 analizadas (21/28; 75 %) con valores de probabilidad posteriori mayores o iguales al 58 %.
Siete (87,5 %) secuencias asociadas a sangrado clínicamente significativo se relacionan filogenéticamente dentro de los clados 4 y 5, con valores de probabilidad posteriori del 58 % y 96 %, respectivamente.
DISCUSIÓN
La circulación de los cuatro serotipos del virus dengue ha sido reportada en el territorio americano, siendo el DENV-2 el más importante en términos de cifras de morbimortalidad (33,34,35). Oficialmente, el primer aislamiento de este serotipo se reporto en Trinidad, 1953 (8,36) y la primera epidemia asociada a su presencia ocurrio en Cuba en 1981, como consecuencia de la entrada de un genotipo asiático (8,37). Existe evidencia derivada de estudios de epidemiología molecular que permite sugerir que el DENV-2 circulante en Colombia, Venezuela y Brasil posee un ancestro común de origen asiático (8,14).
En el presente estudio, las relaciones filogenéticas estimadas bajo los criterios de inferencias bayesiana (Figura 1) no permiten sugerir el origen asiático de las secuencias genomicas de NS1-DENV-2, muy seguramente consecuencia de la no utilización de secuencias representativas del genotipo Ásia-1. En cambio, permiten observar que los aislamientos asociados a sangrado se presentan, en su gran mayoría, en dos clados distinguibles con valores dispares de probabilidad posterior. En coherencia con otros referentes (7,38,39), en la tipología del árbol filogenético obtenido no se identifican clados en términos de pais de origen.
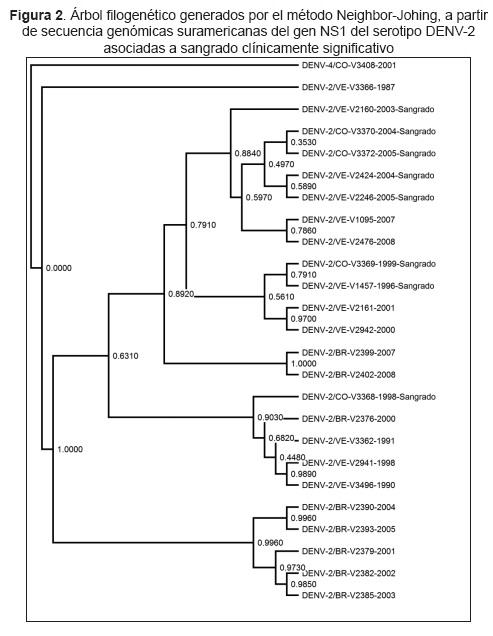
En la Figura 2, se muestran las relaciones filogenéticas estimadas por el método basado por distancia, Neighbor-Joining para las ocho secuencias del gen NS1-DENV asociado a sangrado clínico clínicamente significativo. Los arboles filogenéticos obtenidos por ambos métodos de inferencia son coherentes en sus características filogenéticas.
En cuanto a las sustituciones de aminoácidos derivadas de los SNPs no-sinónimos, es importante señalar que la única de éstas que representa un cambio en la polaridad de la cadena lateral corresponde a isoleucina → treonina en la posición 93. Este cambio en la hidrofilicidad de la proteína podría derivar en variaciones significativas tanto en su estructura secundaria como en su antigenicidad, características que han sido reportadas en otras proteínas no estructurales de este virus (19,40).
En definitiva, no se encontraron características filogenéticas ni tampoco diferencias entre las secuencias de aminoácidos de la proteína NS1-DENV-2 estudiadas, que pudieran ser relacionadas, de manera directa, con la severidad de la enfermedad. Más sin embargo, se reconoce que las diferencias en los genes no estructurales podrían, potencialmente, alterar la eficiencia de la replicación de este agente vírico, lo cual podría verse reflejado en la magnitud y compromiso de las viremias (40)*
REFERENCIAS
1. Simmons CP, Farrar JJ, van Vinh Chau N, Wills B. Current concepts dengue. N Engl J Med. 2012; 366: 1423-1432. [ Links ]
2. Díaz FA, Alves E. Factors associated with dengue mortality in Latin America and the Caribbean, 1995-2009: an ecological study. Am J Trop Med Hyg. 2012; 86(2): 328-334. [ Links ]
3. San Martín JL, Brathwaite O, Zambrano B, Solórzano JO, Bouckenooghe A, Dayan GH, et al. The epidemiology of dengue in the Americas over the last three decades: a worrisome reality. Am J Trop Med Hyg. 2010; 82(1): 128-135. [ Links ]
4. Laughlin CA, Morens DM, Casserri MC, Costero A, San Martín JL, Whitehead SS, et al. Dengue research opportunities in the Americas. J Infect Dis. 2012; 206(7): 1121-1127. [ Links ]
5. Guzmán A, Istúriz RE. Update on the global spread of dengue. Int J Antimicrob Agents. 2010; 36(suppl 1): S40-S42. [ Links ]
6. Mangold KA, Reynolds SL. A review of dengue fever: a resurging tropical disease. Pediatr Emerg Care. 2013; 29(5): 665-669. [ Links ]
7. Mamani E, Álvarez C, García M, Figueroa D, Gatti M, Guio H y cols. Circulación de un linaje diferente del virus dengue 2 genotipo América / Ásia en la región amazonica de Perú, 2010. Rev Peru Exp salud Publica. 2011; 28(11): 72-77. [ Links ]
8. Faria NR, Nogueira RM, de Filippis AM, Simões JB, Nogueira FdeB, da Rocha Queiroz Lima M, et al. Twenty years of DENV-2 activity in Brazil: molecular characterization and phylogeny of strains isolated from 1990 to 2010. PLoS Negl Trop Dis. 2013; 7(3): e2095. doi: 10.1371/journal.pntd.0002095. [ Links ]
9. Rantam FA, Purwati AN, Sasmono T, Lee D, Eryk H, Helen S, et al. Serotype infectivity and phylogenetic of dengue virus cause of dengue fever (DF), dengue hemorrhagic fever (DHF), and dengue shock syndrome (DSS) in surabaya-Indonesia. African J Internal Med. 2013; 1(5): 31-36. [ Links ]
10. Mukherjee S, Hanley KA. RNA interference modulates replication on DENV in Drosophila melagonaster cells. BMC Microbiol. 2010; 10:127 doi: 10.1186/1471-2180-10-127. [ Links ]
11. Gonzalves AP, Engel RE, St Clair M, Purcell RH, Lai CJ. Monoclonal antibody-mediated enhanchment of dengue virus infection in vitro and in vivo and strategies for prevention. Proc Natl Acad Sci USA. 2007; 104(22) 9422-9427. [ Links ]
12. Messer WB, Gubler DJ, Harris E, Sivananthan K, de Silva AM. Emergence and global spread of a dengue serotype 3, subtype III virus. Emerg Infect Dis. 2003; 9(7): 800-809. [ Links ]
13. Loroño MA, Farfán JA, Zapata AL, Rosado EP, Flores LF, García JE, et al. Introduction of the American/Asian genotype of dengue 2 virus into the Yucatan state of Mexico. Am J trop Med Hyg. 2004; 71(4): 485-492. [ Links ]
14. Ricco-Hesse R. Microevolution and virulence of dengue viruses. Adv Virus Res. 2003; 59: 315-341. [ Links ]
15. Blok J, Samuel S, Gibbs AJ, Vitarana UT. Variation of the nucleotide and encoded amino acid sequences of the envelope gene from eight dengue-2 viruses. Arch Virol. 1989; 105(1-2): 39-53. [ Links ]
16. Blok J, Gibbs AJ, McWilliam SM, Vitarana UT. NS1 gene sequences from eight dengue-2 viruses and their evolutionary relationship with other dengue-2 viruses. Arch Virol. 1991; 118(3-4): 209-223. [ Links ]
17. Pandey BD, Igarashi A. Severity-related molecular differences among nineteen strains of dengue type 2 viruses. Microbiol Immunol. 2000; 44(3): 179-188. [ Links ]
18. Mangada MN, Igarashi A. Molecular and in vitro analysis of eight dengue type 2 viruses isolated from patients exhibiting different disease severities. Virology. 1998; 244(2): 458-466. [ Links ]
19. Goncalvez AP, Escalante AA, Pujol FH, Ludert JE, Tovar D, Salas R, et al. Diversity and evolution of the envelope gene of dengue virus type 1. Virology. 2002; 303: 110-119. [ Links ]
20. Whitehorn J, Simmons CP. The pathogenesis of dengue. Vaccine. 2011; 29: 7221-7228. [ Links ]
21. Clyde K, Kyle JL, Harris E. Recent advences in deciphering viral and host determinants of dengue virus replication and pathogenesis. J Virol. 2006; 80(23): 11418-11431. [ Links ]
22. Thomas L, Najioullah F, Verlaeten O, Martial J, Brichler S, Kaidomar S, et al. Relationship between nonstructural protein 1 detection and plasma virus load in dengue patients. Am J Trop Med Hyg. 2010; 83(3): 696-699. [ Links ]
23. Chuang YC, Wang SY, Lin YS, Chen HR, Yeh TM. Re-evaluation of the pathogenic roles of nonstructural protein 1 and its antibodies during dengue virus infection. J Biomed Sci. 2013; 20(1): 42-48. [ Links ]
24. Lin SW, Chuang YC, Lin YS, Lei HY, Liu HS, Yeh TM. Dengue virus nonstructural protein NS1 binds to prothrombin/thrombin and inhibits prothrombin activation. J Infect. 2012; 64(3): 325-334. [ Links ]
25. Pickett BE, Sadat EL, Zhang Y, Noronha JM, Squires RB, Hunt V, et al. ViPR: an open bioinformatics database and analysis resource for virology research. Nucleic Acids Res. 2012; 40(Database issue): D593-8. doi: 10.1093/nar/gkr859. Epub 2011 Oct 17. [ Links ]
26. Posada D. JModelTest: phylogenetic model averaging. Mol Biol Evol. 2008; 25(7): 1253-1256. [ Links ]
27. Ronquist F, Huelsenbeck JP. MRBAYES 3: bayesian phylogenetic inference under mixed models. Bioinformatics. 2003; 19(12): 1572-1574. [ Links ]
28. Page RD. TREEVIEW: an application to display phylogenetic trees on personal computers. Comput App Biosci. 1996; 12(4): 357-358. [ Links ]
29. Hall TA. BioEdit: a user-friendly biological sequence alignment editor and analysis program for Windows 95/98/NT. Nucl Acids Symp Ser. 1999; 41: 95-98. [ Links ]
30. Alfonso HL, Amarilla AA, Gonçalves PF, Barros MT, de Almeida FT, Silva TR, et al. Phylogenetic relationship of dengue virus type 3 isolated in Brazil and Paraguay and global evolutionary divergence dynamics. Virol J. 2012; 9:124. doi: 10.1186/1743-422X-9-124. [ Links ]
31. Tamura K, Peterson D, Peterson N, Stecher G, Nei M, Kumar S. MEGA5: molecular evolutionary genetics analysis using maximun likelihood evolutionary distance, and maximun parsimony methods. Mol Biol Evol. 2011; 28(10): 2731-2739. [ Links ]
32. Cruz CD, Forhey BM, Juarez DS, Guevara C, Leguia M, Kochel TJ, et al. Molecular epidemiology of American/Asian genotype DENV-2 in Perú. Infect Genet Evol. 2013; 18: 220-228. doi: 10.1016/j.meegid.2013.04.029. Epub 2013 May 3. [ Links ]
33. Méndez JA, Usme-Ciro JA, Domingo C, Rey GJ, Sánchez JA, Tenorio A, et al. Phylogenetic reconstruction of dengue virus type 2 in Colombia. Virology J. 2012; 9:64. [ Links ]
34. Padilla JC, Rojas D, Sáenz R, Rojas D, Bello B, Méndez JA. Dengue en Colombia: epidemiología, estrategias de intervención y perspectivas del problema. Ministerio de la Protección Social - Instituto Nacional de Salud Colombia; 2010. [ Links ]
35. World Health Organization. Dengue guidelines for diagnosis, treatment, prevention and control. Special program for research and training in tropical disease. France, World Health Organization; 2009. [ Links ]
36. Anderson CR, Downs WG, Hill AE. Isolation of dengue virus from a human being in Trinidad. Science. 1956; 124(3214): 224-225. [ Links ]
37. Guzman MG, Deubel V, Pelegrino JL, Rosario D, Marrero M, Sariol C, et al. Partial nucleotide and amino acid sequences of the envelope and the envelope/nonstructural protein 1 gene junction of four dengue-2 virus strains isolated during the 1981 Cuban epidemic. Am J Trop Med Hyg. 1995; 52(3): 241-246. [ Links ]
38. Weaver SC, Vasilakis N. Molecular evolution of dengue viruses: contributions of phylogenetics to understanding the history and epidemiology of the preeeminent arboviral disease. Infect Genet Evol. 2009; 9(4): 523-540. [ Links ]
39. Vasilakis N, Fokam EB, Hanson CT, Weinberg E, Sall AA, Whitehead SS, et al. Genetic and phenotypic characterizarion of sylvatic dengue virus type 2 strains. Virology. 2008; 377(2); 296-307. [ Links ]
40. Leitmeyer KC, Vaughn DW, Watts DM, Salas R, Villalobos I, Ramos C, et al. Dengue virus structural differences that correlate with pathogenesis. J Virol. 1999; 73(6): 4738-4747. [ Links ]