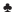La Leucemia Mieloide Aguda (LMA) concentra cerca del 20 % de leucemias en menores de 18 años y no existe evidencia sobre mayor incidencia en algún grupo étnico o de género en particular 1,2.
Colombia no cuenta con estadísticas consolidadas sobre LMA pediátrica, en Bogotá, el informe de vigilancia del comportamiento del cáncer infantil del 2013 reportó 147 casos de leucemias agudas en menores de 18 años y 28 de estos (19 %) fueron leucemias mieloides; para ese mismo año, la Secretaría de Salud de esa ciudad estimó una proporción de incidencia de 14 por millón, mientras que en Cali la estimación en menores de 15 años se ubicó entre 6,7 y 7,9 casos por cada millón de habitantes en ese rango de edad 3.
Son escasos los reportes sobre desenlaces en LMA pediátrica en Colombia, para el año 2003 el Instituto Nacional de Cancerología (INC) estimó una sobrevida del 22 % 4, cifra cercana a la que se registraba en los años setentas en países desarrollados, los cuales para el 2009 ya mostraban tasas de hasta el 64 % 5, por lo que el INC señala la necesidad de mejorar la estrategia de tratamiento, empleando la estratificación de riesgo, con protocolos diferentes y con mayores medidas de soporte.
Según la citogenética del paciente, la LMA se estratifica en tres niveles de riesgo de recaer y morir a causa de la enfermedad, bajo, intermedio y alto; en riesgo intermedio se ubican quienes presentan las alteraciones t(9;n), +21, 11q23, hiperdiploide, hipodiploide, normal y pseudodiploide.; y el riesgo alto reúne a quienes cuentan con las alteraciones t(6;9), -7/7q-, -5/5q- y +8 6-9.
Todos los pacientes deben ser llevados a quimioterapia de inducción y existen solo dos alternativas de tratamiento de consolidación, la quimioterapia y el trasplante con progenitores hematopoyéticos 10. El trasplante puede ser alogénico o autólogo, sin embargo este último no ha mostrado mayor efectividad que la quimioterapia 11 o al trasplante alogénico 12.
Debido a que la quimioterapia de consolidación resulta menos costosa que el trasplante 13, éste pierde efectividad conforme se incrementa el nivel de riesgo 8, por lo que la probabilidad de éxito terapéutico incrementa al realizar las pruebas de estratificación e identificar a tiempo los pacientes que tendrían mejores resultados de ser tratados con trasplante.
El trasplante alogénico en el tratamiento de consolidación de LMA pediátrica en el Sistema de Salud colombiano es costo-efectivo, tanto para el riesgo intermedio 14 como para el alto 15. Sin embargo no se ha establecido si es costo-efectivo realizar las pruebas de estratificación a todos los pacientes pediátricos diagnosticados con LMA, para determinar si se debería realizar trasplante.
Esta evaluación determina la razón de costo efectividad incremental del uso de la evaluación de la t (8;21), inv 16, Flt3, Nucleofosmina, y de las alteraciones citogenéticas denominadas "complejas" en el incremento de la sobrevida libre de evento en población pediátrica diagnosticada con LMA , dentro del sistema de salud colombiano.
MATERIALES Y MÉTODOS
La evaluación se realizó desde la perspectiva del Sistema de Salud colombiano, incluyendo únicamente los costos médicos directos y con los años de vida ganados como medida de efectividad. El umbral de costo efectividad empleado fue tres veces el Producto Interno Bruto (PIB) per cápita, según lo recomendado por el Ministerio de Salud y Protección Social 16, y dado que el PIB utilizado fue el de 2010, todos los valores monetarios se expresaron en pesos colombianos de ese mismo año, ajustando mediante la inflación acumulada.
Se simuló una cohorte de mil pacientes menores de 18 años, diagnosticados con LMA y en remisión completa luego de la quimioterapia de inducción.
Las pruebas para la estratificación del riesgo evaluadas corresponden a la hibridización in situ con fluorescencia (FISH) y a un cariotipo especial para estados leucémicos.
Estas pruebas de estratificación deben efectuarse a todos los pacientes diagnosticados con LMA para establecer si les será más efectivo el trasplante con progenitores hematopoyéticos que la quimioterapia, por esta razón la tamización a todos los pacientes y el trasplante a los que los ameriten hacen parte del mismo brazo del modelo de decisión. Esto equivale a considerar la estratificación parte del esquema de tratamiento de trasplante y la costo-efectividad evaluó a través del balance entre los recursos empleados y los años de vida ganados con el trasplante, imputando a éste el costo de la tamización del riesgo a todos los pacientes.
Se acudió al modelo con el que se ha evaluado la costo-efectividad del trasplante, comparado con la quimioterapia de consolidación, en pacientes pediátricos con LMA 14,15. No se efectuaron cambios en la estructura del modelo. En el brazo de trasplante se adicionó el costo de realizar las pruebas a todos los pacientes, esto incluye las efectuadas a quienes como resultado fueron clasificados en riesgo bajo y en consecuencia tratados con quimioterapia de consolidación. La estratificación será costo-efectiva si el trasplante incluyendo las pruebas de estratificación es costo-efectivo.
El modelo es un árbol de decisión en el que los pacientes son estratificados y reciben trasplante alogénico con progenitores hematopoyéticos no emparentados compatibles, o de donante idéntico emparentado; o no son estratificados y llevados a ciclos de quimioterapia de consolidación.
Las ramas del árbol son de estructura idéntica. En cada alternativa se puede o no sobrevivir al procedimiento; quienes sobreviven cuentan con una probabilidad de desarrollar efectos adversos, y estos pueden eventualmente llevarlos a la muerte; finalmente, quienes no enfrentan complicaciones, o se reponen a ellas, salvo que presenten recaída, alcanzan la expectativa de vida de un niño colombiano sin desarrollar neoplasias.
Salvo por la inclusión de los costos de la estratificación a pacientes de riesgo bajo, no se modelaron desenlaces ni costos de este grupo de pacientes por ser iguales en las dos ramas del árbol (Figura 1).
Las complicaciones modeladas fueron las infecciones en los pacientes consolidados con quimioterapia y la enfermedad injerto contra hospedero en quienes reciben trasplante, asumiendo que ocurrían dentro de los primeros 120 días siguientes al tratamiento y que la recaída implicaba la muerte del paciente. No se incluyeron complicaciones de largo plazo debido a la ausencia de datos en la literatura científica.
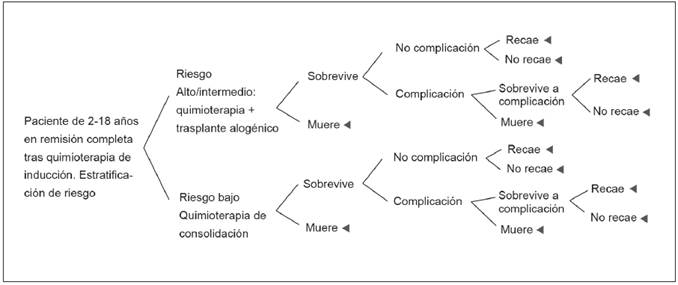
La Tabla 1 contiene los valores de efectividad y costos empleados en el modelo. La información sobre los resultados relevantes en salud fue tomada de ensayos clínicos aleatorizados y del reporte para el 2010 del Center for International Blood & Marrow Transplant Research (CIBMTR) 17.
Las probabilidades de sobrevivir al tratamientoa las complicaciones y de recaída se asumieron iguales para los trasplantes emparentado y no emparentado en razón a que sus curvas de sobrevida son similares 8,17-20 y no hay evidencia de diferencias apreciables en la ocurrencia de eventos adversos 19,21.
Debido a que el objetivo del tratamiento de consolidación es mejorar la sobrevida libre de enfermedad a largo plazo, el horizonte temporal fue la expectativa de vida.
No existen datos de seguimiento a pacientes que han recibido trasplante. Sin embargo, en los modelos de sobrevida reportados en la literatura el porcentaje de pacientes que sobreviven se estabiliza dentro de los cinco años siguientes al procedimiento 6,22, por lo que se asumió que los pacientes que no recaen alcanzan la esperanza de vida promedio de un niño colombiano, 71,8 años 23.
El precio de los medicamentos fue consultado en el Sistema de Información de Precios de Medicamentos SIS-MED del 2008 24, por ser la versión con la mayor cantidad de referencias; y el correspondiente a los insumos se extrajo de licitaciones públicas.
El precio de los procedimientos empleado fue el reportado en el manual tarifario del ISS 2001 25 más el 20 %, en atención a que en Colombia los precios de los procedimientos en salud son establecidos en negociación directa entre aseguradores y prestadores de servicios, usando como punto de partida el valor establecido en el manual del ISS del 2001, obteniendo resultados que van desde el 10 % hasta el 30 % por encima del manual.
Los costos de la quimioterapia corresponden a la consolidación en el esquema BFM 93, que consiste en seis semanas de tratamiento con siete medicamentos: tioguanina 60 mg/m2 vía oral durante los primeros 43 días; prednisona 40 mg/m2 vía oral del día 1 al 28; vincristina 1.5 mg/m2 en los días 1, 8, 15 y 22; doxorubicina 30 mg / m2 en los días 1, 8, 15 y 22; Ara-C 75 mg/m2 en ciclos de tres días con espacio de cuatro días entre cada uno; Ara-C intrate0cal 40 mg en los días 1, 15, 29 y 43; y ciclofosfamida 500 mg/m2 en los días 29 y 43 25.
De acuerdo con el manual tarifario del ISS, el valor cancelado por el procedimiento de trasplante también incluye los medicamentos e insumos necesarios para efectuar el tratamiento y atender las posibles complicaciones, pero no contempla las células a trasplantar, cuyo importe no se encuentra en ninguna fuente oficial. En esta materia se acudió a la opinión del coordinador de uno de los centros que realizan este tipo de trasplante en el país, quien indicó que el valor promedio de los progenitores hematopoyéticos no emparentados provenientes de cordón umbilical, los de mayor disponibilidad en Colombia, ascendía a $30 000 000 (Tabla 1).
Por cuenta de la negociación sobre el costo de los procedimientos y de la existencia de más de un precio para el mismo medicamento, existe variabilidad en el costo final de las intervenciones.
Para determinar el efecto en la razón de costo efectividad de la variabilidad tanto en los costos como en la efectividad de las intervenciones comparadas, se efectuaron análisis de sensibilidad univariados, en los que se permitía a las variables de efectividad tomar los valores extremos reportados en la literatura. El valor mínimo para los costos fue el reportado en el SISMED e ISS. El valor máximo fue el que se obtuvo al construir casos atípicos mediante consulta a expertos, en los que se contemplaron el uso de diferentes protocolos de quimioterapia y el tratamiento de las complicaciones más costosas que pueden presentarse en los brazos de trasplante.
Adicionalmente se realizó un análisis de sensibilidad probabilístico generando diez mil simulaciones, en cada una de las cuales todas las variables tomaban un valor aleatorio de acuerdo con la distribución de probabilidad teórica que se reporta en la Tabla 1.
Por tratarse de una evaluación realizada mediante el análisis de datos secundarios, no requirió revisión por parte de comité de ética.
RESULTADOS
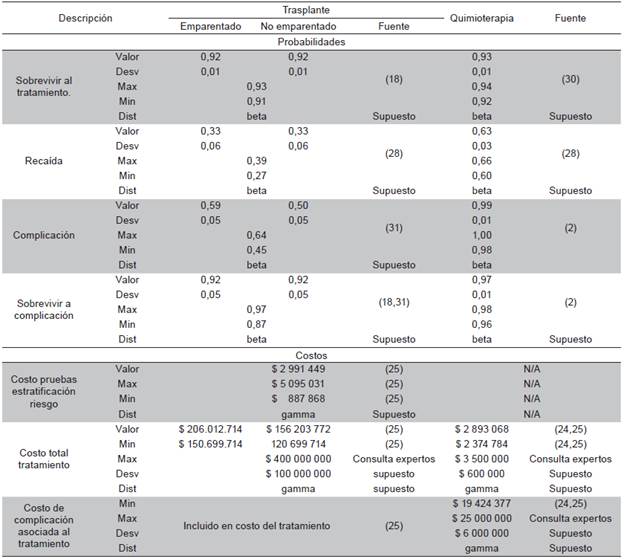
El análisis de costo-efectividad muestra que la estratificación y posterior trasplante con progenitores hematopoyéticos tiene una mayor efectividad, sobrepasando a la quimioterapia en 20,4 años de sobrevida libre de enfermedad por persona, pero superando también su costo en $174 327 544, dando como resultado que cada año de vida adicional a los logrados con quimioterapia le cuesta al sistema $8 559 944. (Tabla 2).
La razón de costo efectividad incremental de la tamización del riesgo y posterior trasplante es inferior a tres veces el Producto Interno Bruto per cápita del año 2010, $36 142 254, con lo que se concluye que, en la población de estudio y dentro del sistema de salud colombiano, realizar las pruebas de estratificación del riesgo es una alternativa costo efectiva para el tratamiento de la LMA.
El análisis de sensibilidad univariado mostró que, tomando los valores extremos posibles para todas las variables de acuerdo con la literatura, en ningún caso la razón de la estratificación del riesgo, sería superior al umbral de costo-efectividad.
En el resultado del análisis de sensibilidad probabilístico, la estratificación fue costo-efectiva en el 74 % de las simulaciones. Por su parte la curva de aceptabilidad indicó que, con una disposición a pagar al menos de $7 200 000 por año de vida ganado, estratificar tiene mayor probabilidad de ser costo-efectivo que no hacerlo.
DISCUSIÓN
La conducción de pruebas para estratificación del riesgo a todos los pacientes pediátricos con LMA resulta costo efectiva para el Sistema de Salud colombiano. No obstante, se requieren estudios complementarios de impacto presupuestal y otros elementos de utilidad para los tomadores de decisiones.
Las conclusiones sobre la costo-efectividad de la estratificación del riesgo concuerdan con otros estudios que evaluaron el trasplante en la consolidación de leucemias agudas en población adulta 26,27 e infantil 14,15, empleando también árboles de decisión, desenlaces agudos y las mismas distribuciones de probabilidad teóricas. Sin embargo, no existen publicaciones que hayan evaluado esquemas de tamización para la estratificación del riesgo.
La dificultad para determinar los costos del manejo clínico de los eventos adversos asociados a las estrategias de consolidación, constituye una de las limitaciones del estudio: No obstante, el análisis de sensibilidad permitió observar que un refinamiento de estos costos no modificaría las conclusiones.
Otra limitante consistió en la falta de evidencia clínica de calidad para los parámetros del modelo. Debido a que no se encontró ningún análisis integrativo o ensayo clínico aleatorizado que comparara las estrategias evaluadas y contuviera todas las probabilidades requeridas, se recurrió a las estadísticas del CIBMTR y a la revisión de diferentes artículos para sustraer la información necesaria, incluyendo datos para población adulta, apoyados en que la evidencia indica que no existen diferencias clínicamente significativas entre los resultados para diferentes grupos etarios de los trasplantes en la consolidación de LMA 12.
Para evaluar posibles sesgos derivados de este supuesto, se consultó con expertos clínicos colombianos, quienes manifestaron que las probabilidades empleadas se encuentran dentro de los resultados observados en la práctica clínica nacional.
Con referencia a la existencia en la actualidad de varios protocolos de quimioterapia utilizados en el tratamiento de la LMA, puede asegurarse que las conclusiones son válidas incluso si se compara frente a un esquema diferente al BFM, en razón a que la falta de consenso obedece a que no hay diferencias significativas entre esquemas, en términos de la sobrevida libre de enfermedad o la sobrevida global 22,28,29; y a que las diferencias en costos fueron cubiertas con el análisis de sensibilidad, concluyendo que la razón de costo-efectividad no superaría el umbral ante diferentes escenarios de costo de la quimioterapia.
Es necesario resaltar que la opinión de expertos en LMA indica que los resultados en Colombia del trasplante se encuentran por debajo de los reportados en la literatura científica. Frente a este punto, el análisis de sensibilidad mostró que los valores de las probabilidades de recaída, sobrevida al tratamiento y complicaciones para los que se modificarían las conclusiones, no se encuentran dentro de los intervalos reportados por la literatura, ni en los sugeridos por los expertos colombianos; con lo que puede asegurarse que las conclusiones son robustas para el país.
Finalmente, la no inclusión del ajuste por calidad de vida a la unidad de efectividad, obedeció a que la evaluación se realizó para población pediátrica y no existen cálculos de años de vida ajustados por calidad (QALYS por su sigla en inglés) para Colombia. En esta materia, la robustez de los resultados nuevamente permite establecer que un ajuste por calidad de vida no modificaría las conclusiones