La implementación de sistemas de tratamiento de aguas residuales hace parte de las estrategias para reducir la contaminación de los ríos; estos sistemas tienen como objetivo reducir los contaminantes orgánicos e inorgánicos de dichas aguas mediante procesos físicos, químicos y biológicos. En este trabajo se estudió el biosólido generado en La Planta de Tratamiento de Agua Residual (PTAR) San Fernando (Itagüí), la cual tiene una capacidad para tratar 1,8 m3/s de las aguas residuales domésticas, industriales y hospitalarias generadas en el sur del Valle de Aburrá (área metropolitana de Medellín), correspondiendo al 20 % del agua residual generada en esta zona del área metropolitana 1,2.
Durante el tratamiento de las aguas residuales se generan los lodos que deben ser sometidos a un tratamiento adicional con el fin de reducir su humedad, convertirlo en una materia orgánica estable y disminuir el contenido de patógenos 3. El tratamiento más utilizado en el mundo para este fin es la digestión anaerobia, debido a su alta eficiencia y a la producción de biogás 4. La Agencia de Protección Ambiental de los Estados Unidos utiliza el término biosólido para referirse a los lodos residuales que han sido estabilizados y pueden ser aplicados en suelos 5.
La composición físico-química y microbiológica de los biosólidos es variable y está relacionada con el tipo de agua tratada (doméstica, hospitalaria o industrial), el método de operación de la planta y la prevalencia de enfermedades infecciosas de la población servida 6,7. Los biosólidos pueden ser utilizados en actividades agrícolas, forestales y recuperación de suelos. Sin embargo, la presencia de metales pesados y microorganismos patógenos puede restringir su aplicación 8,9.
A pesar de los usos potenciales del biosólido, el conocimiento de la abundancia y diversidad de los microorganismos presentes en éstos es muy limitado, especialmente por su gran diversidad y la dificultad para su cultivo.
Como alternativa para caracterizar estas comunidades microbianas se ha utilizado la secuenciación del gen ribosomal 16s 10.
El biosólido es una matriz biológicamente compleja, con una alta diversidad de microorganismos, principalmente bacterias 11. En un estudio realizado en lodos activados de plantas de tratamiento en Asia, Canadá y EEUU, se encontró una gran riqueza de géneros bacterianos (744). Los géneros correspondían en su mayoría a bacterias ambientales relacionadas con la ubicación geográfica, la concentración de oxígeno disuelto, temperatura, salinidad, entre otras 11. Con relación al contenido de bacterias patógenas, en EEUU los patógenos encontrados más frecuentemente fueron Mycobacterium, Clostridium y Streptococcus8.
En países tropicales han reportado la presencia de bacterias patógenas en biosólidos. En México se han reportado coliformes fecales en una concentración de 107 NMP/TS (Número Más Probable por Sólidos Totales) y de Salmonella en una concentración de 106 NMP/TS 12. En Colombia se reportó la presencia de Salmonella y de Enterobacterias en una concentración entre 3 000 y 65 000 NMP/g en el biosólido de la PTAR San Fernando 13. No hay estudios sobre la diversidad bacteriana en biosólidos en Colombia o en otros países tropicales. En este artículo se reporta el primer estudio de la diversidad microbiana de un biosólido en un país tropical.
MATERIALES Y MÉTODOS
Muestreo, análisis y extracción del DNA
Se tomaron 2 kg de muestra de biosólido en febrero del año 2012 en las centrifugas deshidratadoras de la PTAR San Fernando. Los análisis químicos se realizaron en el Grupo Interdisciplinario de Estudios Moleculares-GIEM (Universidad de Antioquia). El DNA genómico fue extraído utilizando el kit comercial PowerMax® Soil DNA Isolation Kit (MOBIO, catalogo#12988-10), y se cuantificó por espectrofotometría y fluorimetría. El DNA se almacenó a una concentración de 80 ng/al a -20°c.
Caracterización fisicoquímica
Se siguieron los parámetros establecidos en la Norma Técnica Colombiana 5167 del año 2011. El carbono orgánico según el método de Walkey Black. Las concentraciones de nitrógeno, fosforo y potasio se midieron aplicando los métodos Kjeldahl, espectrofotometría y electroforesis capilar, respectivamente. Para la cuantificación de los metales pesados (Cr, Pb, Cd, Ni), se llevó el material seco a una mufla durante 4 horas a 600°c para la obtención de cenizas y se realizó una digestión con ácido clorhídrico acuoso y se midió por la técnica de absorción atómica de llama.
Amplificación por PCR del gen ribosomal 16S y se-cuenciación masiva
Se amplificación por PCR las regiones hipervariables VI-V3 del 16s-rRNA. Se utilizaron los oligonucleótidos 27F y 534R (subrayados) acoplados con los adaptadores y barcodes recomendados por roche (14,15):
>16s_VI3_454_A (534R) CCATCTCATCCCTGCGTGTCTCCGACTCAG(BARCODE) ATTACCGCGGCTGCTGG
>16s_454_B (27F)
CCTATCCCCTGTGTGCCTTGGCAGTCTCAGAGAGTTT-GATCCTGGCTCAG
Para la región v6-v9 del 16s-rRNA se utilizaron los oligonucleótidos 926F y 1392R (subrayados)16 a los cuales se acoplaron adaptadores y barcodes recomendados por ROCHE:
>I6s_V69_454_A (926F)
CCATCTCATCCCTGCGTGTCTCCGACTCAG(BARCODE) AAACTYAAAKGAATTGACGG
>i6S_v69_454_B(1392R)
CCTATCCCCTGTGTGCCTTGGCAGTCTCAGACGGGCGGTGTGTRC
La amplificación se realizó en un termociclador Veriti® Applied-Biosystems® y con los parámetros: 95°c 1'; 35 ciclos de 94°c 30"; 55°c 30"; 72°c 1' y al final de 72°c 10'. La amplificación fue verificada por electroforesis en gel de agarosa y los productos fueron purificados con AMPURE XT (cat#A63880) (Bechman-Coulter). Los amplicones purificados fueron cuantificados con PICOGREEN y su pureza medida con electroforesis capilar (bioa-NALYZER-2100-Agilent). La secuenciación masiva se realizó utilizando un 454-FLX-Titanium (ROCHE) en el CNSG.
Construcción de librería plásmidica de amplicones del gen 16S-rRNA
Se amplificó el gen 16s-rRNA con los oligos 27F (5' AGA-GTTTGATCCTGGCTCAG) y 1492R modificado (5' TACTCC-TACCTTGTTACGACTT). Los amplicones obtenidos fueron purificados con kit (QIAGEN, QIAquick, Cat No./ID: 28104) y ligados en un T-vector (Thermo, InsTAclone PCR-Cloning-Kit, CAT# K1213). La librería de plásmidos se transformó en E. coli DH5-alfa y se secuenciaron plásmidos de 5 colonias independientes por el método capilar.
Análisis de las secuencias y asignación taxonómica
El paquete AMPLICONNOISE se uso para remover los errores introducidos por la PCR, el pirosecuenciamiento, las lecturas quiméricas y para agrupar las lecturas en OTUS al 97 % y 95 % de similitud 17.
La asignación taxonómica de OTUS se realizó con el programa RDP-Classifier versión 2.11 (Michigan State University) 18 con nivel de confianza del 80 %.
Los análisis filogenéticos se hicieron con el programa MEGA7. Se calcularon las distancias genéticas usando una matriz de distancia pareada y los árboles filogenéticos se construyeron usando el método Neighbor-Joining con 1000 réplicas de bootstrap. Las secuencias de referencia del gen 16s TRNA fueron extraídas de los genomas depositados en el Genbank (NCBI) bajo los siguientes números de acceso: NZ_BBXW00000000, NC_0I4960, NZ_LGHJ00000000, NZ_BBYH00000000, NZ_LGCK00000000, LGCM00000000, BBXY00000000, LGCL00000000, NZ_LGKO00000000 y LGHA00000000.
Análisis estadístico de los datos
Se realizaron curvas de rarefacción con incrementos de 100 utilizando el programa Analytic Rarefaction (http://strata.uga.edu/software/anRareReadme.html). Los índices Shannon y Pielou fueron obtenidos con la suite de algoritmos incluidos en el AMPLICONNOISE 17.
RESULTADOS
Caracterización fisicoquímica y microbiológica por cultivo del biosólido
Los macro y micronutrientes se encuentran en una concentración apta para su uso como enmienda orgánica no húmica; nitrógeno orgánico total 2,02 %, fósforo total 2,8 %, potasio total 1,19 % y carbono orgánico oxidable total 16,13 %. Es importante resaltar que el contenido de metales pesados se encuentra dentro de los límites permitidos, se midieron las concentraciones de cromo, cadmio, plomo y níquel con resultados de 58,4 mg/kg, <0,003 mg/kg, 34,1 mg/kg y 122,8 mg/kg respectivamente. El ensayo de fitotoxicidad reportó un índice de germinación del 100 %. Se encontraron concentraciones de microorganismos mesófilos aerobios, termófilos y mohos con resultados de 3,3x1010 UFc/g (Unidades Formadoras de Colonia por gramo), 3x107 UF-c/g y 400 UFc/g, respectivamente. No se reportó presencia de Salmonella y las enterobacterias se encontraron a una concentración de 200 UFc/g; por debajo del valor máximo permitido por la norma (I 000 UFc/g).
Análisis microbiológico por secuenciamiento profundo
La secuenciación masiva arrojó un total de 185 777 lecturas crudas para la región variable V1-V3 y 115 163 para V6-V9. La longitud media de estas lecturas fue de 238 bases para el amplicon de la región V1-V3 y de 412 bases para el amplicon v6-v9 (Tabla 1).
Tabla 1 Resultados secuenciamiento, depuración y agrupamiento en OTUs de las lecturas obtenidas. Se indican los resultados del procesamiento de los reads por el programa AMPLICONNOISE para las V1-V3 y V6-V9 del gen ribosomal 16S rRNA.
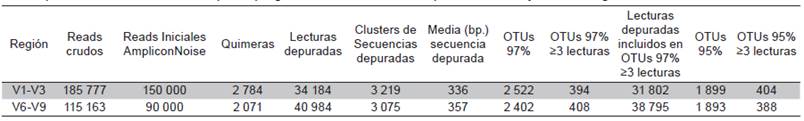
Por una limitación del AMPLICONNOISE se redujo el número de lecturas crudas a procesar a 150 000 para la región variable V1-V3 y 90 000 para la región V6-V9. Los resultados presentados en la Tabla 1 muestran el resultado del procesamiento. Al final se obtuvieron 34 184 lecturas depuradas para la región V1-V3 y 40 984 para la V6-V9. Las lecturas fueron agrupadas en 2 522 y 2 402 OTUS al 97 % y en 1 899 y 1 893 OTUS al 95 %, respectivamente. Para el análisis de clasificación sólo se incluyeron los OTUS al 97 % y que fueran soportados por al menos 3 lecturas. El número de OTUS con este soporte fue similar en ambas regiones estudiadas, ya que se obtuvieron 394 para la región V1-V3 y 408 para la región v6-v9 con corte al 97 % y de 404 y 388 para el 95 % (Tabla 1).
Los análisis de rarefacción mostraron que el muestreo permitió observar con ambas regiones amplificadas la mayoría de las especies presentes en el biosólido; ya que con ambas regiones variables se observó la asíntota de la gráfica después de los 250 individuos analizados. Asignación taxonómica de OTUS al 97 %
Estos OTUS seleccionados estuvieron soportados por 31 802 (VI-V3) y 38 795 (V6-V9) lecturas depuradas. Según el clasificador del RDP, el 100 % de las lecturas de la región V1-V3 fueron asignadas al dominio Bacteria; mientras que para la región V6-V9, 38 761 fueron asignadas a este Dominio. El RDP logró clasificar con un bootstrap >0.6 a nivel de Familia el 91,5 % de los OTUS de la región V1-V3 y el 89,5 % de la región V6-V9. A nivel de género la clasificación fue menos exitosa, reduciéndose al 55 % para ambas regiones estudiadas. Esto muestra la riqueza del biosólido en especies bacterianas no incluidas aun en la base de datos del RDP (Figura 1).
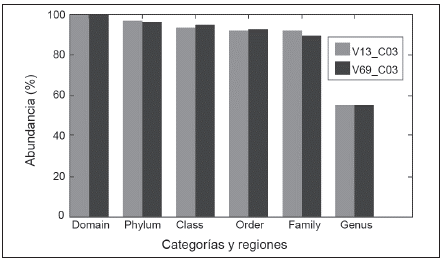
Porcentaje de reads, respecto al total, asignados con un nivel de boostrap mayor a 0.6 esto para las categorías taxonómicas de Dominio, Phylum, Clase, Orden, Familia y Género para los OTUS al 97 % de identidad para las regiones V1-V3 (V13_C03) y V6-V9 (V69_C03).
Figura 1 Porcentaje de lecturas clasificadas en categorías y por las regiones variables del gen 16S rRNA analizadas Ambas regiones coincidieron en que los 5 Phyla más abundantes fueron Chloroflexi, Bacteroidetes, Proteo-bacteria, Actinobacteria y Firmicutes. En el caso de la región VI-V3, Chloroflexi fue el más dominante con 9 230 lecturas, mientras que para la región v6-v9 lo fue Proteobacteria con 14 250. En general, se observaron los mismos Phyla con ambas regiones variables, sin embargo, variaron las abundancias relativas y solo con la región V1-V3 se lograron detectar algunas lecturas del Phylum Acidobacteria (Figura 2A).
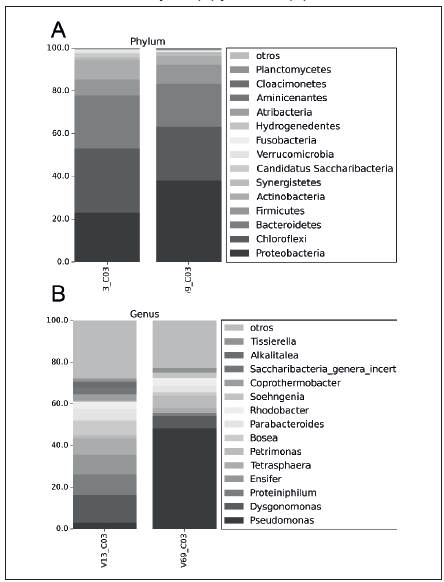
A. Se muestra un gráfico de frecuencia de los 15 Phyla más abundantes en los OTUs al 97 % según su abundancia en lecturas depuradas para las regiones V1-V3 (V13_C03) y V6-V9 (V69_C03). B. Se muestra un gráfico de frecuencia de los 15 Géneros más abundantes en los OTUs al 97 % según su abundancia en lecturas depuradas para las regiones V1-V3 (V13_C03) y V6-V9 (V69_C03).
Figura 2 Grupo taxonómicos clasificados en categorías Phylum (A) y Genero (B)
El 55 % de los otus fueron clasificados a nivel de genero; 121 con la región VI-V3 y 119 con V6-V9, el 45 % restante solo se pudo asignar hasta familia. Los géneros más abundantes clasificados con ambas regiones fueron Pseu-domonas, Dysgonomonas, Proteiniphilum, Ensifer, Tetras-phaera, Petrimonas, Bosea, Parabacteroides, Rhodobacter, Soehngenia, Coprothermobacter y Tissierella. Pseudomo-nas fue el género dominante en la región v6-v9, mientras que Dysgonomonas lo fue con la región V1-V3 (Figura 2B). Se detectaron 77 géneros en común con ambas regiones, mientras que 44 y 42 géneros detectados fueron específicos en las regiones V1-v3 y v6-v9, respectivamente.
El OTU más abundante de la región V1-v3, con 8 838 lecturas, solo pudo ser clasificado hasta Anaerolineaceae con un soporte de bootstrap de 1. Este OTU quedo relacionado débilmente con el género Longilinea, ya que su valor de bootstrap bajó a 0,36. De manera similar, en el caso del amplicón de la región v6-v9, el segundo OTU más abundante (8 861 lecturas) fue clasificado en Anae-rolineaceae con un bootstrap similar. Este mismo grupo fue clasificado como género Anaerolinea con bootstrap de 0,6, inferior al umbral establecido. Estos resultados muestran el predominio de una bacteria del grupo Anae-rolineaceae; no incluida en la base de datos del RDP. Para confirmar este hallazgo, se decidió hacer una librería en plásmidos de amplicones del i6s-TRNA, usando los oligo-nucleótidos 27F y una versión modificada del 1492R que favoreciera la hibridación en Anaerolineaceae (ver materiales y métodos). Al ser el organismo dominante, esperábamos que el I6s-TRNA de Anaerolineaceae estuviera abundantemente representado. De 5 clones secuenciados, 3 correspondían a la Anaerolineaceae detectada con ambas regiones variables. Mas aún, el alineamiento de la secuencia depurada por el AMPLICONNOISE para los respectivos OTU V1-V3 y v6-v9, mostró un 100 % de similitud a nivel de nucleótidos, confirmado la concordancia de los datos. Para determinar la posición taxonómica de este OTU se utilizó la nueva secuencia del gen i6s-trna y secuencias homólogas de especies de referencia de esta familia que tuvieran genoma de referencia. Se usaron: Levilinea, Anaerolinea, Longilinea, Leptolinea, Bellilinea, Flexilinea, Ornatilinea, Thermanaerothrix y un aislado ambiental del taxón Anaerolineaceae denominado 46_22. Los resultados del análisis filogenético (Figura 3) agrupan las Anaerolineaceas de la PTAR San Fernando y la ambiental 46_22. Sin embargo, la distancia filogenética entre ambas Anaerolineacea es superior (0,091) a la observada entre los géneros Belilinea y Levilinea, 0,061, que son los que muestran una menor distancia.
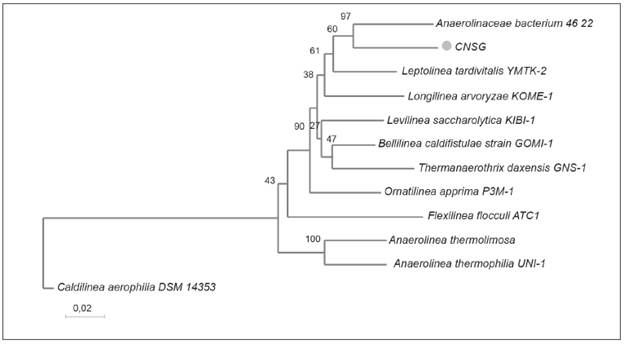
Relaciones evolutivas entre las secuencias del gen 16S rRNA de la Anaerolineaceae de la PTAR San Fernando (siglas CNSG en el árbol), Itagüí, con los genes homólogos de las especies descritas para esta misma Familia y que tiene genoma de referencia en el GenBank. Árbol construido utilizando el método de Neighbor-Joining, con 1000 replicas de bootstrap. Los números en la base de las ramas del árbol corresponde a los valores calculados de bootstrap.
Figura 3 Árbol Filogenético de la Anaerolineaceae no clasificable en categoría genero
Presencia de enterobacterias y géneros patógenos Con la región variable v6-v9 se lograron detectar bacterias de la Familia Enterobacteriaceae, comúnmente conocidas como enterobacterias. Los géneros encontrados fueron Morganella, Providencia y Proteus. Sin embargo, se encontró que estos géneros se vieron representados con pocas lecturas, entre 9 y 42.
En el caso de géneros con especies patógenas, se lograron detectar 11 entre ambas regiones estudiadas, los cuales incluyeron a: Pseudomonas, Mycobacterium, Neisseria, Bordetella, Corynebacterium, Streptococcus, Treponema, Bacillus, Proteus, Enterococcus y Campylobacter. Es importante resaltar la preponderancia del género Pseudomonas, el cual fue el más abundante en la región v6-v9 y el noveno en la región V1-V3. El género Mycobacterium estuvo representado por 350 y 79 lecturas en las regiones V1-V3 y v6-v9, respectivamente. Los demás géneros con especies patógenas estuvieron poco representados, con un número de lecturas que como máximo llegaron a 30; coincidiendo con lo observado en los métodos de cultivo donde se ve una baja proporción de enterobacterias. No se detectaron los géneros Salmonella, Escherichia o Shigella.
DISCUSIÓN
Los sistemas de tratamiento de aguas residuales permiten reducir o eliminar patógenos bacterianos, virales, fúngicos o parásitos que vienen en las excretas de humanos y animales. Estos sistemas de tratamiento producen toneladas diarias de biosólido rico en microorganismos que, si el sistema funciona adecuadamente, pueden ser de carácter inocuo para la salud humana y el ambiente. Estos sistemas deben ser estudiados y monitoreados para evaluar la efectividad del tratamiento anaerobio y verificar la reducción o eliminación de la carga de patógenos para así mitigar el riesgo en la salud pública. En este trabajo nos concentramos en usar las tecnologías NGS para caracterizar la microbiota de estos lodos y así generar información que permita evaluar el riesgo que tienen este material al ser vertido en el ambiente.
Se han publicado investigaciones que describen las comunidades microbianas presentes en lodos activados, reactores anaerobios y biosólidos que son generados en PTAR de diferentes países 11,19. En Latinoamérica no hay a la fecha, en literatura científica pública, estudios sobre la composición bacteriana de los biosólidos generados en las PTAR existentes en la región. Nuestra investigación es de gran valor por la novedad para Colombia y la subregión, ya que por primera vez se describen en detalle los grupos taxonómicos presentes en este subproducto, gracias al uso de métodos de secuenciamiento profundo de las regiones V1-V3 y v6-v9 del i6s.trna. Nuestros resultados estiman un número mínimo de especies bacterianas cercano a 400.
Un total de 163 géneros fueron clasificados usando los resultados de las regiones variables V1-V3 y v6-v9 y cerca de la mitad de los OTUS solo se asignó hasta familia. Este resultado es similar a lo observado por Zhang y colaboradores quienes, en lodos activados, encontraron que entre el 50 % y el 60 % de las secuencias no se clasificaron a nivel de género 11. En esta misma investigación se estudiaron los lodos activados de países como China, Singapur, Estados Unidos y Canadá y se encontró que los Phyla más representativos son Proteobacteria, Bacteroidetes, Firmicutes y Actinobacteria 11. Estos 4 Phyla también están presentes en el biosólido estudiado en esta investigación, sin embargo, nuestros resultados muestran al Phylum Cloroflexi dentro de los más abundantes. Esto es esperable, dado que este Phylum agrupa géneros bacterianos presentes en ambientes anaerobios, en los cuales tienen una participación importante fermentando mono-sacáridos, péptidos y aminoácidos 20.
En este trabajo se encontró a Pseudomonas, Dysgonomonas y Anaerolineaceae como organismos dominantes. Dysgonomonas fue inicialmente descrito en el año 2000 y ha sido aislada de muestras clínicas humanas o incluso del intestino de termitas. Al día de hoy no se ha confirmado su potencial patogénico y sus características metabólicas han sido poco descritas 21-23.
El OTU más dominante según los resultados de la región variable V1-V3 solo logró ser asignado hasta Anaerolineaceae. Este mismo OTU en la región v6-v9 fue el segundo en abundancia a nivel de Familia y tampoco pudo ser clasificado a género. Los resultados filogenéticos obtenidos con el 16s-rRNA completo confirmaron su asignación dentro de Anaerolineaceae pero por fuera de los géneros de referencia, ya que la distancia filogenética calculada excede las observadas entre los organismo de referencia. Estos resultados muestran no solo que la Anaerolineaceae de la PTAR San Fernando es una especie no descrita, sino que puede tratarse de un nuevo género. Es importante mencionar que al hacer una comparación del gen 16S-TRNA de la Anaerolineaceae de la PTAR San Fernando por BLASTN contra la base de datos nr/nt del NCBI, aparecen secuencias con un 99 % de identidad de clones de estudio metagenómicos de lodos activados y digestores productores de biogás en Europa. Sin embargo, algunos de estos estudios no fueron publicados o en las publicaciones no hay análisis de la Anaerolineaceae observada 24.
Otro de los géneros reportados en el presente estudio es Coprothermobacter, una bacteria que ha sido aislada a partir de reactores anaerobios de tratamiento de residuos de curtimbres y que ha llamado la atención por sus propiedades proteolíticas. Adicionalmente, participa como productora de hidrógeno, el cual es importante para la formación de metano por las arqueas metanogénicas hidrogenotrópicas 25.
La riqueza de géneros potencialmente patógenos fue reducida, se encontraron 11, dentro de los que destacaron por su abundancia Pseudomonas y Mycobacterium. Los demás estuvieron en baja proporción, con una cantidad de lecturas igual o inferior a 30.
Estudios previos en este biosólido mostraron presencia de Salmonella y fluctuación en las enterobacterias a lo largo del año 13. En la muestra que analizamos en este trabajo se detectaron bajas cargas de enterobacterias, tanto en el secuenciamiento masivo como en técnicas de cultivo. En el caso de Salmonella, no fue detectada por ninguna de las técnicas usadas. Las causas que modulan este fenómeno aun se desconocen, pero se sospecha pueden estar asociadas con el desempeño de los microorganismos que estabilizan la materia orgánica en el tratamiento de la PTAR.
Pseudomonas fue el género potencialmente patógeno dominante representado con casi 11 000 lecturas acumuladas entre las dos regiones variables. Este taxón contiene varias especies patógenas, pero también es importante resaltar que este es uno de los géneros bacterianos más ubicuos, con un espectro de distribución que va desde los trópicos hasta la Antártida y que ha sido aislado de aguas, suelos y muestras tanto ambientales como clínicas 26. La abundancia de Pseudomonas en el biosólido puede explicarse por su gran capacidad para resistir ambientes agresivos y, a pesar de ser aerobia, por su capacidad para proliferar en ambientes anaerobios usado el no3 como aceptor de electrones 26.
Desde el punto de vista de la salud pública, los resultados de esta investigación muestran que el tratamiento de aguas residuales en la PTAR San Fernando esta siendo efectivo, ya que el biosólido estudiado presenta una concentración alta de microrganismos ambientales, muchos de ellos anaerobios, y la carga de patógenos como Salmonella y E. coli/Shigella es indetectable. La única bacteria potencialmente patógena detectada en concentración significativas fue Pseudomonas, pero no está incluida en la norma nacional que controla estos lodos. Es de resaltar que este proceso de fermentación microbiana es muy sensible a cambios ambientales y contaminantes químicos industriales y por esta razón debe hacerse un monitoreo constante de la composición microbiana de estos lodos antes de ser vertidos en el ambiente *














