La organización mundial de la salud (OMS) declaró la lepra como problema de salud pública a nivel mundial en el año 1991 y creó estrategias para su eliminación para el año 2000, lo que se definió como menos de 1 caso por 10 000 habitantes lo cual significa reducción de la prevalencia de la enfermedad mas no la erradicación; la nueva tasa de prevalencia mundial fue de 0,29 por 10 000 habitantes y la incidencia mundial fue de 3,2 casos por 100 000 habitantes. En Colombia la enfermedad comprende una tasa de incidencia menor a 0,1 por cada 100 000 habitantes desde el año 2008 a la fecha 1,2.
La lepra ahora denominada enfermedad de Hansen es causada por el Mycobacterium Leprae y Mycobacterium Lepromatosis 3. El bacilo ingresa por vías aéreas superiores o por pequeñas abrasiones de la piel 1. El periodo de incubación es prolongado.
El diagnóstico de la lepra es clínico, todo paciente sintomático de piel o de sistema nervioso periférico con factores de riesgo puede ser un paciente con enfermedad de Hansen 1-4.
En el 2010 la OMS estableció nueve países en tres continentes (Colombia, Brasil, china, Pakistán, India, Myanmar, filipinas, Vietnam, Yemen), países centinelas responsables del seguimiento de resistencia antimicrobiana (RAM) 5.En un último reporte en Colombia llevado a cabo en 14 Departamentos (Amazonas, Antioquia, Atlántico, Bolívar, Caquetá, Cesar, Chocó, Cundinamarca, Huila, Magdalena, Norte de Santander, Santander, Tolima y Valle) se encuentran mutaciones del gen folP, rpoB responsables de la resistencia para rifampicina y dapsona y en los genes gyrA y gyrB para fluoroquinolonas; encontrando que la resistencia tiene asociación con las zonas donde hay gran concentración de pacientes con la enfermedad dentro de ellos albergues de contratación (Santander) y albergues de agua de dios (Cundinamarca) 6. Las bases moleculares han llevado a los estudios del genoma del Mycobacterium leprae, el mapeo por la OMS en el 2009 igualmente ha evidenciado sitios de mutaciones iguales que confieren RAM a la PQT 7-9.
Se reporta el caso de un paciente masculino de 41 años de edad, procedente de Argelia, Cauca, residente actual en Agua de Dios Cundinamarca (albergue Boyacá).
Inicia sus primeros síntomas representativos en su segunda década de vida dados por lesiones cutáneas de larga evolución que no respondían a tratamientos tópicos múltiples. Lesiones cutáneas relacionadas con placas y pápulas eritematosas que fueron generando sensación de hipoestesia, alopecia y anhidrosis en extremidades y tronco, además pápulas que fueron evolucionando a nódulos generalizados. Adicionalmente presentaba dolor en trayecto de tronco nervioso cubital bilateral. Paciente quien entonces no consultó.
A los 34 años de edad presentó empeoramiento de su condición clínica con madarosis, ausencia de pestañas, rinorrea sero-sanguinolenta seguida de epifora constante, lesiones cutáneas que fueron aumentando en número y extensión. En extremidades superiores e inferiores alteraciones sensitivas sin captación ante estimulo doloroso, pérdida de fuerza en manos, deformidades osteoarticulares.
Antecedente familiar de primera línea de consanguinidad de enfermedad de Hansen (madre), quien recibió monoterapia con dapsona, mantuvo convivencia estrecha previo a tratamiento, actualmente madre con dato de fallecimiento por patología no relacionada.
Es valorado por primera vez en el Sanatorio Agua de Dios Cundinamarca. Al examen físico se evidenció facies leoninas, lesiones cicatriciales difusas de características hipercromicas, madarosis, ausencia de pestañas, no se encuentra alteración en cámara anterior del globo ocular, perforación del septum con colapso del dorso nasal, pabellón auricular con nódulos eucromicos múltiples con elongación del lóbulo de las orejas. Lesiones dermatoneurológicas en extremidades y tronco dadas por nódulos múltiples difusos de bordes regulares, algunas placas eritematosas sin anhidrosis y sin alopecia, engrosamiento de tronco nervioso cubital radial y mediano no dolorosos a la palpación con alteraciones sensitivo-motoras relacionadas; en manos reabsorción ósea con conservación del lecho ungueal, manos en garra con pérdida de fuerza con vencimiento escaso de gravedad y sin vencer resistencia, amiotrofia tenar e hipotenar , zonas cicatriciales por quemaduras previas (Figuras 1, 2).
Se realizó diagnostico presuntivo de lepra hacia el polo lepromatoso por clínica y se indican apoyos paraclínicos confirmatorios como:
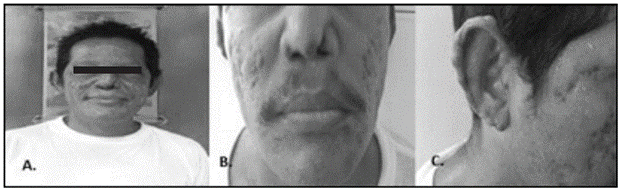
Figura 1 A-B En rostro: madarosis, múltiples cicatrices hiperpigmentadas atróficas residuales, nariz en silla de montar, colapso pirámide nasal; C. Pabellones auriculares: múltiples pápulas y nódulos eucrómicos, firmes e infiltrados de apariencia queloidea
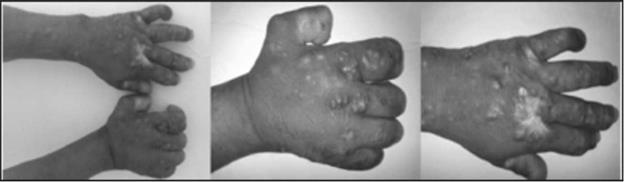
Figura 2 Lepromas múltiples, secuelas cicatriciales por alteración sensitiva, compromiso del nervio cubital radial y mediano - mano péndula - mano en garra
1. Baciloscopia de moco nasal y líquido intersticial con reporte de datos con escala semicuantitativa Colombiana.
- Baciloscopia inicial con índice bacilar (IB) de 2,2 sin estudios de morfología, se confirma diagnostico bacteriológico de lepra multibacilar.
2. Biopsia de piel con técnica incisional.
- Histopatología: reportó epidermis adelgazada ortoqueratósica separada por amplia banda colágena de infiltrado dérmico difuso, extenso, constituido por células fusiformes incluidas en colágeno denso con algunos macrófagos de citoplasma vacuolado. Con la coloración de Fite-Faraco se ven algunos bacilos y formas granulosas. No se ven nervios. Diagnostico concluyen-te de lepra lepromatosa Histioide. Se inició tratamiento con PQT multibacilar adulto (ri-fampicina 600 mg una vez al mes, dapsona 100 mg diarios y clofazimina 300 mg una vez al mes y 50 mg diarios) con esquema de 24 meses sin interrupción según establecía en ese tiempo la OMS, con supervisión de medicamentos suministrados en el albergue Boyacá. A los 24 meses paciente sin mejoría clínica, persistencia y aumento de lesiones cutáneas, poli-neuropatía con alteración sensitivo-motora creciente. Controles bacteriológicos con evidencia del aumento del índice bacilar y test de viabilidad morfológica con alto porcentaje de bacilos sólidos.
- A los seis meses en tratamiento con PQT MB adulto IB de 2,6 con estudio morfológico con 90 % sólidos y 10 % fragmentados.
- A los 11 meses en tratamiento con PQT MB adulto con IB: 0,4.
- A los 24 meses en tratamiento PQT MB adulto según esquema para época por 24 meses con IB: 2,4. Dado empeoramiento de manifestaciones clínicas dermato-neurológicas y asociación bacteriológica con viabilidad bacilar se inician estudios de resistencia.
3. Estudios de resistencia, prueba de sensibilidad genotípica de Mycobacterium leprae, Método, Genotype Leprae-DR. Identificación mediante genética molecular y de sus mutaciones de los genes rpoB, gyrA y folpi. índice bacilar evaluado 1,3; se obtiene notificación que reporta que no hubo amplificación de ADN a partir de la muestra procesada, la prueba requiere un índice bacilar superior a 2.5.
DISCUSIÓN
Se tomó como referencia el caso clínico de un paciente albergado (Albergue Boyacá); paciente con noción probable de contagio familiar, haciendo hipótesis que la madre bacilifera sumada la convivencia estrecha le pudo desencadenar la enfermedad. Posteriormente se presentan manifestaciones clínicas que se fueron desarrollando concordantes con el curso inmunológico contra la Mycobacteria.
La clínica, los estudios bacteriológicos, los estudios histopatológicos y estudios biomoleculares para el seguimiento y comportamiento del antimicrobiano contra la Mycobacteria son indispensables para establecer y evaluar resistencia 11. Sin embargo, el criterio clínico en este paciente fue decisivo para idear planes de terapia alterna. Los criterios paraclínicos son operadores dependientes su toma y lectura debe hacerse por profesionales capacitados, su seguimiento idealmente por un mismo operador, la zona de toma de muestras idealmente la más representativa.
En los estudios bacteriológicos del paciente la escala semicuantitativa colombiana fue un obstáculo por ser una escala no homologable a nivel mundial, la escala logarítmica de Ridley y Jopling se debe implementar a nivel nacional. La toma de muestra de moco no se usa para seguimiento bacteriológico. El índice morfológico se recomienda para evaluar muerte bacilar 4.
Los estudios histopatológicos base fundamental y mucho más específica para evaluar comportamiento bacilar es indispensable en todos los casos de lepra 1.
Los estudios biomoleculares son patrones paraclínicos específicos y sensibles sin embargo, requiere de un índice bacilar alto para amplificación de ADN (IB +2 por Ridley y Jopling), además solo amplifica dos de los tres medicamentos antimicrobianos de la PQT (Rifampicina y Dapsona) 10-12. En este paciente se encuentra un índice bacilar inferior al sugerido por parte de la OMS y el Instituto Nacional de Salud para estudios biomoleculares por este motivo esta herramienta diagnostica no dio ningún dato para corroborar diagnóstico de resistencia. Los estudios biomoleculares son herramientas que no brindan oportunidad de acceso en Colombia por lo que limita su solicitud.
En este paciente se encuentran criterios de resistencia a favor y en contra: A favor:
Persistencia de lesiones e in crescendo en piel y/o SNP durante la PQT MB.
BAAR viables e in crescendo 2+ en escala semicuantitativa colombiana, a los 24 meses IB: 2,4.
Índice morfológico a los 6 meses con bacilos sólidos. En contra:
No se practica cultivo en almohadilla plantar de ratón.
Baciloscopias con muestra de moco que impiden datos objetivos bacilares.
Baciloscopia a los 11 meses con disminución inespecífica del IB.
Baciloscopia en escala semicuantitativa Colombiana.
No se continuo test de viabilidad morfológica en los otros reportes baciloscopicos con PQT convencional.
No se hizo otros estudios de viabilidad.
Índice bacilar detectado de posible lesión "no representativa" que no amplifica genes por PCR.
En conclusión la enfermedad de Hansen sigue siendo de gran interés en salud pública; en Colombia con reconocí-miento internacional como país centinela en resistencia a la PQT responsable de contribuir con la eliminación y finalmente la erradicación de la enfermedad. Las estadísticas nacionales indican cumplimiento de metas de eliminación. Sin embargo, cabe pensar que pudiesen existir subregistros de diagnóstico por desconocimiento de la enfermedad en el personal de salud y en la población general; no obstante los casos de resistencia demuestran trasmisión activa y posiblemente aumento de la incidencia de la enfermedad; su periodo de incubación hace lento el proceso de detección. Por lo tanto es importante reconocer si realmente nos estamos acercando a la erradicación de la enfermedad o simplemente nos estamos alejando de la eliminación. Existe poca literatura médica sobre resistencia a la PQT en pacientes con enfermedad de Hansen, el reconocer estos casos le brinda al personal de salud la importancia de conocer la enfermedad y la existencia de la misma, así mismo ayuda a abrir espacios de discusión sobre la enfermedad y la importancia actual de la resistencia a la PQT, sin dejar atrás aquellos pacientes que aún siguen sufriendo el cataclismo de llevar bajo su espalda una enfermedad que puede ser discapacitante y aquellos que llevan la enfermedad aun latente •














