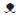La leishmaniasis visceral es una enfermedad causada por una variedad de especies de Leishmania donovani y Leishmania infantum, protozoos intracelulares del orden kinetoplastida; la infección se adquiere a través de la picadura del vector hembra del género flebotomus en el viejo mundo y lutzomya en el nuevo mundo 1,2. El cuadro clínico depende de: determinantes genéticos, la respuesta inmune, estado nutricional del huésped y de factores ambientales 3. En los niños se manifiesta con fiebre prolongada, hepatoesplenomegalia, y leucopenia; facilitando infecciones bacterianas recurrentes y trombocitopenia severa que se ha asociado con un aumento de la mortalidad. Es una enfermedad de progresión lenta que sin tratamiento puede ser mortal 4.
En el mundo 200 millones de personas, distribuidas en 70 países de los cinco continentes, están en riesgo de adquirir la enfermedad 5. Brasil es el país latinoamericano con mayor carga de enfermedad, el reporte de la Organización Mundial de la Salud (OMS) es de 3 481 casos por año en el periodo de 2004 hasta el 2008 6. Durante este mismo periodo Colombia alcanzó un reporte de 60 casos por año, ocupando el segundo lugar en latinoamérica 7. Los casos de leishmaniasis visceral se describen desde México hasta Argentina 8,9. En Colombia se concentran en los departamentos de Córdoba, Sucre, Bolívar, Tolima y Huila 10.
Los vectores de la leishmaniasis corresponden al género Lutzomyia. Se demuestra su presencia desde el nivel del mar hasta los 3 500 metros sobre el nivel del mar (msnm), Los hábitos y la bionomía del vector son las determinantes de la dinámica de la transmisión 11.
La leishmaniasis es una zoonosis de las zonas rurales tropicales, sin embargo las constantes incursiones del hombre al nicho ecológico de los vectores, involucrándose como hospederos y la adaptación de algunas especies a los nuevos hábitats, han condicionado un cambio en la incidencia de la patología 6,8. En Colombia se ha documentado el impacto de estos cambios con la presencia de casos aislados en zonas urbanas de Cartagena 12. En el presente trabajo se describe el primer brote de leishmania-sis urbana en Neiva, capital del departamento del Huila; localizada entre las Cordillera Central y Oriental; cruzada por los ríos Las Ceibas, del Oro y Magdalena. Se encuentra a 442 msnm y tiene una humedad relativa del 66%.
A nivel mundial se han considerado las sales antimoniales como el tratamiento de primera línea. Sin embargo, en India se observó un aumento dramático en la falla terapéutica hasta del 65% de los casos 13; estos hallazgos también se han encontrado en otros estudios y han llevado al cambio de los esquemas de tratamiento.
METODOLOGÍA
Se realizó un estudio descriptivo de casos con diagnóstico de leshmaniasis visceral en niños menores de cinco años, procedentes de la zona urbana de Neiva, durante el brote presentado desde el mes de abril hasta el mes de junio de 2012. Se revisaron las historias clínicas de los pacientes y la información fue recolectada en un instrumento previamente diseñado. La estadística utilizada es descriptiva, con análisis univariado. Los datos fueron relacionados en el programa Excel 2010. Los resultados se presentarán en tablas y gráficas.
El estudio fue aprobado por el comité de bioética en investigación del Hospital Universitario de Neiva.
Los casos fueron notificados a la entidad municipal y departamental de Salud Pública, quienes realizaron visitas a los domicilios, e iniciaron búsqueda activa de los vectores, reservorios y nuevos casos.
Para la localización de los vectores, se utilizaron trampa CDC (luz y ventilación), en un total de 100, las cuales fueron ubicadas en las viviendas localizadas hasta 300 metros del caso índice, instaladas intra, peri y extradomicilio durante tres noches continuas y se lograron capturar Lutzomias en todas las comunas.
Para la búsqueda de los reservorios fueron evaluados muestra de sangre de los caninos que habitaban hasta 200 metros alrededor de la vivienda de cada caso índice.
RESULTADOS
En la ciudad de Neiva, durante los meses de abril a junio del año 2012, se presentó un brote de leishmaniasis visceral con siete casos. Los niños eran menores de cinco años, cinco de género femenino, sin antecedentes de desplazamientos. Solo un paciente presento desnutrición.
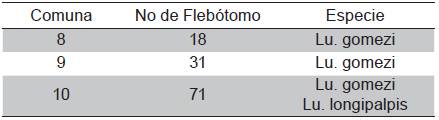
La presentación clínica más frecuente fue el síndrome febril prolongado y hepato-esplenomegalia Todos los pacientes al momento del ingreso tenían un marcado compromiso hematológico; la característica común fue anemia severa y marcada leucopenia con neutropenia severa (Tabla 1).
Tabla 1 Características clínicas y paraclínicas de los pacientes
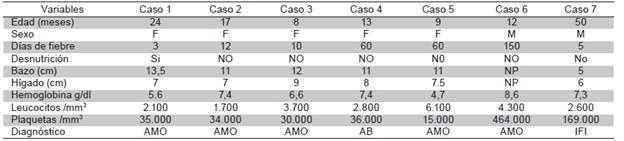
g/dl: gramos/decilitros cm: centímetros x-mm3 : por milímetros , AMO: Aspiración Medula de Ósea. AB: Aspirado de bazo. cm: centímetros. NP: No palpable, F: Femenino, M: Masculino
Dentro de los marcadores bioquímicos, se encontró una disminución de los niveles séricos de albúmina e hipergammaglobulinemia, ningún paciente presentó elevación de transaminasas ni de bilirrubinas.
El diagnóstico en cinco pacientes se realizó durante los primeros cinco días de su estancia hospitalaria con aspirado de médula ósea. En el sexto caso se confirmó el diagnóstico por aspirado de bazo. El último de los casos se detectó por búsqueda activa con serología por IFI de 1/128.
El tratamiento en seis pacientes fue con miltefosine inicialmente, cinco presentaron fracaso terapéutico, por lo que se escalonó a anfotericina B; dos niños recibieron tratamiento exitoso con anfotericina B liposomal y tres con anfotericina de-oxicolato. El último paciente del presente brote ingresó a una clínica privada de la ciudad y recibió tratamiento con glucantime con respuesta clínica favorable.
Durante la hospitalización un paciente presentó síndrome hemofagocítico como complicación y recibió ciclo corto de esteroides con resolución del cuadro.
Las viviendas de los pacientes se encuentran ubicadas en cinco asentamientos urbanos de las comunas: 8, 9 y 10, sobre las riberas de los ríos Las Ceibas, Río del Oro y Magdalena; rodeadas de árboles, arbustos y gallineros.
Todas las comunas presentaban características geográficas y culturales similares; con índice de pobreza alto, vivienda con piso de tierra, techo en zinc, paredes de madera y ladrillo. No cuentan con servicios públicos básicos (alcantarillado, acueducto, recolección de basuras).
Para el estudio entomológico, se realizó muestreo con trampas CDC (luz y ventilación), las cuales funcionan entre las 6 p.m. a 6 a.m. Estas fueron instaladas en el intra, peri y extradomicilio de los casos índices durante tres noches continuas, y se lograron capturan lutzomias en todas las comunas (Tabla 2).
En las visitas domiciliares realizadas por los entes de salud pública, se documentaron reservorios caninos del parásito, dentro de las viviendas, y en las zonas alrededor de las mismas. A todos los perros identificados se les tomó una muestra sanguínea para serología. En total se recogieron 33 muestras de las cuales fueron positivas 21.
DISCUSIÓN
La leishmaniasis visceral, es una enfermedad de importancia en salud pública, con incremento de casos en áreas suburbanas. Los factores determinantes y tradicionalmente conocidos de la transmisión de leishmaniasis son las relaciones que el hombre establece con el medio ambiente; la deforestación y la presencia de nuevos asentamientos humanos con modificaciones al ambiente que permiten la adaptación de vectores y reservorios de la enfermedad a nuevos hábitat 10. En la ciudad de Neiva se evidencia estos factores, una situación similar a la presentada en Brasil donde se han aumento los casos de leishmaniasis visceral por la urbanización no planificada 14.
En este brote la población afectada fue la pediátrica, concordante con lo descrito en estudios de Paraguay, España, Brasil y Colombia, 10,15,16. Se ha demostrado que en los lactantes existe un aumento de la actividad Th2 con niveles de IFN bajos y aumento de IL-10 16.
Se ha identificado como factor de riesgo la desnutrición. Sin embargo, el compromiso del estado nutricional se debe interpretar cuidadosamente porque puede ser causa y/o consecuencia de una enfermedad crónica que en muchos casos se asocia a infecciones de origen bacteriano; como neumonía y diarrea 17. En el brote aquí descrito, la desnutrición solo se documentó en un caso, lo cual supone que en este grupo hay otros factores más importantes relacionados con el ambiente que facilitan la transmisión.
En estudios previos se han establecido factores de riesgo para mortalidad como: trombocitopenia menor a 50 000 con (OR 11,7; IC 5,4-25,1), leucopenia menor a 2 500 (OR 3.1; IC 1.4-6.9), dificultad respiratoria (OR 2.8; IC 2.8- 6.1), coinfección bacteriana (OR 2.7; IC 1,2 - 6,1) e hipoalbuminemia (OR: 7; IC 1-27) 8,19,20. En nuestros pacientes todos presentaron hipoalbuminemia; cinco pacientes cursaron con trombocitopenia menor a 50 000, sin embargo ninguno presentó manifestaciones hemorrágicas; dos pacientes presentaron leucopenia severa con recuentos de leucocitos menores a los 2 500, y todos cursaron con coinfección bacteriana; en piel o tracto respiratorio, y recibieron tratamiento antimicrobiano de amplio espectro de forma oportuna. A diferencia de los estudios reportados en Brasil donde el compromiso más severo fue en la función hepática, en nuestros niños el compromiso más marcado fue hematológico. Sin embargo estos no presentaron alteraciones hemodinámicas o signos de bajo gasto debido a los mecanismos compensatorios desarrollados por la cronicidad de la misma. A pesar de los factores de riesgo de mortalidad documentados en los niños afectado 19,20, no se presentó mortalidad en este brote.
El método de confirmación diagnóstico descrito más sensible es el AMO (90%) y el método más específico es el aspirado de bazo (98%). Eso se pudo confirmar con los pacientes de este estudio; cinco niños tuvieron confirmación diagnóstica por demostración parasitológica en aspirado de médula ósea, y solo en uno, donde el estudio de médula ósea fue negativo, el diagnóstico se confirmó con aspirado de bazo. Los métodos serológicos tienen una menor sensibilidad (60%) y especificidad (70%), sin embargo son de utilidad en tiempos de brotes epidémicos, como se vio en el paciente que fue captado por medio de búsqueda activa, después del reporte de los casos a las entidades de salud pública municipal 2,21,22.
Tradicionalmente, el tratamiento de esta patología se ha basado en el uso de los derivados del antimonio. Desde la década de 1980, la anfotericina B deoxicolato se ha utilizado cada vez más en los países de alta prevalencia. Un avance importante en el manejo del paciente con lv fue la introducción del primer tratamiento oral de la miltefosina, sin embargo rápidamente se reportaron casos de falla terapéutica 23. En los últimos años se introdujo la anfotericina B liposomal para el manejo de la lv por su baja toxicidad e igual efectividad, convirtiéndose en el tratamiento de primera elección aprobado por la Agencia de Administración de Alimentos y Medicamentos (FDA) en EE.UU. De igual manera la OMS en sus recomendaciones considera su uso como primera línea en los casos de LV por L. infantum; principal agente causal en nuestro continente 5,24.
En el Hospital Universitario de Neiva, en los últimos diez años se ha encontrado una mala respuesta clínica y parasitológica al tratamiento tradicional con sales antimoniales; lo cual sugiere resistencia del parasito a ese medicamento y por lo cual se ha considerado el tratamiento con miltefosine 25. Sin embargo en el brote aquí descrito se pudo apreciar falla en la respuesta en cinco pacientes, lo que llevó al uso de anfotericina B; siguiendo las recomendaciones de tratamiento de la OMS 5,26. Sin embargo en nuestro medio la anfotericina B liposomal es de difícil acceso por lo cual solo a dos pacientes se les pudo asegurar el tratamiento completo con este medicamento y tres recibieron anfotericina B deoxicolato. Los siete pacientes presentaron recuperación clínica, paraclí-nica y parasitológica. Ninguno ha presentado recaída ni complicaciones durante dos años de seguimiento 4.
Los factores de riesgo para el desarrollo de la infección tales como bajo nivel socioeconómico, edad pediátrica, y hacinamiento, fueron comunes en todos los casos aquí descritos 2.
El principal vector identificado fue la Lutzomyia gomezi, contrario a lo documentado en estudios previos en el país 27, donde se ha reportado como principal vector a la Lutzomyia longipalpis. En Panamá, han encontrado como principal vector a la Lutzomyia gomezi, lo cual concuerda con los hallazgos del presente estudio, sugiriendo que estamos enfrentados a un posible cambio en la epidemiología en nuestra región.
Es el primer brote urbano descrito en Colombia lo cual sugiere un cambio en las condiciones ambientales y un posible incremento vectorial. La vigilancia entomológica y de reservorios debe hacerse de manera constante en zonas endémicas facilitando el control oportuno de situaciones de brote. En la literatura internacional, actualmente la anfotericina B liposomal tratamiento de eleccion por su efectividad, menores efectos secundarios y disminución de estancias hospitalarias, como se asocia en el presente brote