El estado de pandemia a partir de la rápida propagación del COVID-19 constituye una de las principales amenazas que enfrentan los sistemas sanitarios a escala mundial durante las últimas décadas. Esta enfermedad, que puede presentar síntomas de una neumonía atípica severa 1 es causada por un nuevo agente infeccioso denominado SARS-COV-2, que, si bien pertenece a la familia de los coronavirus como MERS-COV y SARS-COV 2, presenta mayores niveles de infectividad 3-5. La COVID-19, desde su descubrimiento en Wuhan 6 se ha extendido a más de 190 países 7 y ha alcanzado tasas de propagación exponenciales 1,8-10. Esta situación ha generado un incremento en la tensión sobre la capacidad de los sistemas sanitarios, hecho que puede conducir a un aumento de la tasa de mortalidad por el eventual colapso de las unidades de cuidado intensivo (UCI) o por una saturación del personal de salud 8,11-14.
La evidencia disponible indica que, del total de contagiados, un 5% va a necesitar ventilación artificial en UCI 15-17, cifra que pone en evidencia cómo el número de camas y respiradores artificiales convierte en un cuello de botella la capacidad de atención, hecho que aumenta la letalidad de pacientes como consecuencia de la saturación del sistema sanitario 8,11-14. A su vez, a medida que aumenta la razón paciente:personal especializado en UCI se puede incrementar la probabilidad de ocurrencia de infecciones nosocomiales y paros respiratorios, entre otros, que elevan los costos y la incidencia de la mortalidad 18-21. En este sentido resulta imperioso que Colombia, generalmente con menor capacidad sanitaria que otros países 22, adopte medidas rápidas con el propósito de disminuir el contagio y fortalecer la capacidad de atención de los sistemas de salud para evitar el desborde ante el avance de la enfermedad.
En Colombia las autoridades han ido adoptando políticas con el fin de aumentar la capacidad instalada. Para el mes de marzo el sistema sanitario contaba con 5 300 UCI, de las cuales cerca de un 80% se encontraban en uso 23,24. Sin embargo, el Ministerio de Salud y Protección Social anunció a comienzos de abril la compra de 1 510 ventiladores, con los que se amplió la capacidad instalada a 2 570 25. Al mismo tiempo, se anunció un plan contingente que permitirá orientar recursos con el objetivo de incrementar la capacidad de atención de pacientes críticos en fases sucesivas, con el que se podría aumentar la disponibilidad a 5 150 ventiladores (fase Il), a 7 650 (fase m) y hasta un máximo de 9 826 (fase iv) 26. En cuanto a la disponibilidad de personal especializado, el país cuenta con aproximadamente 1 200 médicos intensivistas y 706 terapeutas respiratorios (TR) y fisioterapeutas (FT), según la Asociación Colombiana de Medicina Crítica 24. Finalmente, se han implementado estrategias de distanciamiento social como lo fue el cierre de fronteras, universidades y colegios 27. Al mismo tiempo, a partir del 25 de marzo se decretó confinamiento preventivo por 19 días (hasta el 13 de abril) a nivel nacional 28 y se renovó hasta el 11 de mayo 29. En Bogotá la cuarentena comenzó desde el 20 de marzo.
El objetivo de este artículo es analizar la evolución temporal de la primera etapa del COVID-19 en Colombia a través del modelo SIRD, modificando la tasa de transmisión bajo diferentes escenarios para predecir el número de casos totales, qué cifra representaría el 5% de infectados en UCI, y estimar la demanda de servicios en UCI, con el fin de evaluar la efectividad de las políticas implementadas por las autoridades sanitarias y evitar el colapso del sistema de salud.
MATERIALES Y MÉTODOS
Datos epidemiológicos
Se utilizó como muestra el número de casos positivos con COVID-19 entre el 6 de marzo y el 15 de abril 2020 a nivel nacional. La muestra estuvo representada por 3 105 individuos infectados, de quienes se obtuvo la información correspondiente al sexo, edad, ciudad, fecha de diagnosis, departamento de residencia, tipo de transmisión y estado del paciente.
Para efectos de la modelación se consideró que el número de casos positivos corresponde al total de infectados existentes en la población o que, en su efecto, la diferencia entre ambos permanece constante en el tiempo 30. Adicionalmente, el 26 de marzo del 2020 el Instituto Nacional de Salud presentó problemas con el equipo de extracción de ADN, razón por la cual a partir de esa fecha se realizaron algunas muestras de forma manual, lo que subrepresenta el número de contagiados a partir de esa fecha.
Modelo SIRD
Se utilizó el modelo epidemiológico SIRD 30 en tiempo discreto para evaluar la población de individuos susceptibles (S), infectados (I), resistentes (R) y fallecidos (D) en la población. Se considero que la población total (N) sería la suma de S + I + R + D. Para los ajustes y proyecciones del modelo se empleó el programa R31.
S (t +1 ) = S - bSI/N
I (t +1 ) = I+ bSI/N - gI - dI
R (t +1 ) = R + gI
D (t +1 ) = D + dI
Para la realización del modelo fue necesario ajustar los valores de los parámetros b, g y d que representan la tasa de transmisión entre I y S, la tasa de recuperación de I y la tasa de mortalidad de I, respectivamente. Para ajustar la tasa de recuperación y muerte, se calculó la tasa de cambio diaria, para luego calcular el promedio general y dividirlo entre el número total de casos (Tabla 1).
El parámetro de tasa de transmisión (b) se modeló en función del tiempo siguiendo una caída logarítmica a partir de un parámetro inicial, representando con ello el potencial efecto de las medidas de distanciamiento adoptadas por el gobierno (Figura 1A). Una vez ajustada la curva se proyectaron los valores del modelo SIRD para tres escenarios: cuarentena (20/25 marzo al 1 de junio), cuarentena flexible1 y flexible2 (entre 20 y 25 marzo al 11 mayo), donde la primera tiene un b de 4% y la segunda de 8% (Figura 1B). Para esto se utilizaron dos ecuaciones, la 1) para el escenario de cuarentena y la 2) para los escenarios cuarentena flexible1 y flexible2.
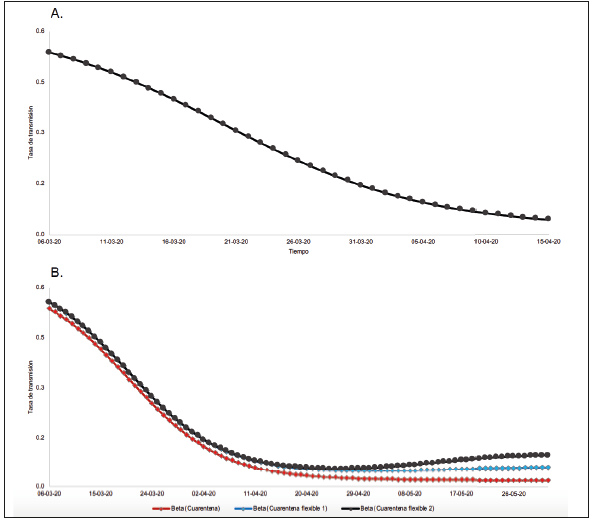
Tasa de transmisión. A. Ajuste de la tasa de transmisión entre el período observado (6 marzo al 15 abril). B. Tasa de transmisión para los escenarios 1) cuarentena del 20-25 marzo al 1 julio con un b 2%, 2) cuarentena flexible! del 20-25 marzo al 11 mayo con un b 4%, y 3) cuarentena flexible2 del 20-25 marzo al 11 mayo con un b 8%
Figura 1 Dinámica de la tasa de transmisión
b = b 2 + (b 0 -b 2 ) * (1 - 1 / (1 + exp (-theta * (t-bt)))) (1)
b = b 2 + (b 0 -b 2 ) * (1-1 / (1 + exp(-theta * (t - bt)))) + (b 3 + (b 2 - b 3 )*(1 -1/(1 + exp (-theta * (t - bt)))) (2)
Donde b 0 (63%) es el nivel inicial del coeficiente de transmisión, b 2 (2%) es la tasa de transmisión en el escenario cuarentena, y b3 tiene dos valores: 4% para el escenario cuarentena flexible1 y 8% para cuarentena flexible2, theta regula la inclinación de la curva cuando existe alguna medida de mitigación donde se disminuye la tasa de transmisión, y t-b es el tiempo de intervención, i.e. el inicio de cuarentena y/o su flexibilización.
Para establecer si el modelo ajustó correctamente a los datos observados, se realizó un coeficiente de predicción (pseudoR2) según los valores de cada ecuación del modelo. Adicionalmente, con las estimaciones de las ecuaciones se simularon las trayectorias del total de los casos con COVID-19 para predecir los casos hasta el 1 de junio. Esta simulación recalculó los casos diarios de acuerdo con los datos de días anteriores y con los parámetros del modelo 32.
Se calculó el 5% de los individuos infectados (restando el número de individuos recuperados y muertos por día) con base en las predicciones arrojadas por el modelo, con el fin de analizar si la capacidad instalada de camas y personal de salud especializado (intensivistas y personal de enfermería) son suficientes para la población infectada en UCI. Para esto se usaron dos estimadores de camas en UCI, cada uno correspondiente a los valores límites de la fase I y III del plan contingente anunciado por el Ministerio de Salud 26: 2 650 y 7 560 camas 15,19,20, y 1 200 intensivistas 24 y 1 424 personal de enfermería especializado en UCI. Para el personal de enfermería utilizamos el valor máximo de suficiencia (según la capacidad instalada) estimado por Pérez y Rodríguez 18. Finalmente, el 5% de individuos infectados se dividió entre el número de camas (2 650, 7 560) y el personal disponible en UCI (1 200 intensivistas y 1 424 enfermeras).
RESULTADOS
En Colombia hubo un total de 3 105 casos de individuos con COVID-19 entre el 6 de marzo y el 15 de abril. Hasta el momento, 153 de las 1 118 ciudades que hay en Colombia presentan casos; la prevalencia se encuentra en Bogotá, con el 41%; Cali, con 14%, y Medellín con el 6%. Así mismo, se cuenta con un total de 29 departamentos de 32 con individuos infectados, en donde Bogotá tiene la mayoría de los casos seguida por Valle del Cauca, Antioquia, Cartagena y Cundinamarca (Figura 2).
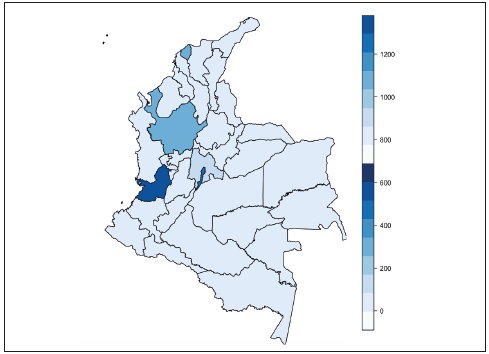
Figura 2 Número de casos infectados con COVID-19 por departamentos. La escala de colores (0 a 400) muestra el número de casos por departamento del 6 de marzo al 15 abril de 2020
Los resultados mostraron que el 67% de los infectados se encuentran en casa, el 11% en el hospital, el 3% en unidades de cuidados intensivos, 14% recuperados y 4% muertos, donde los mayores de 60 años son el 69% de los fallecidos en todo el país. La mayoría de los adultos mayores infectados se encuentran en Bogotá sin necesidad de acudir al servicio médico, ya que el 46% se encuentran en casa; el 21%, en el hospital; el 8%, en UCI; 10% recuperados, y 14%, fallecidos.
La tasa de cambio entre los nuevos casos sobre el total evidenció una disminución en la tasa de transmisión (b) a lo largo del tiempo, lo que muestra la efectividad de las medidas implementadas por el Gobierno. Se observó que en los primeros días (6 al 15 marzo) la tasa de cambio tuvo una gran amplitud, posiblemente debido a la falta de detección de los casos. Pero desde el 16 de marzo el reporte de la dinámica mejoró hasta el 24 de marzo, cuando disminuyó y se estabilizó (Figura 3A). Así mismo, al comparar los valores predichos por el modelo SIRD con los valores reportados, se obtuvieron pseudoR2 de 98% para los casos totales e infectados (restando recuperados y fallecidos). Estos resultados evidencian que los parámetros del modelo se ajustaron de forma precisa con los valores observados, y con esta certeza se realizaron las proyecciones hasta el 1 de junio (Figura 3B).
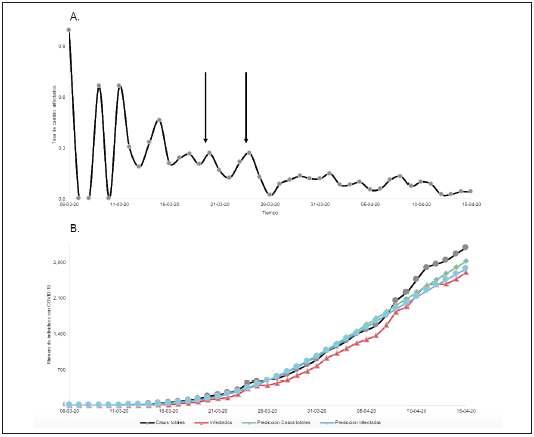
A. Tasa per cápita de cambio (casos nuevos/totales). Las flechas representan los días donde se instauró la cuarentena: 20 marzo para Bogotá y 25 marzo para el resto del país. B. Ajuste matemático del modelo SIRD con casos totales acumulados e infectados y sus respectivas predicciones
Figura 3 Dinámica de la tasa de cambio per cápita diario y ajuste de modelo SIRD
Se evidenció una clara diferencia entre los escenarios, donde la cuarentena (20-25 marzo al 1 junio, b 2%) mostró los menores valores con 5 589 casos totales para el 11 de mayo y 8 239, para el 1 junio. A diferencia de los escenarios cuarentena flexible1 y cuarentena flexible2, cuando se liberaría la cuarentena, el 11 de mayo, de acuerdo con el último comunicado de presidencia. En estos escenarios se evaluaron dos tipos de tasas de transmisión (b): 4% y 8% para analizar una tasa de contagio baja y una más realista, respectivamente. Este último escenario contempla la apertura de sectores como manufactura, construcción y comercial, lo que permite una mayor movilidad de individuos. Siendo así, la cuarentena flexible1 obtendría 18 807 casos totales para el 11 de mayo y 54 105 para el 1 julio, y la cuarentena flexible2, 22 868 para el 11 de mayo y 116 081 para el 1 de junio (Figura 4A).
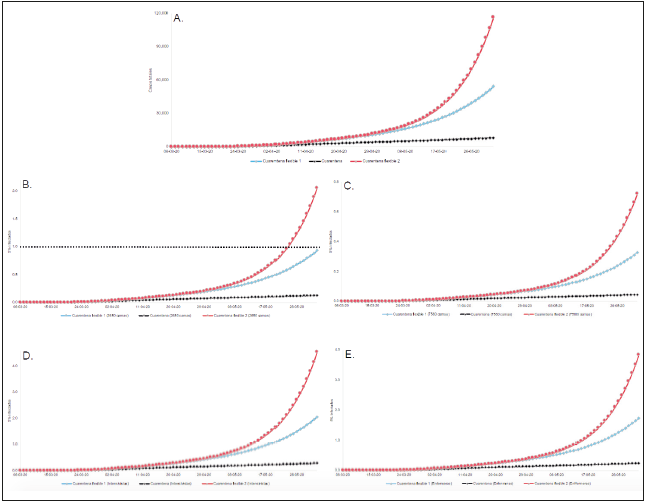
A. Predicciones del modelo SIRD con casos totales de COVID-19 al 1 junio bajo tres escenarios: 1) cuarentena del 20-25 marzo al 1 junio con un b 2%, 2) cuarentena flexible] del 20-25 marzo al 11 mayo con un b 4%, y 3) cuarentena flexible2 del 20-25 marzo al 11 mayo con un b 8%. B. y C. Predicciones del modelo SIRD con 5% infectados de COVID-19 en UCI sobre la disponibilidad de camas (2650 y 7560) bajo los tres escenarios. La línea horizontal punteada evidencia cuando se llega al colapso de las camas. D. y E. Predicciones del modelo SIRD con 5% infectados de COVID-19 en UCI sobre la disponibilidad del personal en UCI (1200 intensivistas y 1424 enfermeras) bajo los tres escenarios
Figura 4 Predicciones del modelo SIRD para los 3 escenarios
Se estimó el 5% de los individuos infectados para establecer los posibles pacientes en UCI, considerando dos capacidades de camas: 2 650 (fase I) y 7 569 (fase m). Los resultados establecieron que, para el escenario de cuarentena, la capacidad de camas (2 650) no llegaría a su tope, ya que para el 11 de mayo y 1 junio se tiene una relación de infectados:camas de 0,1. Para la cuarentena flexible1 la capacidad de camas no es superada al 11 de mayo (0.3), pero estaría muy cerca de saturarse para el 1 de junio (90%). Finalmente, en el escenario de cuarentena flexible2, el número de camas colapsaría el 1 de junio (210%) (Figura 4B). Cabe destacar que el colapso de las 7560 camas no se consigue en los escenarios cuarentena y cuarentena flexible1 (valores entre 0,03 y 0,3), mientras que la cuarentena flexi-ble2 mostró que para 1 junio se alcanzaría un 72% de camas utilizadas (Figura 4C).
Finalmente, al evaluar una posible saturación del personal de salud especializado en UCI, el escenario de cuarentena mostró valores de un intensivistas por cada paciente y una enfermera por paciente en UCI. El escenario cuarentena flexible1 tuvo valores de 1:2,1 para intensivistas y de 1:1,7 para personal de enfermería. El último escenario de cuarentena flexible2 obtuvo valores entre 1:4,5 intensivista:paciente y 1:3,8 para enfermeras en UCI (Figura 4C y D).
DISCUSIÓN
En Colombia las autoridades han aplicado un modelo mixto donde se combinan medidas de mitigación con políticas de supresión 27-29,33-35. De acuerdo con la dinámica observada en nuestros resultados y comparando con algunos estudios previos, existen fuertes indicios para manifestar que la estrategia seguida por las autoridades está teniendo resultados positivos, pues logró una disminución sustancial de la tasa de transmisión. El comportamiento actual de la epidemia en Colombia, a nivel macro, no se ajusta a las proyecciones basadas en escenarios catastróficos 27,34,36,37. González-Jaramillo y colaboradores (2020) proyectaron en un escenario sin medidas de distanciamiento social, el colapso total del sistema sanitario a mediados del mes de abril, ya que para la fecha existirían según sus proyecciones alrededor de 500 mil infectados; esto significa que se requiere un aproximado de 36 782 camas UCI 34. Un resultado similar fue reportado por Amariles y colaboradores (2020) quienes bajo los mismos supuestos proyectaron para comienzos del mes de abril alrededor de 40 535 infectados 36 (alrededor de 2 000 camas UCI). Al mismo tiempo, De Castro 37 usó un modelo SIR y, estimando parámetros a partir de la experiencia de Corea del Sur, predijo, en un escenario sin medidas de control, que la epidemia alcanzaría 44 millones de infectados para comienzos del mes de mayo. A su vez, Manrique-Abril etál.27, ajustando un modelo SIR entre el 6/3 y el 20/3 (cuarentena en Bogotá), obtuvieron un R o cercano a 1,5, valor con el que predijeron alrededor de 696 000 casos positivos para mediados de abril y 20 300 000 para comienzos de mayo.
El fuerte contraste entre las anteriores predicciones y la dinámica de la enfermedad en Colombia es, en gran medida, consecuencia de la tendencia seguida por la variación de la tasa de contagio per cápita la cual en nuestros resultados evidenció una importante caída a partir del 24 de marzo. El comportamiento de esta variable parece sugerir que las medidas de contención han tenido un fuerte impacto en la ralentización de la epidemia, esto como consecuencia del efecto sobre el parámetro b. En efecto, los valores de los casos totales, infectados y nuevos casos predichos a partir de nuestro modelo SIRD, donde b cae siguiendo una ecuación logística, producto de la implementación de políticas de cuarentena, se ajustan de manera efectiva a la dinámica de la epidemia observada en Colombia. En este sentido, y según lo predicho por el modelo, se observa un decrecimiento paulatino de la tasa per cápita de contagio, que varía entre un 56% a comienzos de marzo y alcanza un 4% a mediados del mes de abril. Esta disminución de b podría explicar en gran medida las diferencias observadas entre aquellos escenarios que proyectaban un colapso del sistema sanitario para mediados de abril y la actual disponibilidad de atención en UCI.
A pesar del efecto que han tenido las medidas de distanciamiento en el ritmo de propagación, las autoridades habían anunciado la intención de flexibilizar el estado de cuarentena a partir de mediados de mayo. Esta medida era razonable, dado que la estrategia de supresión extrema es difícil de sostener durante largos períodos de tiempo para economías de ingresos medios o bajos, sobre todo ante un escenario de caída del precio de los productos primarios y una eventual recesión mundial 33,34. Es importante señalar que un escenario de flexibilización implica el riesgo de que si no se cuenta con una estrategia eficiente de detección y aislamiento de los casos positivos (y personas relacionadas), el número de infectados puede aumentar a gran velocidad haciendo inmanejable la situación para los sistemas de salud 18,20,33. Estableciendo esta problemática, se modeló una dinámica SIRD prediciendo valores hasta el 1 junio bajo tres escenarios: "cuarentena", que representa una eventual prorrogación en las medidas de distanciamiento social estrictas (caída continua de la tasa de transmisión hasta alcanzar un valor de 2%), y dos escenarios de "cuarentena flexible", que representan la decisión de distender las actuales restricciones para dar paso a un contexto de distanciamiento social dinámico o "inteligente". En el caso de "flexible/' se simuló un contexto en donde, si bien hay un crecimiento de la tasa de transmisión a partir del 11 de mayo (liberación de cuarentena), la misma se presenta a un ritmo moderado (b3=4%) siendo este escenario análogo a un contexto en donde la capacidad de detección y aislamiento de los casos positivos se da de manera eficiente. En lo que respecta al escenario "flexible2", se simuló una situación donde la tasa de contagio crece a un ritmo más acelerado (b3=8%) como consecuencia de un eventual fallo en las capacidades de detección temprana de casos positivos y en un aislamiento tardío y menos eficaz de las personas contagiadas.
Los resultados muestran cómo en un escenario de "cuarentena" (dado el bajo ritmo de propagación en términos macro y sin considerar las dinámicas locales), el servicio de atención estaría garantizado. Si bien este representa un escenario ideal desde la perspectiva de la atención médica, es un contexto improbable dado el alto costo económico que implica sostener estas medidas durante largo tiempo 33. Por lo tanto, es probable que la dinámica de la epidemia esperada en Colombia a partir del 11 de mayo sea similar a los escenarios de "cuarentena flexible". En este sentido, observamos que, según nuestras estimaciones, para comienzos de junio el sistema sanitario podría empezar a experimentar tensión, ya que para el escenario "flexible1" se esperaría un aproximado de 2 700 pacientes con requerimientos UCI, demanda que estaría cerca de sobrepasar la capacidad de camas instaladas en la fase I 26.
Al mismo tiempo, la razón intensivista:paciente es de 1:2, lejos de la razón reportada como ideal (1:8 o 1:10). En el caso del servicio de enfermería, este radio alcanzaría un valor cercano a 1:1,7 aproximándose al 50% de la relación ideal (1:3) 18,24. Este panorama de tensión se hace más evidente en el caso de las proyecciones realizadas en el escenario "flexible2", en donde la demanda de camas UCI para comienzos de junio alcanza valores cercanos a 5804 pacientes, rebasando completamente la capacidad instalada de la fase II del plan contingente del Gobierno, alcanzando una ocupación cercana del 72% del límite de la fase III 26. Al mismo tiempo, la razón personal de enfermería: paciente sobrepasa el valor crítico, siendo esta de 1:3,8, mientras que la de intensivista:paciente alcanza la relación 1:4,5.
El panorama con respecto a las proyecciones de los escenarios "cuarentena flexible" muestra la necesidad por parte del Gobierno y de las autoridades sanitarias de disponer de recursos suficientes en el corto plazo para ampliar las capacidades del sistema sanitario en cuanto a la atención en UCI. Al considerar que en nuestros escenarios hicimos la simplificación de considerar que todo el stock de camas UCI, así como el 100% del personal especializado está dispuesto de manera exclusiva para la atención de la contingencia, lo que constituye una clara sobreestimación. Solo a comienzos de marzo, la ocupación de los espacios de UCI era cercano al 80% 22-24, lo que es indicativo de la alta preexistencia de condiciones epidemiológicas que requieren de una importante utilización de estos servicios de salud.
A futuro se vislumbran algunos escenarios que podrían incrementar la demanda de atención e instalaciones especializadas, ya que para los meses de mayo y junio aumentaría el número de personas que requiere atención, producto de enfermedades respiratorias habituales 36. Además, en los primeros meses del año se registró un número atípico de personas con dengue 38. Ambas situaciones podrían afectar la disponibilidad de camas, la incidencia de comorbilidades y la saturación del personal especializado. Por tanto, una posible coocurrencia de brotes de enfermedades hace más imperiosa la necesidad de aumentar en el corto plazo la capacidad del sistema sanitario. Así mismo, se debe hacer énfasis en el incremento de la tensión sobre el personal de salud en UCI, sobre todo en lo que respecta al escenario "cuarentena flexible2". Las autoridades sanitarias cuentan con un plan de ampliación de la capacidad de camas UCI instaladas, la cual podría incrementarse hasta un límite de 9 826 camas 26. Sin embargo, la disponibilidad de condiciones óptimas para el buen desempeño del personal en UCI impone restricciones que podrían ser inelásticas. Existen estudios que apuntan a la potencial ocurrencia de una sobrecarga del personal de salud especializado en UCI, donde, a razones mayores a 1:8 o 1:10 intensivista:paciente y 1:3 para el personal de enfermería, aumenta la probabilidad de ocurrencia de infecciones nosocomiales, paros respiratorios, entre otros eventos que podrían incrementar la mortalidad 18-21. Por ello, algunas investigaciones sugieren que actualmente no se dispone de todo el personal especializado para cubrir toda la capacidad instalada 18, donde se reporta que la relación paciente:personal de enfermería en UCI podría alcanzar razones de 1:6 pacientes: enfermera 20,21. Por todo lo anterior, resulta necesario desarrollar planes que permitan que el personal UCI cuente con todos los insumos para protegerse de una posible infección, ya que experiencias como la italiana o la china muestran que alrededor del 20% del personal posiblemente contraerá COVID-19 39.
Es importante que las medidas que adopten las autoridades sanitarias con el propósito de mitigar y contener la epidemia sigan nociones similares al principio precautorio. En este sentido, es relevante que se consideren de manera integral todas las capacidades y límites del sistema sanitario del país. Según nuestros resultados, si bien el Gobierno colombiano ha adoptado medidas efectivas para disminuir el ritmo de propagación de la enfermedad, es importante redoblar esfuerzos en la ampliación del número de test que se realizan, para así lograr un sistema de detección eficiente que permita identificar los casos positivos (y contactos) para poder aislarlos y evitar un incremento en la tasa de contagio. Así mismo, se necesita avanzar en el plan contingente de ampliación de la capacidad instalada de camas UCI y orientar recursos que permitan rápidamente iniciar la fase IV (9 826 camas). Finalmente, se necesita generar condiciones que garanticen la dotación de equipos de protección personal a médicos y enfermeros que se encuentren atendiendo la emergencia sanitaria a nivel nacional para evitar un incremento adicional en la tensión creciente sobre los radios óptimos de atención, e implementar programas que permitan instruir rápidamente a los trabajadores del sector salud en los requerimientos del área de cuidados intensivos ♠















