Introducción
Manihot esculenta Crantz, comúnmente conocida como yuca, es una planta lechosa originaria de Brasil, cuya altura puede alcanzar hasta 3 metros (Suárez y Mederos, 2011). La raíz de la yuca contiene desde el exterior al interior, la peridermis (cáscara), el parénquima cortical (corteza) y el parénquima interior, que es la pulpa de color blanco, la cual es comestible como tubérculo con alto poder calórico representado en alrededor de 2,0 %, grasas (1,0 %) y minerales o cenizas (2,0 %), aproximadamente el 45 % en materia seca, de la cual un 90 a 95 % corresponde al contenido de carbohidratos (Chaiareekitwat et al., 2022). Contiene a su vez una composición de alrededor de 11,8 % de lignina, 38,8 % de celulosa y 7,2 % de hemicelulosa (Alves-Pereira et al., 2022; Reales, Castaño y Zapata, 2016).
La producción mundial de Manihot esculenta Crantz en el año 2019 alcanzó alrededor de 27 millones de toneladas; el 20 % se produce en América Latina, en Colombia ocupa el tercer lugar con 2,1 millones de toneladas producidas anualmente (FAO, 2020; Wellens et al., 2022; Suárez y Mederos, 2011). El parénquima interior a nivel industrial se utiliza de acuerdo con la concentración de cianogénicos presentes. Cuando la cantidad de este compuesto está en niveles tóxicos para el consumo humano se emplea la pulpa para la producción de bioetanol (Aristizábal y Sánchez, 2007). Cuando la raíz se usa para el consumo humano se retira el 30 % del peso, el cual se considera desecho, que es llevado a rellenos sanitarios. En Latinoamérica esto genera gastos en logística y contaminación del suelo, aire y recursos hídricos, por lo que derivar los residuos de pulpa a nuevos materiales como el biocarbón contribuiría al aprovechamiento de este desecho (Murthy, y Ramakrishna, 2022).
El biocarbón es un sólido de color negro, estable, amorfo que posee una alta porosidad y su estructura está ligada al tipo y el tiempo de la pirólisis (Ahmed, Kurian y Raghavan, 2016). Es un producto obtenido por la descomposición térmica de biomasa lignocelulosa bajo un suministro limitado de oxígeno e hidrógeno que se da a temperaturas por debajo de 973 K, lo cual le confiere principalmente grupos funcionales ácidos como fenoles y carboxilos (de Mendonça et al., 2017), otorgando al material una carga negativa superficial y pH generalmente alcalino, con porosidad variada: nanoporos (< 0,9 nm), microporos (< 2 nm) y macroporos (> 50 nm) que dependen de la concentración de lignina y el tratamiento térmico (Yang et al., 2017).
El uso del biochar a partir de la pulpa de yuca para la remoción de contaminantes como Rhodamine B ha demostrado ser eficiente por la generación de interacciones electrostáticas y puentes de hidrógeno entre la superficie del biochar y el contaminante (Wu et al., 2020), lo anterior permite la remoción de otros colorantes industriales como los tintes usados en algunas industrias como textil, de papel, de alimentos y de cosméticos, que son unas de las principales fuentes de contaminación, provocando grandes daños a la flora y la fauna, con efectos mutagénicos y carcinogénicos (Sharma, Saikia y Das, 2014).
Existe una gran variedad de colorantes, entre los que se encuentran los azoicos, que en su estructura poseen un grupo (-N = N-) que está conjugado con anillos aromáticos en ambos extremos y son los más usados en la industria (Hunger, 2007) como naranja y verde de metilo, los cuales articulan la presente investigación que busca el aprovechamiento de desechos de la yuca mediante la síntesis de biochar a baja temperatura para obtener un material útil en la remoción de los colorantes industriales del tipo azocompuestos.
Metodología
Síntesis del biochar
Se recolectaron 50 kg de residuos de yuca provenientes de la plaza de mercado central de Pamplona (Norte de Santander, Colombia), a los cuales se les retiró la peridermis y el parénquima cortical. Posteriormente se lavó y se fraccionó en tiras de 2 cm de largo y 0,5 cm de ancho, las cuales se deshidrataron por 12 h a 373 K. El sólido obtenido se pulverizó por molturado, obteniendo harina de yuca que se llevó a un reactor de vidrio de 500 mL, al cual se le aplicó una rampa de calentamiento de 5° C/min desde temperatura ambiente hasta 573 K a una presión de 80 mbar, manteniendo constate la temperatura (573 K) por 30 minutos. Después se aumentó la temperatura hasta 673 K y se mantuvo constante por 40 minutos. Al finalizar este tiempo se enfrío el sistema a 10° C/min y al llegar a la temperatura ambiente (∼293 K) se hizo un barrido de gases con argón. Durante todo el proceso, los residuos fueron condensados en una trampa de agua a 275 K. El sólido obtenido se lavó con 100 mL de HCl 3X10-4 M por 30 minutos a 760 rpm, se filtró, se lavó con 50 mL de agua destilada y se secó a 323 K por 12 h.
Caracterización
En la caracterización espectroscópica de infrarrojo se empleó un espectrofotómetro Shimadzu Prestige-21, 48 scan, rango 4.000 a 400 cm-1, resolución 4 cm-1, adaptador ATR. Por otro lado, para los análisis por espectroscopia UV-Vis se empleó un espectrofotómetro Shimadzu UV-2401PC con lámpara de cátodo hueco, barrido de 190 a 900 nm, celda de muestra y referencia de cuarzo, con paso óptico de 1 cm. Mientras para los análisis térmicos de TGA-DSC se empleó un equipo SDT-Q-600 (T.A. Instruments). La muestra fue pulverizada y se agregó a una celda de alúmina, y se calentó a una rampa de 10° C/min bajo una atmósfera de N2(g), desde temperatura ambiente (291 K) hasta 1.073 K. Para la caracterización mediante microscopía electrónica de barrido (SEM) se empleó un equipo FEI Quanta 200, con un alcance 260.000 aumentos, las micrografías se complementaron con un microscopio óptico Olympus BX51 y se tomaron con luz paralela con objetivos de 60X y 100X (inmersión). Por último, para la difracción de rayos X de muestras policristalinas (PDRX) se empleó un difractómetro D8 Advance, marca Bruker con geometría Davinci, los perfiles se midieron con fuente de cobre slipt 0,1, paso 0,015° 2 theta, medido de 2 a 50° 2 theta.
Preparación de las soluciones de naranja y verde de metilo
La solución de naranja y verde de metilo se preparó a 30 mg/L empleando sólidos grado reactivo Sigma-Aldrich y aforados en balón ámbar certificado.
Remoción de naranja y verde de metilo
Para la remoción de los colorantes, se utilizaron muestras de 0,15 g de biochar que se disolvieron en 300 mL de solución de naranja de metilo de 30 mg/L, las cuales se agitaron a 760 rpm por 30 minutos, al término del tiempo, las mezclas se filtraron y se analizaron a una longitud de onda máxima de 454 nm por espectroscopía UV-Vis, empleando un espectrómetro Shimadzu UV-2401PC, celda de cuarzo de 1 cm. Se utilizó como blanco una solución obtenida del lavado de 0,15 g de biochar con 30 mL de agua destilada por 30 minutos. Para la cuantificación de la concentración de colorante se realizó una curva de calibración con el blanco como diluyente a 0, 2, 4, 6, 8, 10 y 12 mg/L de naranja de metilo. El estudio de remoción se repitió por quintuplicado. El procedimiento descrito se replicó para la remoción del verde de metilo. En este caso, la curva de calibración se realizó con las siguientes concentraciones del colorante: 0, 1, 2, 3, 4, 5 y 6 mg/L, y se analizó a una longitud de onda máxima de 631 nm.
Resultados
El retiro de la peridermis y el parénquima cortical representa una pérdida de peso del residuo de 12,00 ± 0,04 %, el cual se debe a la pérdida de la corteza retirada y la tierra adherida que tiene la peridermis. Después del proceso de secado a 373 K, se registró una pérdida de peso del 15,00 ± 0,05 %, que se debe a compuestos volátiles y agua, el valor reportado está acorde lo encontrado por Coelho et al. (2020).
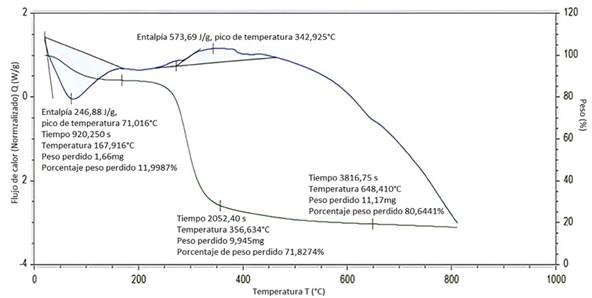
El análisis térmico de la harina de yuca (Figura 1) muestra una endoterma centrada a 71°C, la cual refleja una pérdida de peso de alrededor de 12 %. Esto se debe a que la harina de yuca que ha sido deshidratada previamente adsorbe agua al volver a temperatura ambiente.
Adicionalmente, se presenta una exoterma cercana a 343° C, la cual centra su pérdida de peso alrededor de 357° C, indicando que esta es la temperatura a la cual la harina se descompone por pirólisis, siendo la temperatura usada en la síntesis del biochar. Otro dato importante del análisis térmico es la cantidad de materia orgánica degradable bajo N2(g), la cual fue del 69,65 %. Estos resultados son similares a los obtenidos por Uzun, Apaydın Varol y Pütün (2016) para biomasas degradables y derivación de biodiesel, pero superior al 2,5 a 3,5 % de ceniza reportado por Veiga et al. (2016) en atmósfera oxidante. Lo anterior se debe a que el caso estudiado se realizó bajo atmósfera de N2(g) para conocer la máxima capacidad de autooxidación.
El sólido obtenido del biochar presentó un color negro, homogéneo y con un porcentaje en peso con respecto al inicial de 58,08 ± 0,07 %. Al tener en cuenta los resultados del análisis TGA/DSC (Figura 1), la masa recuperada debería haber sido del 20 %, por lo tanto se puede afirmar que la ruta planteada permite recuperar un 38,08 % de masa adicional. Estos resultados son indicativos de la retención de oxígeno y carbono por parte del biochar, los cuales son comparables con reportes de pirólisis a 1073 K publicados por de Mendonça et al. (2017), con la ventaja de que en este trabajo se obtiene 673 K. La masa pérdida se debe a procesos de combustión incompleta que liberan gases como metano, monóxido de carbono, dióxido de carbono, SOx y NOx, y biodiesel recuperado en la trampa de condensación (Soni y Karmee, 2020).
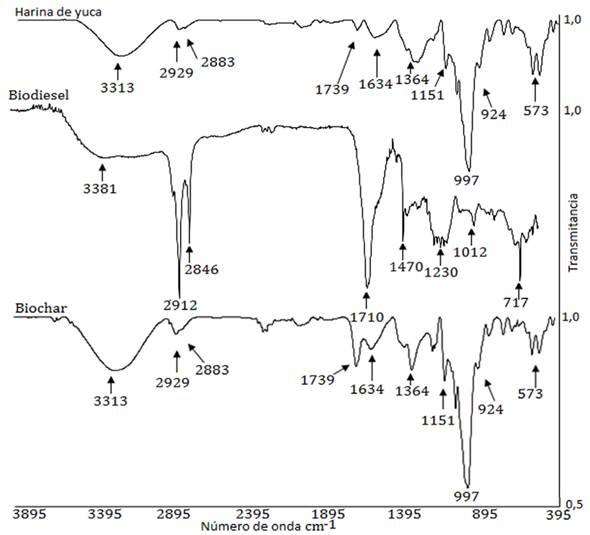
Los espectros de ATR-IR muestran que la harina de yuca y el biocarbón tienen una distribución de grupos funcionales similares entre sí (Figura 2). Una banda ancha de 3.310 a 3.330 cm-1 se atribuye al estiramiento OH por parte de compuestos fenólicos, alcoholes y agua adsorbida, comportamiento característico de los carbohidratos (Versino, López y García, 2015).
Las señales presentes a 2.920 - 2.889 cm-1 se deben al estiramiento C-Hn alquilo, alifático y aromático; se observa mayor intensidad en el espectro IR del biocarbón debido al reordenamiento que conlleva a una estructura aromática tipo grafeno que se forma (Huang et al., 2018). Dos bandas de baja intensidad a 1.738,1 y 1.634,5 cm-1 corresponden a vibraciones C = O de carbonilo de ácidos carboxilos y aldehídos, con mayor intensidad para el biocarbón, debido a la oxidación en la pirólisis que procede de la hemicelulosa y la lignina (Jindo et al., 2014; Luo et al., 2013).
Para el biocarbón se observó una mayor intensidad y mejor definición de las señales en la región del espectro de 1.300 a 1.500 cm-1 atribuibles a flexiones C-H de diferentes tipos, debido a los anillos aromáticos presentes, mientras que en 1.150 cm-1 se observa un estiramiento C-O-C del enlace aril-alquil-éter (Razali, Ismail y Ariffin, 2015). Una banda a 997,5 cm-1 de alta intensidad se observa debido al estiramiento C-O-C asimétrico de los componentes lignocelulósicos. A 924 cm-1 se obtuvo una pequeña señal que se debe a la vibración C-O de la celulosa, mientras que en la región de la huella dactilar diferentes señales se atribuyen a estiramientos C-H y C-C del esqueleto aromático (Soni y Karmee, 2020; Mei et al., 2015).
Para el caso del biodiesel condesado en la trampa de salida, el espectro ATR-IR muestra la presencia de grupos -CH3 y -CH2 de cadenas alquílicas, grupo carbonilo alrededor de 1.710 cm-1, correspondiente a esteres y señales de bandas situadas en la región de 1.200 - 1.400 cm-1 pertenecientes a los grupo O-CH3 y la banda situada entre 1.425 - 1.447 cm-1 pertenecientes al grupo -CH3, finalmente, la banda ancha centrada 3.823 cm-1 se debe al agua fisisorbida en la que se atrapó el gas del biodiesel (Soni y Karmee, 2020). Los resultados de los espectros evidencian que el proceso de pirólisis se lleva a cabo generando un biochar con retención de carbón y como producto derivado un éster alquílico.
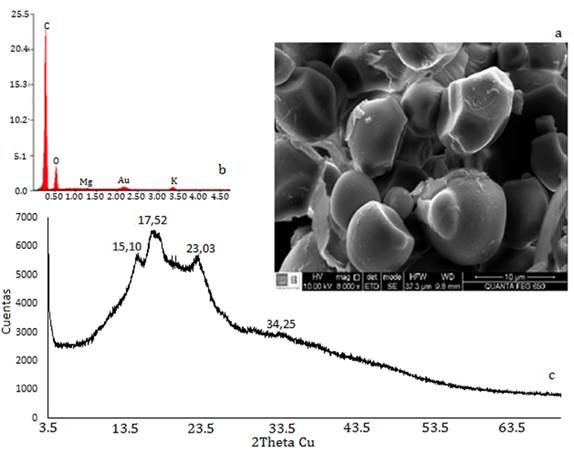
El biochar, según el análisis SEM (Figura 3a), presentó una morfología esférica con diámetros alrededor de 10 µm y de superficie lisa, lo cual facilita su uso en catálisis, almacenamiento de gases, mejores propiedades eléctricas, ópticas y térmicas que permiten una alta relación superficie-volumen, aislamiento térmico y una alta estabilidad fisicoquímica (Soni y Karmee, 2020; Yang et al., 2017). El análisis elemental EDS (Figura 3b) evidenció que el material tiene C y O en un porcentaje en peso de 67,67 % y 20,36 % respectivamente. Lo anterior es característico de un carbono procedente de biomasa lignocelulósica con pirólisis, lo cual se corrobora con los máximos de difracción 15,10, 17,52, 23,03 y 34,25° (2 theta) (Figura 3c), estos resultados son similares a los obtenidos para la harina de yuca por Lopattananon, Thongpin y Sombatsompop (2012), lo que permite establecer que el biochar obtenido conserva una estructura de almidones cristalinos del tipo A (Zhang et al., 2020).
La remoción de los colorantes mostró una curva de calibración en la que la regresión lineal para el naranja de metilo a longitud de onda máxima = 464 nm es
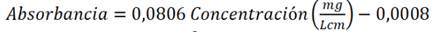 (Ecuación 1) con
(Ecuación 1) con
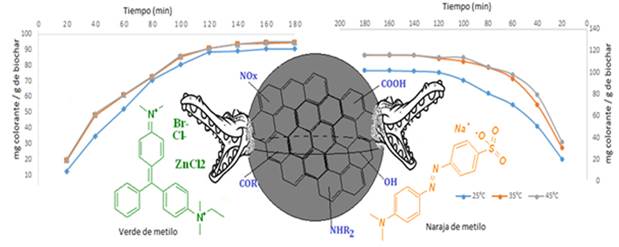
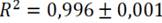 , donde se estableció como límite de detección de 0,050 ± 0,001 mg/L y límite de cuantificación de 0,100 ± 0,001 mg/L, a partir de lo cual se logró determinar que la capacidad de remoción del naranja de metilo fue de 116,4 ± 0,2 mg/g a 35° C, que es superior a la remoción lograda a 25° C (101,9 ± 0,1 mg/g) y similar a la lograda a 45° C (116,7 ± 0,2 mg/g) (Figura 4).
, donde se estableció como límite de detección de 0,050 ± 0,001 mg/L y límite de cuantificación de 0,100 ± 0,001 mg/L, a partir de lo cual se logró determinar que la capacidad de remoción del naranja de metilo fue de 116,4 ± 0,2 mg/g a 35° C, que es superior a la remoción lograda a 25° C (101,9 ± 0,1 mg/g) y similar a la lograda a 45° C (116,7 ± 0,2 mg/g) (Figura 4).
Para el caso del verde de metilo la regresión lineal obtenida a longitud de onda máxima = 631 nm fue
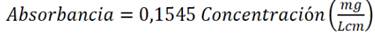 (Ecuación 2) con
(Ecuación 2) con
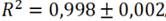 , donde se estableció como límite de detección de 0,060 ± 0,001 mg/L y límite de cuantificación de 0,120 ± 0,001 mg/L, logrando una remoción a 35° C de 94,2 ± 0,2 mg/g pasados los 140 minutos de exposición. Los resultados fueron similares a los obtenidos en el ensayo a 45° C (94,4 ± 0,2 mg/g) y ligeramente superiores a los de la temperatura de 25° C (90,3 ± 0,1 mg/g).
, donde se estableció como límite de detección de 0,060 ± 0,001 mg/L y límite de cuantificación de 0,120 ± 0,001 mg/L, logrando una remoción a 35° C de 94,2 ± 0,2 mg/g pasados los 140 minutos de exposición. Los resultados fueron similares a los obtenidos en el ensayo a 45° C (94,4 ± 0,2 mg/g) y ligeramente superiores a los de la temperatura de 25° C (90,3 ± 0,1 mg/g).
Los anteriores datos indican que el biochar mostró buena capacidad de adsorción de los colorantes azo benzoicos, lo cual se explica por los grupos funcionales del tipo acetatos, fenólicos, esteres, ácidos y aminas catiónicas generados durante la pirólisis, estos grupos funcionales facilitan la interacción mediante fuerzas electrostáticas catión-anión, puentes de hidrogeno, interacciones π-π y de Van der Waals (Qiu et al., 2009; Huang et al., 2019).
Los resultados obtenidos son superiores para biochar derivado de otras biomasas de yuca como su corteza y película suberosa, y en cuanto a la capacidad de absorción, se ha reportado alrededor de 78 mg/g para verde de malaquita (Leng et al., 2015), de 80 mg/g para contaminantes orgánicos y de alrededor de 90 mg/g para la remoción de metales con alto nivel de toxicidad ambiental (Oladipo y Ifebajo, 2018; Fan et al., 2017; Li et al., 2018). Los materiales con estas propiedades de adsorción son comparables a los aluminosilicatos, que pueden contener contaminantes orgánicos e inorgánicos, lo cual amplía su uso en reacciones catalíticas, buscando procesos ambientalmente aplicables que cumplan los principios de la química verde (Lyu, Zhang y Shen, 2020; López et al., 2020).
Conclusiones
A partir de los desechos de yuca se logró deshidratar y pirolizar el parénquima interior de la yuca (Manihot esculenta) a 673 K, con una recuperación del 71 % de la materia orgánica degradable. También se obtuvo un biochar con agregados esféricos de diámetro 10 µm y estructura de cristal del tipo lignocelulosa y de estructura cristalina de almidón tipo A, que demostraron una capacidad de adsorción de naranja de metilo de 116,4 ± 0,2 mg/g y de verde de metilo de 94,2 ± 0,2 mg/g a 35° C. Lo anterior es prometedor para el tratamiento de residuos orgánicos y fuentes hídricas con desechos industriales.