Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Perspectivas en Nutrición Humana
versão impressa ISSN 0124-4108
Perspect Nut Hum v.12 n.1 Medellín jan./jun. 2010
INVESTIGACIÓN
Efecto de la administración de lípidos intravenosos desde el primer día sobre el nivel de plaquetas en recién nacidos a término y pre término
Effect of parenteral nutrition intravenous lipids on platelet blood counting in term and preterm newborns
Carlos Alberto Velasco Benítez 1; Liliana Ladino Meléndez2; Ángela Patricia Luna Medicis2
1Grupo de Investigación Gastrohnup. Universidad del Valle. Cali–Colombia. carlos.velasco@correounivalle.edu.co
2Pontificia Universidad Javeriana. Bogotá–Colombia.
Artículo recibido: 23 de abril de 2010
Aceptado: 2 de junio de 2010
Como citar este artículo: Velasco Benítez CA, Ladino Meléndez L, Luna Medicis AP. Efecto de la administración de lípidos intravenosos desde el primer día sobre el nivel de plaquetas en recién nacidos a término y pre término. Perspect Nutr Humana. 2010;12:25-32.
Resumen
Introducción: la nutrición parenteral en recién nacidos es una alternativa cuando tienen alterada la vía enteral. La trombocitopenia ha sido reportada como efecto adverso del uso de lípidos intravenosos. Objetivo: evaluar el efecto la administración intravenosa de lípidos sobre el recuento de plaquetas en recién nacidos. Materiales y métodos: estudio prospectivo en todos los recién nacidos que necesitaron nutrición parenteral, hospitalizados en un centro asistencial de Bucaramanga (Colombia), durante un mes. Todos recibieron lípidos intravenosos en dosis crecientes de 0,5 g/kg/día el primer día, hasta 3 g/kg/día, fueron monitorizados diariamente y evaluado su recuento de plaquetas al inicio y siete días después. Resultados: ingresaron 22 recién nacidos a término y 29 pretérmino, 55% hombres, con diversas condiciones clínicas, como prematurez (22), enterocolitis necrosante (17), dificultad respiratoria (4), atresia esofágica (2) y otras (6). En el recuento de plaquetas no se observaron diferencias significativas (p>0,05), entre el inicio del estudio y el séptimo día, ni en los niños pretérmino (227.320±86290/mm3 versus 294.930±120.600/mm3), ni en aquellos a término (276.140±130.240/mm3 versus 273.240±96.890/mm3), tampoco se observaron efectos adversos. Conclusión: en recién nacidos a término y pretérmino, la administración de lípidos intravenosos a dosis hasta 3 g/kg/día, es segura, libre de trombocitopenia y otros efectos.
Palabras clave: nutrición parenteral, emulsiones lipídicas intravenosas, trombocitopenia, recuento de plaquetas, recién nacido.
Abstract
Introduction: Parenteral nutrition (NPT) support is another option in newborn when they cannot receive enteral nutrition. Thrombocytopenia has been reported as a complication for the use of NPT intravenous lipids. Objective: To evaluate the effect of NPT intravenous lipids on platelet blood counting in newborns. Materials and methods: this is a prospective study carried out in newborns requiring parenteral nutrition support who were hospitalized in Bucaramanga– Colombia. All patients received intravenous lipids. Doses were increasing of 0,5 g/kg/ day at the first day to reach 3 g/kg/day at the end. They were monitored daily and platelet blood counting was assessed at baseline and seven days later. Results: subjects were 22 term newborns and 29 preterm (55% men), they presenting different clinical conditions like prematurity (22), necrotic enterocolitis (17), respiratory problems (4), esophageal atresia (2) and others (6). The platelet blood counting showed no significant differences between baseline and the seventh day (p> 0.05), no in preterm (227.320±86290/mm3 versus 294.930±120.600/mm3),and either in the newborns (276.140±130.240/mm3 versus 273.240±96.890/mm3) no adverse effects were reported. Conclusion: administration of intravenous lipid at doses up to 3 g/ kg / day in term and preterm newborns is safe, and no thrombocytopenia was not reported and other adverse effects.
Key words: parenteral nutrition, fat emulsions intravenous, thrombocytopenia, platelet count, infant newborn.
INTRODUCCIÓN
La trombocitopenia se define como una disminución de las plaquetas circulantes (recuento total de plaquetas ?100.000/?L) (1) y puede estar asociada a diversos grupos de enfermedades y situaciones complejas en las que múltiples factores contribuyen a la disminución de este tipo de células. Diversos estudios la han citado como un potencial efecto adverso del uso de lípidos intravenosos (IV) (2–5); sin embargo, en recién nacidos a término (RNAT) y recién nacidos pre término (RNPT), quienes requieren de nutricional parenteral, es indispensable el uso de lípidos en estas mezclas, aunque todavía existen controversias en cuanto a su administración, composición y dosis. Además la literatura muestra que es factible iniciar los lípidos IV desde el primer día (6,7). La nutrición parenteral se define como el aporte de nutrientes por vía venosa. La gran mayoría de los RNPT tienen indicación de soporte nutricional parenteral debido a que su tracto digestivo no se encuentra completamente desarrollado; adicionalmente algunos RNAT presentan patologías que comprometen el uso de la vía enteral, por lo tanto, requieren de nutrición parenteral. Una nutrición parenteral completa requiere de la administración de glucosa, lípidos, aminoácidos, vitaminas, minerales y electrolitos, los cuales le garantizan un adecuado aporte energético; si alguno de estos componentes no se suministra, o la cantidad es insuficiente, se pueden presentar deficiencias nutricionales que alteran el estado nutricional y con ello el crecimiento y desarrollo del niño (8,9). Para los recién nacidos las recomendaciones de lípidos para uso parenteral varían entre 40 y 50% del valor energético total, cantidad representativamente alta, debido a que los lípidos son una excelente fuente de energía y hacen parte fundamental para el desarrollo del cerebro porque contienen ácidos grasos esenciales (ácido linolénico y ácido araquidónico) necesarios para el desarrollo de la retina, componentes clave de las células de las membranas, mielinización y crecimiento neuronal (9,10). Es posible que en ciertos recién nacidos pretérmino menores de 32 semanas de gestación, que reciben nutrición parenteral total sin lípidos, presenten signos clínicos de deficiencia de ácidos grasos esenciales desde el segundo día de vida extrauterina. La deficiencia de ácido linolénico o de ácido araquidónico puede producir piel escamosa, dermatitis, caída de pelo, diarrea, defectos de cicatrización de heridas y hasta falla en el crecimiento, lo cual es relevante en pediatría y sobretodo en neonatos (1). A pesar de que esta complicación se presenta cada vez en menor frecuencia, debido a las características actuales de las emulsiones lipídicas comerciales existentes en Colombia, a sus indicaciones precisas en cuanto a la cantidad diaria total recomendada y a la velocidad de administración, y que no existen trabajos relacionados con este tópico en nuestro país, el objetivo del presente estudio fue evaluar el efecto de la administración de lípidos endovenosos al 20% (MCT/LCT) en recién nacidos a término y recién nacidos pretérmino sin trombocitopenia, sobre el recuento total de plaquetas en dosis diarias crecientes desde el primer hasta el sexto día, sin sobrepasar la velocidad de aclaración lipídico.
MATERIALES Y METODOS
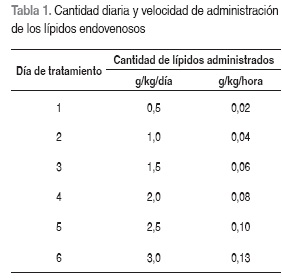
Estudio prospectivo donde por conveniencia se incluyeron todos los recién nacidos de ambos géneros a término y pretérmino, nacidos en la Unidad de Recién Nacidos de la Clínica Los Comuneros del Seguro Social de Bucaramanga, Colombia, entre el 1 y 28 de febrero de 2002, con peso mayor a 1.500 gramos, quienes recibirían únicamente soporte nutricional parenteral (central o periférico) durante seis días, con recuento total de plaquetas superior a 100.000/mm3 antes de iniciar nutrición parenteral y sin sepsis grave, ni trastornos hidroelectrolíticos, ni trastornos metabólicos graves. Fueron excluidos los recién nacidos sin consentimiento informado firmado. Se obtuvieron datos como causa de hospitalización, edad gestacional, género, peso inicial, cantidad de lípidos endovenosos administrados y velocidad de aclaramiento durante los días 1 al 6 de nutricional parenteral total, valores de plaquetas inicial (día 1 previo a la infusión de NPT) y final (día 7). El análisis estadístico paramétrico se basó en la comparación de promedios correlacionados a través de la distribución t de student, y el análisis estadístico no paramétrico por medio de la comparación de dos grupos apareados correlacionados por la prueba de Wilcoxon, siendo significativa una p?0,05. Los valores fueron expresados como promedio ± desviación estándar (X±DS). El aporte y características de la emulsión de lípidos utilizada, se presenta en las Tabla 1 y Tabla 2.
RESULTADOS
Durante el mes del estudio se recolectaron los datos de 51 niños recién nacidos; 33 del género masculino (64,7%); con un peso mínimo de 1.500 g y un peso máximo de 4.100 g (mediana=2.400 g, 2.497±806 g); siendo sus principales causas de hospitalización, la prematurez en 43,1 %, la enterocolitis necrosante (ECN) en 33,3%, el distress respiratorio en 7,8%, la atresia esofágica en 3,9% y otras causas en 11,7%. Todos recibieron lípidos IV durante mínimo seis días a una dosis inicial de 0.5 g/kg/día (día 1), con incrementos diarios de 0,5 g/kg/día hasta llegar a 3 g/kg/día (día 6), sin sobrepasar la velocidad de aclaramiento lipídico de 0,17 g/kg/hora.
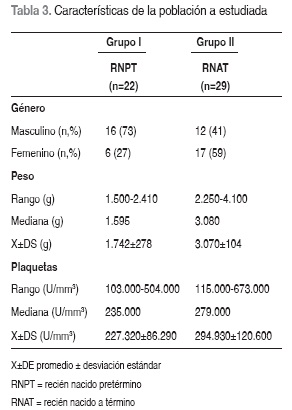
Grupo I: lo constituyeron 22 RNPT, 16 del género masculino (73%); con pesos entre 1.500 y 2.410 g (mediana = 1.595 g, 1.472±276 g). Al día 1, se encontró un valor mínimo de 103.000 mm3 plaquetas y un valor máximo de 504.000 mm3 plaquetas, con una mediana de 235.000 mm3 plaquetas y una media 227.320 mm3 plaquetas ±86.290 mm3. Al día 7, se presentó un valor mínimo de 125.000 mm3 plaquetas y un valor máximo de 493.000 mm3 plaquetas, con una mediana de 216.000 mm3 plaquetas y media 276.140 mm3 plaquetas ±130.240 (Tabla 3).
Grupo II: constituido por 29 RNAT, 17 género masculino (59%); con pesos entre 2.250 y 4.100 g (mediana = 3.080 g, 3.070±104 g). Se encontró un valor mínimo de 115.000 mm3 plaquetas y un valor máximo de 673.000 mm3 plaquetas, siendo la mediana de 279.000 mm3 plaquetas y media de 294.930 mm3 plaquetas ±120.600. Los valores mínimo y máximo de plaquetas fueron de 111.000 mm3 plaquetas y 589.000 mm3 plaquetas respectivamente, con una mediana de 267.000 mm3 plaquetas y una media de 273.240 mm3 plaquetas±96.890 (Tabla 3).
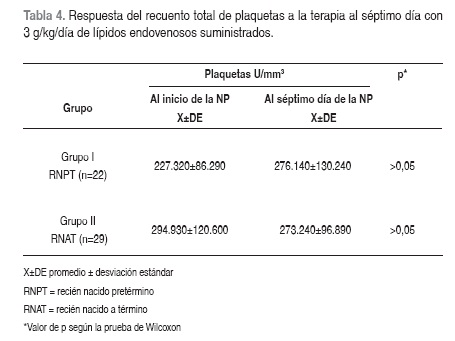
Al comparar los días 1 y 7 de cada grupo por separado y luego los grupos entre sí en el día 1 y 7, para las plaquetas versus la infusión de lípidos endovenosos a dosis crecientes, no se encontraron diferencias estadísticamente significativas (Tabla 4). No se presentaron efectos adversos directos, ni se presentó morbimortalidad asociada al uso de NP, como tampoco signos y síntomas que hicieran sospechar en deficiencia de ácidos grasos esenciales.
DISCUSIÓN
Al revisar los resultados del presente estudio, se aprecia que no hay un efecto adverso sobre el nivel de plaquetas en los grupos de niños RNAT y RNPT que recibieron infusión de lípidos desde el primer día, similar a lo reportado en anteriores estudios, entre ellos el realizado por Spear y colaboradores (11), quienes no observaron efectos adversos de las emulsiones de lípidos administrados a dosis de 0,8 a 3,3 g/kg/día sobre la concentración de plaquetas, ya sea en el corto plazo (48 horas) o en los períodos de estudio a largo plazo (4 semanas). Así mismo, Herson (12) en su estudio examinó los posibles efectos hematológicos adversos del Intralipid® en 10 recién nacidos enfermos quienes fueron estudiados antes y después de 16 horas de una infusión de 1 g/kg de peso corporal de Intralipid®, se midieron recuento de leucocitos polimorfonucleares, quimiocinesis, la quimiotaxis y agregación, los cuales se mantuvieron sin cambios pre y post infusión de Intralipid®. El recuento de plaquetas, tiempo de hemorragia y la agregación plaquetaria se mantiene asimismo sin cambios. También Usmani (13), evaluó el efecto de Intralipid® sobre la función de leucocitos polimorfonucleares neonatal en 14 recién nacidos prematuros a término, se realizó la infusión de Intralipid® en 1 g/kg/24h y tampoco encontró cambios significativos en la función e integridad de los leucocitos polimorfonucleares, similar a los reportes de otros estudios realizados por Baer (14), Coehn (4), Dhanireddy (15), Friedman (16) y Porta (17). De esta forma se demuestra que en cuanto a la administración de lípidos, los resultados de este estudio son significativos con una p<0,05, lo cual ratifica la tesis expuesta de la eficacia que presenta los lípidos sobre la NPT en las primeras semanas de vida.
Con base en estos resultados y de acuerdo a recientes publicaciones, se sugiere que los recién nacidos que no pueden recibir la alimentación enteral suficiente reciban emulsiones de lípidos intravenosos desde las primeras 24 horas de vida (18–20). Así mismo, otros estudios no encuentran resultados adversos que interfieran en el uso de lípidos IV en niños recién nacidos desde las primeras 24 horas, lo anterior ha sido corroborado por diversos autores Spear (11), Usmani (13), Herson (12) y observado también en los resultados del presente estudio. Respecto del uso de la vía oral o parenteral para alimentar recién nacidos a término y pre término con patologías de base, se han reportado controversias que han sido resueltas con estudios actuales que demuestran el uso necesario y adecuado de las dos vías, con un gradual y temprano inicio de la vía oral mientras se disminuye paulatinamente la parenteral, modelo que minimiza las complicaciones (21). Las cantidades máximas diarias aportadas a los grupos I y II, según recomendaciones de la European Society of Paediatric Gastroenterology, Hepatology and Nutrition (ESPGHAN), fueron: 3–4 g/kg/día (0,13–0,17 g/kg/hora) en lactantes, incluidos los RNPT, y 2–3 g/kg/día en niños (0,08–0,13 g/kg/hora), esto muestra que mientras se conserve la velocidad de aclaramiento no se encuentra alteración en los niveles de plaquetas. Como ya se ha mencionado, es más importante que la mezcla total sea equilibrada, que su introducción sea progresiva, los incrementos paulatinos de 0,5 g/kg/día (especialmente en niños pretérmino de muy bajo peso) permiten controlar la hipertrigliceridemia que no debe superar la concentración de 250 mg/dL en lactantes y 400 mg/dL en los niños mayores (22–24).
La American Gastroenterological Association (25) sugiere que en algunas circunstancias como: infecciones graves (disminución de lipoproteinlipasa); hiperbilirrubinemia neonatal (riesgo de kernicterus); trombocitopenia <100.000/mm3; insuficiencia hepática y enfermedades pulmonares, hay que tener precaución y reducir los aportes (0,5–1 g/kg/día) garantizando el suministro de ácidos grasos esenciales. También es importante considerar que no es solamente el aporte de lípidos en cantidad, sino que se debe tener en cuenta su composición respecto al contenido de ácidos grasos (incluyendo la proporción de ácidos grasos saturados, monoinsaturados y poliinsaturados, y la relación omega 6–omega 3) y antioxidantes para prevenir la peroxidación lipídica a la que están expuestos neonatos con oxígeno y ventilación mecánica. Ahora bien, la composición de los lípidos empleados por vía endovenosa ha ido cambiando progresivamente, inicialmente las emulsiones lipídicas contenían aceite de semilla de algodón, que fueron reemplazadas después durante muchos años, por las emulsiones lipídicas que tenían su procedencia del aceite de soya y cártamo con fosfolípidos de huevo como emulsionante, que resultaban ser una buena fuente de ácidos grasos esenciales y demostraron su eficacia y seguridad. Sin embargo, actualmente se consideran seguras las soluciones mixtas de triglicéridos de cadena larga y de cadena media (LCT/MCT) al 50%, y lípidos basados en el aceite de oliva que incorporan un pequeño porcentaje de LCT, que pueden mejorar los niveles de vitamina E y disminuir la peroxidación lipídica, han probado su seguridad en el aporte de lípidos durante el soporte nutricional parenteral en pediatría (26–29).
El uso de emulsiones de lípidos mixtas queda claramente demostrado que es seguro y eficaz con los resultados del anterior estudio, puesto que no se observaron efectos adversos en la cantidad y función plaquetaria de los recién nacidos. De igual forma, se recomienda el uso de soluciones de lípidos al 20% que contienen menos cantidad de fosfolípidos que las emulsiones al 10%, lo cual produce menos acumulación de estos en plasma, también incluyen ácidos grasos omega–3 tales como el ácido linolénico, encontrado en el aceite de soya, por producir menor elevación de lípidos plasmáticos y tener una relación triglicéridos/fosfolípidos más adecuada (30).
En conclusión, este estudio demuestra claramente que la administración a dosis crecientes de emulsiones de lípidos al 20% no produce ningún descenso significativo en la concentración de plaquetas durante los primeros días del soporte nutricional parenteral en los niños RNAT y RNPT. Aunque no se observaron efectos perjudiciales de las emulsiones lipídicas en los niños RNPT y RNAT con prematurez, enterocolitis necrosante (ECN), distress respiratorio, atresia esofágica, debe evitarse un aporte lipídico mayor a las dosis expuestas por la ESPGHAN siendo conveniente en cantidades necesarias para cubrir los requerimientos mínimos de ácidos grasos esenciales mínimo 3% del VET. Es necesario que los RNPT y RNAT que no puedan tener vía oral, reciban lípidos intravenosos desde el primer día, con el fin de prevenir déficit de AGE y todas sus implicaciones como la integridad y la función cerebral y el desarrollo visual durante el desarrollo fetal y neonatal. A los niños sin trombocitopenia previa que se les ofrecen lípidos desde el primer día sin sobrepasar la velocidad de aclaración lipídico no presentan riesgo de trombiocitopenia. Son necesarios más estudios prospectivos controlados aleatorizados, metodológico prospectivos para determinar si el uso de infusiones de lípidos tiene un efecto adverso sobre la concentración de plaquetas y la función.
Referencias
1. Velasco CA, Ladino L. Lípidos y nutrición pediátrica. En: Temas selectos en nutrición infantil. 2 ed. Cali: Gastrphnup Ltda.; 2009. p. 176–206. [ Links ]
2. Lipson AH, Pritchard J, Thomas G. Thrombocytopenia after intralipid infusion in a neonate. Lancet. 1974;2:1462–3. [ Links ]
3. Panter–Brick M, Wagget J, Dale G. Intralipid and thrombocytopenia. Lancet. 1975;1: 857–8. [ Links ]
4. Coehn IT, Dahms B, Hays DM. Peripheral total parenteral nutrition employing a lipid emulsion (Intralipid): complications encountered in pediatric patients. J Pediatr Surg. 1977;12:837–45. [ Links ]
5. Goulet O, Colomb V. Parenteral nutrition in infants and children. In: Guandalini S, editor. Textbook of pediatric gastroenterology and nutrition. London: Taylor and Francis; 2004. p. 555–78. [ Links ]
6. Eleni–dit–Trolli S, Kermorvant–Duchemin E, Huon C, Mokthari M, Husseini K, Brunet ML, et al. Early individualized parenteral nutrition for preterm infants. Arch Dis Child Fetal Neonatal. 2009;94:F152–3. [ Links ]
7. Pérez L, Fernández A, Muñoz P, Villares JM. Emulsiones lipídicas intravenosas en nutrición parenteral pediátrica. Act Pediatr Esp. 2009;67:387–92. [ Links ]
8. Uauy R, Dangour AD. Fat and fatty acid requirements and recommendations for infants of 0–2 years and children of 2–18 years. Ann Nutr Metabol. 2009;55:76–9. [ Links ]
9. Baker RD, Baker SS, Davis AM. Parenteral nutrition for neonates. In: Anderson D, Pittard WB, editors. Pediatric parenteral nutrition. Maryland: Gaithersburg; 2001. p. 301–14. [ Links ]
10. Thureen P, Hay WW. Strategies for feeding the preterm infant. Neonatology. 2008;94:245–54. [ Links ]
11. Spear ML, Spear M, Cohen AR, Pereira GR. Effect of fat infusions on platelet concentration in premature infants. J Parenter Enteral Nutr. 1990;14:165–8. [ Links ]
12. Herson VC, Block C, Eisenfeld L. Effects of intravenous fat infusion on neonatal neutrophil and platelet function. J Parenter Enteral Nutr. 1989;13:620. [ Links ]
13. Usmani SS, Harper RG, Wu SF. In vitro effect of intralipid on polymorphonuclear leukocyte function in the neonate. J Pediatr. 1986;109:710. [ Links ]
14. Baer VL, Lambert DK, Henry E, Christensen RD. Severe thrombocytopenia in the NICU. Am Acad Pediatr. 2009;124:1095–100. [ Links ]
15. Dhanireddy R, Hamosh M, Sivasubramanian KN. Postheparin lipolytic activity and intralipid clearance in very low–birthweight infants. J Pediatr. 1981;98:617–22. [ Links ]
16. Friedman Z. Prostaglandinas y tromboxanos en la medicina perinatal. En: Lebenthal E, editor. Gastroenterología y nutrición en pediatría. 2 ed. Barcelona: Salvat; 1996. p. 496–525. [ Links ]
17. Porta I, Planas M, Padro JB. Effect of two lipid emulsions on platelet function. Infusionsther Transfusionsmed. 1994;21:316–21. [ Links ]
18. Gawecka A, Michalkiewickz J, Kornacka MK, Luckiewicz B, Kubiszewska I. Immunologic properties differ in preterm infants fed olive oil vs soy–based lipid emulsions during parenteral nutrition. J Parent Enteral Nutr. 2008;32:448–53. [ Links ]
19. William W, Hay, Jr. Strategies for feeding the preterm infant. Neonatology. 2008;94:245–54. [ Links ]
20. Gilbertson N, Kovar IZ, Cox DJ. Introduction of intravenous lipid administration on the first day of life in the very low birth weight neonate. J Pediatr. 1991;119:615–23. [ Links ]
21. Chwals WJ. Vascular access for home intravenous therapy in children. J Parent Enteral Nutr. 2006;30:S65–9. [ Links ]
22. Grant J. Recognition, prevention, and treatment of home total parenteral nutrition central venous access complications. J Parent Enteral Nutr. 2002;26:S21–8. [ Links ]
23. Messing B, Man F, Colimon R, Thuillier F, Beliah M. Antibiotic–lock technique is an effective treatment of bacterial catheter–related sepsis during parenteral nutrition. Clin Nutr. 1990;9:220–5. [ Links ]
24. Lehner F, Demmelmair H, Roschinger W. Metabolic effects of intravenous LCT or MCT/LCT lipid emulsions in preterm infants. J Lipid Res. 2005;47:404–11. [ Links ]
25. Drenckpohl D, McConnell C, Gaffney S, Niehaus M, Macwan KS. Randomized trial of very low birth weight infants receiving higher rates of infusion of intravenous fat emulsions during the first week of life. Pediatrics. 2008;122:743–51. [ Links ]
26. Göbel Y, Koletzko B, Böhles HJ. Parenteral fat emulsions based on olive and soybean oils: A randomized clinical trial in preterm. J Pediatr Gastroenterol Nutr. 2003;37:161–7. [ Links ]
27. Goulet O. Parenteral nutrition. In: Gracey M, Walker–Smith JA, editors. Diarrheal disease. Philadelphia: Lippincott–Raven; 1997. p. 317–38. [ Links ]
28. Goulet O, Potter S, Antébi E. Long–term efficacy and safety of a new olive oil–based intravenous fat emulsion in pediatric patients: A double–blind randomized study. Am J Clin Nutr. 1999;70:338–45. [ Links ]
29. Shulman RJ, Phillips S. Parenteral nutrition in infants and children. J Pediatr Gastroenterol Nutr. 2003;36:587–607. [ Links ]
30. Rigo J, De Curtis M. Parenteral nutrition in premature infants. In: Guandalini S, editor. Textbook of pediatric gastroenterology and nutrition. London: Taylor and Francis; 2004. p. 619–38. [ Links ]