INTRODUCCIÓN
Al finalizar la ingesta alimentaria se produce una sensación de saciedad (1,2), lo que implica ciertos eventos posteriores al acto de comer que suprimen el hambre y mantienen una inhibición hacia el consumo de alimentos durante un período de tiempo determinado; mientras que el hambre puede considerarse como la necesidad de comer o un período en el que las señales de saciedad están ausentes. Entre el hambre y la saciedad se produce la saciación, un grupo de procesos que indican la terminación de comidas. Los efectos coordinados de la saciación y la saciedad controlan el tamaño y la frecuencia de los episodios de ingesta de alimentos, definiendo así el patrón de alimentación (3).
La saciedad está regulada por distintas hormonas que proceden del sistema gastrointestinal, del sistema endocrino, del tejido adiposo y del sistema nervioso (4). La iniciación de la alimentación sucede si el sistema nervioso central recibe señales que dan cuenta de una disminución generalizada de la utilización de los macronutrientes que producen energía a nivel celular; una de las hormonas que detecta estados de déficit a corto plazo es la grelina. Esta hormona estimula el consumo de alimentos, y sus niveles plasmáticos disminuyen después de una comida (5). Al consumir altos volúmenes de alimento (400 a 500 ml), se produce distensión abdominal y supresión del apetito por la acción de la hormona colecistoquinina (CCK). Frente al estímulo de hidratos de carbono y grasa, en el íleon se sintetiza el péptido similar al glucagón (GLP-1). Las células L del intestino delgado distal y del colon producen el péptido YY (PYY), cuyos niveles son bajos en ayuno y suben rápidamente después de una comida, para establecerse después de una o dos horas después de la comida. Estas hormonas (CCK y GLP-1) y PYY actúan en la supresión del apetito y la reducción del consumo energético en el corto plazo (2,6,7).
Para evaluar la saciedad que producen los alimentos en los individuos, se utiliza la escala visual análoga (EVA o VAS en inglés), que consiste en una escala de apreciación en la que el valor mínimo corresponde a ausencia de saciedad (tener mucha hambre) y el máximo es su mayor intensidad. Se puede presentar como una línea recta de diferente longitud o puntos (0 a 100 mm, por ejemplo) (2) y se evalúa en distintos tiempos: antes de comer, inmediatamente después de comer, y luego de 2 o 3 horas (8,9); o pueden realizarse mediciones cada 30 minutos hasta completar 3 horas (10). Otra medición de la saciedad corresponde al “cociente de saciedad” (SQ), que relaciona la sensación de apetito (medida con EVA) y la energía del alimento consumido (11,12); se calcula con la siguiente ecuación:
Karalus et al. (13) aplican un cuestionario de cinco factores de saciedad, en el que consideran: factor mental y físico de hambre, factor mental y físico de plenitud y factor de gusto de comida; en cada factor hay de 3 a 20 preguntas y se presentan en escalas de magnitud de 150 mm. Otra metodología para evaluar saciedad consiste en administrar alimentos y permitir su consumo ad libitum, registrando la cantidad de alimentos y energía consumidos (14).
Existen indicadores bioquímicos asociados con metabolismo, saciación y saciedad, estos incluyen glucosa, insulina, grelina, leptina CCK, GLP-1, PYY, que se pueden medir en sangre y permiten evaluar la saciedad (15,16).
En la actualidad, existe un creciente interés en la búsqueda de componentes nutritivos con elevado poder de saciedad, para ser utilizados en formulación de alimentos para personas con sobrepeso u obesidad con la finalidad de que el consumo de alimentos disminuya (17).
La evidencia científica ha demostrado que el consumo de alimentos con alto contenido de fibra dietética produce saciedad y pérdida de peso (18-21). Dentro de los componentes de la fibra dietética, existe un grupo denominado “prebióticos”, que corresponde a todos los ingredientes que posee un alimento que no pueden ser digeridos por las enzimas digestivas y que, además, incitan el desarrollo de bacterias beneficiosas (22-24). De acuerdo con el documento de expertos, Consensus, los prebióticos tienen el potencial de mejorar la salud humana y animal, y reducir el riesgo de enfermedades mediadas por problemas en la microbiota; además, el uso de prebióticos para mejorar la salud no puede ser aislado, sino que debe estar contemplado dentro de una dieta y estilo de vida saludables (25). Si un componente alimenticio resiste la digestión en el intestino delgado, se fermenta parcialmente en el intestino grueso por bacterias propias del medio e induce a ciertas bacterias beneficiosas a desarrollarse, se trata de un prebiótico (24,26-33). Los prebióticos se han calificado como compuestos bioactivos, debido a que modifican positivamente la funcionalidad de procesos fisiológicos del organismo (34).
Dentro de los prebióticos se encuentra la inulina, que, de acuerdo con lo que definen Álvarez‑Barroto et al. (35), “es el nombre genérico para designar a una familia de glúcidos complejos (polisacáridos) formados por cadenas moleculares de fructosa” (p. 132). Estas cadenas de fructosas están unidas por enlaces β-(2-1) fructosil-fructosa con residuo D-glucopiranosil o de α-D-fructopiranosil (32,36).
El objetivo de este artículo de actualización fue evaluar la relación entre el consumo de inulina, ya sea como alimento o como ingrediente de alguna preparación, con la regulación de la saciedad en humanos.
MATERIALES Y MÉTODOS
La búsqueda de información se realizó consultando recursos bibliográficos, como las bases de datos Scielo, Science Direct, Pubmed, Oxford Journals. Se utilizaron las siguientes palabras clave: inulin, satiety, prebiotic, VAS. Se realizó una búsqueda de revistas hasta el año 2010, y en los casos en que en dichos artículos se hacía referencia a artículos de años anteriores, también se incluyeron, dada su relevancia. Las revistas consultadas fueron del área de nutrición y alimentos.
RESULTADOS Y DISCUSIÓN
La inulina corresponde a un hidrato de carbono de origen vegetal que resiste la digestión en el tracto gastrointestinal superior y es fermentada en el colon. Aumenta la biomasa fecal y el contenido de agua en las heces, mejorando así los hábitos intestinales. Gracias a su propiedad de fermentar, afecta distintas funciones involucradas en la protección y reparación de la mucosa del colon, lo que puede contribuir a reducir el riesgo de enfermedades intestinales (37). Tiene efecto prebiótico, es capaz de mejorar la absorción gastrointestinal de minerales, disminuye el riesgo de aterosclerosis y aumenta la saciedad (38).
La inulina tiene bajo valor calórico, es hipoglicemiante y tiene la capacidad de mejorar la biodisponibilidad de calcio y magnesio (32,39). Regula parámetros lipídicos, además fortalece el sistema inmune y puede reducir el riesgo de cáncer (32,36,38-41).
Sus funciones como prebiótico descritas en la literatura están vinculadas principalmente a lo largo del intestino, aumentando la producción de ácidos grasos de cadena corta por la microbiota intestinal (26,29,42), reduciendo el pH intraluminal (26,41,42), disminuyendo los productos nitrogenados (42), modulando el sistema inmune (39,40,41) y generando una alteración hormonal y peptídica sobre la saciedad de las personas (40,42).
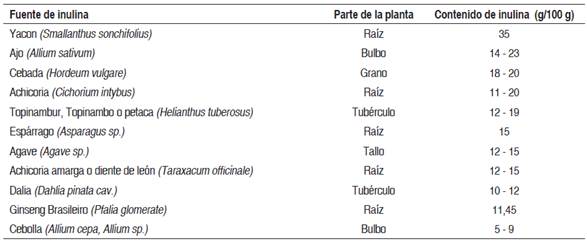
La inulina se encuentra contenida en más de 36 000 plantas de diferentes géneros, está presente en la cebolla, en el ajo, en el plátano y en la raíz de achicoria principalmente (43). En la Tabla 1 se presenta el contenido de inulina en diferentes vegetales (44).
Muchos de los alimentos contenidos en la tabla en mención se consumen directamente (cebolla, ajo, diente de león), aunque en baja cantidad; otros sirven para extraer la inulina e incorporarla como ingrediente en productos alimenticios. Debido al alto contenido de la misma (>10 %), la raíz de achicoria representa la fuente más importante usada en la producción industrial de inulina (38).
La inulina obtenida de achicoria es un polvo blanco de finas partículas de sabor neutro. Se disuelve en agua (aproximadamente 10 % a 25 °C) lo que permite adicionarla en medio acuoso sin que se precipite y presenta baja viscosidad, además de propiedades de gelificación (44). Las moléculas de inulina pueden interactuar con otros constituyentes de los alimentos, tales como almidón e hidrocoloides, produciendo importantes modificaciones que permiten mejorar la textura de los alimentos (38).
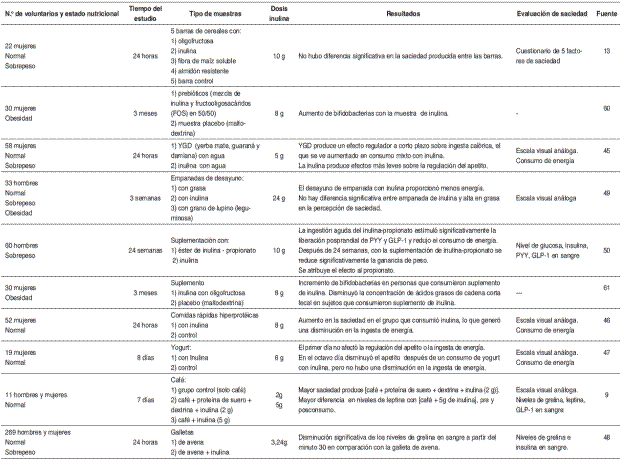
La inulina se incorpora como ingrediente en barritas de cereal, yogurt, galletas, entre otros. Se han realizado investigaciones para evaluar el efecto de la incorporación de inulina en alimentos y bebidas sobre la saciedad, los resultados de dichas investigaciones se presentan en la Tabla 2.
Los estudios mencionados en la Tabla 2 muestran resultados controversiales; en algunos casos se observó disminución parcial o total en la saciedad (9,44-48,50), en estos estudios la saciedad se evaluó por diferentes métodos, como escala visual análoga, consumo de energía, nivel de grelina y otros indicadores bioquímicos en sangre. Mientras que en otros estudios no se observaron cambios significativos en el aumento de la misma (13,49,50). La dosis de inulina no parece tener relación directa con la saciedad, puesto que en los estudios en que se detectó saciedad la dosis administrada fue de 2 a 8 g; sin embargo, en los otros estudios la dosis fue de 8 hasta 24 g.
El hecho de que no se haya comprobado una función reguladora de la saciedad por parte de la inulina se pudo ver afectado por diferentes motivos, como el vehículo que se utilizó para suministrar la inulina, el tiempo de consumo o alguna interacción fisiológica del estado nutricional que pudiera alterar sus características.
Se reporta en la literatura que los alimentos sólidos provocan un mayor efecto de saciedad posingesta y una mayor sensación de plenitud en las horas subsiguientes, en comparación con los alimentos líquidos (51,52). El formato del alimento al que se le agrega inulina puede ser un factor importante en el impacto que tiene sobre la saciedad, confundiendo los efectos reportados del consumo de inulina. Al comparar un alimento sólido con inulina y uno líquido con inulina, puede haber un mayor potencial para que la inulina aumente la saciedad cuando se añade al líquido (47). Esto se debe particularmente a la propiedad de la inulina que le permite retener agua; por lo tanto, si la fibra se dejó hidratar, o no, un tiempo antes del consumo, influirá en el nivel de saciedad que pueda provocar (53). De acuerdo con los estudios presentados en la Tabla 2, existen alimentos que por su consistencia y componentes pueden afectar directamente la saciedad por sí solos, como por ejemplo el yogurt (47), la yerba mate, el guaraná y la damiana (YGD) (45), el café (9) y un alto contenido de proteína (46), pudiendo influir en los resultados.
En los estudios analizados se encontró que se produjo aumento aislado de algunas hormonas anorexígenas, como la leptina, PYY y GLP-1 y una disminución en la hormona orexígena, grelina (9,48,50). Sin embargo, estos resultados siguen siendo controversiales, porque no se puede asegurar que el aumento aislado de dichas hormonas anorexígenas tengan un efecto directo en la regulación en la sensación de saciedad, independiente de la dosis de inulina que se administre, debido a que el mecanismo hambre-saciedad es regulado por un variado número de hormonas y señales gastrointestinales (2,4).
Según Heap et al., no se demostró un efecto de saciedad provocado por la inulina en el primer día de su estudio; a pesar de ello, al octavo día se mostró una disminución en el apetito (47). Con respecto a los demás estudios de la Tabla 2, no se puede asegurar que el consumo repetido de inulina provoque saciedad en todos los individuos, siendo poco claro el mecanismo por el cual actúa la inulina, porque cada microbiota intestinal actúa de manera diferente en cada individuo (54).
De acuerdo con los resultados de la Tabla 2, la inulina produciría saciedad en individuos de peso normal principalmente, aunque no se encontró en la literatura que el estado nutricional de los voluntarios interfiriera en los resultados de la regulación de la saciedad. No obstante, faltan pruebas concluyentes para determinar si en realidad la efectividad de la inulina no se ve alterada por las diferencias en el estado nutricional de las personas (46).
Aun cuando no se ha demostrado completamente el efecto regulador de la saciedad de la inulina por sí sola, se ha sugerido el siguiente mecanismo de acción que puede ayudar a complementar la sensación de saciedad de otras preparaciones. A través de la fermentación producida por las bifidobacterias y lactobacilos, la inulina produce ácidos grasos de cadena corta (AGCC) (24). Meléndez et al. (30) declaran que
el acetato, el propionato y el butirato son los ácidos grasos de cadena corta más importantes y su producción depende del tipo de prebiótico que llega al colon; por ejemplo, la inulina genera la formación de más butirato porque, al parecer, su fermentación es más lenta; en cambio, cuando la fermentación es más rápida, se forma de preferencia más propionato y acetato. (p. 3)
El butirato interactúa con los receptores FFAR3 (Free Fatty Acid Receptor 3), estimulando la producción de péptidos anorexigénicos como PYY y GLP-1 (55). La inulina también logra una importante fermentación a acetato y lactato, actuando a través de FFAR2 para influir en las vías de diferenciación celular y promover una mayor liberación del PYY (46). El aumento de la densidad de las células L proporciona al colon un mayor potencial para la liberación de PYY, reduciendo la ingesta de alimentos (56,57). El mecanismo por el cual PYY produce su efecto anorexígeno es la inhibición de la actividad eléctrica de las terminales sinápticas de neuronas productoras de neuropéptido Y (NPY) y, finalmente, por la activación de las neuronas productoras de proopiomelanocortina (POMC), las cuales son anorexigénicas (58). El GLP-1 estimula la liberación de insulina, disminuye la secreción ácida del estómago y lentifica el llenado gástrico, produciendo sensación de saciedad al activar las células del área postrema y los receptores hipotalámicos de la saciedad (59).
CONCLUSIONES
Los estudios revisados en el presente artículo no son suficientes para afirmar que la inulina por sí sola genera un efecto de saciedad en humanos. Sin embargo, se ve un efecto potenciador de la saciedad al ser añadido a algunas preparaciones que producen saciedad individualmente. Es necesario realizar mayores investigaciones. No obstante, tan solo un consumo diario de inulina en dosis entre 6-10 g permite generar diversos efectos beneficiosos para el organismo.