Introducción
El enclave seco del Cañón del río Chicamocha tiene zonas áridas con una rica avifauna, lo que la ha convertido en un Área de Importancia para la Conservación de las Aves - AICA (Franco et al., 2009). Su orografía tiene un gradiente altitudinal entre 300 y 2300 m n. s. m, favoreciendo el establecimiento de variados hábitats para las aves. En la región se puede encontrar bosque seco tropical, bosque seco premontano, bosque de cañada, bosque de roble mixto, matorral xerofítico, humedales, helechales y afloramientos rocosos (Albesiano et al., 2003; Camargo-Ponce & Agudelo-Álvarez, 2017). De igual manera, la marcada estacionalidad de la cordillera Oriental, ha permitido que algunas especies desarrollen adaptaciones particulares para sobrevivir a las condiciones extremas de sequía, por lo que se encuentra un alto número de endemismos en diferentes grupos taxonómicos en esta región (Hernández-Camacho et al., 1992; Pennington et al., 2006; Chaparro-Herrera et al., 2013).
Lamentablemente, solo un 20 % del área se encuentra protegida bajo alguna figura de conservación de biodiversidad (Franco et al., 2009; Collazos-González & Echeverry-Galvis, 2017), considerándose una región vulnerable a la presión humana (Etter et al., 2017; http://datazone.birdlife.org). En el área aún se encuentran remanentes de bosque seco tropical (BST), un ecosistema fuertemente amenazado por la fragmentación y consecuente pérdida de hábitat, lo que en última instancia afecta a las especies con algún grado de vulnerabilidad (Sánchez-Azofeifa et al., 2005; Miles et al., 2006; Portillo-Quintero et al., 2010; Pizano et al., 2014). Esta condición ha llevado a que extensas áreas del cañón se transformen, amenazando los hábitats y las especies que lo habitan (Delgadillo-Méndez & Delgadillo-Méndez, 2013), y alterando, además, el suministro de agua para las poblaciones humanas de la región. Estos tensores y limitantes hacen prioritario el establecimiento de estrategias integrales que protejan sus valores ecológicos y culturales (Delgadillo-Méndez & Delgadillo-Méndez, 2013).
A pesar de la marcada estacionalidad en su precipitación y las fuertes presiones antrópicas que han sufrido sus ecosistemas, aún es posible observar en el cañón numerosas especies que merecen ser conservadas, por el aporte que pueden tener a la funcionalidad de los mismos (Albesiano & Fernández, 2006; Valencia-Duarte et al., 2012; Etter et al., 2017). En el cañón se pueden encontrar remanentes de vegetación en los cuales hay especies de aves endémicas y amenazadas, entre las cuales se encuentran dos especies focales: el cucarachero de Nicéforo (Thryophilus nicefori) y el colibrí amazilia ventricastaño (Amazilia castaneiventris) (Cortés-Herrera et al., 2016; Collazos-González & Echeverry-Galvis, 2017). No obstante, a pesar de las condiciones únicas de este territorio, la información disponible acerca de la ecología de sus aves es escasa, de modo que es necesario continuar construyendo conocimiento en este tema y, así plantear herramientas para reducir la vulnerabilidad de las especies (Pizano et al., 2014, Collazos-González & Echeverry-Galvis, 2017).
En el Cañón del Chicamocha se han llevado a cabo algunos estudios publicados e inéditos que aportan a la comprensión de su avifauna (Valderrama, 2005, Chaves-Portilla & Cortés-Herrera, 2006; Vargas, 2007; Valderrama et al., 2008; Parra et al., 2010; Gómez & Robinson, 2014; Collazos-González, 2015, Collazos-González, 2016; Collazos-González & Echeverry-Galvis, 2017; Zuluaga-Carrero, 2017; Rico-Guevara, 2018; Orozco-Romero, 2018). Estos estudios permitieron construir el presente listado de especies y reconocer las áreas en las cuales hay mayores necesidades de investigación, así como identificar otras áreas de importancia que podrían requerir acciones concretas de conservación y restauración. Finalmente, esperamos que esta revisión adicione de forma relevante conocimiento a un territorio que está nominado a ser Patrimonio de la Humanidad (UNESCO, 2012), aportando información notable sobre el estado actual de su avifauna.
Materiales y métodos
Área de estudio.
El Cañón del Chicamocha se encuentra ubicado en la vertiente occidental de la cordillera Oriental de los Andes colombianos, entre los departamentos de Boyacá y Santander (Figura 1). Se extiende de sur a norte y pertenece al sistema occidental de la cuenca hidrográfica del río Magdalena (Franco et al., 2009). Hace parte de la provincia biogeográfica de valle medio del río Chicamocha, incluida en el distrito del Cañón del Chicamocha de la provincia geográfica norandina, región árida aislada que estuvo antiguamente unida con las sabanas y bosques secos del valle de Magdalena y el Caribe (Hernández-Camacho et al., 1992). Formado hace 46 millones de años, el Cañón del Chicamocha es uno de los 58 centros de endemismo del país, y cubre alrededor de 3342 km2 en una longitud de 244 km (UNESCO, 2012; Etter et al., 2017). Es uno de los enclaves secos más extensos de Colombia y contiene la mayor cantidad de especies de flora y fauna endémicas en zonas xerofíticas y subxerofíticas (Díaz-Merlano & Roberton, 2013).
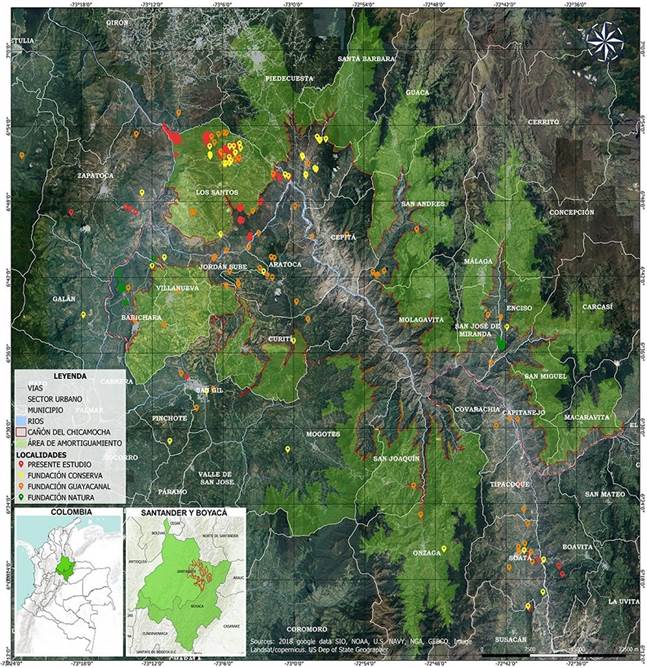
Figura 1 Localidades en las que se han realizado investigaciones sobre la avifauna del Cañón del Chicamocha, Colombia.
En este enclave árido interandino predominan las pendientes fuertes y suelos pedregosos superficiales que presentan procesos avanzados de erosión (Guzmán, 2015; Camargo-Ponce & Agudelo-Álvarez, 2017). El clima está fuertemente afectado por la topografía, en la cual hay valles con una profundidad aproximada de dos kilómetros hacia la localidad del Tabacal y laderas de hasta 71° de inclinación en otras localidades (Díaz-Merlano, 2013; Guzmán, 2015). Según la clasificación de Caldas-Lang (1962) comprende los pisos climáticos cálido árido en zonas bajas, cálido semiárido en alturas medias y templado semihúmedo en sus partes altas (Camargo-Ponce & Agudelo-Álvarez, 2017). En las partes bajas en el bosque muy seco se registran precipitaciones entre 100 y 500 mm y en bosque seco entre 1000 y 2000 mm, con temperaturas que oscilan entre 24 y 32°C; además, en las partes húmedas (>1500 m s. n. m.) las temperaturas pueden estar entre 20 y 24 °C (Albesiano et al., 2003; Valencia et al., 2012). Su estacionalidad está marcada por la distribución de lluvias, siendo los meses de octubre y noviembre los más húmedos del año (Guzmán, 2015).
La vegetación caducifolia del cañón se caracteriza por poseer plantas con hojas pequeñas, con uno o dos estratos de follaje, por lo que la capacidad de retención de humedad es limitada (Albesiano & Rangel, 2006; Camargo-Ponce & Agudelo-Álvarez, 2017). Predominan coberturas vegetales de matorrales microfilo-crasicaule, matorrales nanófilos y pastizales áridos (Albesiano et al., 2003), comprende cinco zonas de vida principales: bosque seco tropical (Bs-T), bosque muy seco tropical (Bms-T), monte espinoso premontano (me-PM), bosque seco premontano (Bs-PM) y bosque húmedo premontano (Bh-PM; Holdridge, 1987). El área de estudio comprende un rango altitudinal entre los 300 m s. n. m. del río Suárez y Chicamocha, hasta los 1904 m s. n. m. en las cotas más altas en la Mesa de Xéridas en Los Santos, Santander y Boavita (Boquerón), Boyacá (Figura 1 y Figura 2).

Fotografías: Juliana Zuluaga-Carrero y Oswaldo Cortés-Herrera.
Figura 2 Paisajes de algunas localidades de estudio visitadas en el Cañón del Chicamocha, Colombia. Santander: A, Jordán-Los Santos; B, Los Fríos-Los Santos; C, La Purnia-Los Santos; D, La Mojarra-Los Santos. Boyacá: E y F, Soatá.
Recolección de datos. El listado se elaboró con datos obtenidos en varias localidades del cañón. Se realizó una síntesis de las observaciones hechas en diferentes localidades en esta región, en los años 2004 y 2008 (Cortés-Herrera, 2004; Cortés-Herrera, 2006; Valderrama et al., 2008; Parra et al., 2010) y en tres quebradas en la Mesa de Xéridas, en el departamento de Santander, en el año 2014 (Camargo-Ponce & Agudelo-Álvarez, 2017; Collazos-González & Echeverry-Galvis, 2017; Zuluaga-Carrero, 2017 ; Figura 1 y Tabla 1).
Adicionalmente esta revisión está basada en la investigación de Zuluaga-Carrero (2017) y Collazos-González & Echeverry-Galvis (2017), quienes obtuvieron una representatividad de muestreo del 94% y 79% para el municipio de Los Santos. En estos estudios se hicieron observaciones directas en campo, acompañadas con registros auditivos y, como método complementario, en algunas localidades se utilizaron redes de niebla con 18 900 metros/hora/red (Collazos-González & Echeverry-Galvis, 2017).
Tabla 1 Localidades con registros de aves en el Cañón del Chicamocha, Colombia. Se incluye tanto la información de las bases de datos del presente estudio como otras localidades consultadas en: A, Instituto de Ciencias Naturales - ICN; B, Instituto Alexander von Humboldt - IAvH; C, Xeno-canto; D, Global Biodiversity Information Facility - GBIF.
| Municipio | Latitud | Longitud | Rango de elevación | Base de datos |
|---|---|---|---|---|
| Aratoca | 6.4446 | -73.3190 | 900 | Presente estudio y A |
| Barichara | 6.6403 | -73.2245 | 750-1300 | Presente estudio, C y D |
| Boavita | 6.1903 | -72.3731 | 1660-1904 | Presente estudio, A y D |
| Butaregua | 6.3955 | -73.1413 | 1300-1400 | Presente estudio |
| Curití | 6.3654 | -73.0000 | 1300-1500 | Presente estudio |
| Encino | 6.3627 | -72.4213 | 1350-1480 | Presente estudio |
| Galán | 6.3912 | -73.1750 | 900-950 | Presente estudio |
| Jordán | 6.4224 | -73.0231 | 400-450 | Presente estudio |
| Los Santos | 6.8846 | -73.1690 | 313-1649 | Presente estudio, C y D |
| Mogotes | 6.2819 | -73.0231 | 1700-1750 | Presente estudio |
| Onzaga | 6.2024 | -72.4716 | 1900-1953 | Presente estudio |
| Pescadero | 6.4959 | -73.0000 | 600 | Presente estudio y A |
| Piedecuesta | 6.5919 | -73.0301 | 1000-1100 | Presente estudio, A y B |
| Pinchote | 6.2859 | -73.1031 | 1100-1131 | Presente estudio |
| San Gil | 6.3462 | -73.9437 | 1168-1200 | Presente estudio, B y C |
| Soatá | 6.1934 | -72.3915 | 1428-1639 | Presente estudio, A, C y D |
| Susacón | 6.1542 | -72.4044 | 1770-1800 | Presente estudio |
| Tipacoque | 6.2528 | -72.4046 | 1840-1900 | Presente estudio |
| Villanueva | 6.4333 | -73.1056 | 300-1450 | Presente estudio |
| Zapatoca | 6.8901 | -73.1769 | 317-1011 | Presente estudio y C |
Con el fin de complementar el listado, revisamos información secundaria (Gómez & Robinson, 2014; Collazos-González, 2015; Collazos-González, 2016; Rico-Guevara, 2018; Orozco-Romero, 2018), e informes técnicos de organizaciones no gubernamentales (Serrano et al., 2009; Ciri et al., 2011; Melo et al., 2012; Pardo & Moreno-Arias, 2018).
Adicionalmente, revisamos las bases de datos del Instituto Alexander von Humboldt (IAvH, 2017), del Instituto de Ciencias Naturales de la Universidad Nacional de Colombia (ICN, 2019), del Global Biodiversity Information Facility GBIF (Montealegre, 2018) y el portal web Xenocanto Foundation (Xenocanto, 2019; Tabla 1). Los registros se validaron verificando su distribución espacial y altitudinal, soportando algunos registros con audios o fotografías, para así determinar con certeza la presencia de la especie en el área de estudio. El listado fue ordenado filogenéticamente siguiendo la clasificación sugerida por el Comité de Clasificación de Aves de Sur América (SACC, 2019) y posteriormente corroborado con las guías y listados de aves de Colombia (Hilty & Brown 1986; Avendaño et al., 2017; Ayerbe-Quiñones, 2018) y conversaciones personales con observadores expertos del país.
Las especies con rango restringido las clasificamos de acuerdo a su estatus de endemismo (Chaparro-Herrera et al., 2013), como Endémica de Colombia (E) o Casi endémica de Colombia (CE). Los hábitos de migración y residencia fueron asignados según las características de orientación geográfica sugeridas por Naranjo et al. (2012) y Avendaño et al. (2017). Adicionalmente se añadieron al listado los nombres comunes en español según la plataforma web Avibase (2019).
Resultados
Se agruparon todos los registros de las especies correspondientes a 20 municipios (Tabla 1 y Figura 1). El municipio que contó con el mayor número de registros fue Los Santos, mientras que los municipios de Curití, Galán, Jordán, Mogotes, Onzaga, Pinchote, Tipacoque y Villanueva, cuentan con el menor número de observaciones. Se obtuvo un total de 291 especies para el Cañón del Chicamocha (Anexo 1), incluidas en 20 órdenes, 50 familias y 216 géneros. La avifauna está compuesta por 238 especies residentes, 53 especies migratorias, 51 de ellas migrantes latitudinales-transcontinentales boreales y dos australes, así como 20 especies que migran local y altitudinalmente (Naranjo et al., 2012). Se registraron siete especies endémicas y doce casi endémicas, ocho de ellas en alguna categoría de amenaza a nivel nacional y mundial; dos Casi Amenazadas, cuatro Vulnerables, una En Peligro y una En Peligro Crítico (Renjifo et al., 2016).
Las familias mejor representadas fueron Tyrannidae (49 especies, 16.2 %), Thraupidae (25, 8.8 %), Trochilidae (25, 8.8 %) y Parulidae (18, 6.1 %). Dentro de estas familias las especies con el mayor número de registros para el Cañón del Chicamocha, tanto en las investigaciones realizadas por los autores, como en las fuentes secundarias consultadas y bases de datos, fueron: Amazilia castaneiventris, Campylorhynchus griseus, Columbina talpacoti, Crotophaga ani, Dendroplex picus, Leptotila verreauxi, Momotus subrufescens, Myiarchus apicalis, Myiozetetes cayanensis, Setophaga pitiayumi, Stilpnia vitriolina, Thraupis episcopus, Thraupis palmarum, Tiaris bicolor, Todirostrum cinereum y Troglodytes aedon. Se encontró un menor número de registros para aves de hábitos nocturnos y especies acuáticas, lo que está relacionado con los limitados muestreos nocturnos, así como también con los pocos cuerpos de agua presentes en el área de estudio (Anexo 1).
Discusión
El listado de especies obtenido en esta revisión representa el 15 % de las especies registradas para Colombia (Avendaño et al., 2017). El número de especies registradas hasta el momento para el Cañón del Chicamocha era de 104 (Parra et al., 2010), cifra que se incrementa considerablemente con el presente estudio alcanzando casi el triple de las especies. Así mismo, al comparar este listado con lo reportado para otros bosques secos en el país, encontramos que, se comparte un 70% de las especies de los valles interandinos en el departamento del Tolima, en donde se registran un total de 297 especies. De igual manera, en este listado se reporta el doble de las especies que han sido registradas para las franjas de bosque seco tropical entre los departamentos de Cundinamarca, Huila y Tolima, que documentan 145 especies (Gómez & Robinson, 2014), un 37.7 % más de las especies que han sido reportadas para el bosque seco tropical en el departamento del Cauca, con 212 especies (Ayerbe-Quiñones & López-O, 2011), un 52% más de las especies reportadas recientemente para el bosque seco tropical de Norte de Santander, con 140 especies, y un 53% más de las especies reportadas para el sur del Valle del Magdalena, con 127 especies (Avendaño et al., 2018; Espejo & Morales, 2019). Considerando dichas cifras, se puede decir que el Cañón del Chicamocha es una de las regiones de bosque seco tropical más diversas en avifauna.
Al revisar los registros de los 20 municipios, se observaron especies que se encuentran en peligro de extinción en el país, como el colibrí amazilia ventricastaño (A. castaneiventris), especie categorizada En Peligro (EN) (Renjifo et al., 2016). Aunque esta especie es una de las que tuvieron un mayor número de registros, su distribución se restinge al área de estudio. Este colibrí fue redescubierto en el año 2003 en el municipio de Soatá, departamento de Boyacá (Cortés-Herrera, 2004). Para entonces, se desconocían sus rasgos de historia de vida, como preferencias alimenticias, requerimientos de hábitat, ecología y comportamiento. En algunos estudios, los registros de la especie permitían establecer un rango de distribución entre 850 y 2220 m s.n.m (Parra et al., 2010). Sin embargo, a partir de los registros obtenidos en este estudio y las observaciones que se han hecho, particularmente en la localidad de Los Santos, deducimos que esta especie se encuentra entre 120 y 2230 m s.n.m.
De igual manera encontramos registros para el cucarachero de Nicéforo (T. nicefori), especie categorizada en Peligro Crítico (CR) (Renjifo et al., 2016), contando con un número limitado de registros en el área de estudio. De esta especie endémica del cañón, hace unos años solo se conocía una población de pocos individuos en el municipio de San Gil, Santander (Valderrama et al., 2005; Parra et al., 2010), y según Collar et al. (1992) se estimaba que su rango altitudinal podría encontrarse entre 1050 y 1250 m s. n. m. En estudios más recientes, la especie ha sido registrada con mayor frecuencia en las zonas húmedas de los escarpes rocosos y los bosques de cañada de las laderas del cañón (Parra et al., 2016; Collazos-González & Echeverry-Galvis, 2017), así como también hacia los bosques más húmedos de Zapatoca (Zuluaga-Carrero obs. pers). Esta información nos permite, por una parte confirmar la distribución de la especie en la localidad de San Gil, y por otra, indicar la extensión hacia las localidades de Los Santos, Galán, Zapatoca y Barichara, registros con los que planteamos una posible ampliación en su rango de distribución altitudinal a zonas más secas, que estaría desde los 680 hasta los 2100 m s. n. m.
Igualmente, en este extenso territorio hay otras especies endémicas para el país, entre ellas la guacharaca colombiana (Ortalis columbiana), el colibrí amazilia frentiazul (Amazilia cyanifrons), el atrapamoscas apical (Myiarchus apicalis) y la subespecie de cucarachero chupahuevos (Campylorhynchus griseus bicolor; Chaparro-Herrera et al., 2013; Figura 3).

Fotografías: Sergio A. Collazos-González.
Figura 3 Especies focales de aves importantes para la conservación en el Cañón del Chicamocha, Colombia. A, cucarachero de Nicéforo (Thryophilus nicefori); B, amazilia ventricastaño (Amazilia castaneiventris); C, turpial guajiro (Icterus icterus); D, pinzón alidorado (Arremon schlegeli canidorsum); E, cucarachero chupahuevos (Campylorhynchus griseus bicolor).
Otras subespecies de interés para la conservación son el pinzón alidorado (Arremon schlegeli canidorsum) y el turpial guajiro (Icterus icterus ridgwayi), que actualmente enfrentan un declive en sus poblaciones por pérdida y fragmentación de hábitat, y se encuentran en categoría Vulnerable (VU) (Renjifo et al., 2016). El pinzón alidorado es frecuentemente registrado en matorrales subxerofíticos en las laderas de los ríos Suárez, Chicamocha y Sogamoso; mientras que el turpial guajiro se observa constantemente en zonas secas de la Mesa de Xéridas en el municipio de los Santos y Piedecuesta, entre la cuenca media de los ríos Chicamocha y Sogamoso, alimentándose de especies de cactos como la pitahaya (Cereus hexagonus), el turmeperro (Opuntia stricta), el tuno (Opuntia schumannii) y el cardón (Stenocereus griseus) (Beltrán et al., 2016; Espejo et al., 2016; Zuluaga-Carrero, 2017; S. Collazos obs. pers).
También, registramos especies casi endémicas, como periquito de anteojos (Forpus conspicillatus), zumbador ventriblanco (Chaetocercus heliodor), esmeralda de pico rojo (Chlorostilbon gibsoni), esmeralda colicorta (Chlorostilbon poortmani), amazilia verdiazul (Amazilia saucerrottei), ala de sable violeta (Campylopterus falcatus), batará crestibarrado (Thamnophilus multistriatus), tángara dorsirroja (Ramphocelus dimidiatus), tángara matorralera (Stilpnia vitriolina), gorrión montés cabecinegro (Arremon atricapillus), reinita gorgigrís (Myiothlypis cinereicollis) y jilguero andino (Spinus spinescens) (Chaparro-Herrera et al., 2013; Avendaño et al., 2017).
Registramos 51 especies de migrantes transcontinentales del norte, destacándose la presencia del pibí boreal (Contopus cooperi) y la reinita cerúlea (Setophaga cerulea), migrantes boreales que se encuentran dentro de las categorías Casi Amenazada (NT) y Vulnerable (VU), respectivamente (BirdLife International, https://www.birdlife.org/). De otro lado, solo obtuvimos registros de dos especies australes, el fiofío piquicorto (Elaenia parvirostris) y la tijereta sabanera (Tyrannus savana) (Naranjo et al., 2012).
Sobresale la presencia de poblaciones estables del atrapamoscas risquero (Hirundinea ferruginea) en zonas de altos escarpes que rodean el Cañón entre los 1300 y 1700 m s. n. m. (S. Collazos obs. pers; J. Zuluaga-Carrero obs. pers; Lopera-Salazar & Chaparro-Herrera, 2017) y observaciones del águila paramuna (Geranoaetus albicaudatus) a 1495 m s. n. m. en los escarpes de la Mesa de Xéridas (Parra et al., 2010; S. Collazos obs. pers; F. Ayerbe com. pers), registros muy por debajo de su rango de elevación para el país.
Encontramos un mayor número de localidades muestreadas en la literatura en el municipio de Los Santos, en el cual se registran el mayor número de especies, lo que probablemente sea resultado de un mayor esfuerzo de muestreo. En esta localidad se resaltan características como la heterogeneidad del paisaje, la diversidad de coberturas presentes a través de su gradiente altitudinal y la accesibilidad, que facilitan su estudio (Figura 2). Por otra parte, se debe continuar haciendo investigación en las localidades de Curití, Galán, Jordán, Mogotes, Onzaga, Peña Colorada, Pinchote, Tipacoque y Villanueva, en las cuales se encuentra un menor número de observaciones.
Las investigaciones realizadas por diferentes organizaciones estuvieron dirigidas al levantamiento de información de línea base de biodiversidad en varias zonas del Cañón del Chicamocha, muchas de ellas con el objeto de consolidar sitios de importancia para la conservación de la flora y fauna regional, teniendo como estrategia la creación de áreas protegidas (Parra et al., 2010). Se destacan los estudios para la declaración del Cañón del Chicamocha como área natural protegida, en jurisdicción de los municipios de Enciso, Capitanejo y San José de Miranda; la declaración de una área protegida de carácter público-regional y la formulación del plan de manejo del distrito de manejo integrado cañón del río Chicamocha en la subcuenca del río Umpalá, cuya información brinda oportunidades para la conservación de sus hábitats (Serrano et al., 2009; Ciri et al., 2011; Melo et al., 2012). No obstante, aún con estos trabajos las áreas protegidas dentro del Cañón siguen siendo mínimas para proteger especies focales y principalmente para el bosque seco tropical, el ecosistema más amenazado del país (Miles et al., 2006; Pizano et al., 2014; Etter et al., 2017).
Recientemente, se han llevado a cabo proyectos a distintas escalas, relacionados principalmente con la presión de transformación del área y su efecto en la riqueza de aves de la región (Camargo-Ponce & Agudelo-Álvarez, 2017; Pardo & Moreno-Arias, 2018). A partir de ellos, se han podido plantear como factores determinantes de la no persistencia de la avifauna, los procesos de erosión y escasez de agua, presiones antrópicas y la variabilidad ocasionada por el cambio climático (Collazos-González, 2016; Camargo-Ponce & Agudelo-Álvarez, 2017; Orozco-Romero, 2018). Los proyectos mencionados han permitido plantear e implementar iniciativas de manejo y uso, estrategias de restauración ecológica y monitoreos de biodiversidad (Collazos-González, 2015; Collazos-González, 2016; Camargo-Ponce & Agudelo-Álvarez, 2017; Orozco-Romero, 2018). Es necesario ampliar la información, dirigiendo esfuerzos hacia el conocimiento ecológico e historia natural de las especies focales, con el objeto de disminuir sus amenazas (Piñeros-Quiceno, 2017). Asimismo, estas iniciativas deben incluirse en diferentes escenarios e instrumentos de planificación a partir de proyectos de educación ambiental y participación comunitaria (Hoyos et al., 2019).
Como lo definen Renjifo et al. (2016) y Piñeros-Quiceno (2017) es el momento de implementar iniciativas de gran alcance para llenar los vacíos en la representación de la biodiversidad, con el fin de garantizar la supervivencia de las especies amenazadas, incluyendo mayores esfuerzos en la creación de áreas protegidas en hábitats poco representados, como los bosques secos del valle del río Chicamocha, considerados AICA, y que cuenta con especies de aves prioritarias para la conservación (Franco et al., 2009). Proponemos que se inicien prioritariamente planes de manejo en las especies focales mencionadas, los cuales pueden ser desarrollados desde la academia, organizaciones locales, autoridades ambientales y ONGs. Igualmente, para que su divulgación y protección sea efectiva, se plantea el aviturismo comunitario rural como estrategia de construcción de oportunidades económicas y espacios para la conservación participativa de la avifauna del cañón (Maldonado et al., 2016). Dentro del marco de la iniciativa global Alianza para la Cero Extinción (ACE) y el AICA, consideradas como Áreas Clave para la Biodiversidad, se tendría un mayor alcance para dirigir iniciativas de conservación y manejo de hábitats, lo que aportaría al mantenimiento de los últimos remanentes de las poblaciones de especies evaluadas, como T. nicefori y A. castaneiventris (Cáceres et al., 2015; Piñeros-Quiceno, 2017).
El cañón del Chicamocha es un epicentro para comprender cómo la avifauna se mantiene en condiciones climáticas extremas y constantes presiones antrópicas. El cañón es potencialmente una de las áreas más diversas del país con remanentes de bosque seco, siendo prioritario establecer una figura regional o nacional de conservación que brinde protección a su biodiversidad. De igual forma, al albergar especies focales, ofrece mayores retos para comprender el estado de sus poblaciones, ya que con nuestros registros hemos evidenciado cambios en su distribución vertical. Es preciso tomar medidas para la planeación y el ordenamiento del territorio, incluyendo los actores que han configurado el paisaje actual y que influyen e inciden en la distribución y permanencia de las aves de esta región.















