Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Universidad y Salud
Print version ISSN 0124-7107On-line version ISSN 2389-7066
Univ. Salud vol.16 no.1 Pasto Jan./June 2014
Complicaciones asociadas y análisis de supervivencia de niños con leucemias agudas tratados con el protocolo BFM-95
Associated complications and survival analysis in children with acute leukemia treated with BFM-95 protocol
Julio Alejandro Peña1, Jesús Andrés Pantoja2, Ángela Milena Acosta3, Elehonora Argotty-Pérez4, Ana Cristina Mafla5
1 Estudiante Programa de Medicina. Fundación Universitaria San Martín. Pasto, Colombia. e-mail: jalejandro91@hotmail.com
2 Estudiante Programa de Medicina. Fundación Universitaria San Martín. Pasto, Colombia. e-mail: jpantoja250@hotmail.com
3 Estudiante Programa de Medicina. Fundación Universitaria San Martín. Pasto, Colombia. e-mail: angelm2806@hotmail.com
4 Especialista en Salud Pública. Coordinadora de Investigación. Fundación Universitaria San Martín. Pasto, Colombia. e-mail: eargottyp@hotmail.com
5 Magíster en Salud Pública. Docente, Investigadora. Fundación Universitaria San Martín. Pasto, Colombia. e-mail: anamafla@sanmartinpasto.com
Fecha de recepción: Marzo 11 - 2013 / Fecha de aceptación: Mayo 13 - 2014
Resumen
Objetivo: Determinar las complicaciones y porcentaje de supervivencia de niños con leucemia linfoide y mieloide aguda tratados con el protocolo Berlin-Frankfurt-Münster 95 (BFM-95) de Enero de 2008 a Diciembre de 2010 en el Hospital Infantil "Los Ángeles". Materiales y métodos: Una cohorte retrospectiva fue diseñada para evaluar a niños tratados con el protocolo BFM-95 durante tres años en el Hospital Infantil "Los Ángeles". La información fue obtenida de los datos demográficos del paciente, complicaciones asociadas con el protocolo BFM-95 y supervivencia. Los datos fueron recolectados de las historias médicas y los reportes de fallecimiento del hospital. Las variables nominales fueron presentadas como proporciones y las variables continuas fueron expresadas como medias y desviaciones estándares. El análisis de supervivencia fue realizado por el método Kaplan-Meier. Los datos fueron analizados usando el programa Statistical Package for Social Sciences, version 17,0 (SPSS Inc., Chicago, Illinois, USA). Resultados: Cincuenta y dos niños fueron incluidos en este estudio. De todo el grupo, 47 (90,4%) tuvieron leucemia linfoide aguda y 5 (9,6%) leucemia mieloide aguda. Treinta y cinco (67,3%) presentaron complicaciones. Veintitres niños (65,7%) mostraron complicaciones infecciosas siendo las más frecuentes. El análisis de supervivencia de Kaplan-Meier mostró que los pacientes con complicaciones tuvieron un tiempo más corto de supervivencia comparado a los pacientes sin complicaciones. Conclusiones: La incidencia de complicaciones fue elevada. El análisis Kaplan-Meier reveló diferencias entre la leucemia linfoide aguda y leucemia mieloide aguda de acuerdo a las complicaciones.
Palabras clave: Leucemia linfoide aguda, leucemia mieloide aguda, niño, complicaciones, análisis de supervivencia, epidemiología. (Fuente: DeCS, Bireme).
Abstract
Objective: To determine complications and survival percentage in children suffering from acute lymphoid and myeloid leukemia treated with Berlin-Frankfurt-Münster 95 (BFM-95) protocol from January 2008 to December 2010 at Los Ángeles Children Hospital. Materials and methods: A retrospective cohort was designed to evaluate children treated with BFM-95 protocol during three years at Los Ángeles Children Hospital. The Information was obtained from the patient demographics, complications associated with BFM-95 protocol and survival. Data were collected from medical records and hospital decease reports. Nominal variables were presented as proportions and the continuous variables were presented as means and standard deviations. The survival analysis was performed using Kaplan-Meier method. Data were analyzed using the Statistical Package for Social Sciences, 17.0 version software (SPSS Inc., Chicago, Illinois, USA). Results: Fifty two children were included in this study. From the whole group, 47 (90.4%) had acute lymphoid leukemia and 5 (9.6%) had acute myeloid leukemia. Thirty five (67.3%) presented complications. Twenty three children (65.7%) had infectious complications, being the most frequent ones. Kaplan-Meier survival analysis showed that patients with complications have shorter survival time compared to patients with no complications. Conclusions: The incidence of complications was high in children treated with BFM-95 protocol. Kaplan-Meier analysis revealed differences between acute lymphoid leukemia and acute myeloid leukemia according to complications.
Key words: Acute lymphoid leukemia, acute myeloid leukemia, child, complications, survival analysis, epidemiology. (Source: DeCS, Bireme).
Introducción
La leucemia en la infancia es un cáncer del sistema hematopoyético, que involucra la transformación maligna de células progenitoras.1 Ésta inicia en la médula ósea, puede invadir la sangre y extenderse a otras partes del cuerpo.
Existen dos tipos de leucemia de acuerdo a su manifestación clínica, las de tipo agudo y crónico. Entre las de tipo agudo están las linfoides como leucemia linfoide aguda (LLA) que representa aproximadamente 3 de cada 4 casos de leucemia infantil. Este tipo de leucemia se inicia en las células linfoides de la médula ósea, es decir, es un cáncer de las células productoras de linfocitos, que se llaman linfoblastos.2 De la misma manera, está la leucemia mieloide aguda (LMA), que es un cáncer de las células tempranas (inmaduras) de la médula ósea como eritroides y granulocíticas.3
Se ha establecido que en menores de 15 años, la incidencia de LLA oscila entre 20 a 35 casos por millón.4 Por otro lado, las leucemias en Suramérica, en países como Colombia y Ecuador tienen las tasas de incidencia más altas con 6 casos nuevos por c/100.000 en < 15 años (tasas ajustadas por edad) en niños y 5,6 casos nuevos por c/100.000 en < 15 años en niñas.5
Las estimaciones para Colombia en 2002 fueron de 2.081 casos nuevos de cáncer y 1.181 muertes por cáncer en < 15 años; de éstos, las leucemias aportaron 814 casos nuevos y 608 muertes, con una proporción similar en niños y niñas. Para el año 2005, se registraron en Colombia 18.400 defunciones en < de 15 años, de las cuales 833, (4,5%) fueron cánceres. De éstas, 377 (45%) fueron leucemias de cualquier tipo.6
En el ámbito internacional cerca de 30% de las neoplasias malignas que se presentan en niños son leucemias, y de éstas más de 75% son LLA.7
En relación con el tratamiento, en la LLA, aproximadamente de 1 a 3% de los pacientes mueren durante la terapia de Inducción y otro 1 a 3% muere durante la remisión inicial por complicaciones asociadas con el tratamiento.8
En la actualidad, se trata a la mayoría de los niños recién diagnosticados con LLA sin radiación craneal; muchos grupos administran la radiación craneal sólo a aquellos pacientes considerados con riesgo más alto de recaída posterior del SNC, como aquellos con leucemia del SNC documentada en el momento del diagnóstico (>5 GB/µl con blastocitos; SNC3) o fenotipo de células T con recuento alto de GB.9 El compromiso testicular manifiesto en el momento del diagnóstico se presenta en aproximadamente 2% de los varones. En los primeros ensayos de LLA, este compromiso en el momento del diagnóstico era uno de los factores pronósticos adversos. Sin embargo, con un tratamiento inicial más enérgico no es claro el significado del pronóstico del compromiso testicular inicial.10
En relación con las complicaciones, los niños con LMA quienes normalmente reciben quimioterapia intensiva durante el tratamiento tienen un riesgo elevado de morbi-mortalidad por infecciones invasivas.11 Al respecto, la literatura reporta que estas infecciones son la principal causa de muerte en LMA.12 Lehrnbecher et al.,13 reportan en esta enfermedad la aparición de fiebre sin una causa identificable, infecciones en el flujo sanguíneo por hongos y neumonía en el tratamiento con el protocolo BFM-93.
Por otro lado Portwine et al.,14 reportan que la presencia de estas infecciones difieren según la presencia o no de neutropenia. Creutzig et al.,15 muestran que los pacientes con LMA tratados con BFM-93 y BFM-98 murieron en un tiempo corto después del diagnóstico o como resultado de complicaciones relacionadas al tratamiento. El primer día de tratamiento resultó en sangrado o leucoestasis, hiperleucoestasis e infecciones por bacterias y hongos.
De acuerdo, con las complicaciones posttratamiento, Veringa et al.,16 en 2011 observaron en sobrevivientes de la infancia de LLA, un incremento significativamente más elevado de presión sistólica y diastólica. Además, en mujeres tratadas con radiación craneal se presentó más alta prevalencia y el más alto riesgo de sobrepeso y obesidad. De la misma manera, los efectos a largo plazo de la LLA y LMA pueden estar relacionados con citotoxicidad, malignidad secundaria, anormalidades endocrinas, cambios en la reproducción, déficits neurocognitivos y efectos psicosociales.17
Según la literatura internacional la supervivencia a las leucemias agudas es elevada, aunque, en casos de LMA, se reporta que de un 5 a 15% de los pacientes aún mueren por complicaciones relacionadas al tratamiento.18
El protocolo Berlin-Frankfurt-Münster 95 (BFM- 95) es un tipo de tratamiento quimioterapéutico frecuente para el manejo de pacientes con leucemias pediátricas agudas. Este fue desarrollado por el Grupo BFM y posterior al BFM-90 que introdujo en 1981 una nueva combinación de medicamentos que consistió en dos bloques diferentes de quimioterapia basados principalmente en metotrexate.19
Este protocolo se utiliza porque ha demostrado ser más efectivo, disminuye el tiempo de tratamiento y aumenta la supervivencia, especialmente en pacientes con riesgo alto.20 Sin embargo, existen pocos reportes relacionados con los principales efectos secundarios que los pacientes pueden presentar durante su aplicación y cómo influyen en la supervivencia.
En este sentido, el objetivo de este estudio fue determinar las principales complicaciones asociadas y análisis de supervivencia en el tratamiento de niños y adolescentes diagnosticados con leucemias agudas tratados con el protocolo BFM-95 que asistieron al Hospital Infantil "Los Ángeles" durante el período 2008 a 2010 en Pasto, Nariño, Colombia.
Materiales y métodos
Diseño de estudio
El tipo de estudio es observacional tipo cohorte de temporalidad retrospectiva, para evaluar la evolución de niños con diagnóstico de leucemia aguda (linfoide y mieloide) tratados con el protocolo BFM-95. La muestra incluyó a 52 niños que fueron atendidos en el período entre Enero de 2008 y Diciembre de 2010 en el Hospital Infantil "Los Ángeles", de Pasto, Nariño, Colombia (HILA).
En este estudio se incluyeron a niños y adolescentes, que fueron evaluados bajo los siguientes criterios diagnósticos de leucemia aguda: Se consideró caso confirmado de leucemia linfoide aguda pediátrica, a todo ≤ de 15 años con aspirado o biopsia de médula ósea donde el 25% o más de las células nucleadas son blastos linfoides (LLA) y de leucemia mieloide aguda pediátrica, a todo ≤ de 15 años con aspirado o biopsia de médula ósea donde el 20% o más de las células nucleadas son blastos mieloides (LMA) y para su confirmación se realizaba un análisis morfológico y citometría de flujo (inmunofenotipo).21,22
Criterios de inclusión y exclusión
De acuerdo con los criterios de selección, se incluyeron a niños y adolescentes que estuvieran en edades de 0 a 15 años, en cualquier fase de tratamiento de leucemia aguda, cuyo estado al final de estudio fuera vivo o muerto, según diagnóstico de egreso por los médicos del hospital de referencia.
En este sentido, la supervivencia global fue determinada para 120 semanas del protocolo. Por otra parte, se excluyeron a niños y adolescentes diagnosticados con leucemia crónica, quienes abandonaron el tratamiento para leucemia aguda en la fase inicial (Inducción) de la terapia y con historia clínica incompleta que permitiera el análisis de todas las variables.
Protocolo BFM-95
El protocolo BFM 95 es una modificación del protocolo BFM 90. Este protocolo establece dos tipos de tratamiento diferentes según la clasificación de la leucemia linfoide y mieloide. En forma general, el procedimiento consiste en una fase de Inducción, donde hay una reducción de 2 dosis de daunorubicina, una reducción de la dosis L-asparaginasa y un incremento en el número de veces que el metotrexate intratecal es administrado en pacientes con compromiso del SNC. Por otro lado, en la fase de Re-Inducción también es administrada a pacientes de riesgo medio y hay un incremento del número de veces que el metotrexate intratecal es administrado en pacientes con compromiso del SNC.23 El hospital Infantil "Los Ángeles", inicia el tratamiento con una Prefase (ambientación) y realiza dos fases de Mantenimiento.
Complicaciones
Las complicaciones, se catalogaron de acuerdo al protocolo de vigilancia de salud pública para leucemias agudas pediátricas en infecciosas, síndrome de lisis tumoral, trombosis, hemorragias, crisis convulsivas y otras que se presentaron durante el período de observación.
En este sentido, se registró como infecciosas a todas las alteraciones causadas por la disminución de los polimorfos nucleares asociadas a bacterias Gram-positivas como Staphylococcus aureus, Streptococcus hemolytico, Corynebacterium, o bacilos Gram-negativos, como Pseudomona aeruginosa, E. coli, bacilos como Klebsiella. Además se incluyeron infecciones por hongos como Candida albicans, Aspergillus, o fiebres persistentes.
Por otro lado, se registraron infecciones de tipo viral como herpes virus. También infecciones por pneumocystis carinii que son comunes en las vías respiratorias altas y neumonía. El síndrome de lisis tumoral (SLT) se definió como una alteración metabólica caracterizada por hiperuricemia, hiperfosfemia e hiperkalemia, asociado con frecuencia a hipocalcemia e insuficiencia renal aguda que se manifiesta dentro de los primeros 3 a 5 días de iniciada la quimioterapia. Se clasificaron como hemorrágicas, a todas las alteraciones debidas a una marcada reducción de plaquetas que facilitaron sangrado en el tracto respiratorio, digestivo, urinario o hemorragia intra-craneal.
De la misma forma, se tomó la trombosis cuando existió daño del endotelio vascular debido al tratamiento y cuando la quimioterapia produjo un estado de hipercoagulabilidad, y crisis convulsivas se diagnosticaron como efecto secundario de la toxicidad de la terapia dirigida al Sistema Nervioso Central (SNC).
En relación con otras, se definieron la mucositis como una alteración en los pacientes cuando presentaron signos de palidez de la mucosa, infiltrados gingivales, hemorragias gingivales, petequias, úlceras de la mucosa necróticas o hemorrágicas y la hipoplasia de médula ósea como una disminución de los neutrófilos (neutropenia).
Procedimiento
Una vez aprobado el proyecto de investigación por el Comité de Investigación y Ética de la Fundación Universitaria San Martín, sede Pasto, se remitió al HILA para la aprobación de su respectivo Comité de Ética y así, obtener el aval para acceder a la base de datos. Posteriormente, se solicitó autorización para revisar el protocolo de manejo y determinar la muestra tentativa de casos de leucemia aguda al Servicio de Estadística del hospital.
Para la recolección de datos de las historias clínicas se realizó una revisión retrospectiva y consecutiva en los meses de junio a noviembre de 2011, para lo cual se diseñó un formato donde se tomaron variables de tipo socio-demográfico, tipo de complicaciones, componentes del BFM-95, duración de tratamiento, y supervivencia; además, se hizo una calibración previa al trabajo de campo con base en la literatura, protocolo y experiencia. Las complicaciones fueron diagnosticadas por los médicos pedíatras del Hospital con experiencia en el manejo de leucemias agudas.
Plan de análisis estadístico
Para el análisis de la información se construyó una base de datos en el programa estadístico S.P.S.S. (Inc., Chicago, IL, USA) y se utilizaron medidas estadísticas descriptivas como tasa de incidencia anual, frecuencias y porcentajes, de tendencia central como media y su respectiva desviación estándar para variables como la edad y analíticas como Chi2 para la comparación de grupos, y de efecto e impacto como riesgo relativo con sus respectivos intervalos de confianza al 95% para las complicaciones más frecuentes y mortalidad.
El análisis de supervivencia fue realizado por medio del método de Kaplan-Meier para los niños con leucemia linfoide y mieloide aguda tratados con el protocolo BFM-95 en los años de estudio (2008-2010), de acuerdo a la presencia o no de complicaciones, teniendo en cuenta: la evolución de la patología en cada paciente, la muerte por cualquier causa y mejoría.
Aspectos éticos
El proyecto de investigación fue avalado por el Comité de Investigación y Ética de la Facultad de Medicina de la Fundación Universitaria San Martín (FUSM) Acta No. CIET–CIE 001/2011. La investigación fue diseñada en el marco de los principios éticos de la investigación biomédica del país (Resolución 13437- 1991 del Ministerio de Salud de Colombia).
Los registros encontrados fueron de uso exclusivo del grupo de investigadores y docentes relacionados con la investigación. Estos documentos se guardarán por 2 años en la Coordinación de Investigaciones de la Facultad de Medicina, cumpliendo así el principio de confidencialidad.
Resultados
El presente estudio se realizó mediante la evaluación de historias clínicas de pacientes diagnosticados con leucemia aguda pediátrica en el periodo 2008 a 2010, un total de 52 niños y adolescentes pertenecieron a esta cohorte, la media de edad fue 7,8 ± 4,0.
Las leucemias pediátricas se presentaron en edades de 7 a 15 años con 28 (53.8%) niños y adolescentes, y con picos de edad en los 5 y 9 años con un 15,4% y 9,6% respectivamente. Estas leucemias fueron mayores en sexo masculino con 29 (55,8%) casos. En relación con la distribución de sexo en la LLA se observó que 27 (57,4%) eran masculinos y 20 (42,6%) femeninos. Por otra parte, en la LMA, se presentaron 2 hombres (40%) y 3 mujeres (60%).
De acuerdo a la edad, el mayor número de casos de LLA se presentó a los 5 años con 8 pacientes (17,0%), seguido de 5 (10,6%) casos a los 8 años principalmente y en la LMA se observó 1 caso (20%) a los 2, 6, 9, 13, y 15 años lo cual no implicaba una tendencia, ya que sólo existían 5 pacientes en total.
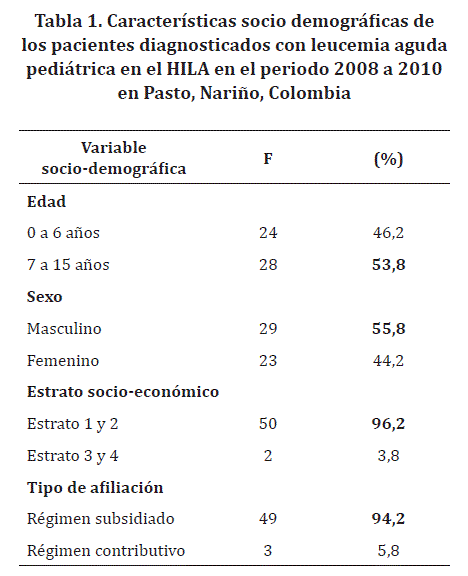
La razón hombre: mujer para LLA fue 1,35:1 y paras las LMA fue mayor en las mujeres que los hombres con 1,5:1. Estas alteraciones fueron más frecuentes en estrato 1 y 2 en 50 (96%) y en quienes pertenecían al régimen de afiliación a salud subsidiado en 49 casos (94%) (Tabla 1); lo que corresponde con la población más atendida en el HILA. De acuerdo a la temporalidad, se identificó que el mayor número de casos se observaron en los meses de febrero con 7 (13,5%), julio con 8 (15,4%) y septiembre con 9 (17%) según mes de ingreso.
Se encontró de manera global que los casos de leucemia se incrementaron en 2009 en 24 y corresponden a una tasa de incidencia anual de 426 por c/100.000. En la tabla 2, se exponen las tasas de incidencia anuales de leucemias agudas pediátricas para el período 2008 – 2010.
El mayor número de casos (3) de leucemias agudas mieloides, fueron observados en el año 2010 que correspondió a una tasa de incidencia de 68 por c/100.000 hab. De acuerdo con la incidencia ajustada por sexo, en el año 2008 en el sexo femenino se presentaron 142,8 por c/100.000 hab (8 casos), en el año 2009 160 por c/100.000 hab (9 casos) y en el año 2010 135,3 por c/100.000 hab (6 casos). En el sexo masculino la incidencia fue 160,7 por c/100.000 hab (8 casos) en el año 2008, de 266,7 por c/100.000 hab (15 casos) en el año 2009 y en el año 2010 112,8 por c/100.000 hab (5 casos).
La incidencia de complicaciones fue de 35 casos (67,3%). Las principales fueron infecciones con 23 casos (65,7%), hemorragias con 4 (11,4%) y otras con 8 (22,9%). En el seguimiento de la cohorte de estudio se encontró que 4 (11,4%) de los pacientes abandonaron el tratamiento, 6 (17,1%) aplazaron el tratamiento en alguna fase del protocolo y de estos 4 (11,4%) debido a que la Entidad Promotora de Servicios (EPS) a la cual estaba afiliado no hizo entrega oportuna del medicamento y 3 (5,7%) por motivos económicos. Dentro del grupo de otras complicaciones una de las más frecuentes que se encontró fue la mucositis con 8 casos (15,3%), una complicación infecciosa grave en los pacientes con estas leucemias fue la sepsis aunque no se presentó con mucha frecuencia, sólo en 3 pacientes (5,7%) y 2 de ellos en la etapa de Inducción. En la anterior etapa, es decir, al inicio se presentó el mayor número de complicaciones.
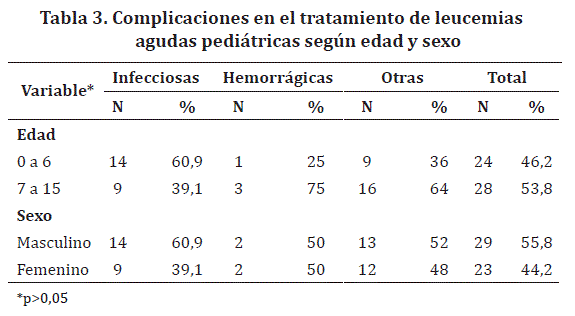
Durante la cohorte de estudio de forma global se encontró que el sexo masculino presentó complicaciones en 29 casos (55,8%) siendo la infecciosa la más frecuente con 14 casos (60,9%). En cuanto a la edad, el grupo etario de 0 a 6 años presentó 24 casos (46,2%) con complicaciones y las principales fueron infecciosas con 14 (60,9%). Sin embargo, el grupo de 7 a 15 años tenía otro tipo de complicación con 16 casos (64%). De acuerdo al número de complicaciones en cada fase de tratamiento, el mayor número fue de orden infeccioso, y se presentaron en la etapa de Inducción con 8 casos (22,8%). No obstante, las complicaciones hemorrágicas se observaron con mayor frecuencia durante la fase de Intensificación en 3 (33,3%), y otro tipo de complicaciones tienen la misma frecuencia de casos durante las fases de Inducción, Intensificación y Mantenimiento con 5 casos (19,2%) (Tabla 3) y (Tabla 4).
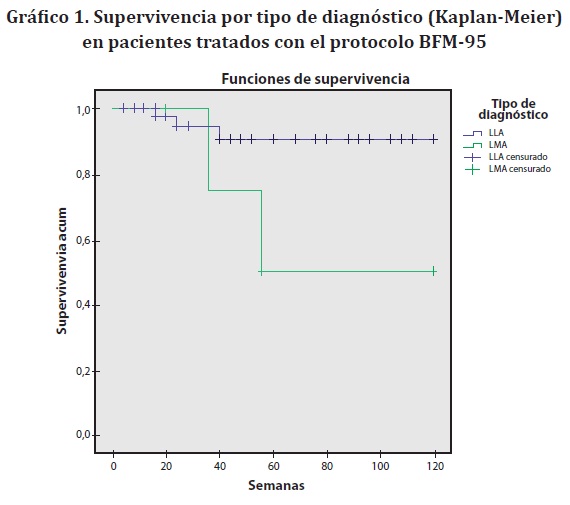
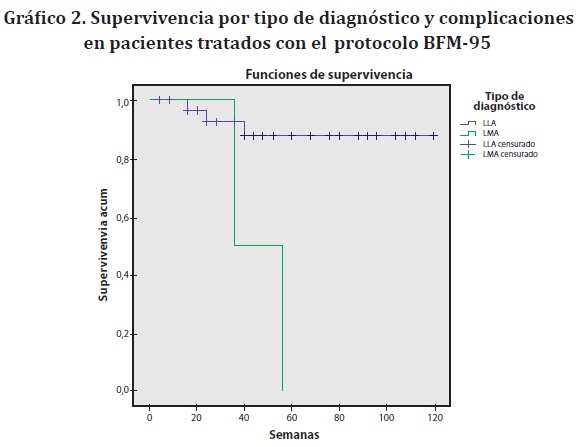
El riesgo relativo (RR) fue calculado con las complicaciones de tipo infeccioso, hemorrágico y la mortalidad. El riesgo de presentar complicaciones de tipo infeccioso y de morir fue de 2,06 IC al 95%: 0,26-16,65 y de 1,93 con IC al 95%: 0,28-13,32 para hemorrágicas, aunque los resultados no fueron estadísticamente significativos (p>0,05). La supervivencia global fue de 90,4% a las 120 semanas, mayor para LLA (93,6%) que para la LMA (60%) (Gráfico 1). Al relacionar la supervivencia global con la presencia de complicación se observó una disminución en este nivel de 4,7%, es decir, la supervivencia de los pacientes que se complicaron fue 85,7% mientras que 100% de los pacientes que no se complicaron sobrevivieron. La diferencia fue del 14,3% entre los pacientes complicados y no complicados. Ninguno de los pacientes con diagnóstico de leucemia mieloide aguda que se complicó durante el tratamiento, sobrevivió (Gráfico 2).
Discusión
Las leucemias agudas son un tipo de cáncer de médula ósea que afectan principalmente a menores de 15 años, se caracterizan por tener un curso rápido entre el tiempo de inicio de la enfermedad y el momento del diagnóstico. La leucemia es el cáncer más común en niños (0- 14 años), lo que representa un tercio de todas las neoplasias malignas. Las tasas de incidencia aumentan a un máximo alrededor de los 3-4 años y luego existe un declive. Unos 400 niños son diagnosticados en Inglaterra y Gales cada año, y cerca de 100 mueren por esta causa. Cuatro de cada cinco casos de leucemia en los niños son LLA, y el resto de casi todos son LMA.24
En nuestro estudio se encontró una relación de leucemia linfoide aguda de 9 a 1 con respecto a la leucemia mieloide aguda, lo cual equivale a 47 casos de LLA (90,4%) y 5 casos de LMA (9,6%) esta diferencia tan marcada puede explicarse debido a un aumento de la incidencia de LLA en las últimas décadas de 1975 a 2006, con un porcentaje de cambio anual de 0,8%.25 La LLA en la presente investigación, es más frecuente a los 5 años con un 17,0% similar a lo observado por Pérez-Saldivar et al.,26 en 2011 en un estudio previo en la Ciudad de México, donde los picos de incidencia de LLA fueron en edades de 1 a 4 años. En este estudio la razón hombre: mujer para LLA fue 1,35:1, levemente superior a lo observado por Müller et al.,27 en niños de Hungría de 1,27:1. Sin embargo, para LMA fue mayor para las mujeres que para los hombres (1,5:1).
Los meses en los cuales ingresaron más pacientes fueron febrero, julio y septiembre con un 13,5%, 15,4% y 17,3 % respectivamente. La variación temporal en la incidencia de leucemias ha sido reportada por Ross et al.,28 para el diagnóstico específico de LLA, ellos mostraron que existió una diferencia estadística para su mayor frecuencia en el verano (p = 0.01). Por otra parte, Harris et al.,29 compararon el período de riesgo de la LLA infantil de casos diagnosticados en Estados Unidos en diferentes zonas, en el norte (superior a 40° de latitud), como Seattle, Nebraska, Iowa, Detroit y Connecticut con los casos diagnosticados en el sur de Estados Unidos (menos de 40° de latitud), incluyendo San Francisco, Utah, Nuevo México y Atlanta y encontraron patrones trimodales más complejos, con picos estacionales en abril, agosto y diciembre para el norte, del total de los casos, y picos estacionales en febrero, julio y octubre para localidades del sur. Los autores sugieren que estos picos podrían coincidir con elevaciones estacionales en la aparición de alergias y procesos infecciosos, elementos que son capaces de promover la proliferación linfocítica.
La incidencia de complicaciones observada fue de 35 casos (67,3%). Las principales fueron infecciosas en 23 casos (65,7%), de éstas el 22,8% se presentaron en la fase de Inducción, como lo encontró Tang et al.,30 en Japón en 2009, en el cual el 27,2% de las complicaciones infecciosas se encontraron en esta etapa.
La sepsis es una complicación grave pero no frecuente en este estudio se presento en 5,7% y en su mayoría durante la fase de Inducción, de forma similar (5,6%) en el estudio realizado por Imaizumi et al.,31 en Japón en 2011, sin embargo, la mayoría de casos fue en la fase de Consolidación. Al parecer este cambio se presentó debido a que en Japón se utilizan dosis más altas de antineoplásicos durante la fase de Consolidación mientras que en el Hospital de referencia las dosis son mayores en la fase de Inducción, lo cual predispone a que se presente este tipo de complicación por depresión del sistema inmunológico.
La mucositis se presentó en un 15,3% de los pacientes, porcentaje inferior a lo observado por Ponce-Torres en pacientes LLA que fue de 38.7%.32 La mucositis oral es una complicación de las LLA y representa la principal causa de dolor y malestar por la promoción de la colonización y proliferación bacteriana. La presentación de la mucositis oral es eritema seguido de placas blancas descamadas que son dolorosas a la palpación. Una forma más pronunciada de mucositis oral es caracterizada por costras y ulceración epitelial.33 Figliolia et al.,34 mostraron que existía un riesgo significativo para el desarrollo de mucositis oral en pacientes con LLA atendidos con el protocolo BFM-95, este resultado sugiere una mayor estomato-toxicidad del mismo.
Las complicaciones hemorrágicas fueron las más frecuentes después de las infecciosas (11,4%), porcentaje inferior a lo encontrado por Kim et al.,35 en Korea en 2006 en donde estas se presentaron en 18,9% con los protocolos de BFM- 90 y 95. Este tipo de complicaciones es común en este tipo de alteraciones. Los individuos con cáncer hematológico presentan sangrado por diferentes razones, entre ellas, alteración en la función y número de las plaquetas, deficiencias en los factores de coagulación, anticoagulantes que circulan y defectos en la integridad vascular.36 Se ha considerado que la hemorragia es una causa de muerte prematura en niños con leucemia. Los riesgos potenciales asociados incluyen hiperleucocitosis, immunofenotipo de leucemia, especialmente, leucemia aguda promielocítica, trombocitopenia y asociada a infecciones.37
La supervivencia a las 120 semanas obtenida para los pacientes con LLA mediante el método de Kaplan-Meier en este estudio fue de 93,6% y para LMA fue 60%. Las diferencias encontradas entre las dos entidades también han sido reportadas por otros autores.38 En relación con las complicaciones, para el caso de la LLA, el porcentaje de supervivencia se reduce a 90,9%, mientras para la LMA ninguno de los pacientes sobrevivió. Lo anterior, puede ser el resultado de la variación existente en la biología del cáncer en las mismas.
Los resultados de esta investigación deberían ser tomados con precaución debido a las limitaciones de los estudios retrospectivos, en los cuales la evidencia podía perder peso por deficiencias en la información y la selección de caso.
Agradecimientos
Los investigadores agradecen a la Dra. Doris Sarasty de Rosero Directora del Hospital Infantil "Los Ángeles" por todo su apoyo en el desarrollo de este trabajo. A las doctoras Julie Andrea Benavides Melo y Myriam Jiménez Quenguán por su colaboración en este manuscrito.
Referencias
1. Margolin J, Poplack D. Acute lymphoblastic leukemia. In: (Pizzo P, Poplack D, eds). Principles and Practice of Pediatric Oncology. Philadelphia: Lippincott-Raven; 1997. pp. 409-462. [ Links ]
2. National Cancer Institute. Childhood Acute Lymphoblastic Leukemia Treatment (PDQ®). (Online). Citado en 2011. (fecha de acceso: 17 de Junio de 2011). Disponible en: http://www.cancer.gov/cancertopics/pdq/treatment/childALL/Patient/page1 [ Links ]
3. National Cancer Institute. Childhood Acute Myeloid Leukemia/Other Myeloid Malignancies Treatment. (Online). Citado en 2010. (fecha de acceso: 17 de Junio de 2011). Disponible en: http://www.cancer.gov/cancertopics/pdq/treatment/childAML/Patient/page1#Keypoint4 [ Links ]
4. Parkin DW, Stiller CA. Childhood cancer in developing countries: Environmental factors. Int J Pediatr Hematol Oncol 1995; 2:411-417. [ Links ]
5. Ferlay J, Bray F, Pisani P, Parkin DM. GLOBOCAN 2002 Cancer Incidence, Mortality and Prevalence Worldwide IARC Cancer Base No. 5, version 2.0 IARC Press, Lyon, 2004. [ Links ]
6. Ministerio de Protección Social. Instituto Nacional de Salud. Instituto Nacional de Cancerología. Protocolo de vigilancia centinela en salud pública de las leucemias agudas pediátricas. (Online). Citado en 2005. (fecha de acceso: 16 de mayo de 2011). Disponible en: http://www.dssa.gov.co/index.php/salud-publica/protocolos [ Links ]
7. Belson M, Kingsley B, Holmes A. Risk factors for acute leukemia in children: A review. Environ Health Perspect. 2007;115:138-145. [ Links ]
8. Christensen MS, Heyman M, Möttönen M, Zeller B, Jonmundsson G, Hasle H; Nordic Society of Paediatric Haematology and Oncology (NOPHO). Treatment-related death in childhood acute lymphoblastic leukaemia in the Nordic countries: 1992-2001. Br J Haematol 2005; 131:50-58. [ Links ]
9. Pui CH, Howard SC. Current management and challenges of malignant disease in the CNS in paediatricleukaemia. Lancet Oncol. 2008;9:257-268. [ Links ]
10. Hijiya N, Liu W, Sandlund JT, Jeha S, Razzouk BI, Ribeiro RC, et al. Overt testicular disease at diagnosis of childhood acute lymphoblastic leukemia: lack of therapeutic role of local irradiation. Leukemia. 2005;19:1399-1403. [ Links ]
11. Hann I, Viscoli C, Paesmans M, Gaya H, Glauser M. A comparison of outcome from febrile neutropenic episodes in children compared with adults: results from four EORTC studies. International Antimicrobial Therapy Cooperative Group (IATCG) of the European Organization for Research and Treatment of Cancer (EORTC). Br J Haematol. 1997;99:580–588. [ Links ]
12. Molgaard-Hansen L, Möttönen M, Glosli H, Jónmundsson GK, Abrahamsson J, Hasle H; Nordic Society of PaediatricHaematology and Oncology (NOPHO). Treatment-related deaths in second complete remission in childhood acute myeloid leukaemia. Br J Haematol 2011; 152:623-630. [ Links ]
13. Lehrnbecher T, Varwig D, Kaiser J, Reinhardt D, Klingebiel T, Creutzig U. Infectious complications in pediatric acute myeloid leukemia: analysis of the prospective multi-institutional clinical trial AML-BFM 93. Leukemia. 2004;18:72-77. [ Links ]
14. Portwine C, Mitchell D, Johnston D, Gillmeister B, Ethier MC, Yanofsky R, et al. Infectious events prior to chemotherapy initiation in children with acute myeloid leukemia. PLoS One. 2013;8:e61899. [ Links ]
15. Creutzig U, Zimmermann M, Reinhardt D, Dworzak M, Stary J, Lehrnbecher T. Early deaths and treatment-related mortality in children undergoing therapy for acute myeloid leukemia: analysis of the multicenter clinical trials AML-BFM 93 and AML-BFM 98. J Clin Oncol. 2004;22:4384-4393. [ Links ]
16. Veringa SJ, van Dulmen-den Broeder E, Kaspers GJ, Veening MA. Blood pressure and body composition in long-term survivors of childhood acute lymphoblastic leukemia. Pediatr Blood Cancer. 2012;58:278-282. [ Links ]
17. Fulbright JM, Raman S, McClellan WS, August KJ. Late effects of childhood leukemia therapy. Curr Hematol Malig Rep. 2011;6:195-205. [ Links ]
18. Molgaard-Hansen L, Möttönen M, Glosli H, Jónmundsson GK, Abrahamsson J, Hasle H; Nordic Society of Paediatric Haematology and Oncology (NOPHO). Early and treatment-related deaths in childhood acute myeloid leukaemia in the Nordic countries: 1984-2003. Br J Haematol. 2010;151:447-459. [ Links ]
19. Möricke A, Reiter A, Zimmermann M, Gadner H, Stanulla M, Dördelmann M, et al. Risk-adjusted therapy of acute lymphoblastic leukemia can decrease treatment burden and improve survival: treatment results of 2169 unselected pediatric and adolescent patients enrolled in the trial ALLBFM 95. Blood. 2008;111:4477-4489. [ Links ]
20. Magyarosy E. Hungarian experience in the treatment of childhood acute lymphoblastic leukemia. Magy Onkol. 2000;44:255-259. [ Links ]
21. Ministerio de Protección Social. Instituto Nacional de Salud. Instituto Nacional de Cancerología. Protocolo de vigilancia centinela en salud pública de las leucemias agudas pediátricas. Definiciones operativas y clasificación de casos para la vigilancia. (Online). Citado en 2005. (fecha de acceso: 16 de Mayo de 2011). Disponible en: http://www.dssa.gov.co/index.php/saludpublica/protocolos [ Links ]
22. Vardiman JW, Thiele J, Arber DA, Brunning RD, Borowitz MJ, Porwit A, Harris NL, Le Beau MM, Hellström-Lindberg E, Tefferi A, Bloomfield CD. The 2008 revision of the World Health Organization (WHO) classification of myeloid neoplasms and acute leukemia: rationale and important changes. Blood. 2009;114:937-951. [ Links ]
23. Laks D, Longhi F, Wagner MB, Ramos-García PC. Survival evaluation of children with acue lymphobastic leukemia treated with Berlin- Frankfurt-Munich trial. J Pediatr (Rio J). 2003;79:149-158. [ Links ]
24. Shah A, Coleman MP. Increasing incidence of childhood leukaemia: A controversy re-examined. Br J Cancer. 2007;97:1009–1012. [ Links ]
25. Smith MA, Seibel NL, Altekruse SF, Ries LA, Melbert DL, OLeary M, Smith FO, Reaman GH. Outcomes for children and adolescents with cancer: challenges for the twenty-first century. J Clin Oncol. 2010;28:2625-2634. [ Links ]
26. Pérez-Saldivar ML, Fajardo-Gutiérrez A, Bernáldez-Ríos R, Martínez-Avalos A, Medina-Sanson A, Espinosa-Hernández L, et al. Childhood acute leukemias are frequent in Mexico City: descriptive epidemiology. BMC Cancer. 2011;11:355. [ Links ]
27. Müller J, Kovács G, Jakab Z, Rényi I, Galántai I, Békési A, et al. Treatment results with ALL-BFM-95 protocol in children with acute lymphoblastic leukemia in Hungary. Orv Hetil. 2005;146:75-80. [ Links ]
28. Ross JA, Severson RK, Swensen AR, Pollock BH, Gurney JG, Robison LL. Seasonal variations in the diagnosis of childhood cancer in the United States. Br J Cancer. 1999;81:549–553. [ Links ]
29. Harris RE, Harrell FE Jr, Patil KD, Al-Rashid R. The seasonal risk of pediatric/juvenile acute lymphocytic leukemia in the United States. J Chronic Dis. 1987;40:915-923. [ Links ]
30. Tang JY, Gu LJ. Report on induction efficacy of protocol ALL-2005 and middle term follow-up of 158 cases of childhood acute lymphoblastic leukemia. ZhonghuaXue Ye Xue ZaZhi. 2009;30:289-293. [ Links ]
31. Imaizumi M, Tawa A. Prospective study of a therapeutic regimen with all-trans retinoic acid and anthracyclines in combination of cytarabine in children with acute promyelocyticleukaemia: the Japanese childhood acute myeloid leukaemia cooperative study. Br J Haematol. 2011;152:89-98. [ Links ]
32. Ponce-Torres E, Ruíz-Rodríguez M del S, Alejo-González F, Hernández-Sierra JF, Pozos-Guillén Ade J. Oral manifestations in pediatric patients receiving chemotherapy for acute lymphoblastic leukemia. J ClinPediatr Dent. 2010;34:275-279. [ Links ]
33. Javed F, Utreja A, Bello-Correa FO, Al-Askar M, Hudieb M, Qayyum F, et al. Oral health status in children with acute lymphoblastic leukemia. Crit Rev Oncol Hematol. 2012;83:303-309. [ Links ]
34. Figliolia SL, Oliveira DT, Pereira MC, Lauris JR, Maurício AR, Oliveira DT, Mello de Andrea ML. Oral mucositis in acute lymphoblastic leukaemia: analysis of 169 paediatric patients. Oral Dis. 2008;14:761-766. [ Links ]
35. Kim H, Lee JH, Choi SJ, Lee JH, Seol M, Lee YS, et al. Risk score model for fatal intracranial hemorrhage in acute leukemia. Leukemia. 2006;20:770-776. [ Links ]
36. Green D. Management of bleeding complications of hematologic malignancies. Semin Thromb Hemost. 2007;33:427-434. [ Links ]
37. Athale UH, Chan AK. Hemorrhagic complications in pediatric hematologic malignancies. Semin Thromb Hemost. 2007;33:408-415. [ Links ]
38. Smith MA, Seibel NL, Altekruse SF, Ries LA, Melbert DL, O'Leary M, et al. Outcomes for children and adolescents with cancer: challenges for the twenty-first century. J Clin Oncol. 2010;28:2625-2634. [ Links ]