INTRODUCCIÓN
En una reacción fotocatalítica se emplea radiación ultravioleta (UV) o visible, para oxidar CO2 y H2O, los componentes orgánicos adsorbidos por un semiconductor [1]. Cuando un semiconductor se ilumina con fotones, cuya energía es mayor o igual a su propia energía de banda gap (Eg), los absorbe, produciendo una excitación de electrones de la banda de valencia (BV), a la banda de conducción (BC) (fotoelectrones) dejando en la BV huecos (fotohuecos). Algunos de estos pares e--h+ (electrón-hueco) fotogenerados, migran hacia la superficie del sólido, donde inician reacciones de óxido-reducción con las especies adsorbidas. Entre los semiconductores más empleados en fotocatálisis heterogénea se encuentran: TiO2, ZrO2, SnO2, CeO y Nb2O5 [2], característicos por tener vacancias aniónicas O2- en la red. En particular, el Nb2O5 presenta ventajas significativas en su desempeño foto-catalítico debido a que, durante el proceso de síntesis, es posible lograr el control de variables como la concentración de los reactivos, el pH, la temperatura y el tiempo, las cuales inciden directamente en la estructura y la morfología del compuesto [3]. Por ejemplo, varios estudios han mostrado que el Nb2O5 presenta propiedades fotocatalíticas como oxidación selectiva de contaminantes orgánicos [4], [5], fotodegradación de tintes orgánicos y producción de hidrógeno [6].
El pentóxido de niobio (Nb2O5) es un compuesto inorgánico, con E g de alrededor de 3,4 eV, que se utiliza principalmente en la producción de condensadores, niobato de litio, vidrio óptico, ferroeléctricos y mecanismos electrocrómicos [7]-[10]. En general, presenta una estructura poliédrica con 6 oxígenos alrededor de 1 niobio y estructuras polimórficas basadas, en su mayoría, en átomos de niobio coordinados octaédricamente [11], [12] como lo son la forma TT a baja temperatura, entre 500°C y 590°C (estructura pseudohexagonal); las formas T- y M-temperatura media, hasta 900 °C (estructura ortorrómbica); y la forma H- temperatura alta, entre 900 °C y 960°C (estructura monoclínica). La estructura comúnmente más encontrada es la monoclínica H-Nb2O5, cuya celda unitaria contiene 28 átomos de niobio y 70 de oxígeno, donde 27 de los átomos de niobio están coordinados octaédricamente y uno tetraédricamente. [13]
En diferentes investigaciones se ha reportado la influencia de un agente dopante en las propiedades fisicoquímicas y fotocatalíticas del Nb2O5. En el trabajo de Falcomer et al. [14] se reporta la preparación de polvos cristalinos nanométricos de Nb2O5 dopados con tierras raras, usando el método Pechini y oxalato amoniacal de niobio, como precursor de partida; posteriormente, este fue tratado a 600°C. Los materiales allí obtenidos presentaron una fase estructural con nanopartículas rectangulares, mostrando una longitud cristalina promedio y un ancho de 26 y 19 nm, respectivamente; entre todos los polimorfismos del niobio, allí se detectó la estructura ortorrómbica. En el trabajo de Hu y Liu [15] un arreglo de nanocintas de Nb2O5 dopado con nitrógeno se preparó, mediante procesamiento hidrotermal y se sinterizó en atmósfera de NH3; en este trabajo se ajusta la temperatura de sinterización para variar la cantidad de agente dopante. Este sistema mostró una buena respuesta en la evaluación de su actividad fotocatalítica, por lo que puede ser prometedor en procesos de descontaminación de agua. En otro trabajo [16] se sintetizó silica mesoporosa (SBA15) soportada en pentóxido de niobio, a lo largo de paladio (II), obteniéndose los nanocom-puestos PdSBA y NbPdSBA. En este estudio la impregnación y estabilidad de los nanocom-puestos obtenidos, se observó a través de las técnicas FTIR, DRS/UV-Vis, XRD, XPS, BET, TGA, SEM y TEM; y la actividad catalítica se analizó en oxidación del benzhidrol/H2O2, en fase líquida y a través de la fotodegradación de Rodamina-B bajo irradiación con luz UV. En esta investigación se encuentra que la actividad catalítica del nanocompuesto NbPdSBA es más alta en ambos procesos catalíticos y además, que la reutilidad del catalizador tiene un alto grado de eficiencia. La presencia de agentes diferentes al óxido también se reporta en [17]. En este trabajo se preparó por molienda hexagonal una aleación de Nb2O5, Mn y Ni; posterior a un tratamiento térmico, estos investigadores repitieron la molienda en molino planetario, encontrando resultados relevantes en tamaño de partícula, hecho que muestra uno de los efectos que puede exhibir el óxido con la presencia de un agente metálico, en el óxido puro.
Es de interés actual desarrollar compuestos de energía de banda gap bajo, ya que serían competitivos frente al óxido de titanio (TiO2), material comúnmente empleado en aplicaciones fotocatalíticas [18]. Buscando mejorar su comportamiento en reacciones de óxido-reducción, para degradar compuestos orgánicos en solución acuosa y ser activo con la luz visible, se eligió dopar el pentóxido de niobio (Nb2O5) con hierro (Fe) a distintas concentraciones en peso (2,5 %, 5 % y 10 %) empleando el método Pechini, que consiste básicamente en la formación de un quelato entre los cationes metálicos (en este caso niobio contenido en sales disueltas), en solución acuosa con un ácido carboxílico [19]. Se eligió el Nb2O5 ya que, a pesar de tener un valor de E g más alto que el del TiO2, tiene las ventajas de no ser tóxico, sencilla separación de la solución reacción lo que se traduce en alta recuperabilidad del medio acuoso y posterior reutilización. Además, se eligió el Fe debido a que sus subcapas d incompletas lo hacen más atractivo de utilizar como impureza en semiconductores, volviéndolos materiales de energía de banda gap más angostos. Esto les confiere mayor susceptibilidad a la radiación visible, hecho que favorecería el desempeño fotocatalítico de óxidos como el Nb2O5.
El estudio propuesto permitió establecer indicios sobre el comportamiento de propiedades estructurales, superficiales y ópticas del Nb2O5 con la inclusión de iones Fe; se analizó la posibilidad de sustitución de cationes Nb5+, en la red cristalina del óxido [18], con lo que se exploró la factibilidad de que solo los cationes pentavalentes de niobio pudieran ser remplazados. En general, se investigó el efecto de la concentración del dopante y de la temperatura de cristalización en las propiedades estructurales, empleando Difracción de Rayos X (DRX) morfológicos, a través de Microscopía Electrónica de Barrido (MEB), y superficiales, por medio de fisisorción de nitrógeno, del Nb2O5 a través de la síntesis del sistema Nb2O5:Fe (a concentraciones en peso del 2,5 %, 5 % y 10 %) por el método Pechini.
2. MATERIALES Y MÉTODOS
Modificando el procedimiento reportado en [20], se prepararon soluciones acuosas de citrato de nióbio y del dopante metálico para las distintas concentraciones en peso (2,5 %, 5 % y 10 %), el nitrato de hierro nonahidratado (Merck), completamente solubilizado en agua destilada, se adicionó a cloruro de nióbio (Merck 98 %), totalmente solubilizado en agua destilada; posteriormente se adicionó la dilución anterior a ácido cítrico (Panreac 99,5 %) diluido en agua destilada, bajo agitación constante y sometido a una temperatura de 90°C. Transcurrida media hora se adicionó etilenglicol (Panreac 99,8 %), para que ocurriera una reacción de poliesterificación; se mantuvo constante la temperatura hasta que se conformó la resina. Luego, la solución precursora se sometió a una pre-calcinación a 300°C (a una tasa de calentamiento de 1,2 °C/min); el material resultante se sometió a molturación en mortero de ágata. Para la cristalización de las partículas se emplearon temperaturas de 600°C (a una tasa de calentamiento de 4,8 °C/min) y 700°C (a una tasa de calentamiento de 5,6 °C/min).
Para el análisis estructural de las muestras y la determinación de las fases cristalinas se empleó un Difractómetro Xpert PANalytical Empyrean Serie II Alpha 1 con radiación Cu Ka2, λ = 1,54442 Å, operando a 40 mA, a un paso de 0,05° en 50 segundo, en un rango 28 de 5-80°. La identificación de las fases cristalinas se realizó usando el software X'Pert HighScore PANalytical y la identificación del Nb2O5 y de la presencia del Fe, se realizó contrastando los resultados obtenidos con los almacenados en el Power Difraction File (PDF). Con el fin de detectar cambios físicos y químicos del óxido dopado (únicamente precalcinado), en función de la temperatura, mientras que está sujeto a un programa controlado de temperatura, se midieron porcentajes de pérdida en peso en función de la temperatura, a través de un equipo DSC/ TGA y aplicando una tasa de calentamiento de 10°C/min. Las curvas se analizaron con el software TA Instruments Universal Analysis 2000. Para realizar el análisis morfológico de los materiales obtenidos, se empleó un Microscopio Electrónico de Barrido FEI QUANA 200, operando a 5,0 kV. Se determinó la energía de banda gap de las muestras obtenidas, a partir de los espectros de reflectancia conseguidos con espectrofotómetro UV-vis Cary 5000 en el modo de reflectancia difusa. Finalmente, para obtener medidas del área de superficie específica, S BET , tamaño y volumen de poro, se utilizó el método de Brunauer Emmett Teller-BET empleando adsorción de Nitrógeno en un equipo Micromeritics ASAP 2020 a 77 K.
3. RESULTADOS Y DISCUSIÓN
Las muestras de Nb2O5 se caracterizaron por su coloración blanca y las de Nb2O5:Fe por poseer una tonalidad naranja, debido a la incorporación del dopante, la cual se incrementó aumentando la concentración del mismo. Con el incremento en la concentración de Fe en el Nb2O5 se aumenta la concentración de portadores que cambian la configuración energética del sistema, estimulando la producción de transiciones de excitación que pueden llegar a absorber en el visible, específicamente a longitudes de onda más larga. En este caso los portadores son huecos debido a que la subcapa 3d del hierro se encuentra incompleta. Esta impureza aceptora se ubica cerca de la banda de valencia, facilitando la movilidad electrónica hacia la banda de conducción, lo que se puede interpretar como una disminución de la energía de banda gap del sistema, como se verá más adelante.
3.1 Análisis de DRX
Los difractogramas de la figura 1 corresponden a (a) los polvos de Nb2O5 no dopado, sometido a 600°C y 700°C y (b) los polvos de Nb2O5 dopado con Fe al 5 %, bajo los mismos tratamientos térmicos. Los difractogramas de la figura 1 (a) permiten inferir que, a 600°C los sólidos cristalizaron bajo la estructura hexagonal y a 700°C cristalización bajo la estructura ortorrómbica, acorde con los PDF No. 28-0317 y No. 30-0873, respectivamente. Se destacan los picos de la estructura ortorrómbica ya que es esta la que, para el caso del pentóxido de niobio, presenta mejor comportamiento fotocatalítico.
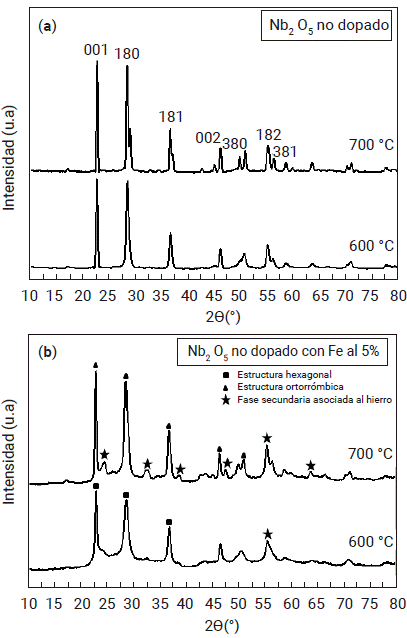
Figura 1 (a) Difractogramas de los polvos de Nb2O5 no dopado, sinterizados a 600°C y 700°C. Se destacan las posiciones de los picos más notables en la fase con estructura ortorrómbica. (b) Difractogramas de los polvos de Nb2O5 dopado con Fe al 5 %, sometidos a tratamientos térmicos de 600°C y 700°C.
De los difractogramas de la figura 1 (b) se pudo establecer que las estructuras predominantes son las asociadas al Nb2O5 no dopado. A pesar de que los picos presenten un ensanchamiento mayor, sus posiciones corresponden a las estructuras hexagonal y ortorrómbica, respectivamente. También se aprecia cómo la intensidad de los picos se incrementa con el aumento de la temperatura de sinterización, lo cual es un indicador de una mayor cristalización. Teniendo en cuenta estos aspectos, los picos en común identificados en el difractograma, indican que el Fe sustituye al Nb sin variaciones estructurales drásticas. El difractograma de los sólidos que contenían Fe al 2,5 %, sometido a 600°C, permitió establecer que la muestra presentaba cristalización, bajo una fase mayoritaria con estructura hexagonal.
En la figura 2 se presentan los difractogramas de los sólidos de Nb2O5 no dopado y dopado con Fe al 2,5 %, 5 % y 10 %, sinterizados a 700°C. En estos difractogramas se aprecia cómo el incremento en la concentración del dopante, afecta la intensidad de los picos asociados a la fase que exhibe el pentóxido de niobio no dopado, además de la aparición de picos diferentes a los asociados con la estructura ortorrómbica del Nb2O5. De esta manera, a pesar de que es posible que se dé la sustitución del niobio por el hierro, este último se segrega como una fase secundaria, lo cual se verifica a través de los resultados de difracción de rayos X. Los picos asociados a esta fase secundaria se indican en la figura 2. Para los dopajes 2,5 % y 5 %, se identificaron picos asociados al óxido Fe2O3, acordes con el PDF No. 19-0615; y para el dopaje al 10 %, se identificaron picos asociados al óxido Fe3O4, de acuerdo con el PDF No. 26-1136.
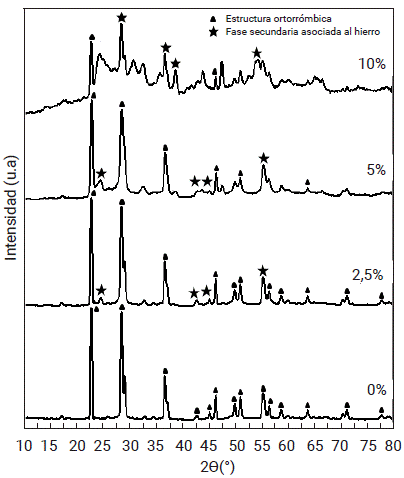
Figura 2 Difractogramas de los polvos de Nb2O5 no dopado y dopado a tres distintas concentraciones, sinterizado a 700°C.
Para analizar el crecimiento cristalino de los polvos obtenidos se calculó el tamaño de cristalito (L) con la ecuación (1) de Scherrer:
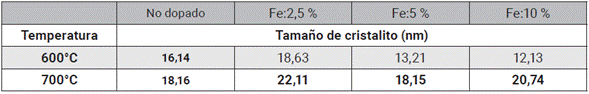
Donde K es el factor de forma, 0,9 para un L tomado como la dimensión del volumen promedio de un cristal, perpendicular al plano de difracción hkl; λ es la longitud de onda usada; 8 el ángulo de difracción de Bragg, medido para el pico hkl; y β representa el valor del ancho completo a la mitad de la altura (sigla en inglés FWHM por Full width at half maximum), medido en radianes sobre el eje 2θ [21]. La línea elegida para estimar L corresponde a la de máxima intensidad en el difractograma (180). En la Tabla 1 se presentan los valores obtenidos para el tamaño de cristalito.
Los resultados presentados en la tabla 1 indican que el crecimiento cristalino se ve favorecido con el incremento en la temperatura de cristalización, lo cual se debe al proceso de transformación de energía térmica en energía necesaria para formar cristales de mayor tamaño. Para el caso de las muestras dopadas y sinterizadas a 600°C, el tamaño de cristalito disminuye con el aumento de la concentración del dopante, acorde con los difractogramas obtenidos, ya que el Nb2O5:Fe se aleja de la cristalinidad alcanzada por el Nb2O5 no dopado. A 700°C el crecimiento cristalino de la muestra dopada al 5 % es comparable con el del óxido no dopado, hecho que hace de esta muestra promisoria, en pruebas de desempeño fotocatalítico. Para el caso de la muestra Nb2O5:Fe10%-700°C se obtiene un valor de L alto, posiblemente debido a que parte del Fe esté formando fases secundarias, por ejemplo, la hematita, con cristales más grandes.
3.2 Análisis TGA
En la figura 3 se presentan las curvas de porcentaje en peso perdido, en función de la temperatura para las muestras precalcinadas de Nb2O5, dopadas con Fe al 2,5 %, 5 % y 10 %. En estas se distingue una región sobresaliente de pérdida de peso entre 320°C y 500°C, asociada a las temperaturas de inicio y finalización de descomposición de especies orgánicas (provenientes del template orgánico empleado en la síntesis) aún presentes en el sistema, que es todavía amorfo. Comparando, de manera general, el porcentaje en peso perdido en cada muestra, se evidencia que la muestra que más peso pierde es la muestra Nb2O5:Fe5 % y la que menos peso pierde es la Nb2O5:Fe2,5 %. Con estos análisis se determinó que la temperatura elegida para la precalcinación de los materiales, 300°C, fue adecuada. Así, el crecimiento de las partículas de Nb2O5:Fe estuvo influenciado por la descomposición térmica de los precursores empleados y como se ve en la figura 4, los polímeros presentes promovieron la formación de granos, luego de los tratamientos térmicos finales empleados.
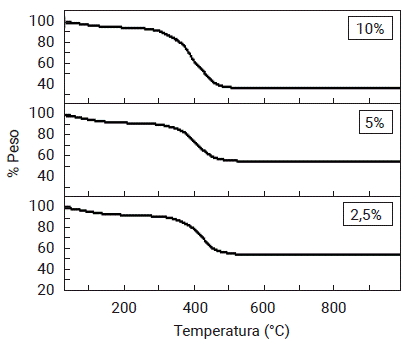
Figura 3 Curvas de porcentaje en peso, en función de la temperatura; determinadas por TGA para las muestras precalcinadas de Nb2O5, dopadas con Fe al 2,5 %, 5 % y 10 %.
3.3. Análisis de imágenes obtenidas por MEB
En la figura 4 se observan las imágenes obtenidas con MEB de las muestras de (a) Nb2O5 no dopado y de Nb2O5:Fe dopado al (b) 5 % y (c) 10 %, sinterizadas a 700°C. (La barra guía en las imágenes es de 5 µm, para el caso (a); y 2 µm para (b) y (c)). Se distingue la presencia de granos grandes que, en concordancia con los resultados obtenidos de DRX, tienen nanoestrucutra interna con una distribución de tamaño de cristalito nanométrica, indicando que el tratamiento térmico a 700°C por 2 horas favorece el crecimiento de granos nanométricos. No fue posible establecer la distribución del tamaño de grano, pero se infiere que esta varía con la concentración del dopante. En general, la conformación de granos nanométricos confirma el hecho de que pre-calcinando el polímero rígido como precursor, se obtienen partículas compuestas de nanoestructuras [22].
3.4 Análisis de medidas de espectroscopia de reflectancia difusa UV-vis
En la figura 5 se presentan los espectros de reflectancia difusa para las muestras de Nb2O5 dopado con Fe al 2,5 %, 5 % y 10 %, sinterizadas a (a) 600°C y (b) 700°C. En estas se aprecia una considerable reducción en el valor de la reflectancia a, alrededor de 710 nm para el caso (a); y 520 nm, para el caso (b).
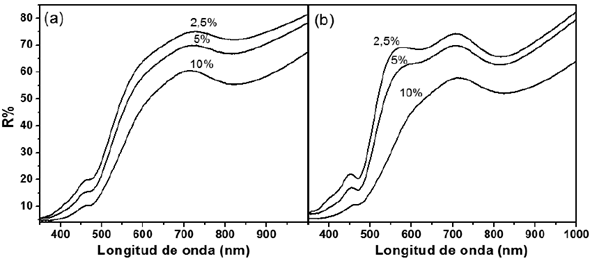
Figura 5 Espectros de reflectancia difusa, en función de la longitud de onda para los polvos de Nb2O5 dopado con Fe, sinterizados a (a) 600°C y (b) 700°C.
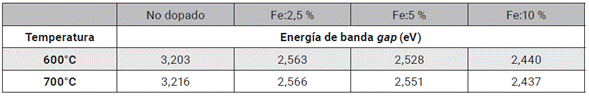
El valor de la energía de banda gap, E g de las muestras analizadas por reflectancia difusa, se obtuvo utilizando el método de Kubelka-Munk, empleado en [23]; a partir de los datos de reflectancia se obtuvo la función de Kubelka-Munk, F(R), y posteriormente se graficó [F(R)hv] 2 en función de la energía hv, para obtener así la energía de banda gap. Los valores de energía de banda gap obtenidos para las muestras dopadas, presentados en la tabla 2, tablamenores que 3,4 eV (generalmente reportado para el Nb2O5), debido al comportamiento conductor del hierro. Estos valores hacen que el sistema Nb2O5:Fe sea un buen candidato para desarrollar pruebas de desempeño fotocatalítico. Los valores obtenidos muestran una tendencia a disminuir con el incremento de la temperatura de calcinación, para la muestra Nb2O5:Fe 10 %-700°C, hecho que puede atribuirse a la excesiva presencia de Fe. En cuanto a las muestras obtenidas al 2,5 % de presencia de Fe, se aprecia una tendencia de estabilidad en el valor de la energía de banda gap. El análisis óptico permitió establecer que la muestra Nb2O5:Fe 5 %-700°C es la mejor candidata para desarrollar pruebas de desempeño foto-catalítico, esto acorde con los resultados del análisis estructural de la muestra. Se puede esperar de esta una mejor activación bajo radiación visible y así posiblemente, un mejor desempeño fotocatalítico.
3.5. Análisis de fisisorción de nitrógeno
En la tabla 3 se presentan los resultados de área superficial específica, S BET , volumen de poro y tamaño de poro determinados al someter los sólidos, cristalizados a 700°C, a fisisorción de nitrógeno. Posteriormente, estos datos se analizaron mediante el método BET. Según los resultados de tamaño de poro, los tres óxidos dopados con Fe y sinterizados a 700°C son mesoporosos. El valor del área superficial específica, aumenta con el incremento de la concentración de hierro, debido a que la morfología de las partículas de Nb2O5:Fe se aleja de la equidimensionalidad; hecho que además, está de acuerdo con los resultados obtenidos para el tamaño de cristalito, el cuál disminuyó con el aumento de la concentración del dopante. El valor de S BET de la muestra Nb2O5:Fe10 %-700°C la haría la más efectiva en procesos fotocatalíticos, pero estructuralmente esta no presenta las características deseadas. En cuanto a la muestra a la muestra Nb2O5:Fe 2,5 %-700°C su valor de S BET es demasiado bajo, pero tiene un tamaño de poro alto, el cuál facilitaría la acción del óxido con moléculas grandes presentes en muchos contaminantes. Finalmente la muestra Nb2O5:Fe 5 %-700°C resulta ser la mejor candidata para emplearse como fotocatalizador, esto teniendo en cuenta que un buen fotocatalizador requiere de una alta área superficial y crecimiento cristalino suprimido.
4. CONCLUSIONES
La ruta de síntesis empleada permitió la obtención de polvos del sistema Nb2O5:Fe. Los resultados de caracterización estructural permitieron inferir que se obtuvo el Nb2O5:Fe en la fase ortorrómbica, para las concentraciones en peso de 2,5 % y 5 %, y una temperatura de sinterización de 700°C. Esta fase, aún mayoritaria para estos casos, estuvo acompañada de una fase secundaria asociada a la presencia del hierro, la cual se destacó notablemente para la concentración en peso del 10 %.
A pesar de que, desde las imágenes de MEB, no se pudo establecer una morfología bien definida, sí se determinó la presencia de granos con estructura nanométrica, corroborándolo con los cálculos de tamaño de cristalito.
El análisis por espectroscopía de reflectancia difusa UV-vis permitió establecer el valor de la energía de banda gap de manera empírica. En general, los valores obtenidos para el sistema Nb2O5:Fe son más bajos que los del óxido no dopado, por lo que se infiere que la modificación del pentóxido de niobio con hierro permitiría mejorar su potencial activación bajo radiación visible.
La caracterización estructural, superficial y óptica, de los polvos obtenidos, permitió establecer que la muestra más óptima para pruebas de desempeño fotocatalítico es la muestra Nb2O5:Fe 5 % calcinada a 700°C, correspondiente a sólidos con tamaño de cristalito de alrededor de 18 nm, con morfología de grano nanoestructurado, E g de aproximadamente 2,68 eV y área superficial específica de 20,51 m2/g.