Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Facultad Nacional de Agronomía Medellín
Print version ISSN 0304-2847
Rev. Fac. Nac. Agron. Medellín vol.62 no.2 Medellín July/Dec. 2009
REDUCCIÓN DE FACTORES ANTINUTRICIONALES DE LA SEMILLA DE VITABOSA (Mucuna deeringiana) MEDIANTE PROCESOS FISICO-QUÍMICOS
ANTINUTRIENTS REDUCTION OF VITABOSA SEEDS (Mucuna deeringiana) WITH PHYSICOCHEMICAL PROCESSES
Sandra Patricia Chaparro Acuña1; Iván Darío Aristizabal Torres2 y Jesús Humberto Gil González3
1 Estudiante Maestría en Ciencia y Tecnología de los Alimentos. Universidad Nacional de Colombia, Sede Medellín. Facultad de Ciencias Agropecuarias. A.A. 1779. Medellín, Colombia. <spchaparroa@unal.edu.co>
2 Profesor Asociado. Universidad Nacional de Colombia, Sede Medellín. Facultad de Ciencias Agropecuarias. A.A. 1779. Medellín, Colombia. <idaristi@unal.edu.co>
3 Profesor Asociado. Universidad Nacional de Colombia, Sede Medellín. Facultad de Ciencias Agropecuarias. A.A. 1779. Medellín, Colombia. <jhgilg@unal.edu.co>
Recibido: Septiembre 1 de 2009; Aceptado: Octubre 28 de 2009.
Resumen. Se determinó el efecto de varios métodos de procesamiento doméstico (hidratación, tostado y germinación) sobre el contenido de cuatro factores antinutricionales (L-Dopa, fenoles totales, taninos e inhibidores de tripsina) presentes en la Mucuna deeringiana. Además, se evaluó el impacto de algunos de los procedimientos sobre la composición proximal de la semilla. El tostado durante 60 minutos, y la hidratación seguida por cocción ocasionan el mayor descenso en la concentración de L-Dopa y de los fenoles totales. Así mismo, los tratamientos con disoluciones básicas (hidróxido de calcio o bicarbonato de sodio) fueron los procesos más efectivos en la reducción de taninos. Los niveles de inhibidores de tripsina disminuyeron significativamente después de someter las semillas a hidratación y cocción en agua o a remojo en disolución de hidróxido de calcio. De otro lado, no se observaron diferencias apreciables en la composición proximal entre las semillas crudas y procesadas. Estos resultados indican que algunas sustancias antimetabólicas presentes en la vitabosa se logran reducir con procesos sencillos y eficaces que podrían ser usados por los cultivadores, sin necesidad de utilizar equipos sofisticados, a fin de aprovechar esta leguminosa como fuente de proteína.
Palabras claves: Mucuna deeringiana, L-Dopa, vitabosa, factores antinutricionales.
Abstract. The effect of several processing methods (soaking, roasting and germination) on the level of four antinutrients (L-Dopa, phenolics, tannins and trypsin inhibitors) present in the seeds of Mucuna deeringiana was studied. Futhermore, the impact of these processing methods on the levels of proximate composition was also assessed. Roasting for 60 minutes and soaking followed cooking reduced the content of L-Dopa and total phenolics. Basic solutions treatments (calcium hydroxide or sodium bicarbonate) were the most effective processes in reducing the tannins content. Soaking and cooking method and calcium hydroxide process significantly diminished trypsin inhibitors content. On the other hand, there were no significant differences in proximate composition between raw and processed seeds. These findings indicate that secondary compounds can be reduced with simple and efficient processes that could be used by farmers, without any expensive equipment to take advantage of this legume as a source of protein.
Key words: Mucuna deeringiana, L-Dopa, vitabosa, antinutrients.
La vitabosa (Mucuna deeringiana) es una leguminosa poco utilizada que se cultiva principalmente en Asia, África y Centroamérica (Vadivel y Janardhanan, 2000). Como la mayoría de las legumbres, estas semillas contienen varios factores antinutricionales (L-Dopa, fenoles, taninos, inhibidores de proteasas) (Ravindran y Ravindran, 1988; Siddhuraju et al., 1996) que causan trastornos en la salud y que limitan su consumo (Infante et al., 1990). La L-Dopa es uno de los principales antinutrientes encontrados en las semillas del género Mucuna. El consumo en exceso de este compuesto puede ocasionar un incremento en la temperatura corporal, erupciones en la piel, vómito y diarrea en humanos y animales (Janardhanan et al., 2003). Los fenoles totales bajan la digestibilidad de las proteínas, los carbohidratos y minerales. Además, disminuyen la actividad de las enzimas digestivas y puede causar daño en la mucosa del tracto gastrointestinal (Gurumoorthi et al., 2003). Los taninos causan una reducción en el crecimiento por la baja asimilación de las proteínas y los carbohidratos, debido a que forma con éstos, sustancias resistentes a las enzimas (Liener, 1994). También, decrecen la tasa de crecimiento y la biodisponibilidad de minerales debido a la formación de complejos insolubles que son difíciles de asimilar por el organismo (Frossard et al., 2000; Guzmán et al., 2000). La ingestión excesiva de inhibidores de tripsina interrumpe el proceso digestivo y puede ocasionar reacciones fisiológicas indeseables. Estos compuestos inhiben la actividad de la tripsina lo cual influye sobre la secreción de otras enzimas pancreáticas, como en el aumento de producción la colecistiquinina, que conlleva a una hipertrofia pancreática (Grant et al., 1995). Por lo tanto, es importante reducir estos factores antinutricionales ya que, aunque son un método de defensa de la planta contra plagas, su presencia es indeseable en productos destinados a la alimentación. Varios autores han realizado estudios para disminuir los niveles de sustancias antimetabólicas en especies del genero Mucuna (M. pruriens principalmente), con el fin de utilizarlas como una fuente alternativa de proteína. Los métodos hidrotérmicos, fermentativos y de germinación han demostrado ser efectivos en la reducción de estos factores antinutricionales (Gurumoorthi et al., 2008; Siddhuraju y Becker, 2001; Wanjekeche et al., 2003). Si bien existe información respecto a M. pruriens, son escasos los estudios relacionados con otras especies de Mucuna.
En particular, M. deeringiana es una legumbre silvestre utilizada en el control de malezas, plagas, y en recuperación de suelos. Sin embargo, son pocas las investigaciones orientadas a establecer su inclusión en la alimentación animal o humana, debido a una limitación preponderante que es su contenido de constituyentes antinutricionales. Por lo tanto, el principal objetivo del presente estudio fue establecer el impacto de algunos métodos de procesamiento doméstico, sobre las concentraciones de algunos factores antinutricionales de las semillas de M. deeringiana para su posible aprovechamiento en la alimentación animal.
MATERIALES Y MÉTODOS
Materiales. Se utilizaron semillas de vitabosa (Mucuna deeringiana) provenientes del Centro Agropecuario Cotové de la Universidad Nacional de Colombia, ubicado en Santa Fe de Antioquia, 6º33’32’’ latitud norte y 1º44’43’’ longitud oeste (bosque seco Tropical, 550 msnm, 27,3 ºC temperatura promedio, 55,4 % de humedad relativa, 1.919,3 milímetros de precipitación promedio, suelo de origen aluvial proveniente de calizas y arcillas calcáreas) (Arango, 2004). La leguminosa se recolectó cuatro meses después de la floración cuando los granos se desarrollaron por completo en la vaina, de tal modo que se pudo desgranar fácilmente. Para los ensayos se dispuso de una muestra representativa de 7,5 kg, previamente sometida a un proceso de limpieza de impurezas y clasificación por tamaño, la cual fue subdividida en diez partes (de aproximadamente 250 g) correspondientes a cada una de las 9 diferentes técnicas de procesamiento y al control (semillas crudas). De los reactivos utilizados la L-Dopa fue adquirida a Alfa Aesar, y la Tripsina (EC 3.4.21.4.), la catequina, el Benzoil DL-arginina-p-nitroanilide (BAPNA) y el ácido gálico fue suministrado por Sigma® (St. Louis, MO, USA).
Métodos de procesamiento
Tostado. La vitabosa (250 g) fue sometida a tostado en un horno (Thermolab, Modelo DIES) durante 15, 30 y 60 minutos a 130 ºC. Los granos de vitabosa se enfriaron a temperatura ambiente. Luego, las semillas fueron molidas en un molino de martillos, hasta lograr un tamaño de las partícula de 0,5 mm. La harina obtenida se almacenó en bolsas plásticas con cierre hermético a temperatura ambiente (25 °C) para su posterior análisis fisicoquímico.
Hidratación en diferentes soluciones. Lotes separados de semillas (250 g) fueron hidratados en agua potable, solución de bicarbonato de sodio (NaHCO3) (0,1 g/100 mL, pH 8,5), hidróxido de calcio Ca(OH)2 (0,1 g/100 mL, pH 8,8) y cloruro de sodio NaCl (0,1 g/100 mL pH 8,2) por 24 horas a temperatura ambiente, y en una proporción de uno a diez (10 g/100 mL). Las soluciones fueron drenadas y los granos lavados y secados a 55 ºC durante 48 horas. El molido y el almacenamiento se realizaron según lo descrito anteriormente.
Hidratación y cocción. Las semillas (250 g) fueron hidratadas en agua destilada (10 g/100 mL) por 24 horas a temperatura ambiente. El agua fue drenada y la muestra sometida a cocción en agua destilada (100 °C) (10 g/100 mL) durante 60 minutos. Posteriormente, los granos se lavaron y secaron a 55 °C por 48 horas. El molido y el almacenamiento se realizaron según lo descrito anteriormente.
Germinación. La vitabosa (250 g) fue esterilizada con hipoclorito de sodio al 0,7%, lavada e hidratada en agua destilada a 4 °C por 12 horas. Seguidamente, se colocó sobre una doble capa de papel filtro en cajas de Petri esterilizadas e incubadas a 30 °C, y se dejó germinar por 120 horas. La muestra fue hidratada con agua destilada regularmente en intervalos de 12 horas. Las semillas germinadas fueron lavadas con agua destilada, secadas a 55 °C durante 48 horas. Posteriormente se procedió al molido y almacenamiento.
Análisis químicos. El contenido de proteína cruda, humedad, cenizas, fibra cruda, y grasa fueron determinados por los métodos estándar 979. 09B, 945.09B, 923.03, 962.09E y 920.39C respectivamente (AOAC, 2000). La extracción de la L-Dopa se hizo utilizando el procedimiento descrito por Daxenbichler et al. (1971). La cuantificación de la L-Dopa en los extractos de vitabosa se estableció mediante un equipo HPLC (Shimadzu serie 204 Prominence), provisto de un detector UV. Se empleó una columna C-18 (250 x 4,6 mm, tamaño de partícula de 120 Å) con un flujo de 1,0 mL/min y a 33 °C. El volumen de inyección fue de 20 µL y como fase móvil se utilizó una mezcla de metanol - agua (70:30) a un pH de 3,0 (ácido fosfórico); la detección se llevó a cabo a una longitud de onda de 280 nm. Las concentraciones de L-Dopa fueron determinadas con referencia a una curva estándar construida a partir de una solución patrón de L-Dopa (Alfa Aesar) y usando el software de cromatografía LC Solution. Los fenoles totales fueron extraídos según Rosset et al. (1982) y cuantificados por el método de Folin-Ciocalteau utilizado por Kumazawa et al. (2004). Para la extracción y cuantificación de taninos, se utilizó el procedimiento de vainillina-HCl, utilizado por Burns (1971); la extracción se llevó a cabo de acuerdo a la técnica descrita por Adebowale et al. (2005). Se determinó el contenido de inhibidores de tripsina en las diferentes muestras, utilizando como sustrato el Benzoil-DL-arginina-p-nitroanilida (BAPNA) y los resultados se expresaron en Unidades de Tripsina Inhibidas (TUI) por mg de muestra (Gómez et al., 1998).
Análisis estadístico. Las diferencias significativas entre las medias se calcularon mediante el análisis de varianza de una vía y una prueba de comparación múltiple (Diferencia mínima significativa de Fisher) con un nivel de significancia del 5%. Se utilizó el programa estadístico Statgraphics Plus 5.1.
RESULTADOS Y DISCUSIÓN
Efecto de los métodos de procesamiento sobre la concentración de antinutrientes
L-Dopa. Los resultados obtenidos se pueden observar en la Tabla 1. El valor de L-Dopa en la semilla sin ningún tratamiento se encuentra dentro del rango de algunas especies del género Mucuna (Gurumoorthi et al., 2008; Adebowale et al., 2005; Siddhuraju y Becker, 2005; Janardhanan et al., 2003). La variación de este compuesto en la vitabosa puede ser atribuida a las condiciones del medio ambiente (latitud, intensidad de luz, fuente de nitrógeno, etc.) y al control genético (Lorenzetti et al., 1998; Wichers et al., 1985).
Tabla 1. Efecto de los diferentes tratamientos sobre el contenido de factores antinutricionales de la semilla de vitabosa (Mucura deeringiana).
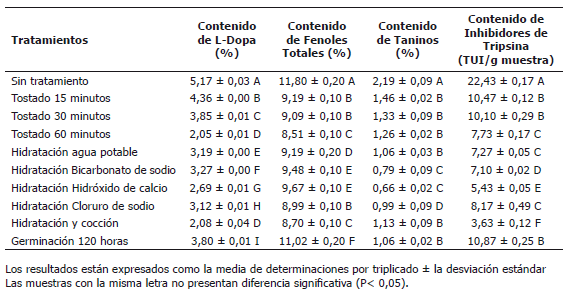
La concentración de L-Dopa después de los tratamientos alcanzó valores del 4,36 a 2,05%, que corresponde a una reducción entre el 15,66 y el 60,34%, respectivamente. Los tratamientos más eficaces en la reducción de este antinutriente fueron el tostado (60,34%) y la hidratación y cocción (59,76%). Respecto al tostado, pudo observarse que con el incremento del tiempo de exposición se disminuye el contenido de este factor antinutricional. Esto pudo ser ocasionado por una oxidación parcial (Siddhuraju y Becker, 2001) o una racemización de este compuesto (Siddhuraju et al., 1996). En este proceso, las proteínas pueden cambiar químicamente debido a la desnaturalización térmica, en donde los residuos de aminoácidos, especialmente los básicos, que contienen residuos ß-hidroxi y sulfuro, son descompuestos ocasionando la producción de cetoácidos. Esta racemización disminuye el contenido nutricional de la proteína (Hayase et al., 1975).
La hidratación y cocción de la semilla disminuyó los niveles de L-Dopa significativamente, debido posiblemente a que la aplicación de temperaturas altas incrementó la solubilidad de la L-Dopa en agua o causó degradación térmica de ésta. Se han encontrado efectos similares en semillas de Mucuna hidratadas en agua y sometidas posteriormente a cocción (Lorenzetti et al., 1998). Adicionalmente, Janardhanan et al. (2003) lograron una reducción de 56 a 60% de L-Dopa en M. pruriens luego de someter siete veces a cocción las semillas por un periodo de 15 minutos cada cocción.
De los tratamientos de hidratación con soluciones iónicas, el proceso con Ca(OH)2, fue el más eficaz en la reducción de L-Dopa seguido por el NaCl y el NaHCO3, debido posiblemente a que la disolución de Ca(OH)2 presentó un pH más alcalino. El decrecimiento de este antinutriente durante la hidratación de las semillas con soluciones de diferente fuerza iónica, pudo ser ocasionado por los cambios en la permeabilidad de la cáscara y variación en el rango de difusión de este compuesto. Además, en medio alcalino probablemente se producen fenolatos, que incrementan la solubilidad del compuesto en agua, o se favorece la oxidación de la L-Dopa, según las observaciones realizadas por Siddhuraju y Becker (2001).
Fenoles totales. La concentración media de estos antinutrientes fue más alta en comparación con la observada en otras semillas de Mucuna (Bhat et al., 2007; Vadivel y Janardhanan, 2005; Gurumoorthi et al., 2003). Luthria y Pastor (2006) explican que las diferencias en el contenido de fenoles totales pueden ser atribuidas a varios factores como el genotipo, las prácticas agronómicas, la madurez en la cosecha, la poscosecha, las condiciones climáticas y las condiciones de crecimiento y almacenamiento.
El tostado fue el tratamiento más eficaz en la reducción de los fenoles totales (27,8 %), seguido por la hidratación y cocción (26,2%). La disminución de estos compuestos a altas temperaturas, pudo ser ocasionada por la oxidación degradativa, la cual parece ser acelerada con el incremento de la temperatura (Nasar-Abbas et al., 2007). El contenido elevado de fenoles puede afectar el valor nutricional de las semillas y la oxidación de sus productos, e interactuar con aminoácidos libres, especialmente los grupos amino de la lisina (Chavan et al., 1999).
Taninos. El contenido de taninos en las semillas crudas es elevado respecto a lo encontrado en otras especies (Vadivel y Janardhanan, 2005; Guromoorthi et al., 2003; Barampama y Simard, 1994). La concentración media de taninos de los granos tratados osciló entre 0,66 y 1,46%, correspondiente a una reducción entre 69,86 y 33,33%. La hidratación con Ca(OH)2 es el proceso que más disminuye la cantidad de taninos, esto se debe posiblemente a que el potencial iónico de la solución incrementa la permeabilidad de la cáscara y estos compuestos, que son hidrosolubles y que pueden escindirse en medios alcalinos, lixivian de la semilla. Lo mismo sucede con el NaCl y el NaHCO3. También, la oxidación de estos factores antinutricionales a pH alcalinos puede contribuir a este descenso.
La germinación también presentó un efecto reductor de los taninos (51,5%). Siddhuraju y Becker (2001) encontraron que a medida que aumentaba el tiempo del tratamiento había una disminución más pronunciada de estos antinutrientes. Esto puede ser ocasionado probablemente por la presencia de la polifenoloxidasa y la hidrólisis enzimática o cambios estructurales de este compuesto (Sharma y Sehgal, 1992).
Inhibidores de tripsina. Los resultados obtenidos en la vitabosa sin tratamiento son bajos comparados con los de otras especies del género Mucuna (Vadivel y Janardhanan, 2005; Gurumoorthi et al., 2003) y otras leguminosas (Apata y Ologhobo, 1997). Los mejores tratamientos fueron la hidratación y cocción en agua, y en Ca(OH)2 con descensos del 83% y 76%, respectivamente. Los inhibidores de tripsina son termolábiles y su actividad inhibitoria puede disminuirse considerablemente con tratamientos térmicos (Liener, 1994). La cocción normal y en autoclave aumentan la digestibilidad de la proteína de las leguminosas, lo que puede ser atribuido no sólo a la remoción de los antinutrientes, sino también a la desintegración estructural de la proteína nativa incluyendo a los inhibidores de enzimas (Moneam, 1990). Este es un proceso efectivo para el descenso de los factores antinutricionales; sin embargo, una cocción excesiva puede bajar el contenido de nutrientes (Wang et al., 1997).
El remojo en agua potable disminuyó el contenido de inhibidores de tripsina (67,5%) de la M. deeringiana. Wang et al. (2008) observaron un aumento en el contenido de estos compuestos en Pisum sativum y relacionan este resultado con el bajo peso molecular de estos antinutrientes, que aumenta su retención en las semillas hidratadas. De otro lado, Admassu y Kumar (2007) apreciaron una reducción mayor de este antinutriente en Phaseolus vulgaris L. cuando se utilizó un tratamiento de hidratación en solución de NaHCO3 (12 horas) (reducción 11%) en comparación con agua potable (12 horas) (reducción 9%). Sin embargo, estos resultados son muy bajos comparados con los encontrados en este estudio. La hidratación con Ca(OH)2produce un cambio en el pH del medio y, por ende, produce un desbalance de las proteínas, lo que puede acarrear modificaciones importantes en su conformación debido a cambios en la ionización de las cadenas laterales cargadas, que a su vez afectan el número de los puentes salinos que estabilizan la estructura nativa de las proteínas. En los procesos tecnológicos que involucran la obtención de aislados proteínicos vegetales es el tratamiento alcalino el que se aplica con mayor frecuencia. En los tratamientos alcalinos se puede presentar también la racemización y formación de aminoácidos modificados (Badui, 2006).
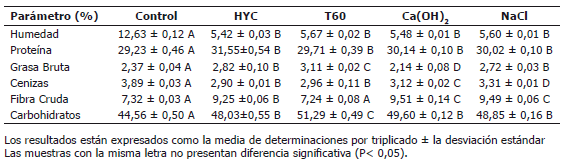
Efecto de los métodos de procesamiento sobre la composición proximal. Para acceder al valor nutricional de las semillas, se evaluó el impacto de algunos métodos de procesamiento sobre la composición proximal (Tabla 2). Las harinas obtenidas mediente técnicas de procesado económicas y de alta eficiencia en la reducción de los antinutrientes (hidratación y cocción (HYC), tostado durante 60 minutos (T60), e hidratación en Ca(OH)2 y en NaCl) fueron seleccionadas para la caracterizacion físico-química. El contenido de proteína cruda, grasa, fibra y carbohidratos no difiere apreciablemente entre la harina no tratada y las procesadas. La humedad disminuyó significativamente, debido posiblemente a diferencias en el secado por aire caliente al que fueron sometidas las muestras durante 48 horas, después del proceso de hidratación. La reducción del contenido de cenizas, después del remojo, podría ser atribuidas a la difusión de ciertos minerales hacia la disolución de hidratación.
Tabla 2. Análisis proximal de la semilla de vitabosa (Mucuna deeringiana) posterior al tratamiento físico-químico.
CONCLUSIÓN
En el presente estudio, todos los métodos de procesamiento doméstico investigados parecen ser efectivos en el decremento del contenido de varios antinutrientes presentes en la vitabosa. El tostado durante 60 minutos ocasionó la máxima reducción de la L-Dopa (60%) y los fenoles totales (28%), mientras que la hidratación seguida de cocción en agua y el remojo en Ca(OH)2 causaron la mayor disminución de inhibidores de tripsina y taninos, 84 y 70% respectivamente. Sin embargo, para obtener mejores resultados se recomiendan futuras investigaciones en donde se combinen varios de los tratamientos evaluados a fin de lograr más bajos niveles de los factores antinutricionales.
AGRADECIMIENTOS
Los autores agradecen a la Dirección de Investigación de la Universidad Nacional de Colombia; Sede Medellín por el apoyo financiero del proyecto.
BIBLIOGRAFÍA
Adebowale, Y.A., A. Adeyemi and A.A. Oshodi. 2005. Variability in the physicochemical, nutritional and antinutritional attributes of six Mucuna species. Food Chemistry 89(1): 37-48. [ Links ]
Admassu, E. and S. Kumar. 2007. Effect of processing on antinutrients and in vitro protein digestibility of kidney bean (Phaseolus vulgaris L.) varieties grown in East Africa. Food Chemistry 103(1): 161-172. [ Links ]
Association of Official Analytical Chemists-AOAC. 2000. Official Methods of Analysis. 16th edition. University of California, Washington D.C. 1200 p. [ Links ]
Apata, D. and A. Ologhobo. 1997. Trypsin inhibitor and other antinutritional factors in tropical legume seeds. Tropical Science 37(1): 52–59.
Arango, L. 2004. Efecto de la variabilidad espacial de algunas propiedades físicas y químicas del suelo relacionadas con la producción del forraje del pasto ángleton (Dichanthium aristatum (Poir) C. E. Hubbard). Tesis Maestría en Geomorfología y Suelos. Facultad de Ciencias. Universidad Nacional de Colombia. Medellín. 77 p. [ Links ]
Badui, S. 2006. Química de los Alimentos. pp. 170-179. Cuarta edición. Pearson Educación, México. 716 p. [ Links ]
Barampama, Z. and R.E. Simard. 1994. Oligosaccharides, antinutritional factors and protein digestibility of dry beans as affected by processing. Journal of Food Science 59(4): 833–838.
Bhat, R., K. Sridhar and K. Tomita-Yokotani. 2007. Effect of ionizing radiation on antinutritional features of velvet bean seeds (Mucuna pruriens). Food Chemistry 103(3): 860-866. [ Links ]
Burns, R.E. 1971. Method for estimation of tannin in grain sorghum. Agronomy Journal 63: 511–512.
Chavan, U.D., F. Shahidi, A.K. Bal and D.B. McKenzie. 1999. Physico-chemical properties and nutrient composition of beach pea (Lathyrus maritimus L.). Food Chemistry 66(1): 43–50.
Daxenbichler, M.E., C.H. VanEtten, E.A. Hallinan, F.R. Earle and A. Barclay. 1971. Seeds as sources of L-Dopa. Journal of Medicinal Chemistry 14(5):463-465. [ Links ]
Frossard, E., M. Bucher, F. Machler, A. Mozafar and R. Hurrell. 2000. Potential for increasing the content and bioavailability of Fe, Zn, and Ca in plants for human nutrition. Journal of the Science of Food and Agriculture 80(7): 861-879. [ Links ]
Gómez, G., S. Quesada y C. Nanne. 1998. Efecto de factores antinutricionales en el pejibaye (Bactris gasipaes) sobre el metabolismo de ratas jóvenes. Agronomía Costarricense 22(2): 191-198. [ Links ]
Grant, G., P.M. Dorward, W.C. Buchan, J.C. Amour and A. Pusztai. 1995. Consumption of diets containing raw soya beans (Glycine max), kidney beans (Phaseolus vulgaris), cowpeas (Vigna unguiculata) or lupin seeds (Lupinus angustifolius) by rats for up to 700 days: effects on body composition and organ weights. British Journal of Nutrition 73(1): 17–29.
Gurumoorthi, P., K. Janardhanan and R. Myhrman. 2008. Effect of differencial processing methods on L-Dopa and protein quality in velvet bean, an underutilized pulse. LWT-Food Science and Technology 41(4): 588-596. [ Links ]
Gurumoorthi, P., M. Pugalenthi and K. Janardhanan. 2003. Nutritional potential of five accessions of a South indian tribal pulse Mucuna pruriens var utilis: ii. Investigations on total free phenolics, tannins, trypsin and chymotrypsin inhibitors, phytohaemagglutinins, and in vitro protein digestibility. Tropical and Subtropical Agroecosystems 1: 153–158.
Guzmán, S., J. Acosta and O. Paredes. 2000. Protein and mineral content of a novel collection of wild and weedy common bean (Phaseolus vulgaris L.). Journal of the Science of Food and Agriculture 80(13): 1874-1881. [ Links ]
Hayase, F., H. Kato and M. Fujimaki. 1975. Racemization of amino acid residues in proteins and poly(L-amino acids) during roasting. Journal of Agriculture and Food Chemistry 23(3): 491-494. [ Links ]
Infante, M.E., A.M. Perez, M.R. Simao, F. Manda, E.F. Baquete, A.M. Fernández and J.L. Cliff. 1990. Outbreak of acute toxic psychosis attributed to Mucuna pruriens. The Lancet 336(8723): 1129. [ Links ]
Janardhanan, K., P. Gurumoorthi and M. Pugalenthi. 2003. Nutritional potential of five accessions of a South Indian tribal pulse, Mucuna pruriens var. Utilis I. The effect of processing methods on the content of L-Dopa, phytic acid and oligosaccharides. Journal of Tropical and Subtropical Agroecosystems 1: 141-152. [ Links ]
Kumazawa, S., T. Hamasaka and T. Nakayama. 2004. Antioxidant activity of propolis of various geographic origins. Food Chemistry 84(3): 329-339. [ Links ]
Liener, I.E. 1994. Implications of antinutritional components in soybeans foods. Critical Review of Food Science and Nutrition 34(1): 31–67.
Lorenzetti, F., S. MacIsaac, J.T. Arnason, D.V.C. Awang and D. Buckles. 1998. The phytochemistry, toxicology and food potential of velvetbean (Mucuna adans. spp., Fabaceae). pp. 67–84. In: Buckles, D., A. Eteka, O. Osiname, M. Galiba and N. Galiano (eds.). Cover Crops in West Africa: contributing to sustainable agriculture. IDRC, IITA and SG-2000, Ottawa. 291 p.
Luthria, D. and M. Pastor. 2006. Phenolic acids content of fifteen dry edible bean (Phaseolus vulgaris L.) varieties. Journal of Food Composition and Analysis 19(2-3): 205-211. [ Links ]
Moneam, N. 1990. Effects of presoaking on faba bean enzyme inhibitors and polyphenols after cooking. Journal of Agricultural and Food Chemistry 38(7): 1479–1482.
Nasar-Abbas, S.M., J.A. Plummer, H.M. Siddique, P. White, D. Harris, D. and K. Dods. 2007. Cooking quality of faba bean after storage at high temperature and the role of lignins and other phenolics in bean hardening. LWT - Food Science and Technology 47(7): 1260-1267 [ Links ]
Rosset, J., F. Bärlocher and J.J. Oertli. 1982. Decomposition of conifer needles and deciduous leaves in two Black Forest and two Swiss Jura streams. International Revue Gesamten Hydrobiologie 67(5): 695-711. [ Links ]
Sharma, A. and S. Sehgal. 1992. Effect of domestic processing, cooking and germination on the trypsin inhibitor activity and tannin content of faba bean (Vicia faba). Plant Foods for Human Nutrition 42(2): 127–133.
Siddhuraju, P. and K. Becker. 2005. Nutritional and antinutritional composition, in vitro amino acid availability, starch digestibility and predicted glycemic index of differentially processed mucuna beans (Mucuna pruriens var. Utilis): an under-utilised legume. Food Chemistry 91(2): 275-286. [ Links ]
Siddhuraju, P. and K. Becker. 2001. Effect of various domestic processing methods on antinutrients and in vitro protein digestibility and starch digestibility of two indigeous varieties of Indian tribal pulse, Mucuna pruriens var. Utilis. Journal of Agricultural and Food Chemistry 49(6): 3058–3067.
Siddhuraju, P., K. Vijayakumari and K. Janardhanan. 1996. Chemical composition and protein quality of the little known legume velvet bean (Mucuna pruriens L. DC.). Journal of Agricultural and Food Chemistry 44(9): 2636–2641.
Ravindran, V. and G. Ravindran. 1988. Nutritional and anti-nutritional characteristics of Mucuna (Mucuna utilis) bean seeds. Journal of the Science of Food and Agriculture 46(1): 71–79.
Vadivel, V. and K. Janardhanan. 2005. Nutritional and antinutritional characteristics of seven south indian wild legumes. Plant Foods for Human Nutrition 60(2): 69–75.
Vadivel, V. and K. Janardhanan. 2000. Nutritional and anti-nutritional composition of velvet bean: an under-utilized food legume in South India. International Journal of Food Sciences and Nutrition 51(4): 279-287. [ Links ]
Wang, N., D. Hatcher and E. Gawalko. 2008. Effect of variety and processing on nutrients and certain anti-nutrients in field peas (Pisum sativum). Food Chemistry 111(1): 132-138. [ Links ]
Wang, N., M.J. Lewis, J.G. Brennan and A. Westby. 1997. Effect of processing methods on nutrients and antinutritional factors in cowpea. Food Chemistry 58(1-2): 59–68.
Wanjekeche, E., V. Wakasa and J.G. Mureithi. 2003. Effect of germination, alkaline and acid soaking and boiling on the nutritional value of mature and immature Mucuna (Mucuna pruriens) beans. Tropical and Subtropical Agroecosystems 1: 183–192.
Wichers, H. J., R. Wijnsma, J.F. Visser, T.H.M. Malingre and H.J. Huizing. 1985. Production of L-DOPA by cell suspension cultures of Mucuna pruriens. II. Effect of environmental parameters on the production of L-DOPA. Plant Cell, Tissue Organ Culture 4(1): 75–82.














