Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Facultad Nacional de Agronomía Medellín
Print version ISSN 0304-2847
Rev. Fac. Nac. Agron. Medellín vol.63 no.2 Medellín July/Dec. 2010
EVALUACIÓN DE MICROORGANISMOS AISLADOS DE GALLINAZA POR SU POTENCIAL PARA EL BIOCONTROL DE FUSARIUM (F. OXYSPORUM) EN PLÁNTULAS DE UCHUVA (PHYSALIS PERUVIANA)
EVALUATION OF MICROORGANISMS INSOLATED FROM HEN MANURE FOR THEIR POTENCIAL AS BIOCONTROL AGENTS OF FUSARIUM (F. OXYSPORUM) IN GOOSEBERRY (PHYSALIS PERUVIANA) SEEDLINGS
Jorge Enrique Rodríguez Amézquita1; Jorge Velandia Monsalve2 y Silvio Edgar Viteri Rosero3
1 Investigador. Corporación Centro de Investigaciones en Palma de Aceite (CENIPALMA). Programa de Plagas y Enfermedades. A.A. 252171, Bogotá, Colombia. <jerodriguez@cenipalma.org>
2 Profesor Asociado. Universidad Pedagógica y Tecnológica de Colombia. Programa de Ingeniería Agronómica, Avenida Central del Norte. Tunja, Colombia. <jvelandi@hotmail.com>
3 Profesor Titular. Universidad Pedagógica y Tecnológica de Colombia. Programa de Ingeniería Agronómica, Avenida Central del Norte. Tunja, Colombia. <silvio.viteri@uptc.edu.co>
Recibido: Noviembre 2 de 2010; Aceptado: Diciembre 20 de 2010.
Resumen. En Colombia, las pérdidas económicas ocasionadas por Fusarium oxysporum en el cultivo de uchuva son considerables. Se evaluaron hongos y bacterias aislados de 2 fuentes de gallinaza, su potencial como agentes de biocontrol de este patógeno. La evaluación se realizó en cajas de Petri con PDA para lo cual se colocó en el centro de las mismas, un disco de 5 mm de diámetro colonizado por el patógeno y a 3 cm del centro, sobre los ejes horizontal y vertical, cada uno de los aislamientos de la gallinaza. Los aislamientos que mostraron antagonismo fueron posteriormente evaluados in vitro por su capacidad de restringir el crecimiento y esporulación de F. oxysporum. Cada uno de los aislamientos que mostró el mayor potencial antagónico fue inoculado simultáneamente con el patógeno en plántulas de uchuva y evaluado por sus efectos en contra de la incidencia de la enfermedad y la muerte de las plántulas. Los resultados indicaron que de los 39 microorganismos aislados de la gallinaza pura, 6 mostraron antagonismo contra F. oxysporum y entre ellos los más efectivos para restringir in vitro su crecimiento y esporulación fueron los hongos H2 y H6 y las bacterias B17 y B19. Las bacterias B17 y B19 resultaron ser las más efectivas en reducir no sólo la incidencia sino también la muerte de plántulas ocasionada por el patógeno. Según los resultados de la identificación, los hongos H2 y H6 pertenecen a los géneros Geotrichum sp. y Trichoderma sp, respectivamente y las bacterias B17 y B19 al género Bacillus.
Palabras clave: Antagonismo, control biológico, Trichoderma, Geotrichum, Bacillus.
Abstract. In Colombia, economic losses due to attack of Fusarium oxysporum in the gooseberry plantation are considerable. Fungi and bacteria isolated from 2 hen manure sources were evaluated for their potential as biological control agents of this pathogen. The evaluation was conducted in Petri dishes containing PDA by placing a 5 mm diameter disk, colonized by this pathogen, in the center of the plates and at 3 cm from the center, over the horizontal and vertical axis, each of the microorganisms isolated from the hen manure. The isolated microorganisms that showed antagonism were later evaluated in vitro for their capacity to inhibit growth and sporulation of F. oxysporum. Each of the microorganisms that showed the greatest antagonism potential was simultaneously inoculated with the pathogen in gooseberry seedlings and evaluated for their effects against the incidence of the disease and the death of the seedlings. The results indicated that of the 39 microorganisms isolated from the pure hen manure, 6 showed antagonism against F. oxysporum and among them the most effective to inhibit in vitro its growth and sporulation were the fungi H2 and H6 and the bacteria B17 and B19. The bacteria B17 and B19 resulted to be the most effective in reducing not only the incidence, but also the death of the seedlings caused by the pathogen. According to the identification results, the H2 and H6 fungi belong to the genera Geotrichum and Trichoderma, respectively and the B17 and B19 bacteria to the genus Bacillus.
Key words: Antagonism, biological control, Trichoderma, Geotrichum, Bacillus.
La uchuva es una especie frutícola andina que ha adquirido gran importancia en Colombia por su potencial para la exportación como fruta fresca. Las divisas generadas representan varios millones de dólares al año, posicionándose en el segundo lugar después del banano (Zapata, Saldarriaga y Londoño, 2002). Las principales zonas productoras del país, localizadas en los Departamentos de Cundinamarca, Boyacá y Antioquia con más de 600 ha (Fischer, 2000), corresponden a explotaciones de economía campesina, con mano de obra familiar.
Las exigencias de calidad que impone el mercado externo están referidas a frutos de apariencia llamativa por su color y tamaño, ausencia de plagas y enfermedades y por supuesto, buen sabor (Gómez 2006). En términos fitosanitarios los problemas más serios que enfrentan los productores son las enfermedades causadas por hongos, bacterias, virus y nematodos, las cuales inciden no sólo sobre la calidad sino también en la cantidad de la producción (Zapata, Saldarriaga y Londoño, 2002).
Las investigaciones desarrolladas acerca del control de patógenos en el cultivo de uchuva son muy escasas (Tamayo, 2006); por lo tanto, el avance en este campo requiere la unión de esfuerzos de parte de los investigadores para explorar e identificar alternativas que sean efectivas y viables para el agricultor. En los últimos años, las pérdidas debidas al marchitamiento vascular ocasionado por Fusarium oxysporum han llegado hasta la totalidad del cultivo (Estupiñán y Ossa, 2007), situación que preocupa a los productores ya que ello significa reducciones considerables en volúmenes de exportación, incremento en los costos de producción y disminución de la rentabilidad.
F. oxysporum es un patógeno del suelo de difícil control, su diseminación en el campo se efectúa a través de material de propagación infectado, fragmentos de plantas enfermas y movimiento de suelo infestado con clamidosporas, las cuales pueden sobrevivir hasta por más de 20 años (Haglund y Kraft, 2001). Este patógeno tiene la capacidad de penetrar en los haces vasculares del centro de la raíz produciendo oclusión y de difundirse fácilmente sin activar los mecanismos de detección y defensa del huésped (Beckman y Roberts, 1995). Se ha reportado la existencia de una especie de F. oxysporum que infecta específicamente a la uchuva y no presenta ningún grado de patogenicidad en otras solanáceas (Estupiñán y Ossa, 2007), esto se debe a que los exudados radicales de dicho huésped satisfacen exclusivamente los requerimientos nutricionales del hongo (Gordon y Martín, 1997). Bajo condiciones de campo, los primeros síntomas de la enfermedad pueden observarse en las plantas desde los 3 meses de la siembra hasta la fase de plena producción; los síntomas se manifiestan en amarillamiento, marchitamiento y muerte de las plantas (Góngora y Rojas, 2006).
En el campo relativo al biocontrol de F. oxysporum, numerosos estudios se han realizado con Trichoderma sp. y Bacillus sp. pero en otros cultivos como arveja (Calderón et al., 2000), fríjol (Avendaño y Arbeláez, 2006) y tomate (Herrera, 2005). En dichos estudios se ha reportado que Trichoderma sp. es un hongo antagónico muy eficiente en contra de Fusarium sp. y que bacterias de los géneros Bacillus sp. y Pseuodomonas sp. restringen efectivamente el crecimiento de hongos (Johansson, 2003), mediante mecanismos de antibiosis, micoparasitismo o competencia (Gary y Kubicek, 1998).
En uchuva el uso de gallinaza es generalizado, en cantidades de 1 a 2 kg por planta al momento del establecimiento del cultivo y de 2 a 4 kg después, cada 3 ó 4 meses (Ramírez et al., 2008; Zapata, Saldarriaga y Londoño, 2002). La incorporación de gallinaza tiene un impacto benéfico sobre las propiedades físicas, químicas y biológicas del suelo. Entre las propiedades físicas se reduce la densidad aparente y se aumenta la porosidad y la capacidad de retención de humedad. Desde el punto de vista químico los trabajos de López et al. (2001), Adeleye, Hallen y Ojeniyi (2010), Ruiz, Piña y Túa (2008) y Higashikawa, Silva y Bettiol (2010) reportan que la gallinaza es una importante fuente de materia orgánica y de macro y micro nutrimentos que son indispensables en la producción sostenible de los cultivos (Ayola y Makinde, 2007). En cuanto a lo biológico, la gallinaza sirve de soporte nutricional a la microflora y fauna del suelo, resultando en un incremento de la población de hongos, bacterias y actinomycetes (Estrada, 2005; Aviles et al., 2010; Peacock et al., 2001; Lin et al., 2009) que tienen potencial en el biocontrol de enfermedades causadas por nemátodos fitoparásitos y hongos fitopatógenos del suelo. La reducción en la población de nemátodos se ha reportado en maíz (Hassan et al., 2009), en tomate (López, Routsova y Ploeg, 2005; Pakeerathan, Mikunthan y Tharshani, 2009) y en pimentón (Yánez et al., 2001) y con relación a los hongos la aplicación de gallinaza ha resultado efectiva en el control de Sclerotium cepivorum en ajo (Ulacio et al., 2003), F. oxysporum fsp cubensis en plátano (Saravan et al., 2004), F. oxysporum en tomate (Sahar, 2007), F. solani en aji (Yelmame et al., 2010) y Verticillium dahliae y Spongospora subterranea en papa (Conn y Lazarovit, 1999).
Lo anterior permite inferir que existe la posibilidad de encontrar agentes de control biológico para el F. oxysporum del cultivo de uchuva. El uso de gallinaza compostada tiene un alto potencial ya que además de su contribución a la nutrición de los cultivos con un amplio rango de minerales (Hansen et al., 1993) y su impacto en el incremento de la microflora del suelo (Estrada, 2005; Aviles et al., 2010; Peacock et al., 2001; Lin et al., 2009) el proceso de compostaje, en su última fase, favorece el crecimiento y colonización de agentes de control biológico de varios fitopatógenos (Hadar y Gorodecki, 1991). El objetivo principal del presente trabajo fue investigar si entre la microflora de la gallinaza existen agentes para el biocontrol del F. oxysporum que se ha constituido en un factor muy limitante de la producción de uchuva.
MATERIALES Y MÉTODOS
Aislamiento del F. oxysporum. De un cultivo de uchuva, localizado en el municipio de Cómbita – Boyacá (Colombia), se tomaron muestras de raíces de plantas que presentaban síntomas de amarillamiento y marchitamiento ocasionados por F. oxysporum. Las muestras se depositaron en bolsas plásticas y se llevaron al laboratorio de Fitopatología del programa de Ingeniería Agronómica de la Universidad Pedagógica y Tecnológica de Colombia (UPTC), con sede en Tunja, donde se realizó el aislamiento del hongo. Siguiendo el protocolo de Agrios (1996), se sembraron cortes de raíces infectadas en cajas Petri que contenían medio de cultivo papa-dextrosa-agar (PDA) y se dejaron en una incubadora a 25 °C durante una semana, para crecimiento del hongo. Al término de la semana, del borde de la colonia se realizaron repiques en medio PDA hasta lograr una colonia pura. De la colonia pura se multiplicó el hongo por medio de siembras en cajas de Petri con medio PDA e incubación a 25 °C durante 10 días. Al término de los 10 días se agregaron 10 mL de agua destilada esterilizada por caja y con un portaobjeto esterilizado se frotó la colonia del hongo con el fin de desprender las conidias del micelio. La suspensión de conidias obtenida se depositó en un erlenmeyer y se realizaron las pruebas de patogenicidad.
Prueba de la patogenicidad del aislamiento de F. oxysporum. Semillas de uchuva del cv. Colombia, fueron sembradas en una bandeja que contenía turba. A los 30 días, las plántulas fueron trasplantadas a bolsas plásticas, cada una de las cuales contenía 500 g de suelo, sometido previamente a temperatura de 80 °C, durante 8 horas, en una mufla. Para comprobar la patogenicidad del aislamiento, de acuerdo con los postulados de Koch, las raíces de 10 plántulas fueron inoculadas con 7 mL de la suspensión de conidias, a una concentración de 1 x 106 conidias • mL-1. De las plantas inoculadas que presentaron los síntomas de la enfermedad se realizaron varios re-aislamientos del hongo en medio PDA, siguiendo nuevamente el procedimiento de Agrios (1996). Una vez comprobada la similitud de los re-aislamientos con el aislamiento inicial y su patogenecidad se procedió a su identificación, utilizando las claves taxonómicas de Barnett y Barry (1960). Los re-aislamientos fueron luego conservados en refrigeración para las pruebas de antagonismo con los microorganismos aislados de la gallinaza.
Aislamiento de microorganismos de la gallinaza. Dos clases de gallinaza (pura y de piso) fueron sometidas a un proceso de descomposición en el invernadero de la UPTC, durante 30 días. De cada una de las fuentes de gallinaza se tomaron 100 g, se colocaron en un erlenmeyer y se adicionó agua destilada estéril hasta completar 1 L, luego se agitó durante 20 min y se prepararon diluciones desde 1x10-1 hasta 1x10-4.
De cada una de las tres mayores diluciones se tomaron 0,5 mL y se depositaron en el centro de cajas de Petri que contenían medio de cultivo PDA o agar nutritivo (AN), las cajas se agitaron en forma circular, en el sentido y en contra de las manecillas de reloj, hasta que la suspensión cubrió por completo la superficie del medio. Las diluciones se realizaron con el fin de facilitar el crecimiento y la diferenciación de colonias individuales de los microorganismos procedentes de la suspensión. Las colonias de hongos y bacterias que crecieron fueron purificadas realizando repiques consecutivos en cajas de Petri con medio PDA o AN, según la clase de microorganismo. Para su reconocimiento en las pruebas, a cada uno de los aislamientos se les asignó un código compuesto de una letra (H para hongo y B para bacteria) seguida de un número. Los aislamientos de los microorganismos purificados fueron almacenados en condiciones de refrigeración, en tubos inclinados con medio PDA o AN, hasta la realización de las pruebas de antagonismo in vitro.
Preselección de los aislamientos por su antagonismo contra el F. oxysporum. En el centro de cajas Petri, con medio de cultivo PDA, se colocó un disco de 5 mm de diámetro de medio PDA colonizado por F. oxysporum durante 10 días y sobre los ejes horizontal y vertical, a una distancia de 3 cm del centro, el microorganismo aislado de la gallinaza. Las cajas de Petri se llevaron a incubación, a 25 °C. El registro del crecimiento de la colonia de F. oxysporum fue diario, durante 10 días. Para mayor seguridad, la prueba se repitió con los hongos y bacterias que afectaron el crecimiento de F. oxysporum.
Evaluación de la capacidad antagónica de los aislamientos. Siguiendo la metodología anteriormente descrita para la preselección de los aislamientos, se evaluó la capacidad antagónica de cada uno de los hongos y bacterias contra F. oxysporum. Una vez realizados los montajes respectivos, las cajas de Petri se incubaron a 25 °C durante 10 días. El crecimiento de la colonia de F. oxysporum se registró diariamente. Para esta prueba se utilizó el diseño experimental completamente al azar con cuatro repeticiones por tratamiento (aislamiento del agente bioantagonista). El testigo consistió en cajas de Petri sembradas con solo el patógeno. La unidad experimental consistió de una caja de Petri con su tratamiento respectivo. La prueba se dio por terminada cuando el medio de cultivo en las cajas testigo fue invadido en su totalidad por el patógeno. Al finalizar la prueba se cuantificó la esporulación de F. oxysporum en cada uno de los tratamientos.
Para la cuantificación de la esporulación, sobre cada uno de los ejes horizontal y vertical y a 18 mm del centro de la caja de Petri con crecimiento de F. oxysporum se cortó un disco en el medio de cultivo, utilizando un sacabocados de 5 mm de diámetro. Los 4 discos obtenidos por caja fueron suspendidos en un tubo de ensayo que contenía 10 mL de agua destilada estéril, se adicionó una gota de Tween 20 y se agitó vigorosamente por 5 min, para facilitar el desprendimiento de las conidias del micelio. El conteo de las conidias se realizó en un microscopio Nikon®, utilizando la cámara de Newbauer. Los datos tanto del crecimiento de la colonia como de la esporulación de Fusarium, fueron sometidos al análisis de varianza y en dependencia de la significancia, las medias se compararon mediante la prueba Tukey (Gómez y Gómez, 1984). Los aislamientos de hongos y bacterias que más afectaron el crecimiento y esporulación del F. oxysporum in vitro fueron luego evaluados por su capacidad de biocontrol del F. oxysporum en plántulas de uchuva.
Evaluación de la efectividad de los aislamientos en el biocontrol de F. oxysporum en plántulas de uchuva. Las plántulas de uchuva fueron obtenidas mediante la siembra de un semillero que fue mantenido por 2 meses bajo condiciones de invernadero. A los 56 días de la siembra del semillero se realizó la multiplicación de los aislamientos, que en las pruebas in vitro afectaron significativamente el crecimiento y esporulación de F. oxysporum. La multiplicación de los hongos se efectuó en medio PDA y la de las bacterias en medio AN. La inoculación de las plántulas con los agentes de biocontrol se realizó con cultivos de 8 días de crecimiento en el caso de los hongos y de 4 días con las bacterias, a una concentración de 1 x 106 conidias• mL-1 y de 1 x 108 células • mL-1, respectivamente. Para cada aislamiento biocontrolador se seleccionaron 10 plántulas y las raíces se sumergieron por 15 min en una suspensión ya sea de conidias o de bacterias, preparada a la concentración indicada anteriormente. Después de la inoculación, las plántulas fueron trasplantadas en bolsas de polietileno que contenían 1 kg de suelo, tratado a 80 °C durante 8 horas en una mufla. Inmediatamente después del trasplante, a cada una de las raíces se le ocasionó una herida con un bisturí y con una jeringa se le aplicó en volumen 7 mL de la suspensión de conidias de F. oxysporum, preparada igualmente a una concentración de 1 x 106 conidias • mL-1. Finalmente, las raíces se cubrieron con suelo, el cual fue asperjado con el sobrante de la suspensión del inóculo respectivo. En esta prueba se utilizaron 2 testigos, uno inoculado con F. oxysporum y otro sin inoculación. Las plántulas se mantuvieron en casa de malla por 8 semanas, se regaron y se aplicó fertilizante 13-26-6 (1 g • L-1) semanalmente, hasta cuando ocurrió la muerte de la primera plántula, en cualquiera de los tratamientos. El diseño experimental utilizado fue completamente al azar con 6 tratamientos y 10 repeticiones. Se llevó un registro semanal del porcentaje de incidencia de la enfermedad y de la muerte de plántulas. Los resultados obtenidos en cada variable fueron sometidos al análisis de varianza y a la prueba Tukey (Gómez y Gómez, 1984), utilizando el paquete estadístico SPSS 11.5.
Identificación de los aislamientos antagónicos. Los hongos más eficientes en el biocontrol de F. oxysporum fueron identificados a nivel de género, con base en las características morfológicas de los conidióforos y de las conidias, siguiendo el protocolo descrito en la clave taxonómica de Barnett y Barry (1960). La identificación de las bacterias se realizó en el laboratorio de Fitopatología de CORPOICA en el Centro de Investigación Tibaitatá, siguiendo el protocolo de Schaad, Jones y Chun (2001).
RESULTADOS Y DISCUSIÓN
Aislamiento y patogenicidad del F. oxysporum. El aislamiento de F. oxysporum de cortes de raíces de uchuva sembrados en medio PDA fue positivo. De acuerdo con los postulados de Koch, al inocular plántulas de uchuva con una suspensión de conidias procedentes del aislamiento, a una concentración de 1 x 106 conidias • mL-1, se comprobó su veracidad y patogenicidad, puesto que de las 10 plántulas de uchuva inoculadas con el patógeno, el 80% presentó síntomas de marchitamiento a los 12 días de la inoculación y el 100% murió a los 20 días. Al hacer un corte longitudinal de la raíz se observó necrosamiento del sistema vascular, este síntoma concuerda con lo descrito por Gonzales (1976), quien afirma que F. oxysporum obstruye el flujo de agua en los conductos del xilema mediante la presencia de micelio y conidias, ocasionando la necrosis de los tejidos. Las colonias de microorganismos aislados de gallinaza por su potencial para el biocontrol re-aisladas de las plántulas de uchuva coincidieron con la contramuestra. En medio de cultivo PDA presentaron un color rosado y al realizar montajes y observarlos al microscopio, se constató la presencia de numerosas microconidias unicelulares, macroconidias de 4 a 6 células y clamidosporas globosas formadas dentro del micelio.
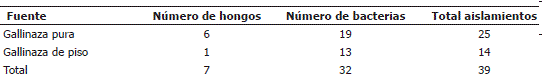
Microorganismos aislados de la gallinaza. En total se obtuvieron 39 aislamientos de la gallinaza (Tabla 1). Entre los aislamientos figuraron hongos y bacterias procedentes principalmente de la gallinaza pura, en comparación con la gallinaza de piso. El mayor número de hongos y bacterias en la gallinaza pura se debe posiblemente a una mayor disponibilidad de nutrimentos en dicho sustrato, como lo mencionan Velandia y Ricardo (1998). Otra posibilidad es que la gallinaza de piso para su comercialización es sometida a un tratamiento térmico, proceso que puede reducir considerablemente su población microbiana.
Tabla 1. Microorganismos aislados de gallinaza evaluados por su potencial para el biocontrol de Fusarium oxysporum en plántulas de uchuva.
Aislamientos antagónicos al F. oxysporum. De los 39 microorganismos aislados y evaluados in vitro por su antagonismo, 3 aislamientos de hongos y 3 de bacterias, procedentes de la gallinaza pura, redujeron el crecimiento de F. oxysporum. Los hongos fueron identificados como H2, H3 y H6 y las bacterias como B17, B18 y B19. Ninguno de los demás aislamientos limitó el crecimiento del patógeno, el cual llegó a cubrir la superficie del medio de cultivo en su totalidad, a los 9 días de incubación. Entre los hongos, el aislamiento H6 mostró el mayor potencial de antagonismo puesto que su crecimiento fue más rápido que el de F. oxysporum. De acuerdo con Gary y Kubicek (1998), es posible que el mecanismo ejercido por el hongo H6 contra F. oxysporum fue el de competencia; los autores afirman que los microorganismos compiten por nutrimentos y el que tiene mejor capacidad para adquirir dicho factor de crecimiento, coloniza el medio de cultivo impidiendo el crecimiento del otro, como ocurrió en este caso. Estos resultados confirman que la gallinaza compostada es una fuente de microorganismos agentes de control biológico como lo exponen Hadar y Gorodecki (1991) y Hoitink, Stone y Han (1997) y documentan que entre los agentes biocontroladores se encuentran hongos y bacterias antagonicos a F. oxysporum. Según Kuter et al. (1983), la cantidad y diversidad de biocontroladores dependen de varios factores, entre los cuales figuran el pH, el contenido de nitrógeno amoniacal, el grado de descomposición de la materia orgánica, la naturaleza de los materiales utilizados y el lugar donde se produzca.
Potencial antagónico de los aislamientos. De los seis aislamientos seleccionados inicialmente como antagónicos, los hongos H2 y H6 y las bacterias B17 y B19 resultaron ser los aislamientos más efectivos en cuanto a la restricción del crecimiento y esporulación de F. oxysporum in vitro. En la Figura 1 se ilustra la restricción del crecimiento de F. oxysporum por dos de estos aislamientos. En la Figura 1A se puede apreciar que como consecuencia del antagonismo ejercido por la bacteria B19, el crecimiento de la colonia de F. oxysporum fue en forma rectangular y no radial como sucedió en el testigo (Figura 1C). Es posible que el mecanismo ejercido fue el de antibiosis, debido a la producción de metabolitos secundarios de parte del microorganismo antagónico, los cuales pueden ser volátiles o difusibles, pero que en cualquiera de los casos, sin entrar en contacto físico con el patógeno pueden inhibir o restringir su crecimiento, como lo registran Howell y Stipanovic (1993); citados por Gary y Kubicek (1998). Estos autores informaron que cepas de los hongos Trichoderma y Gliocladium producen metabolitos que se denominan gliotoxin, viridin y gliovirin. En la Figura 1B, se puede apreciar claramente que el crecimiento de este patógeno fue inhibido en su totalidad por el hongo H6.
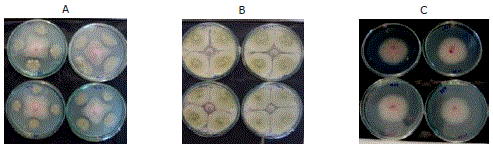
Figura 1. Restricción del crecimiento del Fusarium oxysporum (centro) en cortes de raíces de uchuva, por microorganismos antagónicos aislados de la gallinaza. A. F. oxysporum vs bacteria B19. B. F. oxysporum vs hongo H6. C. F. oxysporum solo (Testigo).
Los resultados del crecimiento de la colonia y de la esporulación de F. oxysporum en presencia de los microorganismos antagónicos se muestran en la Tabla 2.
Tabla 2. Crecimiento y esporulación de Fusarium oxysporum en cortes de raíces de uchuva, en presencia de los microorganismos antagónicos.
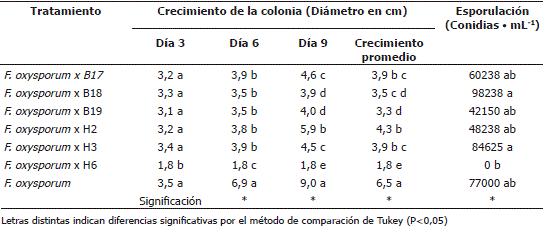
Los datos de la Tabla 2, relativos al crecimiento de la colonia, confirman que el hongo H6 es el aislamiento con el mayor potencial de antagonismo contra F. oxysporum. En efecto, en presencia de este aislamiento, el crecimiento de la colonia de F. oxysporum fue consistentemente menor a los 3, 6 y 9 días de incubación, con diferencias estadísticas en comparación a los otros aislamientos y al testigo. Estos resultados concuerdan con lo observado en la Figura 1B, en la cual se ilustra la contundencia del antagonismo ejercido por este aislamiento en contra de F. oxysporum. Al final de la prueba, a los 9 días de incubación, los aislamientos que en orden descendente siguieron al H6 en su capacidad de restringir el crecimiento de F. oxysporum fueron B18, B19, H3, B17 y H2. Se destaca que todos los aislamientos se diferenciaron del testigo, lo cual indica que efectivamente los microorganismos evaluados limitaron en gran medida el crecimiento del patógeno ya sea mediante los mecanismos de competencia o de antibiosis. Los resultados obtenidos siguen los lineamientos expuestos por Herrera (2005), en el sentido que la selección de bioantagonistas potenciales debe ser realizada primero por medio de pruebas in vitro y posteriormente en exposición con la planta, en condiciones de invernadero o de crecimiento en el campo.
Respecto al efecto de los aislamientos antagónicos sobre la esporulación del F. oxysporum, los resultados confirman la muy promisoria capacidad antagónica del aislamiento H6, al inhibir por completo la esporulación del patógeno en las pruebas in vitro, siguiendo posiblemente el mecanismo de competencia según Gary y Kubicek (1998), como ya se anotó anteriormente. Con los demás aislamientos, incluyendo el testigo, la esporulación osciló entre 42.150 y 98.238 conidias • mL-1 (Tabla 2), sin diferencias estadísticas entre sí. Aunque sin diferencias significativas frente al testigo, la esporulación del F. oxysporum en presencia de la bacteria B18 y el hongo H3 fue considerablemente superior. De acuerdo con Charles (1991), existe la posibilidad que estos dos aislamientos microbianos produzcan metabolitos secundarios que en lugar de restringir estimulan la esporulación del F. oxysporum.
Efectividad del F. oxysporum en plántulas de uchuva, bajo la presencia de los aislamientos biocontroladores. Los primeros síntomas de la enfermedad causada por F. oxysporum, caracterizados por flacidez de las hojas, fueron observados a partir de la tercera semana en las plántulas tratadas con los aislamientos B19, H2 y H6, con un rango de incidencia que fluctuó entre el 20% y el 30%, en comparación al testigo que fue del 50% (Tabla 3). A diferencia de los otros tratamientos, en las plántulas tratadas con el aislamiento B17 los síntomas de la enfermedad se presentaron a partir de la cuarta semana, con un porcentaje de incidencia del 40%. Al final de la prueba, en la octava semana, el porcentaje de plántulas afectadas fue del 60% en los tratamientos con los aislamientos B19 y H6, 70% con el aislamiento H2 y el testigo y 80% con el aislamiento B17.
Tabla 3. Efecto expresado en porcentaje de microorganismos biocontroladores de la patogenicidad de Fusarium oxysporum en plántulas de uchuva.
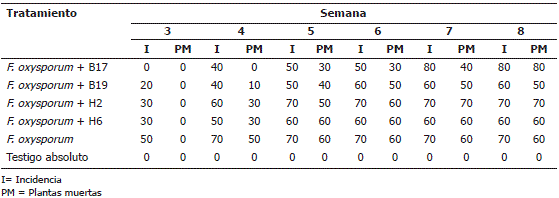
La muerte de plántulas a causa del hongo empezó a observarse a partir de la cuarta semana con un 10% en el tratamiento con el aislamiento B19, 30% con los aislamientos H2 y H6 y 50% en el testigo inoculado. En estos tratamientos, el incremento en el porcentaje de plántulas muertas fue muy considerable de la cuarta a la quinta semana y luego muy leve o nulo hasta el final de la prueba. En el tratamiento con el aislamiento B17, al igual que para la incidencia de la enfermedad, la muerte de plántulas empezó una semana más tarde, en la quinta semana con un 30%, y se mantuvo con el porcentaje más bajo hasta la séptima semana. Otro de los aislamientos que merece destacarse es el B19, ya que el porcentaje de plántulas muertas fue el más bajo tanto en la cuarta semana (10%) como al final de la prueba en la octava semana (50%). Independientemente de la capacidad demostrada in vitro por el aislamiento H6 para inhibir tanto el crecimiento de la colonia como la esporulación de F. oxysporum (Tabla 2), el porcentaje de plántulas muertas en este tratamiento resultó similar al del testigo, a lo largo del tiempo de la prueba.
Respecto a la manifestación del efecto del biocontrol de F. oxysporum en la planta, es conveniente poner de relieve que independientemente del potencial antagónico de determinados microorganismos, este puede ser limitado debido a que es un patógeno del sistema vascular y una vez que ha penetrado en el tejido su control es casi imposible, por lo cual de acuerdo con Yadida y Chet (2004) y Ahmad y Baker (1988) la aplicación de microorganismos antagónicos en contra de este patógeno debe ser de manera que el efecto sea preventivo y no curativo. Lo anterior sugiere que para potenciar el biocontrol de F. oxysporum en la planta es necesario la inclusión de prácticas de manejo del cultivo que permitan maximizar el efecto de los microorganismos antagonistas, justo antes de que el F. oxysporum penetre en la planta. Al respecto, se sugiere incluir la aplicación localizada de gallinaza compostada antes del establecimiento del cultivo, en adición a las cantidades y épocas mencionadas por Ramírez et al. (2008) y Zapata, Saldarriaga y Londoño (2002), con el fin de introducir los bioantagonistas propios de la gallinaza (Hadar y Gorodecki, 1991 y Hoitink, Stone y Han, 1997) y promover además la población de los agentes de control biológico nativos del suelo (Estrada, 2005; Aviles et al., 2010; Peacock et al., 2001; Lin et al., 2009).
Identificación de los microorganismos biocontroladores. Los resultados de las pruebas in vitro e in vivo condujeron a la identificación de los hongos H2 y H6 y de las bacterias B17 y B19, como los aislamientos más promisorios para el biocontrol de F. oxysporum en el cultivo de la uchuva.
Caracterización de las mejores cepas bioantagonistas
Hongo H2: El crecimiento en el medio de cultivo PDA a 25 °C fue rápido con micelio escaso, de color blanco y apariencia polvorienta. Los microcultivos observados al microscopio se caracterizaron por la formación de artroconidias de forma rectangular, obtenidas por la fragmentación del micelio. De acuerdo con la clave taxonómica de Barnett y Barry (1960), el hongo corresponde al género Geotrichum sp, familia Endomycetaceae y orden Saccharomycetales. El efecto antagónico de Geotrichum fue demostrado por Boivin (2004), quien además propone que dicho hongo puede ser una opción futura en el biocontrol de enfermedades causadas por F. oxysporum.
Hongo H6: Este hongo presentó un crecimiento muy rápido en PDA, cubriendo el medio a los 3 días de incubación a 25 °C, con colonias de color verde. De acuerdo con la clave taxonómica de Barnett (1960), el hongo pertenece al género Trichoderma. La presencia de este hongo en la gallinaza confirma lo expuesto por Arcos y Elias (2004), quienes afirman que este hongo es muy común y abundante en la materia orgánica. El efecto antagónico del Trichoderma sobre Fusarium fue demostrado por Avendaño y Arbeláez (2006) y Marois et al. (1981) en diferentes cultivos.
Aislamiento B17: Esta bacteria presentó un crecimiento rápido en medio AN, a 25 °C, cubriendo el medio de cultivo a los 6 días de incubación. Las colonias presentaron un color crema de consistencia butírica, ligeramente elevadas, de bordes indefinidos, Gram+. Las células son en forma de bastones. La bacteria es aeróbica, licúa la gelatina y no presenta reacción con la urea, indicando que no tiene capacidad de metabolizar este sustrato, debido a la ausencia de la enzima ureasa que libera el nitrógeno en forma inorgánica.
Bacteria B19: Esta bacteria presentó un crecimiento más rápido en medio AN, a 25 °C, cubriendo la superficie del medio a los 5 días de incubación. Las colonias presentaron también un color crema, de consistencia butírica, ligeramente elevadas, de bordes indefinidos. La bacteria es Gram+, produce esporas subterminales y células en forma de bacilos. Bioquímicamente, es anaeróbica facultativa, no presenta reacción de la ureasa y tampoco licua la gelatina.
La tinción con verde de malaquita, para determinar la presencia de endosporas fue positiva para las dos bacterias (B17 y B19), conduciendo por lo tanto a su identificación como correspondientes al género Bacillus.
CONCLUSIONES
Existen microorganismos presentes en la gallinaza, capaces de actuar como biocontroladores de F. oxysporum.
A diferencia de la gallinaza de piso, la gallinaza pura es una fuente muy diversa de microorganismos, entre los cuales se encuentran antagonistas que representan una alternativa muy promisoria para el biocontrol de F. oxysporum.
De los 39 microorganismos aislados de la gallinaza, seis mostraron antagonismo contra F. oxysporum y entre ellos los más efectivos para restringir in vitro su crecimiento y esporulación fueron los hongos H2 y H6 y las bacterias B17 y B19.
De los cuatro aislamientos seleccionados por su mayor antagonismo contra F. oxysporum, las cepas bacterianas B17 y B19 resultaron ser las más promisorias ya que redujeron no sólo la incidencia sino también la muerte de plántulas ocasionada por el patógeno.
Los hongos H2 y H6 pertenecen a los géneros Geotrichum y Trichoderma, respectivamente y las bacterias B17 y B19 al género Bacillus.
AGRADECIMIENTOS
Los autores expresan sus agradecimientos al Dr. Clímaco Hio del laboratorio de Fitopatología de CORPOICA, con sede en el Centro de Investigación Tibaitatá, por su valiosa colaboración en la identificación de las bacterias biocontroladoras.
BIBLIOGRAFÍA
Adeleye, E.O., L.S. Ayeni and S.O. Ojeniyi. 2010. Effect of poultry manure on soil physical and chemical properties, leaf nutrient contents and yield of yam (Dioscorea rotundata) on an Alfisol in Southwestern Nigeria. Journal of American Science 6(10): 871-878. [ Links ]
Agrios, G. 1996. Fitopatología. Segunda edición. Limusa, México. 838 p. [ Links ]
Ahmad, J. and R. Baker. 1988. Implications of rhizosphere competence of Trichoderma harzianum. Canadian Journal of Microbiology 2(34): 694-696. [ Links ]
Arcos, O. y R. Elías. 2004. Antagonismo de algunas especies de Trichoderma aisladas de suelos colombianos en el control de Fusarium oxysporum, http://www.agro.unalmed.edu.co/publicaciones/revista/docs/11%20Propagacion%20uchuva.pdf.; consulta: junio 2009. [ Links ]
Avendaño, C. y Arbeláez, G. 2006. Control biológico del marchitamiento vascular causado por Fusarium oxysporum f. sp. phaseoli en fríjol, mediante acción combinada de Entrophospora colombiana, Trichoderma sp. y Pseudomonas fluorescens. Agronomía Colombiana 24(1): 62-67. [ Links ]
Avilés, E., P. Núñez, A. Pérez, I. Almonte, G. López y C. Martínez. 2010. Caracterización física y biológica de materiales alternativos para la elaboración de sustratos, http://www.cedaf.org.do/eventos/cfcs_2010/presentaciones/04_miercoles/manana/20p.pdf; consulta: noviembre 2010. [ Links ]
Ayola, T. and E.A. Makinde. 2007. Complementary Organic and inorganic fertilizer application: Influence on growth and yield of cassava/maize/melon Intercrop with a relayed cowpea. Australian Journal of Basic and Applied Sciences 1(3): 187-192. [ Links ]
Barnett, H. y B. Barry. 1960. Illustrated Genera of imperfect fungi. Third Edition. APS PRESS. St. Paul, Minnesota. USA. 218 p. [ Links ]
Beckman, C. and E. Roberts. 1995. On the nature and generic basis for resistance and tolerance to wilt diseases of plants. Advanced Botanical Research 24(3): 35-77. [ Links ]
Boivin, P. 2004. Biological control of fungal contamination by applying Geotrichum candidum, http://www.freepatentsonline.com/20040081639.pdf, 4 p. consulta: marzo 2009. [ Links ]
Calderón, L., A. Estrada, J. Morales y V. Salguero 2000. Evaluación de Bacillus subtilis en el control biológico de Fusarium oxysporum en arveja china. Trabajo de grado Ingeniero Agrónomo. Universidad de San Carlos. Facultad de Agronomía, Guatemala. 67 p. [ Links ]
Conn, K.L. and G. Lazarovit. 1999. Impact of animal manures on Verticillium kilt, potato scab, and soil microbial populations. Canadian Journal of Plant Pathology 21: 81-92. [ Links ]
Charles, J. 1991. Combinaciones microbicidas sinérgicas. Traducción de patente. 6 p. [ Links ]
Estupiñan, H. y J. Ossa. 2007. Efecto del agente causal de la marchitez vascular de la uchuva (Physalis peruviana L) el hongo Fusarium oxysporum, sobre algunas solanáceas y otras especies cultivadas afectadas por formas especiales del microorganismo. Trabajo de Grado Microbiología Agrícola. Universidad Javeriana. Facultad de Ciencias, Bogotá. 89 p. [ Links ]
Estrada, P.M.M. 2005. Manejo y procesamiento de la gallinaza. Revista Lasallista de Investigación 2(1): 43-48. [ Links ]
Fischer, G. 2000. Crecimiento y desarrollo. p. 9-26. En: Flórez, V.J., G. Fischer y A.D. Sor (eds.). Producción, poscosecha y exportación de la uchuva (Physalis peruviana L.). Unibiblos, Universidad Nacional de Colombia, Bogotá. [ Links ]
Gary, E. and C. Kubicek 1998. Trichoderma and Gliocladium, enzymes, biological control and commercial applications, http://www.amazon.com/Trichoderma-Gliocladium-Biological-commercial-applications/dp/0748408053#reader_0748408053.2. 396 p.; consulta: mayo 2009. [ Links ]
Gómez, W. 2006. Plan de mercadeo para la comercialización de uchuva fresca en Alemania. Trabajo de grado Ingeniería Industrial. Universidad Javeriana. Facultad de Ingeniería. Bogotá. 62 p. [ Links ]
Gomez, K.A. and A.A. Gomez. 1984. Statistical procedures for agricultural research. Second Edition. John Wiley and Sons, New York. 680 p. [ Links ]
Góngora, A. y P. Rojas 2006. Incidencia de las enfermedades en uchuva Physalis peruviana L. por estado fenológico y de acuerdo con la ubicación en los diferentes estratos de la planta, en el departamento de Cundimarca. Trabajo de grado Microbiología Agrícola. Universidad Javeriana. Facultad de Ciencias Básicas.Bogotá. 87 p. [ Links ]
González, L. C. 1976. Introducción a la fitopatología. Editorial IICA, Costa Rica. 174 p. [ Links ]
Gordon, T. and R. Martyn. 1997. The evolutionary biology of Fusarium oxysporum. Annual Review of Phytopathology 35(1): 111-128. [ Links ]
Hadar, Y. and B. Gorodecki. 1991. Suppression of germination of Sclerotium rolfsii in compost. Soil Biology and Biochemistry 23: 303-306. [ Links ]
Haglund, W. and J. Kraft 2001. Fusarium wilt. p. 14-16. In: Kraft, J.M. and Pfleger, F.L. (eds.). Compendium of pea diseases and pests. The American Phytopatological Society Press, Minnesota, USA. 84 p. [ Links ]
Hansen, R.C., H.M. Keener, C. Marugg, W.A. Dick and H.A. Hoitink. 1993. Composting of poultry manure. p. 131-153. In: Hoitink, H.A.J. and Keener, H.M. (eds.). Science and engineering of composting: design, environmental, microbiological and utilization aspects. Renaissance, Worthington, Ohio. 84 p. [ Links ]
Hassan, J. M.Z, M. Chishti, I. Rasheed, F. Ahmad, D. Ahmad, and B.A. Lone. 2009. Nematodes associated with Zea mays and their control through organic soil amendments. International Journal of Plant Protection 3(4): 1735-1843. [ Links ]
Herrera, R. 2005. Control biológico de Rhizoctonia solani, Fusarium oxysporum f. sp. lycopersici y Fusarium solani en tomates bajo invernaderos. Universidad de Chile. Facultad de Ciencias Agronómicas, Santiago. 60 p. [ Links ]
Higashikawa, F., C.A. Silva, and W. Bettiol. 2010. Chemical and physical properties of organic residues. Revista Brasileira de Ciência do Solo 34(5): 1742-1752. [ Links ]
Hoitink, H.A., A.G. Stone, y D.Y. Han. 1997. Supresión de enfermedades de plantas mediante compost. Agronomía Costarricense 21(1): 25-33. [ Links ]
Johansson, M. 2003. Biocontrol of Fusarium in wheat introducing bacteria to a system of complex interactions. Tesis doctoral. Swedish University of Agricultural Science. Uppsala. 74 p. [ Links ]
Kuter, G.A., E.B. Nelson, H.A. Hoitink, L.V. Mad Den. 1983. Fungal populations in container media amended with composted hardwood bark suppressive and conducive to Rhizoctonia damping-off. Phytopathology 73: 1450-1456. [ Links ]
Lin, X.J., F. Wanga, H.S. Cai, R.B. Lin, C.M. He, Q.H. Li, and Y. Li. 2009. Effects of different organic fertilizers on soil microbial biomass and yield of peanut. Chinese Journal of Eco-Agriculture 17(2): 235-238. [ Links ]
López, M.J.D., E.A. Díaz, R.E. Martínez, D. Ricardo y C.R.D. Valdez. 2001. Abonos orgánicos y su efecto en las propiedades físicas y químicas del suelo y rendimiento en maíz. Terra 19: 293-299. [ Links ]
López, P.J.A., T. Routsova, and A. Ploeg. 2005. Effect of three plant residue and chicken manure used as biofumigants at three temperatures on Meloidogyne incognita infestation of tomato in greenhouse experiments. Journal Nematology 37(4): 489-494. [ Links ]
Marois, J., D. Mitchell and R. Sonoda. 1981. Biological control of Fusarium crown row of tomato under field conditions. Ecology and Epidemiology 71(12): 1257–1259.
Pakeerathan, K., G. Mikunthan and N. Tharshani. 2009. Effect of different animal manures on Meloidogyne incognita (Kofoid and White) on tomato. World Journal of Agricultural Sciences 5(4): 432-435. [ Links ]
Peacock, A.D., M.D. Mullen, D.B. Ringelbergc, D.D. Tyler, D.B. Hedrick, P. Gale, and D.C. White. 2001. Soil microbial community responses to dairy manure or ammonium nitrate applications. Soil Biology and Biochemistry 33: 1011-1019. [ Links ]
Ramírez, G.M., H.G. Roveda, B.R. Bonilla, J.L. Cabra, R.A. Peñaranda, J.M. López, D.P. Serralde, V.A. Tamayo, R.G.E. Navas, y D.C.A. Diaz. 2008. Uso y manejo de biofertilizantes en el cultivo de la uchuva. CORPOICA, Bogotá. 56 p. [ Links ]
Ruiz C, Z. Piña y D. Túa. 2008. Fertilizantes orgánicos procedentes del municipio Federación, estado Falcón. INIA Divulga 11: 27-30. [ Links ]
Saravanan, T., M. Muthusamy, M. Loganathan, and R.K. Prabakar, 2004. Antifungal effects of organic amendments against Fusarium wilt pathogen in banana. Madras Agricultural Journal (IND) 91(7-12): 526-529. [ Links ]
Sahar, A.Y. 2007. Evaluation of composted chicken manure in biocontrolling Fusarium wilt on tomato. Egyptian Journal of Phytopathology 35(1): 61-72. [ Links ]
Schaad, N.W., J.V. Jones. and W. Chun. 2001. Laboratory guide for identification of plant pathogenic bacteria. Third edition. University of Minnesota, St. Paul. 373 p. [ Links ]
Tamayo, A. 2006. Diagnóstico de la problemática actual de enfermedades en el cultivo de uchuva Physalis peruviana L. en el departamento de Antioquia. Trabajo de Grado Microbiología Agrícola. Universidad Javeriana. Facultad de Ciencias. Bogotá. 117 p. [ Links ]
Ulacio, O.D., M.E. Zavaleta, R. García-Espinosa, F. Delgadillo-Sánchez, A. Pedroza-Sandoval, y A. Martínez-Garza. 2003. Materia orgánica y microorganismos antagonistas como estrategias de manejo de Sclerotium cepivorum Berk. y su impacto en el progreso de la pudrición blanca en ajo (Allium sativum L.). Revista Mexicana de Fitopatología 21: 346-354. [ Links ]
Velandia, J. y G. Ricardo. 1998. Evaluación de la gallinaza en el control de Plasmodiophora brassicae en repollo. Agronomía Colombiana 22(3): 30- 34. [ Links ]
Yadida, I. and I. Chet. 2004. Effect of Trichoderma harzianum on microelement concentrations and increased growth of cucumber plants. Plant and Soil 235(2): 235- 242. [ Links ]
Yanez, S.G.M., M.E. Zavaleta, R.C. Flores, A.J.J. Chavez and A.R. Valdivia. 2001. Management of wilting (Phytophthora capsici), root gallina (Nacobbusaberrans Thorne and Allen) and virosis on pepper (Capsicum annuum L). Revista Mexicana de Fitopatología 19(1): 40-48. [ Links ]
Yelmame, M.G., B.P. Mehta, A.J. Deshmukh, and V.A. Patil. 2010. Evaluation of some organic extracts in in vitro to control Fusarium solani causing chilli kilt. International Journal of Pharma and Bio Sciences 1(2): 1-4. [ Links ]
Zapata, J.L., A. Saldarriaga, y A. Londoño. 2002. Manejo del cultivo de uchuva en Colombia. Corporación Colombiana de Investigación Agropecuaria (CORPOICA), Regional 4, Centro de Investigación La Selva. Boletín Técnico. Rionegro, Antioquia. 42 p [ Links ]














