Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Facultad Nacional de Agronomía Medellín
Print version ISSN 0304-2847
Rev. Fac. Nac. Agron. Medellín vol.64 no.2 Medellín July/Dec. 2011
Efecto Antagónico in vitro de Actinomicetos Aislados de Purines de Chipaca (Bidens pilosa L.) Frente a Phytophthora infestans (Mont) de Bary
In vitro Antagonistic Effect of Actinomycetes Isolated from Chipaca (Bidens pilosa L.) Purins Against Phytophthora infestans (Mont) de Bary
Yudy Astrid Fonseca Ardila1; Diana Edith Castellanos Suárez2 y Tomás Enrique León Sicard3
1 Bacterióloga. Universidad Colegio Mayor de Cundinamarca. Calle 28 No. 5B-02, Bogotá, Colombia. <yudyfonseca@gmail.com>
2 Microbióloga. Universidad Nacional de Colombia - Sede Bogotá - Centro Internacional de Física - Laboratorio de Microbiología. Carrera 45 No. 26-85, Bogotá, Colombia. <decastellanoss@unal.edu.co>
3 Profesor Asociado. Universidad Nacional de Colombia - Sede Bogotá - Instituto de Estudios Ambientales (IDEA). Calle 44 No. 45 - 67 Bloque B2 Unidad Camilo Torres, Bogotá, Colombia. <teleons@gmail.com>
Recibido: Junio 08 de 2011; aceptado: Agosto 09 de 2011.
Resumen. Se estudió el efecto inhibidor de los actinomicetos presentes en purines o extractos fermentados de plantas de chipaca (Bidens pilosa L.), sobre el crecimiento de Phytophthora infestans (Mont) de Bary, causante del tizón tardío de la papa. Se elaboraron cuatro purines de flores, raíces, hojas-tallos y su mezcla. De estos purines se obtuvieron 25 aislamientos de actinomicetos, cada uno de los cuales se enfrentó con P. infestans en placas de medio de cultivo, utilizando la técnica de anillos de Gauze y estableciendo las concentraciones iniciales de esporas mediante conteos microscópicos en cámara de Neubauer. Los actinomicetos no crecieron en el purin de flores debido, posiblemente, a que en él no se utiliza suelo rizosférico o porque su pH (9) es mayor que el rango normal de crecimiento de estos microorganismos ( pH 6 -; 8). Se evidenció inhibición del crecimiento del oomycete por parte de 8 aislamientos de actinomicetos con porcentajes de inhibición entre 33,3 - 77,8%, provenientes de los purines de raíces, tallos-hojas y mezcla de partes de la planta. La mayor inhibición se obtuvo en los aislamientos AC001, AC010, AC011 y AC025 con conteos de 0,4, 6,0, 3,0, y 3,6 x105 esporas mL-1).
Palabras clave: Agroecología, control biológico, antagonismo, biopreparado, microorganismos.
Abstract. Purins or liquid fermented extracts of chipaca (Bidens pilosa L.) were prepared to establish the inhibitory effect of the actinomycetes found in such biopharmaceutical preparations on the growth of Phytophthora infestans (Mont) de Bary, the causative of potato late blight disease. Four purins made from flowers, roots, leaf-steams and a mixture of them were prepared; 25 actinomycete isolates were obtained from these purins and their ability to resist challenge by P. infestans was ascertained in medium plates using the ring Gauze technique and establishing initial concentrations of spores by microscopic counting in Neubauer chamber. Actinomycetes did not grow in flower purin as rhizosphere soil was not used in its preparation or because this particular pH (9) was higher than the normal range of 6 to 8 pH. Oomycete growth was inhibed in 8 actinomycete isolates (33.3% - 77.8% inhibition) from roots, stem-leaves and plant part purin mixtures. The greatest inhibition was obtained from isolates AC001, AC010, AC011 and AC025 (0.4, 6.0, 3.0 and 3.6 x 105 spore mL-1 count).
Key words: Agroecology, biological control, antagonism, microorganism, bioproducts.
El tizón tardío o gota de la papa, causado por el oomycete Phytophthora infestans (Mont) de Bary es una enfermedad altamente limitante en Colombia, cuyo control, generalmente químico, genera significativos impactos ambientales de tipo social, económico y ecosistémico (Castaño et al., 1996; Jaramillo et al., 1997).
En el control químico, se utilizan productos fungistáticos (inhiben la germinación de las esporas) o fungicidas que matan esporas (Powelson e Inglis, 1999), pero que también causan fitotoxicidad y efectos no deseables en fuentes de agua, suelos y seres humanos (Castaño et al., 1996).
Para evitar estos efectos indeseables del control químico, se han estudiado opciones de control biológico, utilizando hongos, bacterias y actinomicetos. Para el control de P. infestans se han evaluado con éxito bajo condiciones in vitro y como antagonistas directos, algunas especies de Trichoderma, Pseudomonas (Castaño et al., 1996) y Methylobacterium (Poorniammal et al., 2009). También se ha estudiado el efecto de actinomicetos como Streptomyces por la producción de ácido butanoico (tiobutacina) (Lee et al., 2008) y Streptosporangium sp. (Verma et al., 2008).
Por otra parte y también con fines de control o regulación de poblaciones de patógenos, algunos productores ecológicos, utilizan extractos fermentados ó purines de diferentes plantas con características medicinales y alelopáticas. Estos purines se preparan a partir del material vegetal, que se mezcla con un volumen definido de agua y luego se deja descomponer o fermentar durante un mes (Lee, 2003). En el caso de los purines de chipaca o amor seco (Bidens pilosa L.), con excepción de un estudio preliminar realizado por León y Castellanos (2002), hasta el momento no se han evaluado sus principios activos o la acción inhibidora de los microorganismos asociados a este tipo de extractos.
Por tal razón se evaluaron in vitro algunos aislamientos de actinomicetos provenientes de purines o extractos fermentados de Chipaca, con potencial antagónico contra P. infestans.
MATERIALES Y MÉTODOS
Aislamiento y conservación de Phytophthora infestans. P. infestans se obtuvo a partir de hojas y tallos de papa infectados procedentes de un cultivo de papa (Solanum tuberosum), de la vereda Mortiño municipio de Ubaté, departamento de Cundinamarca, Colombia. Se seleccionaron tallos y hojas que presentaban signos del tizón, caracterizados por la aparición de zonas blancas-grisáceas similares a un micelio, con bordes de color amarillo y café. Sobre las áreas afectadas se tomaron improntas utilizando cinta adhesiva, que luego se colocaron en láminas portaobjetos para observar microscópicamente estructuras propias de P. infestans, como esporangios en forma de limón, micelio hialino y cenocítico, y zoosporas flageladas (Agrios, 2002).
Con hisopos estériles humedecidos en agua, se frotó el área afectada de las hojas y tallos para colectar partes del oomycete y el frotado se sembró en placas de medio Agar Centeno (Grünwald et al., 2001), que se incubaron a 20 °C en oscuridad para obtener crecimiento de P. infestans (Riveros et al., 2003). Las características macro y microscópicas del oomycete fueron tomadas en cuenta según la guía de identificación de Waterhouse et al. (1983).
Cada placa sembrada fue controlada semanalmente para determinar posible contaminación durante ocho días. Se realizaron nuevas siembras con el fin de tener suficiente población del fitopatógeno para la preparación de inóculo, necesario para el montaje de las pruebas de antagonismo.
Preparación de los purines. Las plantas de chipaca fueron recolectadas en la finca ecológica Gabeno (Tenjo, Cundinamarca), ubicada a 2.600 msnm con temperatura promedio de 20 ºC y cerca de 900 mm de precipitación anual.
Los purines se prepararon conforme a la guía de Ramírez (1996), tomando 500 g de material vegetal que se colocaron en 1.500 mL de agua destilada estéril adicionando 2 g de levadura. Esta mezcla fue ligeramente licuada, colocándola posteriormente en un recipiente plástico limpio, que se cubrió con un lienzo para evitar el ingreso de otras sustancias o insectos. Cada purin fue preservado por un mes a 20 °C de temperatura y agitado diariamente para favorecer la presencia de oxígeno.
Cumplido el mes de preparación, se filtró cada purín. El líquido obtenido fue depositado en botellas previamente estériles. Al afrecho sobrante se le adicionaron 500 mL de agua destilada estéril tibia, se dejó en reposo por un día más, se filtró y este líquido se adicionó al filtrado anterior, que finalmente fue llevado a condiciones de refrigeración (4 °C).
Aislamiento de microorganismos cultivables. De cada purin se hicieron siembras, por triplicado, mediante el método de dilución de la muestra en placa Agar Caseína Almidón (Madigan et al., 2004), utilizando como diluyente una solución fenólica (Williams y Davies, 1965), que actúa como inhibidor de bacterias no filamentosas, la cual se dejó actuar por 15 min, al cabo de los cuales se sembraron las muestras en las placas del medio de cultivo, colocando 100 µL en la superficie de dicho medio, que posteriormente fueron llevados a incubación por siete días a 28 ºC en oscuridad (Villamil y Tamayo, 2002).
Luego de siete días de crecimiento, se realizó el recuento total y diferencial de las poblaciones de actinomicetos. De las cajas con crecimientos entre 15-150 UFC mL-1, fueron tomadas las colonias que presentaron diferencias macroscópicas como color y forma y producción de pigmentos difusibles. Luego se realizaron observaciones microscópicas y se aislaron nuevamente para garantizar su pureza en el medio Caseína Almidón (Williams y Davies, 1965).
Evaluación de la capacidad antagónica de los microorganismos aislados. Cada uno de los actinomicetos aislados, se enfrentó por triplicado en cajas de Petri con P. infestans, mediante la técnica de anillos de Gauze (Valencia, 2004), que consistió en sembrar tres anillos de plástico en el medio de cultivo Agar PDA (Papa Dextrosa Agar), que permite tanto el crecimiento del patógeno como también de los actinomicetos, previamente inoculado de forma masiva con el patógeno. En cada anillo se adicionaron 50 μL de una suspensión de esporas de actinomicetos con concentración inicial conocida de 10-5 UFC mL-1, la cual se obtuvo realizando conteo de esporas en cámara de Neubauer (Valencia, 2004). Se incubaron por ocho días, al cabo de los cuales se observó la formación de halos de inhibición, cuya longitud del diámetro se midió empleando una regla milimetrada. Para establecer el porcentaje de inhibición, al valor del diámetro total de la zona de inhibición de P. infestans, se le restó el diámetro del área de crecimiento del actinomiceto (expresado en porcentaje).
Análisis estadístico. Se utilizó un diseño completamente al azar, con tres repeticiones referidas a cada prueba de inhibición por aislamiento. Las diferencias significativas entre las medias de porcentaje de inhibición, después de una transformación arcoseno, se calcularon mediante el análisis de varianza de una vía y una prueba de comparación múltiple de Duncan con un nivel de significancia del 5%. Se utilizó el programa estadístico SAS 9.1®.
RESULTADOS Y DISCUSIÓN
Aislamiento de Phytophthora infestans. El crecimiento del patógeno in vitro, se obtuvo en placas de medio de cultivo Agar Centeno conservadas a temperatura ambiente, evidente por la formación de un micelio blanco algodonoso en toda la superficie del medio de cultivo. Microscópicamente se observaron los esporangios típicos en forma de limón, algunos de los cuales contenían zoosporas.
Varios investigadores han mencionado la dificultad de obtener aislamientos de P. infestans en medio artificial (Tsao, 1970), ya que el crecimiento puede ser muy lento debido a la falta de nutrientes, facilitando el desarrollo de otros microorganismos en el medio de cultivo (Sánchez et al., 2000). No obstante en el medio de cultivo Agar Centeno modificado por Grünwald et al., (2001), se obtuvo crecimiento rápido del oomycete y se inhibió el crecimiento de otros microorganismos.
Shaw et al., citados por Sánchez et al. (2000), señalan que algunos aislamientos del oomycete obtenidos de plantas de papa (Solanum sp.), crecen en medios a base de centeno, pero no pueden hacerlo en otros medios. Los mismos autores sugieren que esto podría deberse a la presencia de sustancias inhibidoras o a la ausencia de los nutrimentos requeridos. Erwin y Bartnicki (1983) reportan que las especies de Phytophthora crecen en medios orgánicos como el Agar Centeno posiblemente por la presencia de sitosterol necesario para su desarrollo.
Los sitosteroles son mezclas de β-sitosterol y ciertos esteroles saturados, los cuales se encuentran en aceites de germen de trigo y centeno, aceite de maíz y comúnmente en aceites de semillas. Se ha documentado su importancia en el desarrollo y reproducción de varios organismos del género Phytium y Phytophthora (Englander y Roth, 1980). Es importante aclarar que, a pesar de haberse observado un buen crecimiento del fitopatógeno en este medio, las pruebas de antagonismo se hicieron en agar PDA porque en este medio y teniendo en cuenta las pruebas de crecimiento, los actinomicetos lograron crecer al igual que P. infestans, evitando así condiciones desfavorables debidas al tipo de sustratos para cualquiera de los dos grupos de microorganismos.
Características y conteo de actinomicetos de los purines. Las características organolépticas de los purines variaron desde el principio hasta el final de la preparación. Con excepción del purin de flores (pH 9,0), los demás purines registraron pH estable alrededor de 6 (Tabla 1). Este valor mayor pudo inhibir el crecimiento de los actinomicetos cuyo rango de tolerancia se ubica entre pH 6,0 a 8,0.
Tabla 1. Características organolépticas de purines de chipaca (Bidens pilosa L.).

La cantidad de actinomicetos para los purines mezcla, tallos-hojas, flores y raíces fue de 26 x 102, 16 x 102, < 102 y 35 x 103 UFC mL-1, respectivamente. De estos, se aislaron 25 morfotipos, 9 de ellos del purín de la mezcla y 8 en los purines hojas -; tallos y raíces (Tabla 2). Su denominación para efectos de identificación siguió el consecutivo AC001 hasta AC025.
Tabla 2. Morfotipos de actinomicetos aislados de diferentes purines de chipaca (Bidens pilosa L.).
En el purin de flores se obtuvieron conteos muy bajos, casi indetectables, de actinomicetos, esto debido o bien a que en su preparación no interviene suelo rizosférico, que es el hábitat donde se encuentran estos microorganismos (Sylvia et al., 1998) o a efectos del pH del purín. En este último aspecto Madigan et al. (2004), indican que pH entre 6,5 y 7,5 permite el desarrollo de la mayoría de las poblaciones microbianas, en tanto que para otros investigadores, los actinomicetos se desarrollan en valores de pH alcalinos y neutros (6,0-8,0) (Villamil y Tamayo, 2003; Ferrera y Alarcón, 2007). En este trabajo solamente el purin de flores registró altos niveles de alcalinidad (9,0), factor que pudo influir en el crecimiento de estos microorganismos.
Los conteos de actinomicetos del purin de raíz obtenidos en este estudio, son similares a los mencionados para este tipo de microorganismos a partir de biopreparados semejantes y los cuales se encuentran en el orden 103-105 UFC mL-1 (Díaz y Enríquez, 2009). Villamil y Tamayo (2003), registraron el crecimiento de actinomicetos en cantidades mayores de 104 UFC mL-1 en caldos microbianos de rizosfera de plantas sanas de papa, a los cuales les adicionaron sustratos como harina de arroz y avena como fuente de carbono para favorecer el crecimiento de estos microorganismos.
Evidencias de antagonismo. De las 25 cepas de actinomicetos aislados, 8 presentaron efecto inhibidor in vitro (placas de medio) del crecimiento del fitopatógeno (Figura 1). El purín que presentó la mayoría de aislamientos con efecto antagónico frente a P. infestans fue el que se obtuvo de la mezcla de todas las partes de la planta (aislamientos AC001, AC010, AC011 y AC012), seguido del purin de tallos - hojas (aislamientos AC013, AC021 y AC023) y por último del purin de raíces (con el aislamiento AC001).
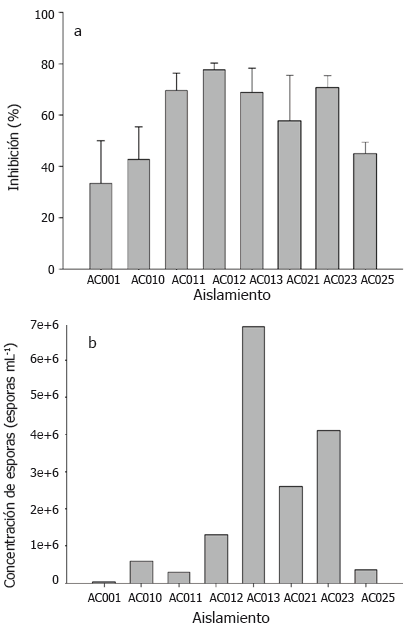
Figura 1. Inhibición en placas de medio de cultivo (a) y concentración de esporas (b) de los actinomicetos enfrentados a Phytophthora infestans. Las líneas sobre las barras indican la desviación estándar.
A pesar de que no se evidenciaron diferencias significativas entre los promedios del porcentaje de inhibición por las cepas seleccionadas, los aislamientos AC012 y AC023 expresaron los mayores halos de inhibición, con concentraciones de 13 x 105 y 41 x 105 esporas mL-1, respectivamente (Figura 1). En contraste, el aislamiento AC001 presentó la menor capacidad de inhibición y cantidad de esporas (0,4 x105 esporas mL-1).
Existen dos posibles explicaciones a la inhibición del crecimiento de P. infestans presentada en este estudio. En primer lugar, se observa que los aislamientos con el menor conteo de esporas (AC001, AC011 y AC025 que registraron 0,4, 6,3 y 3,6 x 105 esporas mL-1, respectivamente), se relacionaron con porcentajes medios y altos de inhibición (33,3, 68 y 45,1%), lo que podría indicar que tales aislamientos serian muy efectivos porque con pocas esporas disminuyen sustancialmente el crecimiento de P. infestans (Figura 2) o porque generan algunas sustancias biocidas o antibióticos que se difunden a través de la placa de medio. Sin embargo, no ocurre lo mismo con los aislamientos AC013, AC021 y AC023 que, a pesar de presentar altos porcentajes de inhibición (68,7; 57,8 y 70,7%, respectivamente) lo hacen también con concentraciones altas de esporas (69, 26 y 41 x 105 esporas mL-1). En un lugar intermedio se encuentran los aislamientos AC010 y AC012 que inhibieron el crecimiento de P. infestans en 42,74 y 77,8% pero en conteos de 6 y 13 x 105 esporas mL-1.
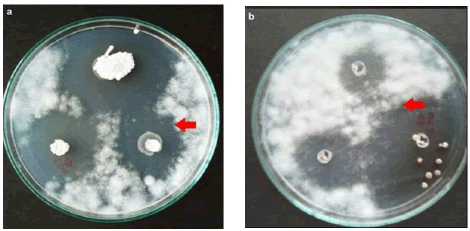
Figura 2. Zonas de trasparencia o halos de inhibición in vitro contra Phytophthora infestans por parte de los aislamientos AC011 (a) y AC001 (b), que presentaron la mejor eficiencia de antagonismo con baja concentración de esporas.
Otra explicación implicaría aceptar que los altos porcentajes de inhibición presentados por los aislamientos que a su vez muestran los mayores conteos de esporas, pueden significar que estos microorganismos, dentro de las placas de medio, compiten eficientemente por espacio y nutrientes afectando el crecimiento del patógeno ya que su esporulación es alta y permite su rápido crecimiento.
Es de anotar que la levadura Saccharomyces cerevisiae utilizada en la preparación de los purines para iniciar los procesos de fermentación, probablemente no posee efectos sobre las poblaciones de actinomicetos, debido a que se agrega en muy bajas cantidades dentro del purín, que es dominado por otros microorganismos provenientes del material vegetal que generan alta competencia por nutrientes.
Por otra parte, no fue posible establecer relaciones entre los aislamientos obtenidos por tipo de purin y su capacidad inhibitoria del patógeno, situación que indica la necesidad de incrementar este tipo de estudios. Además, es necesario realizar pruebas con cada uno de los aislamientos de actinomicetos que mostraron halo de inhibición frente a P. infestans, con el fin de establecer la Concentración Mínima Inhibitoria (CMI) del crecimiento del fitopatógeno.
Los actinomicetos, especialmente los pertenecientes al género Streptomyces sp., han sido utilizados junto a otras poblaciones microbianas, no solo en la inhibición de P. infestans, sino también de otros fitopatógenos (Krupa y Dommergues, 1981; Castillo et al., 2001; Leoni y Ghini, 2003; Tian et al., 2004; Khamna et al., 2009).
Lozoya et al. (2006), enfrentaron diversos microorganismos entre ellos el actinomiceto Streptomyces sp., contra P. infestans utilizando hojas de papa y observaron disminución del desarrollo de la enfermedad por todos los microorganismos utilizados. En otro ensayo de los mismos autores con macetas en campo, la mezcla de Streptomyces sp., Pseudomonas sp. y Burkholderia sp., ejercieron una mejor inhibición que los demás microorganismos probados.
Algunas especies de Streptomyces han sido enfrentadas a fitopatógenos como Rhizoctonia solani y Ralstonia solanacearum, demostrando efectividad en el control in vitro de estos hongos (Krupa y Dommergues, 1981; Castillo et al., 2001). Por otra parte, Gomes et al. (2000), encontraron que ciertos actinomicetos actuaban como biocontroladores de hongos fitopatógenos, debido a que presentaban actividad endoquitinolítica o producción de hexoquinasas y quitobiasas contra estos patógenos.
Los actinomicetos se destacan también dentro de la ecología microbiana del suelo por ser los mayores productores de sustancias biocidas o antibióticas como metabolitos secundarios a su crecimiento y que en determinadas situaciones de competencia por espacio o nutrientes son efectivas para el control de otros microorganismos (Baltz, 2008; Genilloud, 2011). Recientemente, aprovechando esta capacidad de los actinomicetos, se han desarrollado productos de uso agrícola que se comercializan en el mercado de insumos, con buenos resultados en el control biológico de algunas especies de hongos fitopatógenos (Nanjwade, 2010). Cuesta et al. (2010), establecieron el potencial de algunas especies del género Streptomyces provenientes de proceso de compostaje de residuos vegetales, como alternativa de biocontrol de fitopatógenos, lo cual indica la favorabilidad de este tipo de hábitat para albergar actinomicetos.
Los resultados anteriores muestran que existe potencial en algunas cepas de actinomicetos obtenidos de purines de chipaca para inhibir el crecimiento de P. infestans, aunque es necesario profundizar las investigaciones tanto en medios controlados como en campo, para respaldar su uso y diseminación en agricultores ecológicos.
CONCLUSIONES
De los purines de chipaca se aislaron 25 morfotipos diferentes de actinomicetos, de los cuales ocho cepas inhibieron el crecimiento de P. infestans en placas de medio.
El purín que presentó la mayoría de aislamientos con efecto antagónico frente a P. infestans fue el que se obtuvo de la mezcla de todas las partes de la planta (cuatro aislamientos), seguido del purin de tallos - hojas (tres aislamientos) y por último del purin de raíces (con un el aislamiento). Del purín de flores no se aislaron actinomicetos.
Los niveles de pH de los purines de mezcla (6,08), tallos y hojas (6,01) y raíces (6,01), se encontraban en rangos óptimos para el desarrollo de los actinomicetos (pH entre 6,0 y 8,0), pero en el purin de flores el pH se mantuvo en 9,0 a lo largo de todo el estudio, situación que probablemente afectó el crecimiento de actinomicetos en este purín.
La densidad poblacional de actinomicetos más alta se presentó en el purin de raíces, debido a que es el órgano de la planta cuya superficie tiene mayor contacto con el suelo y este constituye el hábitat natural para estos microorganismos.
El promedio del porcentaje de inhibición, obtenido por la medición de las zonas de inhibición o de los halos generados por algunas de las cepas de actinomicetos contra P. infestans, estuvo entre 33% y 77%, con conteos de esporas desde 0,4 hasta 6,9 x 106 esporas mL-1, siendo más efectivos los aislamientos AC001, AC010, AC011 y AC025, que registraron 0,4, 6,3 y 3,6 x 105 esporas mL-1.
BIBLIOGRAFÍA
Agrios, G. 2002. Fitopatología. Segunda edición. Limusa, México D.F. 838 p. [ Links ]
Baltz, R. 2008. Renaissance in antibacterial discovery from actinomycetes. Current Opinion in Pharmacology 8(5): 557-563. [ Links ]
Castaño, J., B. Villegas, B.C. Villegas, M.E. Márquez, J.C. Pérez y J. Gaviria. 1996. Manejo del tizón tardío de la papa: estado actual. pp. 253-263. En: UNIPAPA-ICA-CORPOICA. Papas colombianas, con el mejor entorno ambiental. Comunicaciones y Asociados Ltda, Bogotá. 272 p. [ Links ]
Castillo, E., G. Gallegos, F. Hernández, M. Cepeda y V. Zamora. 2001. Efectividad de actinomicetos aislados de la rizósfera de papa sobre Rhizonctonia solani Kühn in vitro. Revista Mexicana de Fitopatología 22(2): 203-207. [ Links ]
Cuesta, G., R. García, M. Abad y F. Fornes. 2010. Isolation and identification of actinomycetes from a compost-amended soil with potential as biocontrol agents. Article in press. Journal of Environmental Management 1-5 p. [ Links ]
Díaz, L. y A. Enríquez. 2009. Caracterización microbiológica preliminar de diferentes biofertilizantes-bioestimulantes líquidos (bioles) preparados en una finca agroecológica de Tenjo (Cundinamarca). Trabajo de grado Bacteriología y Laboratorio Clínico. Facultad de Ciencias de la Salud. Universidad Colegio Mayor de Cundinamarca, Bogotá. 122 p. [ Links ]
Englander, L. and F. Roth. 1980. Interaction of light and sterol on sporangium and chlamydospore production by Phytophthora lateralis. The American Phytopathological Society 70(7): 650-654. [ Links ]
Erwin, D. and S. Bartnicki. 1983. Phytophthora: Its biology, taxonomy, ecology and pathology. The American Phytopathological Society, St. Paul, Minnesota. 392 p. [ Links ]
Ferrera R. y A. Alarcón. 2007. Microbiología agrícola: hongos, bacterias, micro y macrofauna, control biológico y planta-microorganismo. Editorial Trillas, Mexico D.F. 568 p. [ Links ]
Genilloud, O., I. González, O. Salazar, J. Martín, J. Tormo and F. Vicente. 2011. Current approaches to exploit actinomycetes as a source of novel natural product. Journal of Industrial Microbiology and Biotechnology 38(3): 375-;389. [ Links ]
Gomes, R, L. Semedo, R. Soares, C. Alviano, L. Linhares and R. Coelho. 2000. Chitinolytic activity of actinomycetes from a cerrado soil and their potencial in biocontrol. Letter Applied Microbiology 30(2): 146-150. [ Links ]
Grünwald, N.J., W. Flier, A. Sturbaum, E. Garay, T. Van Den Bosch, C. Smart, J. Matuszak, H. Lozoya, L. Turkensteen and W. Fry. 2001. Population structure of Phytophthora infestans in the Toluca Valley Region of Central Mexico. Phytopathology 91(9): 882-890. [ Links ]
Jaramillo, S., L. Patiño, J. López, P. Buriticá, M. Márquez, J. Zapata y J. Morales. 1997. Historia y origen del patosistema Phytophthora infestans / Solanum. Una revisión. pp. 1-15. En: Memorias. IV Foro de Sanidad Vegetal y Primer Seminario Nacional sobre Gota de la Papa. Universidad Nacional de Colombia, Medellín. [ Links ]
Khamna, S., A. Yokota and S. Lumyong. 2009. Actinomycetes isolated from medicinal plant rhizosphere soils: diversity and screening of antifungal compounds, indole-3-acetic acid and siderophore production. World Journal of Microbiology and Biotechnology 25(4): 649-;655. [ Links ]
Krupa, S.V., and Y.R. Dommergues. 1981. Ecology of root pathogens. Second edition. Elsevier Scientific Publishing Company, New York. 292 p. [ Links ]
Lee, R. 2003. Reconversión de fincas a producción sostenible, metodología interactiva. Fundación Universidad Jorge Tadeo Lozano, Bogotá. 48 p. [ Links ]
Lee, J., D. Sherman and B. Hwang. 2008. In vitro antimicrobial and in vivo antioomycete activities of the novel antibiotic thiobutacin. Pest Management Science 64(2): 172-;177. [ Links ]
León, T. y D. Castellanos. 2002. Aplicación de técnicas de resistencia sistémica con microorganismos de rizosfera para el control de gota en cultivo orgánico y convencional de papa (Tenjo -; Cundinamarca). Informe de actividades, Código Pronatta 201251054. Bogotá. 120 p. [ Links ]
Leoni, C. e R. Ghini. 2003. Efeito do lodo de esgoto na indução de supressividade in vitro a Phytophthora nicotianae. Fitopatologia Brasileira 28(1): 67-75. [ Links ]
Lozoya, H., M. Coyote, R. Cerrato y E. Lara. 2006. Antagonismo microbiano contra Phytophthora infestans (Mont) de Bary. Agrociencia 40(4): 491-499. [ Links ]
Madigan, M., J. Martinko y J. Parker. 2004. Biología de los microorganismos. Decima edición. Pearson Educación S.A., Madrid. 1096 p. [ Links ]
Nanjwade, B., S. Chandrashekhara, P. Goudanavar, A. Shamarez and F. Manvi. 2010. Production of antibiotics from soil-isolated actinomycetes and evaluation of their antimicrobial activities. Tropical Journal of Pharmaceutical Research 9(4): 373-377. [ Links ]
Poorniammal, R., S.P. Sundaram and K. Kumutha. 2009. In Vitro biocontrol activity of Methylobacterium extorquens against fungal pathogens. International Journal of Plant Protection 2(1): 59-62. [ Links ]
Powelson, M. and D. Inglis. 1999. Foliar fungicides as protective seed piece treatments for a management of a late blight of potatoes. Plant Disease 83(3): 265-268. [ Links ]
Ramírez, C. 1996. Purines, herramienta útil para proteger y mejorar cultivos. Guía para su preparación, uso y manejo. En: Agronet,http://www.agronet.gov.co/www/docs_si2/2006718153859_Agricultura%20bajo%20costo%20y%20sostenible.pdf. 8 p.; Consulta: noviembre 2008. [ Links ]
Riveros, F., R. Sotomayor, V. Rivera, G. Secor y B. Espinoza. 2003. Resistencia de Phytophthora infestans (Montagne) de Bary a Metalaxil, en cultivo de papas en el norte de Chile. Agricultura Técnica 63(2): 117-124. [ Links ]
Sánchez, V., R. Shattock y E. Bustamante. 2000. Caracterización de aislamientos de Phytophthora infestans nativos de Costa Rica. Manejo Integrado de la Papa 55(1): 56-63. [ Links ]
Sylvia, D., J. Fuhrmann, P. Hartel, D. Zuberer. 1998. Principles and applications of soil microbiology. Prentice Hall. Upper Saddle River, USA. 640 p. [ Links ]
Tian, X., L. Cao, H. Tan, Q. Zeng, Y. Jia, W. Han and S. Zhou. 2004. Study on the communities of endophytic fungi and endophytic actinomycetes from rice and their antipathogenic activities in vitro. World Journal of Microbiology y Biotechnology 20(3): 303-309. [ Links ]
Tsao, P. 1970. Selective media for isolation of pathogenic fungi. Annual Review of Phytopathology 8(2): 157-186. [ Links ]
Valencia, H.A. 2004. Manual de prácticas de microbiología básica. Unibiblos, Bogotá. 140 p. [ Links ]
Verma, V., S. Gond, A. Kumar, A. Mishra, R. Kharwar and A. Gange. 2008 Endophytic actinomycetes from Azadirachta indica A. Juss.: Isolation, diversity, and anti-microbial activity. Microbial Ecology 57(4): 749-756. [ Links ]
Villamil, M. y S. Tamayo. 2002. Manual de procedimientos microbiológicos, laboratorio de biotecnología. Centro Internacional de Física (CIF), Bogotá. 110 p. [ Links ]
Villamil, M. y S. Tamayo. 2003. Evaluación de crecimiento de actinomicetos en caldos microbianos de rizosfera de papa (Solanum tuberosum). Trabajo de grado Microbiología Industrial. Facultad de Ciencias. Pontificia Universidad Javeriana. Bogotá. 200 p. [ Links ]
Waterhouse, G., F. Newhook and D. Stamps. 1983. Present criteria for clasification of Phytophthora. pp. 139-147. In: D.C. Erwin, S. Bartnicki-Garcia, and P. H. Tsao (eds.). Phytophthora: its biology, taxonomy, ecology and pathology. American Phytopathological Society, St. Paul, Minn. 392 p. [ Links ]
Williams, S. and F. Davies. 1965. Use of antibiotics for selective isolation and enumeration of actinomycetes in soil. Journal of General Microbiology 38(2): 251-261. [ Links ]














