Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Facultad Nacional de Agronomía Medellín
Print version ISSN 0304-2847
Rev. Fac. Nac. Agron. Medellín vol.65 no.1 Medellín Jan./June 2012
Efecto de la Adición ex vivo del Lipopolisacárido de Escherichia coli sobre la Absorción de Lisina en Cerdos Destete
Effect of Adding ex vivo Lipopolysaccharide from Escherichia coli on the Absorption of Lysine in Weaned Pigs
Cristian Gutiérrez Vergara1; Yony Román Ochoa2; Carlos Peláez Jaramillo3; Johana Ciro Galeano4; Albeiro López Herrera5 y Jaime Parra Suescún6
1 Zootecnista. Universidad Nacional de Colombia - Sede Medellín - Facultad de Ciencias Agrarias. A.A. 1779, Medellín, Colombia. <ccgutier@unal.edu.co>
2 Químico. Universidad de Antioquia. Facultad de Ciencias Exactas y Naturales. A.A. 1226, Medellín, Colombia. <yonyroa@gmail.com>
3 Profesor Asociado. Universidad de Antioquia - Facultad de Ciencias Exactas y Naturales. A.A. 1226, Medellín, Colombia. <directorgiem@gmail.com>
4 Zootecnista. Universidad Nacional de Colombia - Sede Medellín - Facultad de Ciencias Agrarias. A.A. 1779, Medellín, Colombia. <jacirog@unal.edu.co>
5 Profesor Asociado. Universidad Nacional de Colombia - Sede Medellín - Facultad de Ciencias Agrarias. A.A. 1779, Medellín, Colombia. <alherrera@unal.edu.co>
6 Profesor Auxiliar. Universidad Nacional de Colombia - Sede Medellín - Facultad de Ciencias Agrarias. A.A. 1779, Medellín, Colombia. <jeparrasu@unal.edu.co>
Recibido: Octubre 14 de 2011; aceptado: Abril 26 de 2012.
Resumen. Con el destete brusco se induce la mortalidad de lactobacilos y el aumento de la población de E. coli, que liberan desde su pared productos proinflamatorios como el lipopolisacárido (LPS). El LPS activa una serie coordinada de señales que involucran a la familia de las MAPK, iniciando una cascada de reacciones que interrumpen los procesos de transporte de nutrientes y pueden progresar a fallo orgánico múltiple. El objetivo de este estudio fue determinar el efecto de la adición ex vivo de diferentes niveles de lipopolisacárido de E. coli sobre la absorción de lisina en cerdos destete. El trabajo de campo se realizó con 16 cerdos destetados a los 21 días de edad. Los animales fueron alimentados durante 10 días con una dieta basal que tuvo como componentes leche y algunos de sus derivados. Los cerdos se sacrificaron escalonadamente los días 1, 5, 7 y 10 posdestete y se realizó extracción del yeyuno, al que se le adicionaron las sustancias: Lisina 0,91 mg mL-1; LPS de E. coli (0,3 µg) y dos inhibidores de la ruta MAPK (a) SB-203580 (10, 20 y 50 mM) (b) U-0126 (10, 20 y 50 mM). La adición de 20 Mm de cualquiera de los inhibidores de MAPK aumentó significativamente la absorción de lisina (P<0,01). Los animales con 10 días posdestete presentaron el mayor porcentaje de absorción (P<0,01). Se concluye que el lipolisacárido de E. coli contribuye a la interrupción de los mecanismos de transporte intestinal de lisina.
Palabras clave: Intestino delgado, MAPK, productos proinflamatorios, transporte intestinal.
Abstract. With the abrupt weaning mortality of lactobacillus is induced and E. coli population is increased, which release proinflammatory products from their wall cell such as lipopolysaccharide (LPS). LPS activates a coordinated series of signs that involve the MAPK family, initiating a cascade of reactions that interrupt nutrient transport processes and can progress to multiple organic failure. The aim of this study was to determine the effect of adding ex vivo different levels of lipopolysaccharide of E. coli on lysine absorption in weaned pigs. The experiment was carried out with 16 weaned pigs 21 days old. Animals were fed during 10 days with a basal diet with milk and some of its derivatives. Pigs were sequentially slaughtered on days one, five, seven, and 10 after weaning, and jejunum extraction was realized to which the following substances were added: Lysine 0.91 mg mL-1, LPS from E. coli (0.3 mg) and two MAPK pathway inhibitor (a) 203580 (10, 20 y 50 mM) (b) U-0126 (10, 20 y 50 mM). The addition of either 20 mm MAPK inhibitors significantly increased the uptake of lysine (P<0.01). Animals with 10 days post-weaning showed the highest percentage of absorption (P<0.01). As conclusion the lipopolysaccharides of E. coli contribute to the disruption of intestinal transport mechanisms of lysine.
Key words: intestinal transport, MAPK, proinflammatories products, small intestine.
El sistema de producción de cerdos no sólo ha avanzado en la obtención de animales destetados a edades más tempranas, sino también hacia la obtención de líneas genéticas precoces con mejores índices de conversión de alimento (Gómez, 2006). Sin embargo, el destete precoz esta siempre relacionado con problemas digestivos y diarreas, lo que frecuentemente se ve traducido en la reducción del crecimiento y utilización de nutrientes (Touchette et al., 2002).
Además de los problemas mencionados anteriormente, existen otros factores que usualmente limitan el crecimiento y la capacidad productiva del cerdo, entre estos se encuentran el desarrollo intestinal, factores ambientales, presencia de estrés y la misma respuesta inmunológica, los cuales afectan los procesos de absorción y uso de nutrientes, principalmente de lisina (Blecha, 2000). Por tal motivo, la práctica del destete tiene implicaciones tanto sobre el bienestar del animal, como en el aspecto económico.
La alimentación del cerdo recién destetado, es uno de los aspectos más críticos en los sistemas de producción porcinos, ya que éstos se basan en suplir en primera instancia los requerimientos de lisina (Lys), el cual se considera como el primer aminoácido limitante en cerdos alimentados principalmente con dietas basadas en maíz-soya (NRC, 1998). Además, los animales con mayor potencial genético para depositar magro (proteína) tendrán un mayor requerimiento de todos los aminoácidos, principalmente Lys, de modo que la selección genética para magro no solo incrementa los requerimientos de Lys, sino de todos los aminoácidos (Friesen et al., 1994). Debido a lo anterior, el diseño de un programa de alimentación acertado tendrá un efecto significativo sobre los rendimientos futuros de los cerdos.
Además, hay que considerar que el posterior consumo de una nueva ración sólida durante la etapa posdestete, resulta en la reducción drástica y posterior mortalidad de la población de lactobacilos y estreptococos, mientras que el número de bacterias coliformes (en especial Escherichia coli) aumentan durante la primera semana posdestete. Esta población al ir aumentando y muriendo, provoca la liberación desde su pared celular de productos proinflamatorios como el lipopolisacárido (LPS). El LPS es un patrón molecular asociado a patógenos (PAMP) que es reconocido en cualquier hospedero mamífero como una entidad patogénica importante (Amador et al., 2007).
Este LPS provoca alteraciones importantes en la estructura intestinal, que conllevan a la interrupción de su capacidad funcional, principalmente de los procesos de digestión y absorción de nutrientes (Pluske et al., 1997; Amador et al., 2007). El daño físico a nivel intestinal inicia la activación de una serie coordinada de señales que involucran varias proteínas quinasas, donde la familia de las protein kinasas activadoras por mitógenos (MAPK) es de gran importancia (Korcheva et al., 2007; Oner et al., 2008).
Las MAPK son un grupo de serina/treonina quinasas presentes en todas las células eucariotas que participan en múltiples procesos celulares, y son activadas en respuesta a una gran variedad de estímulos (Waetzig et al., 2002). Las MAPK desempeñan un papel central en la regulación de una variedad de respuestas inflamatorias, entre las que se encuentran la expresión de mediadores proinflamatorios como el factor de necrosis tumoral alfa (TNF-a) y las (IL) interleuquinas (Ono y Han, 2000; Roy et al., 2010; Yuang et al., 2010).
Algunos autores han reportado que las alteraciones intestinales pueden provocar anormalidades en el transporte intestinal de agua y electrolitos (Amador et al., 2007; García et al., 2008). Sin embargo, el efecto de estas alteraciones sobre la absorción intestinal de nutrientes es menos conocido que su acción sobre los procesos de transporte de agua y electrolitos. En cuanto a los mecanismos de transporte de aminoácidos a través del epitelio intestinal, recientes trabajos han evidenciado que la absorción intestinal de algunos aminoácidos (leucina) es inhibida por la adición al tejido de LPS de E. coli (Abad et al., 2001b; 2002a; Rebollar et al., 2003; Amador et al., 2007).
Dado que la administración de LPS de E. coli es uno de los modelos más empleados en estudios para simular procesos infecciosos agudos, por tener acciones altamente reproducibles y carecer de los efectos secundarios asociados a las infecciones crónicas, el objetivo de este trabajo fue conocer las implicaciones de la inflamación intestinal inducida por la adición ex vivo de diferentes niveles de LPS de E. coli sobre los mecanismos de absorción de lisina y su relación con las proteínas quinasas activadas por mitógeno (MAPK) a nivel intestinal (yeyuno), en cerdos durante varios períodos posdestete.
MATERIALES Y MÉTODOS
Consideraciones éticas. Todos los procedimientos experimentales fueron llevados a cabo de acuerdo a las guías propuestas por "The International Guiding Principles for Biomedical Research Involving Animals" (CIOMS, 1985). Esta investigación fue avalada por el Comité de Ética en la Experimentación Animal de la Universidad Nacional de Colombia, Sede Medellín (CEMED 001 del 26 de enero de 2009).
Localización. El trabajo de campo se realizó en el Centro Agropecuario San Pablo, perteneciente a la Universidad Nacional de Colombia - Sede Medellín, ubicado en el municipio de Rionegro, localizado a 2.100 msnm, con una temperatura entre 12 y 18 °C, correspondiendo a una zona de vida bosque muy húmedo Montano bajo (bmh-MB).
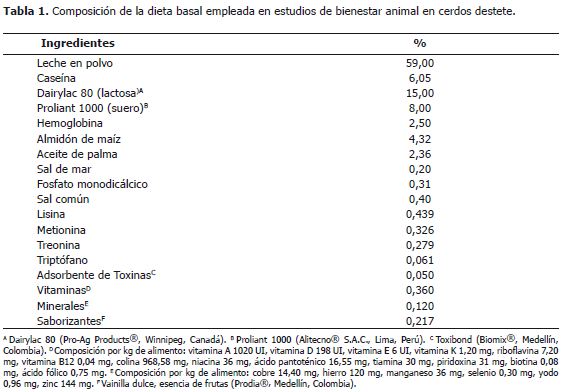
Animales y dieta. Se utilizaron 16 cerdos, resultado de un cruce alterno Duroc x Landrace, destetados exactamente a los 21 días de edad, con un peso de 6,5 ± 0,5 kg. Estos lechones fueron alojados en grupos de cuatro y en jaulas provistas de comedero de canoa, las cuales fueron ubicadas en un cuarto con temperatura controlada a 26 ± 3 °C. Los animales dispusieron de agua a voluntad durante todo el experimento. La dieta basal ofrecida a los animales tuvo como componente leche y algunos de sus derivados. Además, fue enriquecida con vitaminas, minerales y lisina HCL. Las dietas se balancearon para cumplir con todos los mínimos nutricionales requeridos y propuestos por el NRC (1998) (Tablas 1 y 2). La cantidad de alimento ofrecido por jaula fue de 300 g/día; sin embargo, se suministró alimento adicional cuando los animales lo requirieron. La dieta basal se proporcionó desde el día uno al 10 posdestete. Durante la lactancia no se suministró alimento sólido a los lechones.
Tipo de estudio. En este experimento se evaluaron siete soluciones que se adicionaron directamente al medio de incubación a las concentraciones deseadas, para valorar su efecto directo sobre el tejido intestinal. Las sustancias que conformaron las diferentes soluciones en estudio fueron Lys (0,91 mg mL-1), LPS (0,3 mL mL-1), Inhibidor de la vía MAPK 1 (Inhibidor de p38 MAPK quinasa; 10, 20 y 50 Mm), e Inhibidor de la vía MAPK 2 (inhibidor de MAPKK, MEK-1 y MEK-2; 10, 20 y 50 Mm).
Toma de muestras de tejido intestinal. Durante la fase experimental se sacrificaron 16 cerdos de la siguiente forma: el día inicial, o día uno (día del destete), se sacrificaron cuatro cerdos, que representaron el grupo de referencia para determinar la absorción de Lys el día del destete, antes de suministrar las diferentes sustancias en estudio. Los días cinco, siete y 10 posdestete fueron sacrificados cuatro cerdos. Todos los cerdos fueron sacrificados 2,5 horas después de su última comida. Los animales se sedaron por inhalación de dióxido de carbono durante 3 min y fueron sacrificados por exanguinación, mediante sección de la vena yugular. Después del sacrificio, los cerdos se colocaron en posición de cúbito dorsal, se incidió la región abdominal y se extrajo completamente el intestino delgado desde la unión pilórica hasta la válvula íleo-cecal (Segales y Domingo, 2003). El intestino fue alineado y medido en una mesa sin ningún tipo de tensión. Posteriormente éste se dividió en tres regiones: duodeno, yeyuno, e íleon de igual tamaño, y se tomaron 40 cm del centro del yeyuno. El yeyuno se fragmentó en nueve partes, de aproximadamente 2 g cada uno, eliminando las zonas que presenten placas de Peyer. La digesta contenida en cada una de las partes se removió mediante lavado por infusión con solución salina fría según lo descrito previamente (Reis de Souza et al., 2005).
Protocolo para inducción de inflamación ex vivo.
Medio de incubación. Para mantener el tejido intestinal en óptimas condiciones durante los procesos experimentales, se utilizó solución Ringer preparada diariamente a partir de las siguientes soluciones:
1. Solución B: 20,024 g de KHCO3, 1,08 g de K2HPO4 y 1,095 g de KH2PO4; completando hasta un litro con agua destilada.]
2. Solución C: 2,663 g de CaCl2 y 4,880 g de MgCl2.6H2O; completando hasta un litro con agua destilada.
Ambas soluciones fueron conservadas en refrigeración en nevera (4-8 °C) y tuvieron como tiempo de caducidad un mes. El medio de incubación se preparó disolviendo 4,09 g de NaCl en 300 mL de agua destilada, posteriormente se le añadió 25 mL de solución B y por último se adicionaron 25 mL de la solución C enrasando con agua destilada aforando hasta 500 mL. La proporción final de Solución B y C en el Ringer, es de 1:20. El pH del medio fue ajustado a 7,4 con ácido cítrico.
Técnica de medida de acumulación tisular de sustrato. Inmediatamente después del sacrificio, se dejó expuesto el lado mucosal de cada uno de los fragmentos a la acción de las sustancias durante las incubaciones. Cada fragmento fue introducido en tubos de ensayo que contenían 3 mL del medio de incubación, al que se le añadió la concentración deseada de lisina, LPS e inhibidores de la vía MAPK (según el tratamiento) de la siguiente forma:
- Tubo 1 (S1): solución de incubación (nivel basal de Lys en el tejido).
- Tubo 2 (S2): S1 + Lys 0,91 mg mL-1 (nivel de Lys total en el tejido: basal + absorbida).
- Tubo 3 (S3): S2 + LPS de E. coli 7 (0,3 mL mL-1).
- Tubo 4 (S4): S3 + Inhibidor 18 a concentración 10 mM.
- Tubo 5 (S5): S3 + Inhibidor 18 a concentración 20 mM.
- Tubo 6 (S6): S3 + Inhibidor 18 a concentración 50 mM.
- Tubo 7 (S7): S3 + Inhibidor 29 a concentración 10 mM.
- Tubo 8 (S8): S3 + Inhibidor 29 a concentración 20 mM.
- Tubo 9 (S9): S3 + Inhibidor 29 a concentración 50 mM.
7 Serotipo 0111:B4 (Sigma-Aldrich®, St Louis, MO, USA), concentración 0,3 mg mg-1 de alimento.
8 Inhibidor de la vía MAPK 1: SB-203580 (Sigma-Aldrich®, St Louis, MO, USA).
9 Inhibidor de la vía MAPK 1: U-0126 (Sigma-Aldrich®, St Louis, MO, USA).
Los tubos fueron mantenidos a 37 °C en baño termostatizado durante todo el periodo experimental. Bajo estas condiciones, los tejidos fueron incubados durante 3 min adicionando el LPS en primera medida (Tubos 3-9). Posterior a este periodo, los fragmentos intestinales que pertenecían a los tubos 4-9 (con inhibidores de MAPK) fueron incubados por 12 min. Finalmente, cada fragmento (tubos 2-7) se incubó durante otros 3 min con Lys. Transcurrido el tiempo de incubación de 3 min para absorción de Lys, los fragmentos intestinales fueron extraídos y rápidamente lavados con solución Ringer fría. Este paso se realizó con la finalidad de retirar el sustrato no absorbido y adherido al tejido y detener el proceso de acumulación. A continuación los fragmentos fueron secados ligeramente en un papel de filtro previamente humedecido para no dañar el tejido.
Posteriormente, se pesó cada fragmento intestinal y se introdujo en un criovial que fue congelado a -20 °C y transportado para la realización de análisis de laboratorio. Paralelamente, dos de los nueve fragmentos intestinales fueron utilizados para determinar la concentración basal (Tubo 1) y la concentración final absorbida de lisina (adición de Lys 0,91 mg mL-1) en el tejido bajo condiciones normales (Tubo 2). La concentración de Lys acumulada en el tejido fue expresada como porcentaje de lisina absorbida. Lo anterior se calculó con las siguientes ecuaciones:
Lys acumulada testigo 10 = [Lys final tejido]-[Lys basal tejido]
Lys acumulada tratamientos = [Lys final tejido tratamientos] - [Lys basal tejido]
Lys absorbida (%) = [Lys acumulada tratamientos] / [Lys acumulada testigo]*100
Determinación de lisina en mucosa intestinal. Las muestras de mucosa intestinal obtenidas de los diferentes segmentos de intestino delgado fueron procesadas y analizadas en el Laboratorio del Grupo Interdisciplinario de Estudios Moleculares (GIEM) de la Universidad de Antioquia. Las muestras fueron liofilizadas durante dos días a una presión de 133 x 10-3 mbar y una temperatura de -40 °C (Labcondo Freeze Dry System/Freezone 4,5). Una vez liofilizada la muestra, se trituró con una espátula hasta conseguir un material muy fino. Al tubo con la muestra triturada se le agregó 1 mL de HCl 0,01 M y se agitó en un vórtex por dos minutos aproximadamente, hasta conseguir una mezcla homogénea; luego se centrifugó a 12.000 rpm, por 15 min a 4 °C. Posteriormente se recogió el sobrenadante que contenía la extracción de lisina absorbida y se guardó a -20 °C hasta la cuantificación. Se repitió este procedimiento de extracción dos veces hasta que se consideró extraída en su totalidad la lisina. Los sobrenadantes se acumularon en el mismo tubo y se descartó el material sólido. El sobrenadante resultante de las extracciones fue liofilizado en su totalidad. La muestra resultante del liofilizado es la muestra de análisis para la determinación por electroforesis capilar, la cual se reconstituyó en 2,0 mL de HCl 0,01 M.
Se utilizó un sistema de electroforesis capilar (Hewlett-Packard® HP-CE) equipado con un detector UV-Vis de arreglo de diodos. El control del instrumento y el procesamiento de datos fue realizado con el Software Chemstation HP-CE versión A06.03. Para la determinación de lisina por electroforesis capilar, se requirió acondicionar el capilar con un medio electroforético que contenía un visualizador de movilidad similar a la de los analitos y agentes complejantes. De esta forma, se obtuvo una buena separación y mayor sensibilidad. Antes de cada inyección el capilar fue acondicionado por 10 min con el electrolito de corrido (Buffer). La solución electrolítica (buffer) fue preparada con un contenido de 20,0 mM de PDC (2,6-pyridine dicarboxylic acid) y 0,5 mM de CTAB el cual se utilizó para invertir el sentido del flujo electroosmótico (EOF). El pH de este electrolito se ajustó con NaOH 1,0 M hasta un valor de 12,3. La cuantificación se realizó por curva de calibración. Para ello se prepararon estándares de aminoácidos disolviendo patrones de los mismos en NaOH 0,1 M o en HCl 0,01 M con el fin de tener todos los aminoácidos en su forma aniónica. Se realizó una mezcla en un balón de 25,0 mL. De esta mezcla se prepararon diferentes diluciones que permitieron obtener un intervalo de concentraciones amplio para elaborar las curvas de calibración. Los estándares preparados se inyectaron en el equipo de electroforesis capilar.
Diseño estadístico. El experimento se realizó según un diseño de bloques al azar (para un total de dos bloques) en un arreglo factorial de 7X4 (siete soluciones experimentales por cuatro períodos posdestete) (Steel et al., 1997). Para la conformación de los bloques se tomó en consideración el peso inicial de los animales. Cada tratamiento tuvo un total de cuatro repeticiones. El análisis estadístico de los datos obtenidos fue desarrollado utilizando el procedimiento de Modelos Lineales Generales (GLM) del SAS (2006). Para realizar la comparación de los promedios entre tratamientos se utilizó una prueba de Duncan (P<0,05).
RESULTADOS
Los cerdos utilizados presentaron un buen estado de salud y se comportaron normalmente; además, no mostraron incrementos en la temperatura rectal (por encima de 38 °C) durante todo el experimento. Los cerdos no evidenciaron signo alguno de enfermedad que causara su retiro o sacrificio inmediato. Al nivel en que se fijó el suministro diario de alimento no hubo sobrantes.
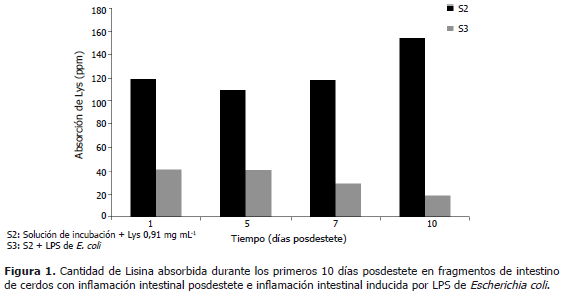
En la Figura 1 puede observarse que a partir del día uno posdestete, en el fragmento intestinal incubado con S2 (solución de incubación + Lys 0,91 mg mL-1), hay una disminución en la absorción de Lys hasta el día cinco posdestete. Sin embargo, a partir de este día, la absorción de Lys aumenta, llegando a su nivel máximo el día 10 posdestete. No obstante, el fragmento que fue sometido a S3 (inducción de inflamación ex vivo) presentó una disminución marcada en la absorción de Lys, donde los días más críticos fueron a partir del día cinco hasta el día siete posdestete, llegando a su mínimo nivel el día 10, momento a partir del cual no se aprecia la recuperación de la absorción de Lys observada en el fragmento incubado con S2.
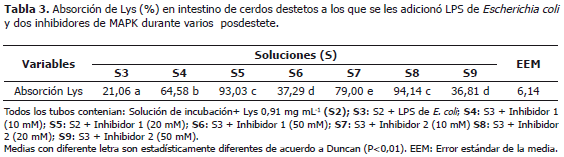
Los promedios generales de absorción intestinal de lisina (Lys) analizados para cada una de las soluciones en estudio y periodos posdestete se pueden observar en las Tablas 3 y 4. Para la variable absorción intestinal de Lys, no se encontró interacción estadística entre las diferentes soluciones experimentales y los períodos posdestete en que fueron sacrificados los cerdos, por lo que no fue necesario analizar y desglosar dichos factores de manera independiente.
Para la variable absorción intestinal de Lys se observó diferencia estadística significativa entre tratamientos (soluciones) (P<0,01), donde el fragmento que fue sometido a S3 (absorción intestinal con inducción de inflamación ex vivo) presentó los menores valores (21%) con respecto a las muestras obtenidas en S5 y S8 (Tabla 3), las cuales presentaron los mayores porcentajes de absorción (93,03 y 94,14%, respectivamente) (P<0,01). S6 y S9 (concentración mayor utilizada, 50 mM) presentaron niveles de absorción de Lys mayores que S3 (P<001); sin embargo, estos porcentajes de absorción son menores al ser comparados con que S5 y S8 (ambos añadidos de inhibidor a la concentración de 20 mM).
Para los períodos posdestete (Tabla 4), el porcentaje de absorción de Lys presentó una disminución estadística significativa (P<0,01) en el día cinco posdestete (53,56%) con respecto al día uno posdestete (73,96%). Sin embargo, los animales con 10 días de destetados presentaron el mayor porcentaje de absorción (80,47%), apreciándose una recuperación total mayor (P<0,01) que la encontrada en los animales del día uno posdestete.
DISCUSIÓN
Este es un estudio pionero en la medición de absorción de lisina en el intestino delgado (yeyuno) de cerdos destetados precozmente (21 días de edad). Para evaluar si la absorción de lisina en cerdos podría ser afectada por inflamación inducida por infecciones bacterianas, se utilizó un modelo experimental ex vivo para inducir inflamación intestinal utilizando LPS de E. coli.
Los resultados observados demuestran que la exposición del intestino al LPS (S3) tiene efectos negativos de gran importancia sobre la permeabilidad, transporte y absorción de algunos nutrientes, específicamente Lys. Estos resultados concuerdan con los publicados por Abad et al. (2001b), quienes encontraron que algunas endotoxinas bacterianas afectan la absorción de azúcares y aminoácidos a nivel intestinal. Esto podría verse representado por el aumento en el catabolismo de la proteína y la disminución en el índice de deposición de la proteína de músculo esquelético de los animales (Liu et al., 2008).
El LPS ha sido catalogado como el principal factor involucrado en la disfunción del intestino durante los procesos de infección causados por bacterias gram-negativas (Abad et al., 2001a; 2002a). Debido a lo anterior, la disminución en el porcentaje de absorción de Lys observada en este trabajo a partir del día uno hasta el día siete posdestete, es consecuencia del efecto del LPS. Estudios in vitro e in vivo indican que ante la presencia de algunas toxinas bacterianas (principalmente LPS) e infecciones microbianas (Stadnyk, 2002; Gopal et al., 2008), y durante los procesos fisiológicos desencadenados por el destete (Pié et al., 2004; Garriga et al., 2005), se estimula la producción de una variedad de citoquinas y de mediadores inflamatorios como TNF-a, IFN-g y ciertas Interleuquinas (IL), los cuales pueden influenciar la permeabilidad y el transporte de iones y nutrientes (Bauer et al., 2006; Davis et al., 2006; Liu et al., 2008).
El TNF-a ha sido involucrado en la disfunción mucosal intestinal inducida por el LPS (Mullin y Smock, 1990), considerándose por tanto, que esta citoquina puede actuar como reguladora directa o indirecta del trasporte iónico y de la permeabilidad epitelial intestinal (McKay y Baird, 1999). Además, la producción de TNF-a durante episodios de estrés e infecciones bacterianas, provoca la reducción del flujo sanguíneo y de la absorción de nutrientes a nivel intestinal y favorece la presentación de diarreas (Koopmans et al., 2006).
Aunado a lo anterior, en este estudio el efecto que tuvo la adición de LPS de E. coli sobre la capacidad funcional del intestino, podría deberse a que este compuesto puede activar una gran variedad de mediadores y rutas de señalización intracelular (Pié et al., 2004; Amador et al., 2007) que afectan el normal desarrollo celular (Garc{ia et al., 2008) e inducen inflamación del tejido. Una vez que se inician estas cascadas de señalización sobreviene una respuesta sistémica no regulada que puede terminar en un estado séptico, fallo orgánico múltiple y por último, la muerte (Hewett y Roth, 1993; Burrell, 1994). Una de las muchas vías de señalización implicadas es la vía de las proteínas quinasas activadas por mitógeno (MAPK) (Ono y Han, 2000).
Las vía de señalización MAPK es una de las más estudiadas, ya que están involucradas en numerosos procesos celulares incluyendo funciones básicas como la proliferación, diferenciación, supervivencia y apoptosis celular (Kolch, 2000). Además, las MAPK desempeñan un papel central en la regulación de una variedad de respuestas inflamatorias, entre las que se encuentran la expresión de mediadores proinflamatorios como el TNF-a y la IL-1 (Waetzig et al., 2002; Roy et al., 2010; Yuang et al., 2010). Como se mencionó anteriormente, el TNF-a disminuye la absorción de algunos aminoácidos por interferir con el funcionamiento de los sistemas de transporte a nivel de membrana de borde en cepillo (Palacin et al., 1998; Abad et al., 2002b).
En esta investigación, la adición de diferentes concentraciones de inhibidores de la vía MAPK al tejido intestinal después del contacto con el LPS aumentó el porcentaje de absorción de Lys, en comparación de los tratamientos que carecían de dichos inhibidores. Esto podría deberse al efecto directo de los inhibidores, ya que la vía de las MAPK está interconectada con la expresión del TNF-a. Esta citoquina activa los tres principales miembros de la familia de las MAPK (p38 MAPK, JNK y p42/44 MAPK) (Amador et al., 2008), los cuales controlan y activan la respuesta celular de la inflamación in vitro (Van den Blink et al., 2001).
En la actualidad se dispone comercialmente de diversos inhibidores de MAPK, los cuales son altamente específicos según el tipo de quinasa a inhibir. El inhibidor SB-203580, es altamente selectivo para la p38 MAPK quinasa (Cuenda et al., 1995) y el inhibidor U-0126 es selectivo de la MAPKK, MEK-1 y MEK-2; además, es un inhibidor débil de PKC, Raf, ERK, JNK, MEKK, MKK-3, MKK-4/SEK, MKK-6, Abl, CdK2 e inhibe la transactivación de AP-1 (Duncia et al., 1998).
Sin embargo, Liu et al. (2008) mencionan que la adición de altas concentraciones de inhibidores de MAPK, podría causar un antagonismo o desequilibrio en los procesos de absorción intestinal de aminoácidos. Este hecho podría haber causado la diminución en los procesos de absorción de lisina a nivel intestinal en esta investigación cuando se adicionó la máxima concentración (50 Mm) de ambos inhibidores de MAPK.
CONCLUSIONES
El LPS de E. coli tiene un gran efecto sobre la funcionalidad intestinal, provocando alteraciones importantes, cuyos efectos contribuyen a la interrupción de los mecanismos de transporte intestinal de lisina.
El uso de inhibidores de MAPK mejoran los mecanismos de transporte y absorción de lisina durante el desarrollo de enteropatías de origen infeccioso en cerdos recién destetados afectados por LPS. Sin embargo, la adición de altas concentraciones de estos inhibidores de MAPK puede afectar igualmente los procesos de absorción de lisina a nivel intestinal. Más investigaciones sobre los mecanismos de acción de estos inhibidores y de las dosis adecuadas, son necesarios para su posible empleo como estrategia terapéutica.
El desarrollo de la técnica de inflamación ex vivo en lechones podría ser utilizada ampliamente como modelo para estudiar la etología de la disfunción intestinal humana. Además, el conocimiento de cómo el LPS de E. coli provoca diarreas y disminuye la absorción de nutrientes a nivel intestinal, podría tener importantes implicaciones tanto para la nutrición animal como para la medicina humana.
BIBLIOGRAFÍA
Abad, B., J.E. Mesonero, M.T. Salvador, J. García and M.J. Rodríguez. 2001a. Effect of lipopolysaccharide on small intestinal L-leucine transport in rabbit. Digestive Diseases and Sciences 46(5): 1113-1119. [ Links ]
Abad, B., J.E. Mesonero, M.T. Salvador, J. García and M.J. Rodríguez. 2001b. The administration of lipopolysaccharide, in vivo, induces alteration in L-leucine intestinal absorption. Life Sciences 70(6): 615-628. [ Links ]
Abad, B., J.E. Mesoreno, M.T. Salvador, J. García and M.J. Rodríguez. 2002a. Cellular mechanism underlying LPS-induced inhibition of in vitro L-leucine transport across rabbit jejunum. Journal of Endotoxin Research 8(2): 127-133. [ Links ]
Abad, B., J.E. Mesoreno, M.T. Salvador, J. García and M.J. Rodríguez. 2002b. Tumor necrosis factor-a mediates inhibitory effect of lipopolysaccharide on L-leucine intestinal uptake. Digestive Diseases and Sciences 47(6): 1316-1322. [ Links ]
Amador, P., J. García, M.C. Marca, J. de la Osada, S. Acín, M.A. Navarro, M.T. Salvador, M.P, Lostao and M.J. Rodríguez. 2007. Intestinal D-galactose transport in an endotoxemia model in the rabbit. Journal of Membrane Biology 215(2-3): 125-133. [ Links ]
Amador, P., M.C. Marca, J. García, M.P. Lostao, N. Guillén, J. de la Osada and M.J. Rodríguez. 2008. Lipopolysaccharide induces inhibition of galactose intestinal transport in rabbits in vitro. Cellular Physiology and Biochemistry 22(5-6): 715-724. [ Links ]
Bauer, E., B.A. Williams, H. Smidt, W.A. Verstegen and R. Mosenthin. 2006. Influence of the gastrointestinal microbiota on development of the immune system in young animals. Current Issues in Intestinal Microbiology 7(2): 35-52. [ Links ]
Blecha, F. 2000. Immune system response to stress. pp.111-121. En: Moberg, G.P. and J.A. Mench (eds.). The biology of animal stress. Basic principles and implications for animal welfare. First edition. CABI Publishing, London, UK. 377 p. [ Links ]
Burrell, R. 1994. Human responses to bacterial endotoxin. Circulatory Shock 43(3): 137-153. [ Links ]
Council for International Organizations of Medical Sciences (CIOMS). 1985. International guiding principles for biomedical research involving animals. CIOMS, Geneva. 28 p. [ Links ]
Cuenda, A., J. Rouse, Y.N. Doza, R. Meier, P. Cohen, T.F. Gallagher, P.R. Young and J.C. Lee. 1995. SB 203580 is a specific inhibitor of a MAP kinase homologue which is stimulated by cellular stresses and interleukin-1. FEBS Letters 364(2): 229-233. [ Links ]
Davis, M.E., S.C. Sears, J.K. Apple, C.V. Maxwell and Z.B. Johnson. 2006. Effect of weaning age and commingling after the nursery phase of pigs in a wean-to-finish facility on growth, and humoral and behavioral indicators of well-being. Journal of Animal Science 84(3): 743-756. [ Links ]
Duncia, J.V., J.B. Santella, C.A. Higley, W.J. Pitts, J. Wityak, W.E. Frietze, F.W. Rankin, J.H. Sun, R.A. Earl, A.C. Tabaka, C.A. Teleha, K.F. Blom, M.F. Favata, E.J. Manos, A.J. Daulerio, D.A. Stradley, K. Horiuchi, R.A. Copeland, P.A. Scherle, J.M. Trzaskos, R.L. Magolda, G.L. Trainor, R.R. Wexler, F.W. Hobb and R.E. Olson. 1998. MEK inhibitors: the chemistry and biological activity of U0126, its analogs, and cyclization products. Bioorganic and Medicinal Chemistry Letters 8(20): 2839-2844. [ Links ]
Friesen, K.G., J.L. Nelssen, R.D. Goodband, M.D. Tokach, J.A. Unruh, D.H. Kropf and B.J. Kerr. 1994. Influence of dietary lysine on growth and carcass composition of high-lean growth gilts fed from 34 to 72 kilograms. Journal of Animal Science 72(7): 1761-1770. [ Links ]
García, J., M.C. Marca, E. Brot-Laroche, N. Guillén, S. Acin, M.A. Navarro, J. Osada and M.J. Rodríguez. 2008. Protein kinases, TNF-a and proteasome contribute in the inhibition of fructose intestinal transport by sepsis in vivo. American Journal of Physiology. Gastrointestinal and Liver Physiology 294(1): G155-G164. [ Links ]
Garriga, C., A. Pérez, A. Concepción, J.M. Campbell, L. Russell, J. Polo, J.M. Planas and M. Moretó. 2005. Spray-dried porcine plasma reduces the effects of staphylococcal enterotoxin B on glucose transport in rat intestine. Journal of Nutrition 135(7): 1653-1658. [ Links ]
Gómez, A. 2006. El destete y la fisiología del lechón. p. 34. En: Memorias. I Seminario Internacional sobre Sistemas Sostenibles de Producción en Especies Menores. Universidad del Cauca, Popayán, Colombia. [ Links ]
Gopal, R., D. Birdsell and F.P. Monroy. 2008. Regulation of toll-like receptors in intestinal epithelial cells by stress and Toxoplasma gondii infection. Parasite Immunology 30(11-12): 563-576. [ Links ]
Hewett, J.A. and R.A. Roth. 1993. Hepatic and extrahepatic pathobiology of bacterial lipopolysaccharides. Pharmacological Reviews 45(4): 382-411. [ Links ]
Kolch, W. 2000. Meaningful relationships: the regulation of the Ras/Raf/MEK/ERK pathway by protein interactions. Biochemical Journal 351(2): 289-305. [ Links ]
Koopmans, S.J., A.C. Guzik, J. van der Meulen, R. Dekker, J. Kogut, B.J. Kerr and L.L. Southern. 2006. Effects of supplemental L-tryptophan on serotonin, cortisol, intestinal integrity. Journal of Animal Science 84(4): 963-971. [ Links ]
Korcheva, V., J. Wong, M. Lindauer, D.B. Jacoby, M.S. Iordanov and B. Magun. 2007. Role of apoptotic signaling pathways in regulation of inflammatory responses to ricin in primary murine macrophages. Molecular Immunology 44(10): 2761-71. [ Links ]
Liu, Y., J. Huang, Y. Hou, H. Zhu, S. Zhao, B. Ding, Y. Yin, G. Yi, J. Shi and W. Fan. 2008. Dietary arginine supplementation alleviates intestinal mucosal disruption induced by Escherichia coli lipopolysaccharide in weaned pigs. British Journal of Nutrition 100(3): 552-560. [ Links ]
McKay, D.M. and A.W. Baird. 1999. Cytokine regulation of epithelial permeability and ion transport. Gut 44(3): 283-289. [ Links ]
Mullin, J.M. and K.V. Smock. 1990. Effect of tumor necrosis factor on epithelial tight junctions and transepithelial permeability. Cancer Research 50(7): 2172-2176. [ Links ]
Oner, C., F. Schatz, G. Kizilay, W. Murk, L.F. Buchwalder, U.A. Kayisli, A. Arici and C.J. Lockwood. 2008. Progestin-inflammatory cytokine interactions affect matrix metalloproteinase-1 and -3 expression in term decidual cells: implications for treatment of chorioamnionitis-induced preterm delivery. Journal of Clinical Endocrinology and Metabolism 93(1): 252-259. [ Links ]
Ono, K. and J. Han. 2000. The p38 signal transduction pathway activation and function. Cellular Signalling 12(1): 1-13. [ Links ]
Palacín, M., R. Estévez, J. Bertrán and A. Zorzano. 1998. Molecular biology of mammalian plasma membrane amino acid transporters. Physiological Reviews 78(4): 969-1054. [ Links ]
Pié, S., S.P. Lallès, F. Blazy, J. Laffitte, B. Sève and I.P. Oswald. 2004. Weaning is associated with an upregulation of expression of inflammatory cytokines in the intestine of piglets. Journal of Nutrition 134(3): 641-647. [ Links ]
Pluske, J.R., D.J. Hampson and I.H. Williams. 1997. Factors influencing the structure and function of the small intestine in weaned pigs: a review. Livestock Production Science 51(1-3): 215-236. [ Links ]
Rebollar, E., E. Guerrero, M.P. Arruebo, M.A. Plaza and M.D. Murillo. 2003. Role of prostaglandins in lipopolysaccharide effects on K+-induced contractions in rabbit small intestine. Acta Physiologica Scandinavica 179(3): 299-307. [ Links ]
Reis, S.T., C.M. Guerrero, B.A. Aguilera y L.G. Mariscal. 2005. Efecto de diferentes cereales sobre la morfología intestinal de lechones recién destetados. Técnica Pecuaria en México 43(3): 309-321. [ Links ]
Roy, S.K., R.K. Srivastava and S. Shankar. 2010. Inhibition of PI3K/AKT and MAPK/ERK pathways causes activation of FOXO transcription factor, leading to cell cycle arrest and apoptosis in pancreatic cancer. Journal of Molecular Signaling 19: 5:10. [ Links ]
Statistical Analysis Systems Institute (SAS®). 2006. SAS/STAT User's Guide. Version 9.1. SAS Institute Inc, Cary, NC. [ Links ]
Stadnyk, A.W. 2002. Intestinal epithelial cells as a source of inflammatory cytokines and chemokines. Canadian Journal of Gastroenterology 16(4): 241-246. [ Links ]
Segalés, J. and M. Domingo. 2003. La necropsia en el ganado porcino, diagnóstico anatomopatológico y toma de muestras. Boehringer Ingelheim, Madrid España. 125 p. [ Links ]
Steel, R.G., J.H. Torrie and D.A. Dickey. 1997. Principles and procedures of statistics: a biometrical approach. Third edition. McGraw-Hill, New York, USA. 356 p. [ Links ]
Touchette, K.J., J.A. Carrol, G.L. Allee, R.L. Matter, C.J. Dyer, L.A. Beausang and M.E. Zannelli. 2002. Effect of spray-dried plasma and lipopolysaccharide exposure on weaned pigs: I. Effects on the immune axis of weaned pigs. Journal of Animal Science 80(2): 494-501. [ Links ]
Van den Blink, B., J. Branger, S. Weijer, S.H. Deventer, T. van der Poll and M.P. Peppelenbosch. 2001. Human endotoxemia activates p38 MAP kinase and p42/44 MAP kinase, but not c-Jun N-terminal kinase. Molecular Medicine 7(11): 755-760. [ Links ]
Waetzig, G.H., D. Seegert, P. Rosenstiel, S. Nikolaus and S. Schreiber. 2002. p38 mitogen activated protein kinase is activated a linked to TNF-a signaling in inflammatory bowel disease. The Journal of Immunology 168(10): 5342-5351. [ Links ]
Yuan, J., B.Z. Xu, S.T. Qi, J.S. Tong, L. Wei, M. Li, Y.C. Ouyang, Y. Hou, H. Schatten and Q.Y. Sun. 2010. MAPK-activated protein kinase 2 is required for mouse meiotic spindle assembly and kinetochore-microtubule attachment. Public Library of Science One 5(6): e11247. [ Links ]