Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Actualidades Biológicas
Print version ISSN 0304-3584
Actu Biol vol.30 no.88 Medellín Jan./June 2008
ARTÍCULOS DE INVESTIGACIÓN
COMUNIDAD DE PECES EN LA CIÉNAGA DE AYAPEL, RÍO MAGDALENA (CÓRDOBA) COLOMBIA: CAMBIOS ESPACIO–TEMPORALES EN SU ASOCIACIÓN
THE FISH COMMUNITY OF THE AYAPEL FLOODPLAIN LAGOON, MAGDALENA RIVER (CÓRDOBA), COLOMBIA: SPACIO–TEMPORAL CHANGES IN ITS ASSEMBLAGE
María I. Ríos–Pulgarín1; Luz F. Jiménez–Segura1; Jaime A. Palacio2; John J. Ramírez–Restrepo1
1 Instituto de Biología, Universidad de Antioquia. A. A. 1226. Medellín (Antioquia), Colombia. mirios@jaibana.udea.edu.co,ljimenez@matematicas.udea.edu.co, jjram@matematicas.udea.edu.co.
2 Departamento de Ingeniería Sanitaria, Universidad de Antioquia. A. A. 1226. Medellín (Antioquia), Colombia. japalaci@jaibana.udea.edu.co.
Resumen
Las variaciones espaciotemporales en la estructura de las asociaciones de especies de peces en la ciénaga de Ayapel (Colombia), fueron estudiadas durante el periodo hidrológico 2004–2005. Se capturaron 46 especies, de las cuales, Cyphocharax magdalenae, Roeboides dayi y el género Astyanax fueron las más abundantes y frecuentes. Los resultados mostraron una relación significativa entre las características ambientales de la ciénaga de Ayapel y las asociaciones de especies. Los cambios en la conformación de las asociaciones fueron más evidentes entre periodos climáticos que entre ambientes. A pesar de la fuerte influencia de la temporalidad climática en la estructura de las asociaciones, el pulso de inundación del río San Jorge, no fue definitivo en estos cambios y si, la hidrología de la cuenca local.
Palabras clave: asociación de peces, ciénaga, pulso de inundación, río Magdalena, Colombia
Abstract
Time and spatial changes in fish assemblage structure in Ayapel floodplain lagoon (Colombia), were observed during the hydrological cycle 2004–2005. Forty six species were captured. Cyphocharax magdalenae, Roeboides dayi and individuals of the genus Astyanax were the most abundant in number of individuals and the most frequent results showed a significant relationship between environmental characteristics of Ayapel floodplain and species assemblage. Changes in fish assemblage structure were defined by hydrological time changes more than spatial ones. Although hydrological time changes were important to fish assemblage, the hydrology of the local basin was more important than the San Jorge river floodplain pulse.
Key words: ciénaga, fish assemblage, flood pulse, Magdalena river, Colombia
INTRODUCCIÓN
Los ambientes lagunares asociados a los planos de inundación de grandes ríos son ecosistemas importantes dentro de la dinámica de la cuenca, debido a que actúan como amortiguadores de crecientes y ofrecen condiciones adecuadas para la alimentación y crecimiento de la biota acuática, incluyendo numerosas especies de peces (Lowe–McConnell, 1987; Welcomme, 1992).
Las fluctuaciones en el volumen de agua en estos sistemas son reguladas por las lluvias a nivel local y regional, afectando directamente las características de los diferentes hábitats y la estructura de las asociaciones faunísticas de estos sistemas. Los cambios más evidentes en las condiciones ambientales son la cobertura de macrófitas y la concentración de oxígeno, los cuales influyen en la composición y la abundancia de los diferentes eslabones de la red trófica (Meerhoff, 2000; Muñoz et al., 2001; Petra et al., 2003; Poi de Neiff, 1977).
De acuerdo con el concepto de pulso de inundación (Junk et al., 1989; Junk y Wantzen, 2003), las interacciones entre el cauce principal y el plano de inundación determinan los flujos bióticos y de materiales entre estos dos ambientes e influye directamente en la disponibilidad de hábitat y alimento para la biota acuática (Drago, 1994; Junk et al., 1989; Junk y Wantzen, 2003; Neiff, 1999; Neiff, 1999; Neiff et al., 1994; Orfeo, 1995). A pesar de que este concepto surge desde la ecología de grandes ríos con extensas planicies inundables (e.g.: ríos Missisipi, Amazonas, Orinoco y Paraná), diversos autores coinciden en que cada humedal tiene una identidad propia (Gopal, 1994; Junk y Wantzen, 2003; Mitsch y Gosselink, 1993; Neiff et al., 1994), incluyendo su biota.
Basados en el estudio de la ictiofauna presente en una laguna de la planicie inundable (localmente llamado ''ciénaga'') del Río Magdalena, presentamos aquí la influencia de la estacionalidad climática y la heterogeneidad espacial sobre la conformación de las asociaciones de especies de peces durante el ciclo anual 2004–2005.
MATERIALES Y MÉTODOS
Área de estudio. El río San Jorge es uno de los principales afluentes del río Magdalena, aportando un caudal superior a 600 m3/seg durante el periodo de lluvias. Nace en el extremo norte de la cordillera Occidental de los Andes colombianos, a una altitud superior a 4.000 m y presenta un régimen hidrológico con un solo periodo de crecientes dentro del ciclo anual (uni–modal). Dentro de su llanura aluvial, se reconocen diferentes lagunas ó ciénagas de gran importancia en el amortiguamiento de crecientes y en la producción pesquera de la cuenca del río Magdalena.
La ciénaga de Ayapel es tal vez, una de las más importantes dentro del sistema inundable del río San Jorge debido a su extensión (45 km2) y su importancia en la economía pesquera local. Se encuentra dentro de una zona de vida de bosque húmedo tropical, con temperaturas mínimas de 26 ºC y máximas de 28,7 ºC y con un promedio anual de lluvias entre 2.000 y 2.500 mm (IGAC, 1986). Posee, además, un sistema hidrológico propio que recoge los aportes de pequeños tributarios localizados en la región suroriental, generando excedentes que drenan hacia el río San Jorge (Restrepo, 2005). Su profundidad media es de 6 m y el nivel del agua fluctúa hasta 4 m entre los periodos de lluvia y sequía (CIA, 1990).
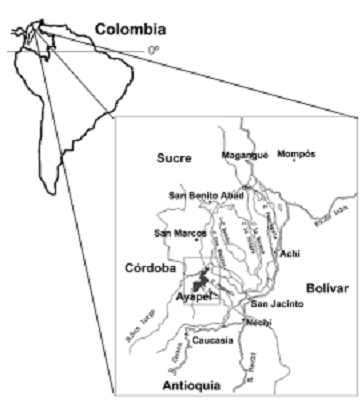
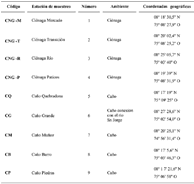
Diseño de muestreo. Se realizaron seis jornadas de campo de dos semanas cada una. Dos de estas jornadas se desarrollaron en el periodo hidrológico de aguas altas (septiembre y noviembre 2004), dos en aguas bajas (febrero y marzo 2005) y los dos restantes en aguas subiendo (abril y junio 2005); el periodo de aguas bajando no fue muestreado. En cada jornada se capturaron peces en diferentes hábitats: 1) pequeños tributarios a la ciénaga principal, 2) ciénagas y 3) caño de conexión con el río San Jorge. Dentro de estos ambientes, se seleccionaron nueve estaciones de muestreo (figura 1, tabla 1).
Figura 1. Ubicación de la ciénaga de Ayapel (Córdoba), Colombia (fuente: Chalarca, 2005)
La pesca experimental se desarrolló durante ocho horas continuas en cada estación (entre las 17:00 y las 01:00 horas del día siguiente); de esta manera se buscó reducir el sesgo en la captura relacionado con la actividad nictimeral de las especies. Las redes estacionarias (90m2 de paño con luz de malla: 3, 4, 5, 6, 7 y 8 cm) y las líneas de anzuelos fueron localizadas en la región litoral. Las redes de caída (atarrayas con luz de malla 0,5, 2 y 3cm) fueron lanzadas dentro de esta misma área y las redes manuales se utilizaron para muestrear bajo los prados de macrófitos. El esfuerzo de pesca en cada uno de los sitios y periodos climáticos de muestreo fue de cinco redes estacionarias, 30 lances con cada una de las atarrayas, 30 lances de red de mano y cuatro líneas de anzuelos de diferente tamaño.
Simultáneamente con la captura de los peces, se midieron algunas características del agua (pH, conductividad, oxígeno disuelto y temperatura) con ayuda de celdas WTW y se estimó la profundidad media con una ecosonda FISHFINDER.
Determinación de las especies. Cada espécimen fue medido con cinta métrica (mm) y pesado con balanzas de precisión al 0,1 y 0,001 g. Los ejemplares fueron fijados en formaldehído al 10% y transportados al laboratorio de Ictiología de la Universidad de Antioquia.
El material fue determinado, en lo posible hasta especie, mediante la utilización de las claves taxonómicas generales de Dahl (1971), Eigenmann (1922), Maldonado–Ocampo et al. (2005), Nelson (1994), y específicas de Covain y Fisch–Muller (2007), Gery (1977), Schultz (1944), Vari (1992, 1995), entre otras. La denominación y clasificación filogenética vigente de las especies se estableció a partir de Reis et al. (2003). Los individuos fueron consignados en la colección de ictiología de la Universidad de Antioquia, bajo los números de colección CIUA–143 al CIUA–198 y CIUA–260 al CIUA–263.
Organización y análisis de la información. Con base en la presencia y abundancia de cada especie en los sitios de muestreo, se estimó la frecuencia de aparición y se verificó su ajuste a los modelos teóricos de abundancia. Como descriptores emergentes de las asociaciones de peces fueron estimados los índices de riqueza (Margalef, 1958), dominancia (Simpson, 1949), diversidad de Shannon–Wiener (1964) y equidad (Pielou, 1969), propuestos en Magurran (1989). El número de especies esperado fue cuantificado a partir de los estimadores de riqueza de Chao (Chao, 1984) y Jack Knife (Palmer, 1990). Todos los índices fueron estimados mediante el programa estadístico BioDiversity Profesional v2 (McAleece, 1997). Adicionalmente se realizó una regresión lineal entre los valores de diversidad y los descriptores: dominancia, equidad y riqueza, con el fin de establecer cual de ellos explica mejor las variaciones en la diversidad de la comunidad.
De acuerdo con la prueba de Shapiro–Wilk, los datos de diversidad, abundancia y biomasa correspondientes a diferentes momentos o estaciones de muestreo no cumplieron los supuestos de normalidad y/o homogeneidad de varianzas (test de Kolmogorov–Smirnov con P > 0,05 basado en la media), aún después de su transformación. Por ello para contrastar tales descriptores entre los diferentes ambientes se utilizó el análisis no paramétrico Contraste de homogeneidad para k muestras independientes: Anova de Friedman (Guisande et al., 2006).
Tabla 1. Coordenadas geográficas de las estaciones de muestreo ciénaga de Ayapel (Córdoba), Colombia
Se aplicó una correlación canónica entre las especies y las variables físicas y químicas a fin de establecer aquellas variables asociadas con la presencia y/o abundancia de especies ícticas particulares (Guisande et al., 2006). La influencia de las variables físicas y químicas sobre la estructura de las asociaciones de especies entre momentos y estaciones de muestreo, se evaluó mediante un análisis directo de redundancia canónica (RDA), precedido por un análisis indirecto –Análisis de Componentes Principales (PCA) con el fin de reducir el número de variables. La significancia de la interacción fue probada mediante una prueba de permutaciones de Monte Carlo (con 499 permutaciones). Los cálculos y estimaciones fueron efectuados a través del los programas Statistica 7.1 (Statsoft, 2005) y Canoco 4.5 para Windows® (Cajo y Petr, 2003).
RESULTADOS
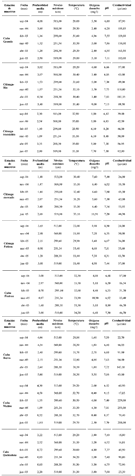
Variables físicas y químicas del agua.Mientras que los valores del pH permanecieron relativamente estables, la profundidad, la temperatura, el oxígeno y la conductividad experimentaron cambios espaciales y/o temporales importantes. Los valores de oxígeno disuelto descendieron en los caños durante los periodos de aguas altas. Por otra parte, el oxígeno, la temperatura y la conductividad mostraron un incremento general durante el estiaje (tabla 2). Sólo se observan diferencias significativas entre estaciones (P < 0,01 y P > 0,004) para las variables temperatura y conductividad, respectivamente. Mientras que las diferencias temporales presentaron P > 0,05 para la mayoría de las variables, excepto el pH y oxígeno.
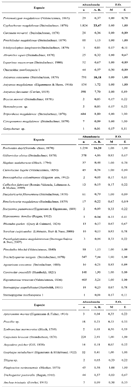
Estructura de las asociaciones de peces. En total se capturaron 7.770 individuos pertenecientes a 40 especies y 6 morfo–especies, 23 familias y 8 órdenes (tablas 3 A, B). Entre las especies capturadas, 39% fueron Characiformes, 28% Siluriformes, 13% Perciformes, 9% Gymnotiformes, y el 11% restante de otros órdenes (Myliobatiformes, Cyprinodontiformes, entre otros). Todas las especies capturadas son actualmente típicas de la cuenca del Magdalena (Dahl, 1971; Galvis y Mojica, 2007 y Mojica, 1999), aún cuando no todas son nativas.
Las especies más importantes en términos de abundancia, biomasa y frecuencia de aparición fueron en su orden Cyphocharax magdalenae (Steindachner, 1878), Roeboides dayi (Steindachner, 1878), el género Astyanax (tres especies), Triportheus magdalenae (Steindachner, 1878), Trachelyoptherus insignis (Steindachner, 1878) y Eigenmania virescens (Valenciennes, 1842). Dichas especies representan el 26,75% de la biomasa y el 83,46% de la abundancia total. Las 38 especies restantes constituyen una pequeña fracción del número de individuos pero hacen un aporte conjunto de biomasa significativo, especialmente las formas residentes de buen tamaño como: Hoplias malabaricus (Bloch, 1794),y Caquetaia kraussii (Steindachner, 1879)y las especies migradoras: Leporinus muyscorum (Steindachner, 1901), Plagioscion surinamensis (Bleeker, 1973) y Prochilodus magdalenae (Steindachner, 1879).
La curva acumulativa de especies alcanzó la asíntota en un valor inferior a las 50 especies. Así mismo, los estimadores de riqueza de Chao y Jack–Knife indicaron que el número de especies esperado para las asociaciones es 46,89 y 45,27, cercano a la riqueza observada. A pesar que el número de especies en cada estación de muestreo fluctuó según el momento hidrológico, no se observaron diferencias significativas entre las ciénagas, el Caño Grande y los caños afluentes (P > 0,09).
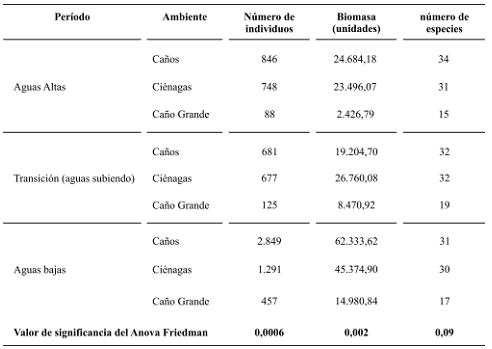
La abundancia y biomasa de peces mostraron variaciones importantes entre los diferentes periodos y estaciones (P = 0,0006 para la abundancia y P = 0,002 para la biomasa), con valores máximos en los períodos de aguas bajas, cuando los aportes de biomasa y el número de individuos es mayor en los caños afluentes (tabla 4).
Características emergentes de las asociaciones ícticas.Las asociaciones observadas se ajustaron al modelo de distribución de abundancia en serie logarítmica en todos los periodos de muestreo e independientemente de las estaciones (P > 0,05).
Tabla 2. Variación espacio–temporal de algunas condiciones físicas químicas del agua en la ciénaga de Ayapel (Córdoba), Colombia, durante el periodo hidrológico 2004–2005
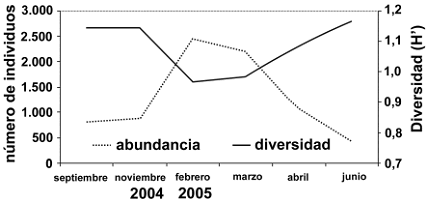
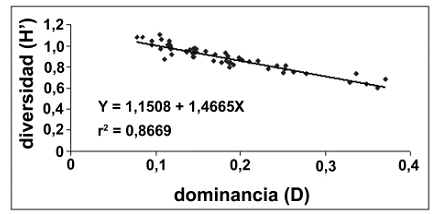
Al superponer las curvas de abundancia, que sigue la misma tendencia que la biomasa, y la diversidad a lo largo del ciclo hidrológico, se encontró que las especies dominantes presentan un incremento importante durante el periodo de estiaje (figura 2, tabla 5). Estos resultados se confirman con los valores de dominancia de Simpson, que explican el 86% de la variación en la diversidad del sistema (figura 3).
Tabla 3A. Abundancia total (n) y relativa (A. R.), y frecuencia de ocurrencia (F. O.) de las especies y morfo–especies capturadas en la ciénaga de Ayapel (Córdoba) en el periodo hidrológico 2004 –2005 (M = Momento; E = Estación)
Tabla 3B. Peso (medio y total) y longitud estándar (L. E.) de especies y morfo–especies capturadas en la ciénaga de Ayapel
Mientras los valores de diversidad (H') fluctuaron entre 0,59 y 1,1 decit/individuo, la equidad varió entre 0,53 y 0, 91 (tabla 5). La mayor variación en sus valores se encontró entre periodos climáticos más que entre estaciones de muestreo. Al agrupar estas estaciones de acuerdo al ambiente que representa se encuentran diferencias significativas (P = 0,029), siendo que las asociaciones son menos diversas durante el estiaje.
Influencia de las variables ambientales sobre las asociaciones de especies. Los cuatro componentes extraídos del PCA explican el 90,9% de la variación encontrada para la fauna íctica . La variación en las asociaciones de especies en la ciénaga de Ayapel estuvo fuertemente vinculado a los patrones de abundancia de C. magdalenae, R. dayi, E. virescens, T. pectorales, T. magdalenae, Astyanax fasciatus (Cuvier, 1819) y Astyanax caucanus (Steindachner, 1879). Estas especies presentaron las mayores abundancias y fueron frecuentes en las asociaciones a través de los muestreos (tablas 3 A, B).
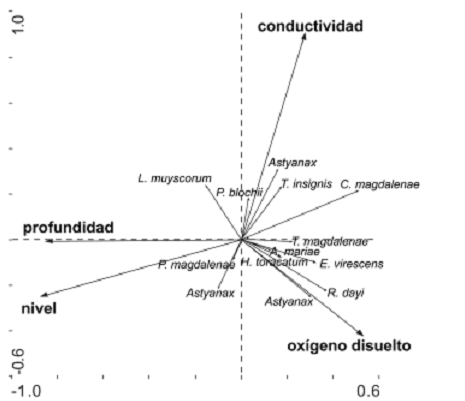
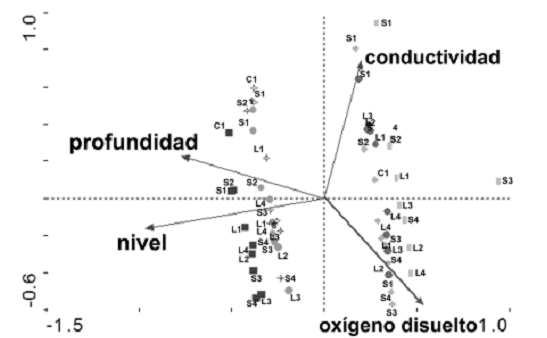
Las características físicas y químicas de la ciénaga de Ayapel (oxígeno disuelto, conductividad, profundidad y temperatura) influyeron en las asociaciones de especies (P = 0,002). Los primeros ejes canónicos reúnen el 98% de la variabilidad acumulada entre las especies y el ambiente y, se observa que las asociaciones cambian entre periodos climáticos más que entre estaciones de muestreo (figuras 4 y 5).
Tabla 4. Variación en la riqueza, abundancia y biomasa de peces en diferentes ambientes en los tres periodos más contrastantes del ciclo hidrológico 2004–2005 de la ciénaga de Ayapel (Córdoba), Colombia
Figura 2. Relación entre la diversidad y la dominancia de la asociación de especies ícticas en la ciénaga de Ayapel (Córdoba), Colombia (capturas realizadas entre septiembre de 2004 y junio de 2005)
Tabla 5. Valores de diversidad, dominancia y equidad en la asociación de peces de la ciénaga de Ayapel (Córdoba), Colombia (capturas realizadas entre septiembre de 2004 y junio de 2005)
La abundancia y frecuencia de las especies más importantes aparece relacionada con la sensibilidad relativa de las especies a las limitaciones ambientales (tabla 6). Se observa una relación negativa entre las especies C. kraussii, R. dayi y T. magdalenae, y la profundidad, es decir, dichas especies prefieren aguas someras. La especie Gilbertolus alatus (Steindachner, 1878)está asociada positivamente con la saturación de oxígeno disuelto y las especies T. magdalenae y C. magdalenae con la conductividad (R = 0,990; Chi² (64) = 94,742; P = 0,007).
Figura 3. Asociación entre la diversidad y la abundancia encontradas en la asociación de peces de la ciénaga de Ayapel (Córdoba), Colombia, durante el ciclo hidrológico 2004–2005
DISCUSIÓN
Variabilidad ambiental.La masa de agua en la ciénaga de Ayapel presenta cambios importantes asociados a los periodos climáticos más que a los ambientes que dentro de ella se presentan. En general, se encontraron mayores valores de saturación de oxígeno, conductividad y temperatura durante el estiaje. Junk y Wantzen (2003) explican estas variaciones como un efecto esperado del pulso de inundación en sistemas con conexiones hidráulicas a grandes ríos. El alto porcentaje de saturación de oxígeno, de la temperatura y de la conductividad en el agua de la ciénaga de Ayapel durante este periodo pudo ser influenciado por la reducción en el área del espejo de agua, en la altura de la columna de agua y en la cobertura de macrófitos. Estas condiciones hacen posible que la influencia del viento en la mezcla de la columna de agua sea mu cho mayor, lo que lleva a la resuspensión de material del fondo sea una constante así como la ausencia de termoclina y la oxigenación mecánica de la masa de agua.
La tendencia a la anoxia en todos los ambientes de la ciénaga de Ayapel durante el periodo de inundación es resultado del aumento en la altura de la columna de agua y la expansión del espejo de agua sobre áreas en las cuales creció vegetación durante el estiaje. Esto es similar a lo reportado por diversos autores (Kapetsky 1977, Lowe–McConnell, 1987; Machado–Allison, 1994; Sánchez–Rueda, 1998; Valderrama y Zarate, 1989; Welcomme, 1992) que afirman que la reducción en la concentración de oxigeno en el agua se debe al incremento en la demanda de oxígeno resultado de la degradación del material vegetal que se inunda con las crecientes.
Figura 4. Representación gráfica del Análisis de Redundancia Canónica basado en la interacción de las variables ambientales y la asociación de especies ícticas de la ciénaga de Ayapel (Córdoba), Colombia
Figura 5. Representación gráfica del Análisis de Redundancia Canónica basado en la interacción de las variables ambientales y la asociación de especies ícticas de la ciénaga de Ayapel (Córdoba), Colombia [factores de análisis: meses en colores; ambientes en letras (L = ciénagas; S = caños; C = Caño Grande)]
Tabla 6. Correlaciones canónicas entre los grupos de variables físicas, químicas y biológicas más importantes en la ciénaga de Ayapel (Córdoba), Colombia, en el periodo 2004–2005
Comunidad íctica y sus asociaciones de especies.La comunidad de peces en la ciénaga de Ayapel esta conformada por 46 especies de 23 familias, superando las 27 especies y 16 familias registradas por el estudio de CVS–Universidad de Antioquia (CIA, 1990) para este sistema lagunar. La importancia relativa de cada orden se mantiene de acuerdo con lo reportado por Lowe–McConnell (1987). Mojica (1999) registra en la cuenca del Magdalena 190 especies pertenecientes a 29 familias, de las cuales Valderrama y Zárate (1989) reporta 42 especies para los planos de inundación, 30 de ellas capturadas en este estudio.
Las especies de peces en la ciénaga de Ayapel presentan una distribución espacial homogénea. Es decir, se observó una única asociación de especies en lugar de diferentes asociaciones vinculadas a cada uno de los tres de ambientes analizados dentro del sistema cenagoso y, esta asociación fue característica del periodo climático de la cuenca local en primer lugar y de la regional, en segundo. Solo durante el estiaje, se diferenciaron levemente las asociaciones de especies a cada uno de los ambientes. Estos resultados son semejantes a los hallados por (Arscott et al., 2000) en lagos de varzea amazónicos, donde la temporada de inundación reduce la heterogeneidad espacial y vincula poblaciones de especies aisladas durante la estación seca, homogenizando la composición de especies del sistema.
Por otro lado, Lasso et al. (1999), Lewis et al. (2000) y, Rodríguez y Lewis (1994, 1997) reportan que en las extensas planicies inundables de los llanos venezolanos, la heterogeneidad espacial es más importante que la temporalidad climática sobre la estructura de la asociación y, que solo se podría definir una asociación típica del estiaje cuando los lagos se aíslan en sub–sistemas y la depredación se convierte en uno de los factores modeladores de estas asociaciones (Rodríguez y Lewis, 1997; Tejerina–Garro et al., 1998). Teniendo en cuenta nuestros resultados en la ciénaga de Ayapel, nos permitimos afirmar que son las características propias a las cuencas las que definen la dinámica de la asociación de las especies de peces y que, los resultados se deben comparar a la luz de estas particularidades.
La diversidad de las asociaciones de especies observadas en cada periodo climático fue diferente; los menores valores se observaron en el periodo de estiaje y los mayores en las aguas altas. Winemiller y Jepsen (1998) encontraron resultados semejantes para planos de inundación de los llanos venezolanos y algunos ríos amazónicos, donde en la época de aguas altas y la transición al estiaje, las asociaciones ícticas tienden a ser más diversas con respecto a la época seca. Estos autores afirman que la reducción en la diversidad durante las aguas bajas es consecuencia de la emigración de especies, la depredación y la hipoxia. En la ciénaga de Ayapel, más que la reducción en el oxígeno, son la migración de las especies de mayor porte hacía el cauce del río y probablemente, la depredación, las que conllevan cambios importantes en la diversidad de la asociación que permanece dentro del complejo lagunar.
Durante el estiaje, la diversidad de las asociaciones fue diferente entre los ambientes del complejo cenagoso; las ciénagas albergaron mayor diversidad que los tributarios a ellas y que el caño de conexión con el río San Jorge. Las migraciones (Suárez et al., 2001; Amoros y Bornete, 2002), las condiciones adversas (Winemiller y Jepsen, 1998) y la conectividad de los ambientes (Suárez et al., 2001; Amoros y Bornette, 2002) causan el cambio en la estructura de las asociaciones de peces. Durante la época seca en la ciénaga de Ayapel, los tributarios reducen el caudal y sus condiciones ambientales se deterioran debido al cambio en la calidad del agua, la reducción en los microhábitats de las márgenes y la eliminación de la interfase macrófitas–aguas abiertas, donde, según Bayley y Petrere (1989), se desarrollan las mayores interacciones tróficas. Esto provoca el movimiento de especies de mayor porte hacia las áreas abiertas (ciénagas) que, en ese momento hidrológico, son los más favorables para su sobrevivencia.
Al observar el comportamiento de la abundancia y la biomasa total, es interesante anotar que las asociaciones de peces en los tributarios fueron las que presentaron más individuos y más biomasa durante los periodos climáticos observados. Aun a pesar de las condiciones del estiaje reducen su calidad ambiental para albergar una ictiofauna diversa, especies de pequeño porte (e.g.: Astyanax spp.) prefieren estos ambientes a los de las áreas abiertas en las ciénagas pues la mayor oferta de hábitats para su refugio, reduce la influencia de los depredadores y, el bosque ripario que bordea los caños, puede ofrecer mas alimento (Bulla et al., 1980; Machado–Allison, 1994; Petry et al., 2003).
Las áreas abiertas (ciénagas) en el complejo cenagoso y el caño de conexión con el río San Jorge fueron los ambientes que presentaron mayores cambios en los descriptores de la asociación de especies (abundancia, biomasa y diversidad) entre los periodos climáticos observados y, los tributarios a la ciénaga presentaron, la mayoría de las veces, los mayores valores en estas características durante el tiempo de observación. Esto nos permite afirmar que estos ambientes juegan un papel fundamental dentro de la dinámica de la ictiofauna en la ciénaga de Ayapel pues ofrecen hábitats diferentes a las áreas abiertas, en especial, durante el estiaje.
La asociación de especies en la ciénaga de Ayapel presenta además dos particularidades: la especies de gran porte y migratorias (e.g.: Pseudoplatystoma magdaleniatum, Sorubim cuspicaudus, Brycon moorei, Prochilodus magdalenae) son poco abundantes y frecuentes y, la especie mas abundante y que aporta la mayor biomasa, es un detritívoro no migratorio, Cyphocharax magdalenae. La importancia de las especies migratorias en la asociación de peces ha sido ya reportado por diversos autores (Kapetsky et al., 1976; Winemiller y Jepsen, 1998) y puede considerarse que su efecto es el cambio temporal en la asociación vinculado con la temporalidad climática, pues dichas especies solo ingresan a la asociación durante las aguas altas, cuando retornan de su migración por el cauce principal.
La mayor abundancia y frecuencia de Cyphocharax magdalenae, coincide con los resultados de Lowe–McConnell (1987) y Provenzano (1984), quienes resaltan que en los ambientes inundables tropicales los peces detritívoros e iliófagos tienden a ser dominantes. Este gremio trófico es uno de los mas importantes dentro de la red del sistema ribereño pues re–incorpora la energía y materia contenida en el fango y en el detrito presente en estos ambientes lagunares (Benedito–Cecilio et al., 2000; Bowen, 1984). A diferencia de Prochilodus magdalenae, que realiza grandes migraciones por los cauces principales y de esta manera redistribuye la materia capturada en los planos inundables a lo largo de la cuenca (Junk y Wantzen, 2003). Cyphocharax magdalenae, es una especie morfológicamente muy similar a P. magdalenae, que utiliza el mismo recurso trófico pero que contrario a éste, no migra así que su aporte al ciclo de materia permanece dentro del sistema de Ayapel.
La asociación de especies de peces en la ciénaga de Ayapel presento un reducido número de especies abundantes y un gran número de especies raras. Estas últimas, si bien contribuyen a la diversidad y complejidad de las cadenas alimenticias, tienen relativamente poca influencia sobre la biomasa y el flujo de materia y energía del sistema, según el modelo presentado por Ludwig y Reynolds (1988) y Winemiller (1998) para sistemas de este tipo.
La conectividad entre el sistema cenagoso–cuenca aportante (local y regional) y su dinámica temporal, dependiente de un pulso de inundación particular, son los factores modeladores de las asociaciones ícticas en la ciénaga de Ayapel. La variación en la profundidad, en el oxígeno disuelto y en la conductividad fueron las variables mas importantes. Diversos autores afirman que la heterogeneidad espacial de los sistemas de inundación unida a una dinámica temporal particular determina la distribución de las especies en el sistema (Granado, 1996; Petry et al., 2003). En la ciénaga de Ayapel, la temporalidad climática fue el factor determinante en la aparición de especies migratorias y en el cambio en la estructura de la asociación de especies de peces.
La diferencia temporal de la asociación de especies de peces en la ciénaga de Ayapel puede obedecer al cambio en las condiciones de los hábitats de este ambiente. Alencar (2001) encontró que en la comunidad de peces de la planicie de inundación del río Paraná, priman las diferencias temporales, en asociación con los cambios en la cobertura de macrófitas, hábitat vital para la protección, alimentación y reproducción de numerosas especies. Es de esperarse que este factor sea igualmente relevante en las diferencias temporales que presenta la ciénaga de Ayapel, donde el movimiento masivo de la vegetación hacía el río San Jorge durante el vaciado de la ciénaga, transforma el paisaje.
CONCLUSIÓN
La ciénaga de Ayapel es un ambiente acuático presente dentro del plano de inundación del río San Jorge, cuya hidrología y físico–química de su masa de agua esta definida por la dinámica hidrológica, en primer lugar de su cuenca local y, en segundo, de la regional. Así que los cambios en la estructura de la asociación de peces provienen principalmente de los cambios temporales que tiene el sistema en cada periodo climático y no de su heterogeneidad espacial.
Nuestros resultados, más que limitar la utilización de los modelos clásicos (e.g.: Concepto del Pulso de Inundación) en la descripción de la dinámica de las planicies de inundación, aportan información nueva que puede llevar a incluir dentro de estos conceptos básicos, sistemas con hidrologías propias y particularidades en la dinámica de su biota.
AGRADECIMIENTOS
Los autores expresan sus mas sinceros agradecimientos al Instituto Colombiano para el Desarrollo de la Tecnología Francisco José de Caldas COLCIENCIAS'' y a la Fundación CORPOAYAPEL por el apoyo económico al proyecto ''Análisis de la relación río–ciénaga y su efecto sobre la producción pesquera en el sistema cenagoso de Ayapel, Colombia'' realizado por el grupo de Gestión y Modelación Ambiental GAIA. A la fundación Idea Wild por el apoyo con equipos de campo. Y, muy especialmente, al Grupo de Ictiología de la Universidad de Antioquia GIUA por su acompañamiento en todas las fases de esta investigación.
REFERENCIAS
1. Alencar MJ. 2001. Estructura de comunidade de peixes em três lagoas marginais do Rio Paraná, no trecho entre os reservatórios de Jupiá e Porto Primavera. Tese Doutorado em ecologia e recursos naturais. Centro de Ciências Biológicas e da Saúde, Universidade Federal de São Carlos. São Carlos, Brasil. [ Links ]
2. Amoros C, Bornette G. 2002. Connectivity and biocomplexity in waterbodies of riverine floodplains. Freshwater Biology, 47:761–776. [ Links ]
3. Arscott DB, Tockner K, Ward JV. 2000. Aquatic habitat diversity along the corridor of an Alpine floodplain river Fiume Tagliamento, Italy. Archiv für Hydrobiologie, 149:679–704. [ Links ]
4. Bayley PB, Petrere M Jr. 1989. Amazon fisheries: assessment methods, current status, and management options. Canadian Journal of Fisheries and Aquatic Science (Special Publication), 106:385–398. [ Links ]
5. Benedito–Cecilio E, Araujo–Lima CARM, Forsberg BR, Bittencourt MM, Martinelli LC. 2000. Carbon sources of Amazonian fisheries. Fisheries Management and Ecology, 7:305–315. [ Links ]
6. Bowen SH. 1984. Detritivory in neotropical fish communities. Pp. 59–66. En: Zaret T (ed.). Evolutionary ecology of Neotropical freshwater fishes. W. Junk Publishers, The Netherlands. [ Links ]
7. Bulla J, Pacheco J, Miranda R. 1980. Ciclo estacional de la biomasa verde, muerta y raíces en una sabana inundada de estero en Mantecal (Venezuela). Acta Científica Venezolana, 31:301–338. [ Links ]
8. CIA (CVS, Universidad de Antioquia). 1990. Estudio de impacto ambiental por minería en la Ciénaga de Ayapel. Casa editora. Medellín, Colombia. [ Links ]
9. Cajo JF, Petr A. 2003. Canoco for Windows version 4.51. Biometrics–Plant Research International. Wageningen, The Netherlands. [ Links ]
10. Chao A. 1984. Nonparametric estimation of the number of classes in a population. Scandinavian Journal of Statistics, 11:265–270. [ Links ]
11. Covain R, Fisch–Muller S. 2007. The genera of the Neotropical armored catfish subfamily Loricariinae (Siluriformes: Loricariidae): a practical key and synopsis. Zootaxa, 1462:1–40. [ Links ]
12. Dahl G. 1971. Los peces del norte de Colombia. INDERENA, Bogotá, Colombia. [ Links ]
13. Drago EC. 2007. The physical dynamics of the river–lake floodplain system. Pp. 83–122. En: Iriondo MH, Paggi JC, Parma MJ (eds.). The middle Paraná river: limnology of a subtropical wetland. Springer–Verlag. Berlin, Alemania. [ Links ]
14. Eigenmann C. 1922. The fishes of Northwestern South America, including Colombia, Panamá and the Pacific slopes of the Ecuador and Perú, together with an appendix upon the fishes of the río Meta in Colombia. Memoirs of Carnegie Museum, 9(1):1–346. [ Links ]
15. Galvis G, Mojica JI. 2007. The Magdalena River fresh water fishes and fisheries. Aquatic Ecosystem Health & Management, 10(2):127–139. [ Links ]
16. Gery J. 1977. Characoids of the World. T.F.H. Publications, Inc. Neptune City (NJ), E. U. A. [ Links ]
17. Gopal B. 1994. The role of ecotones (transiton zones) in the conservation and management of tropical inland waters. Mitteilungen der Internationalen Vereinigung für Limnologie, 24:17–25. [ Links ]
18. Granado, C. 1996. Ecología de peces. Secretariado de publicaciones de la Universidad de Sevilla. Sevilla, España. [ Links ]
19. Guisande GC, Barreiro FA, Maneiro EI, Riveiro AI, Vergara CA. 2006. Tratamiento de Datos. Ediciones Díaz de Santos. Vigo, España. [ Links ]
20. IGAC. 1986. Estudio general de suelos de los municipios de Ayapel, Buenavista, Planeta Rica y Pueblo Nuevo (Departamento de Córdoba). Instituto geográfico ''Agustín Codazzi''. Subdirección Agrológica. Bogotá, Colombia. [ Links ]
21. Junk WJ. 1989. Flood tolerance and tree distribution in central Amazonian floodplains. Pp. 47–64. En: Holm–Nielsen LB, Nielsen IC, Balslev H (eds.). Tropical forests: Botanical dynamics, speciation and diversity. Londres, Inglaterra. [ Links ]
22. Junk WJ, Wantzen KM. 2003. The flood pulse concept: new aspects, approaches and applications – an update. Pp. 117–140. En: Welcomme RL, Petr T (eds.). Proceedings of the Second International Symposium on the Management of Large Rivers for Fisheries, Volume II. Sustaining livelihoods and biodiversity in the new millennium 11–14 February 2003. Phnom Penh, Cambodia. [ Links ]
23. Junk WJ, Bayley PB, Sparks RE. 1989. The flood pulse concept in river–floodplain systems. Pp. 110–127. En: Dodge DP (ed.). Proceedings of the International Large River Symposium. Canadian Special Publication of the Fisheries and Aquatic Science, 106. Canada. [ Links ]
24. Kapetsky JM. 1976. Fish populations in the floodplain lakes of the Magdalena River. Second report. INDERENA–FAO. Bogotá, Colombia. [ Links ]
25. Kapetsky JM. 1977. Some ecological aspects of the shallow lakes of the Magdalena floodplain, Colombia. Paper presented to the Intertropical Symposium on stability and diversity in tropical communities. Panama. [ Links ]
26. Lasso A, Rial A, Lasso–Alcalá O. 1999. Composición y variabilidad espacio–temporal de las comunidades de peces en ambientes inundables de los llanos venezolanos. Acta Biológica Venezolana, 19(2):1–28. [ Links ]
27. Lewis WM Jr, Hamilton SK, Lasi MA, Rodríguez M, Saunders III J. 2000. Ecological determinism on the Orinoco floodplain. BioScience, 50:681–692. [ Links ]
28. Lowe–McConnell RH. 1987. Ecological studies in tropical fish communities. Cambridge University Press. Cambridge, Inglaterra. [ Links ]
29. Ludwig JA, Reynolds JF. 1988. Statistical ecology. John Wiley & Sons, Inc. Nueva York, E. U. A. [ Links ]
30. McAleece N. 1997. BioDiversity Professional Beta [en Línea]. The Natural History Museum y The Scottish Association for Marine Science. Londres, Inglaterra. Disponible en internet: <http://www.sams.ac.uk>. Febrero 14, 2008. [ Links ]
31. Machado–Allison A. 1994. Factor affecting fish communities in the flooded plains of Venezuela. Acta Biológica Venezolana, 15(2):59–75. [ Links ]
32. Magurran AE. 1989. Diversidad ecológica y su medición. Ed. Vedra. Barcelona, España. [ Links ]
33. Maldonado–Ocampo JA, Ortega–Lara A, Usma J, Galvis G, Villa–Navarro F, Vásquez G, Prada–Pedreros S, Ardila C. 2005. Peces de los Andes de Colombia, guía de campo (Fishes of the Colombian Andes, Field Guide. In Spanish). Instituto de Investigación de Recursos Biológicos ''Alexander von Humboldt''. Bogotá, Colombia. [ Links ]
34. Margalef R. 1958. Information theory in ecology. General Systems, 3:36–71. [ Links ]
35. Meerhoff M. 2000. Efecto de la presencia de hidrófitas en la estructura de las comunidades de zooplancton y peces en un lago hipereutrófico somero. Tesis de maestría. School of Sciences, University of Liverpool. Liverpool, England. [ Links ]
36. Mitsch W, Gosselink JG. 1993. Wetlands. Segunda edición. Van Nostrand Reinhold. NuevaYork, E. U. A. [ Links ]
37. Mojica C. 1999. Lista preliminar de las especies de peces dulceacuícolas de Colombia. Revista de la Academia Colombiana de Ciencias, 23 (suplemento especial):547–566. [ Links ]
38. Muñoz E, Mendoza G, Valdominos C. 2001. Evaluación rápida de la biodiversidad en cinco sistemas lénticos de Chile central: macroinvertebrados bentónicos. Gayana Zoología (Chile), 65:173–180. [ Links ]
39. Neiff JJ. 1999. El régimen de pulsos en ríos y grandes humedales de Suramérica. Pp. 99–150. En: Malvárez AI (ed.). Tópicos sobre humedales subtropicales y templados de Sudamérica. Vol. 1, primera edición. Orcyt Mab UNESCO. Montevideo, Uruguay. [ Links ]
40. Neiff JJ, Iriondo MH, Carignan R. 1994. Large tropical South American wetlands: an overview. Pp.156–165. En: Naiman RJ, Link GL (eds.). Proceedings of the International Workshop on the Ecology and Management of Aquatic–Terrestrial Ecotones. University of Washington. Seattle, E. U. A. [ Links ]
41. Nelson J. 1994. The fishes of the World. John Wiley & Sons, Inc. Nueva York, E. U. A. [ Links ]
42. Orfeo O. 1995. Aumento de carga sedimentaria por erosión de taludes en ríos chaqueños. Pp. 117–121. En: Anónimo. Contaminación en cursos de agua del Chaco Oriental. Convenio Gobierno de la Provincia del Chaco (COFEA)–Consejo Nacional de Investigaciones Científicas y Técnicas (CECOAL). [ Links ]
43. Palmer MW. 1990. The estimation of species richness by extrapolation. Ecology, 71:1195–1198. [ Links ]
44. Petry P, Bayley PB, Markle DF. 2003. Relationships between fish assemblages, macrophytes and environmental gradients in the Amazon river floodplain. Journal of Fish Biology, 63(3):547–579. [ Links ]
45. Pielou EC. 1969. An introduction to mathematical ecology. John Wiley & Sons, Inc. Nueva York, E. U. A. [ Links ]
46. Poi de Neiff A. 1977. Estructura de la fauna asociada a tres hidrófitos flotantes en ambientes lemníticos del nordeste argentino. Comunicaciones Científicas del CECOAL, 6:1–16. [ Links ]
47. Provenzano F. 1984. Aspectos reproductivos de peces Gymnotiformes del Bajo Llano venezolano. Facultad de Ciencias. Universidad Central de Venezuela. Caracas, Venezuela. [ Links ]
48. Reis RE, Kullander SO, Ferraris Jr CJ. 2003. Checklist of the freshwater fishes of South and Central America. Edipucrs. Portoalegre, Brasil. [ Links ]
49. Restrepo CA. 2005. Aproximación a la dinámica del transporte del nitrógeno y el fósforo en la ciénaga de Ayapel. Tesis maestría en Recursos hidráulicos. Universidad Nacional de Colombia. Medellín (Antioquia), Colombia. [ Links ]
50. Rodriguez MA, Lewis Jr WM. 1994. Regulation and stability in fish assemblages of neotropical floodplain lakes. Oecologia, 99:166–180. [ Links ]
51. Rodriguez MA, Lewis Jr WM. 1997. Structure of fish assemblages along environmental gradients in floodplain lakes of the Orinoco river. Ecological Monographs, 67(1):109–128. [ Links ]
52. Sánchez C, Rueda M. 1998. Variación de la diversidad y la abundancia de especies ícticas dominantes en el delta del río Magdalena, Colombia. INVEMAR. Santa Marta, Colombia. [ Links ]
53. Shultz LP. 1944. The catfishes of Venezuela, with descriptions of thirty–eight new forms. Proceedings of the United States National Museum, 94:173–338. [ Links ]
54. Shannon CE, Weaver W. 1964. The mathematical theory of communication. University of Illinois Press. Urbana, E. U. A. [ Links ]
55. Simpson EH. 1949. Measurement of diversity. Nature, 1163:688. [ Links ]
56. Statsoft Inc. 2005. Statistica. Data analisis system. Versión 7.1. Disponble en la internet: <www.statsoft.com>. Febrero, 2008. [ Links ]
57. Suárez YR, Petrere Jr M, Catella AC. 2001. Factors determining the structure of fish communities in Pantanal lagoons (MS, Brazil). Fisheries Management and Ecology, 8:173–186. [ Links ]
58. Tejerina–Garro FL, Fortin R, Rodríguez MA. 1998. Fish community structure in relation to environmental variation in floodplain lakes of the Araguaia River, Amazon Basin. Environmental Biology of Fishes, 51(4):399–410. [ Links ]
59. Valderrama M, Zarate M. 1989. Some ecological aspects and present state of the fishery of the Magdalena River basin, Columbia, South America, Pp. 409–421. En: Dodge DP (ed.). Proceedings of the International Large River Symposium. Canadian Special Publication of the Fisheries and Aquatic Science, 106. Canada. [ Links ]
60. Vari R. 1992. Systematics of the neotropical characiform genus Cyphocharax Fowler (Pisces: Ostariophysi). Smithsonian Contributions to Zoology, 529:1–137. [ Links ]
61. Vari R. 1995. The neotropical fish family Ctenoluciidae (Teleostei: Ostariophysi: Characiformes): Supra and intrafamilial phylogenetic relationships, with a revisionary study. Smithsonian Contributions to Zoology, 564:564:1–96. [ Links ]
62. Welcomme RL. 1992. Pesca fluvial. Documento Técnico de Pesca. N.º 262, FAO. Roma, Italia. [ Links ]
63. Winemiller KO. 1998. Floodplain river food webs: Generalizations and implications for fisheries manegement. Department of Wildlife and Fisheries Sciences, Texas A&M University. Texas, E. U. A.
[ Links ]64. Winemiller KO, Jepsen DB. 1998. Effects of seasonality and fish movement on tropical river food webs. Journal of Fish Biology, 53(Supplement A):267–296. [ Links ]