Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Actualidades Biológicas
Print version ISSN 0304-3584
Actu Biol vol.31 no.90 Medellín Jan./June 2009
ARTÍCULOS DE INVESTIGACIÓN
PROPAGACIÓN in vitro y desdiferenciación tisular en Lippia dulcis
In vitro propagation and tisular diferentiation in Lippia dulcis
Aura I. Urrea1; Paula A. Castrillón; Zulma Monsalve1
1 Docente. Instituto de Biología, Universidad de Antioquia. A. A. 1226. Medellín (Antioquia), Colombia.
Correos electrónicos: aurrea@matematicas.udea.edu.co; zmonsalv@matematicas.udea.edu.co.
Resumen
Se describe una metodología para el establecimiento, la multiplicación y la obtención in vitro de callos de Lippia dulcis (Verbenaceae). Adicionalmente, se logró el establecimiento de una suspensión celular. Se utilizaron como explantes iniciales yemas apicales y segmentos nodales de plantas mantenidas en casa malla. El tratamiento más efectivo para el establecimiento y multiplicación de L. dulcis a partir de yemas apicales o segmentos nodales fue el medio MS libre de reguladores de crecimiento. Para lograr la textura y color adecuados, el medio para formación y multiplicación de callos (MS suplementado con 2,4D 0,1 mg/l) requiere ser renovado cada 20 días. El establecimiento de la suspensión celular, con alto porcentaje de viabilidad, fue posible en el medio de cultivo MS y la combinación hormonal 2,4 D (0,5 mg/l) + Kinetina (0,1 mg/l).
Palabras clave: callos, Lippia dulcis, micropropagación, suspensión celular.
Abstract
A methodology for in vitro establishment, multiplication and callus formation of Lippia dulcis (Verbenaceae) is described. Furthermore, an essay for establishment of cellular suspension was realized. Initial explants shoot tips and nodal segments from plants grown under greenhouse were used. The treatment more effective for induction and multiplication of L. dulcis from shoot tips or nodal segments was MS medium free of growth regulators. To achieve the colour and adequate texture, the medium for callus formation and multiplication (MS by adding 2,4D 0,1 mg/l) needs to be renew each 20 days. The cellular suspension establishment, with a high percentage of viability, was possible in MS medium and the hormonal combination 2,4 D (0.5 mg/l) + Kinetina (0.1 mg/l)
Key words: callus, cellular, Lippia dulcis, suspension micropropagation.
INTRODUCCIÓN
Lippia dulcis Trev, conocida como orozú o hierba dulce, es una especie vegetal perteneciente a la familia Verbenaceae, originaria de México y Centro América. Esta planta ha sido de gran importancia ya que además de sus reconocidas propiedades medicinales contra enfermedades respiratorias, gastrointestinales (Pascual et al. 2001), hepáticas, como antihipertensivo, antiproliferativo (Abe et al. 2002) y antiinflamatorio (Pérez 2005), contiene compuestos fenólicos, flavonoides de distintos tipos (Masateru et al. 2005) y sesquiterpenos, principalmente del tipo bisaboleno (Souto et al. 1997), entre otros. La hernandulcina es el bisaboleno que le confiere a la planta su gran capacidad edulcorante (Compadre et al. 1985, 1987), que llega a ser de 1.000 a 1.500 veces más dulce que el azúcar (Compadre et al. 1986, Kaneda et al. 1992, Pascual et al. 2001). Otras propiedades que hacen la hernandulcina especialmente interesante son su carácter no tóxico ni mutagénico (Kinghorn 1998). Adicionalmente, su alta solubilidad y estabilidad térmica en un amplio rango de pH, aunado a que es no calórico, perfilan este compuesto como una alternativa de uso en gran variedad de aplicaciones alimenticias, productos farmacéuticos y de higiene oral. Sin embargo, el rendimiento en la producción de la hernandulcina a partir de hojas y flores es bastante bajo, los porcentajes de rendimiento obtenidos fluctúan entre 0,004-0,154% (Kinghorn et al. 2002). De otro lado, su significativo contenido de alcanfor (Pascual et al. 2001), aunque puede ser el responsable de muchas de sus aplicaciones en medicina tradicional, ha limitado su uso alimenticio ya que confiere un sabor no deseado.
A pesar que el cultivo de tejidos es de reconocida aplicación en la producción y bioconversion de compuestos, en muchos casos la producción de metabolitos secundarios o no se logra o se logra en proporciones muy bajas. Una de las alternativas para superar este inconveniente es evaluar factores como la composición del medio de cultivo (Paniego y Giulietti 1996), la fuente de carbono (Shinde et al. 2009), el pH del medio, el uso de elicitores (Savitha et al. 2006, Zhao 2005) y la inducción de hairy roots (Young-Am 2000) entre otros, a fin de establecer las condiciones apropiadas que permitan superar estas limitaciones (Ramachandra y Ravishankar 2002).
A la fecha, se han reportado sistemas de propagación in vitro y para la obtención de metabolitos secundarios en diversas especies del género Lippia (Capote et al. 1999, Gupta et al. 2001, Julián et al. 1999, Pereira et al. 2006). Sin embargo, en el caso de L. dulcis solo se han reportado el cultivo in vitro de brotes como estrategia para la producción de hernandulcina (Sauerwein et al. 1991b) y el uso de chitosan para aumentar la producción de hernandulcina en raíces inducidas mediante Agrobacterium rhizogenes (Sauerwein et al. 1991a).
En este documento, se describe un sistema eficiente para la introducción in vitro de plantas de L. dulcis, la inducción de desdiferenciación tisular a partir de tejido foliar y el establecimiento de una suspensión celular, como etapas previas para el estudio de la producción de la hernandulcina y su potencial escalado.
MATERIALES Y MÉTODOS
Material vegetal. Como fuente de explantes se usaron plantas de Lippia dulcis adquiridas en un cultivo comercial y multiplicadas por esquejes bajo condiciones de invernadero. Los esquejes de las plantas madre fueron incubados con una solución enraizadora (ANA 10%) durante 2 horas, posteriormente se sembraron en una mezcla tierra arena (2:1), previamente esterilizada. Cada 30 días se fertilizaron con las sales MS a la mitad de la concentración.
Establecimiento y multiplicación in vitro. La desinfección de los explantes (yemas apicales y nudos) provenientes de plantas creciendo en casa malla, se llevó a cabo siguiendo el protocolo que se describe a continuación: un lavado inicial con jabón quirúrgico y abundante agua de grifo, luego en condiciones asépticas, se sumergieron en etanol al 70% durante 10 segundos y finalmente en hipoclorito de sodio durante 10 minutos a concentraciones de 1,5% en el caso de las yemas apicales y 2,0% para los nudos. Se realizaron como mínimo 3 enjuagues con agua destilada estéril antes de la siembra in vitro.
Los tratamientos evaluados para el establecimiento y la multiplicación, se describen a continuación. En todos los casos se usó el medio de cultivo basal MS (Murashige y Skoog 1962) suplementado con sacarosa (30 g/l) y gelrite (1,8 g/l), ajustando el pH a 5,7 antes de esterilizar por autocalve. El medio 1 se mantuvo exento de hormonas; el medio 2 fue adicionado de AIA a 0,1 mg/l; el medio 3 se adicionó BAP a 1 mg/l; y el medio 4 con AIA a 0,1 mg/l y BAP a 1 mg/l.
En cada uno de los tratamientos se utilizó un explante por tubo de ensayo y un tamaño de muestra de 10 explantes por tratamiento. Las condiciones de experimentación fueron fotoperíodo de 16 horas/día (28-35 µmol m-2 s-1) y 22 ± 2 ºC. Los indicadores del efecto de los reguladores de crecimiento considerados fueron: número de explantes vivos y muertos para la etapa de establecimiento; en la multiplicación se evaluó la altura de la planta y el número de nudos (coeficiente de multiplicación). Para esta última etapa, se realizaron subcultivos a medio fresco de la misma composición cada cuatro semanas. Los datos fueron registrados a los 30 días de cultivo y el experimento fue realizado por triplicado.
Inducción y multiplicación de callos. Para la inducción de callos se utilizaron hojas de vitroplantas multiplicadas en medio basal MS exento de hormonas. De las plantas se tomaron hojas expandidas de los segmentos nodales más jóvenes. Porciones de hoja, sin incluir sus bordes, fueron sometidas a diferentes tratamientos hormonales en el medio basal MS suplementado con sacarosa (30 g/l) y mantenidos bajo las condiciones de experimentación antes descritas. Los tratamientos hormonales evaluados fueron: 1) control, sin reguladores de crecimiento; 2) 2,4D a 0,1 mg/l; 3) BAP a 0,5 mg/l; 4) ANA a 0,5 mg/l; 5) 2,4D a 0,5 mg/l y BAP a 0,1 mg/l; 6) 2,4D a 0,1 mg/l y BAP a 0,5 mg/l; 7) ANA a 0,5 mg/l y BAP a 0,1 mg/l; y 8) ANA a 0,5 m/g y BAP a 0,5 mg/l.
En todos los tratamientos se emplearon tres cajas de petri con cinco segmentos de hoja cada una, el experimento se realizó por triplicado. Los indicadores del efecto hormonal fueron porcentaje de formación, color y textura de los callos. Para estudiar el efecto de los tratamientos hormonales sobre la multiplicación de los callos, estos fueron transferidos a medio fresco de la misma composición cada tres semanas durante tres meses, se determinó el porcentaje de multiplicación, color y textura como indicadores de respuesta. Los datos fueron colectados en la tercera y cuarta semana.
Debido a que en todos los tratamientos se presentó oscurecimiento de los callos, apariencia típica de acumulación de etileno o de oxidación fenólica, se decidió evaluar primero tiosulfato de plata (STS) a una concentración de 4uM en los tres medios de cultivo seleccionados, ya que este compuesto ha sido reportado como un inhibidor de la formación de etileno (De Block 1988).
Establecimiento de la suspensión celular. Para el establecimiento de la suspensión celular se utilizaron callos friables en etapa de multiplicación. Para ello se evaluaron dos tratamientos; medio de cultivo basal (MS) líquido suplementado con: 1) 2,4D a 0,1 mg/l y 2) 2,4D a 0,5 mg/l y Kinetina a 0,1 mg/l. Cada frasco de cultivo fue inoculado con 1,0 g de callo friable, usando para ello Erlenmeyers de 250 ml a un cuarto de su volumen e incubados a temperatura de 25 ± 2 °C con agitación constante a 90 rpm. El indicador de crecimiento celular utilizado fue el volumen de células sedimentadas y la viabilidad celular (método de tinción con azul de Evans) los cuales fueron registrados cada 5 días durante cuatro semanas. El experimento se realizó por duplicado.
Análisis estadísticos. Los datos obtenidos se procesaron estadísticamente mediante análisis de varianza (ANOVA). La determinación de grupos homogéneos y significativamente diferentes se llevó a cabo mediante la prueba de Student-Newman-Keuls con un nivel de confianza del 95%, usando el programa Statgraphics 5 plus.
RESULTADOS
Establecimiento y multiplicación in vitro. El material vegetal inicial utilizado fue multiplicado bajo condiciones de casa malla, por lo tanto las plantas estaban expuestas a condiciones ambientales muy variables y en contacto con una gama de fuentes de contaminación. No obstante, el método de desinfección aplicado a las yemas apicales y nudos, permitió obtener bajos porcentajes de contaminación (20-30%). Esto demuestra la eficiencia del método de desinfección, al tiempo que permitió continuar con las demás etapas del trabajo.
Para la obtención de plantas in vitro de L. dulcis, necesarias para la inducción de callo a partir de discos de hoja, se evaluaron tres tratamientos buscando la regeneración de plantas a partir de yemas apicales y nudos. Se evaluaron una auxina, una citoquinina y su combinación, contrastando contra un medio de control sin reguladores de crecimiento.
Para los dos tipos de explante, la altura promedio de las plantas desarrolladas en estos tratamientos fluctuó entre 2,5 y 3,4 cm. sin diferencia estadística, las mayores alturas fueron alcanzadas en el medio exento de hormonas. De igual forma, el mayor número de hojas (10,25) y el mayor tamaño promedio de las hojas, fue obtenido sin la inclusión de hormonas en el medio. El análisis estadístico aplicado tampoco mostró diferencias significativas en el número promedio de nudos comparando los 2 tipos de explante evaluados, sin embargo, el medio basal sin hormonas y el medio suplementado con AIA (0,1 mg/l) favorecieron el desarrollo de plantas con mayor número de nudos (4,5; figura 1).
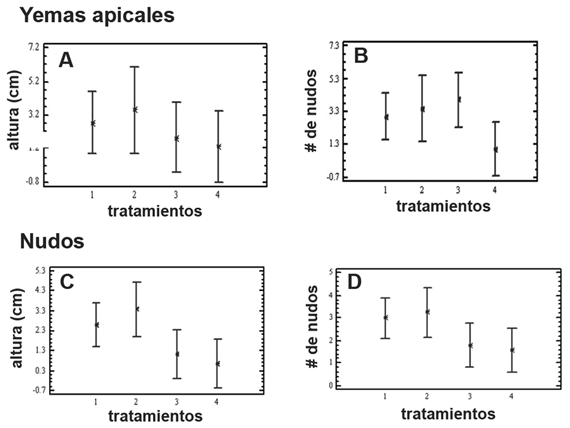
Figura 1. Respuesta de Lippia dulcis después de 30 días en cuatro medios de cultivo diferentes: (0) Medio basal; (1) Medio basal con 0,1 mg/l de AIA; (2) Medio basal con 1 mg/l de BAP; (3) Medio basal con 0,1 mg/l de AIA y 1 mg/l de BAP. A. Respuesta en la altura promedio de la planta. B. Efecto sobre el número promedio de nudos utilizando como explante inicial yemas apicales. C. Respuesta en la altura promedio de la planta. D. Efecto sobre el número promedio de nudos utilizando como explante inicial nudos.
El tratamiento con BAP (1 mg/l) promovió el desarrollo de yemas axilares, sin embargo, se presentó una significativa disminución en la altura de las plantas. Las plantas creciendo en el control se caracterizaron por presentar hojas grandes expandidas de color verde oscuro, contrario a las que se desarrollaron en los medios de cultivo con BAP (1 mg/l) y la combinación AIA (0,1 mg/l) + BAP (1 mg/l), las cuales exhibieron hojas cloróticas con excesiva necrosis (figura 2).

Figura 2. Características de las plantas de L dulcis regeneradas en diferentes tratamientos hormonales 5 semanas después de la iniciación del cultivo. A. En el tratamiento libre de hormonas. B. En medio suplementado con AIA (0,1 mg/l). C. En medio suplementado con BAP (1 mg/l). D. En el medio suplementado con la combinación hormonal AIA (0,1 mg/l) y BAP (1 mg/l).
Para evaluar el potencial de multiplicación, las plantas regeneradas in vitro a partir de ápices y nudos, fueron sometidas a diferentes tratamientos hormonales. En los ensayos realizados con AIA (0,1 mg/l) y el tratamiento control, la altura y el número de nudos de las plantas regeneradas presentaron diferencias significativas con respecto a los tratamientos con BAP (1 mg/l) y la combinación hormonal AIA (0,1 mg/l) + BAP (1 mg/l) (figura 3). En cuanto al tipo de explante utilizado la mayor altura promedio (3,6) se obtuvo cuando se utilizaron los nudos como explantes, para los ápices la altura promedio fue de 3,0 cm.
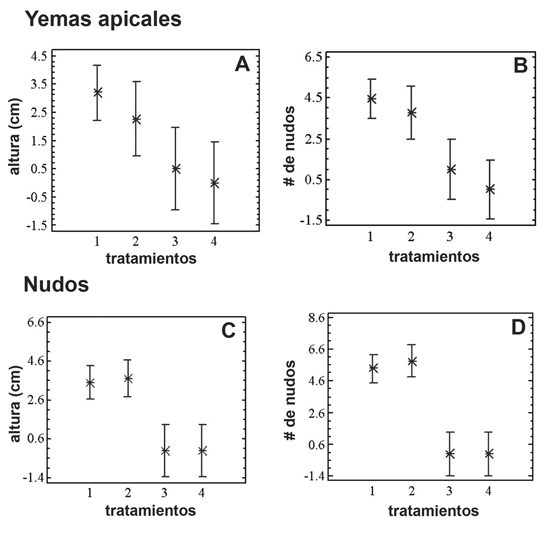
Figura 3. Respuesta de Lippia dulcis en la etapa de multiplicación a cuatro medios de cultivo diferentes: (0) Medio basal; (1) Medio basal con 0,1 mg/l de AIA; (2) Medio basal con 1 mg/l de BAP; (3) Medio basal con 0,1 mg/l de AIA y 1 mg/l de BAP. A. Respuesta en la altura promedio de la planta. B. Efecto sobre el número promedio de nudos utilizando como explante inicial yemas apicales. C. Respuesta en la altura promedio de la planta y D. Efecto sobre el número promedio de nudos utilizando como explante inicial nudos.
Inducción y multiplicación de callos. Durante la fase de inducción de callos, de los ocho tratamientos evaluados inicialmente, se encontró que la formación de callo en porciones de hoja de las vitroplantas es completamente nula en ausencia de auxina (2,4D o ANA). El mayor porcentaje de formación se registró en los medios de cultivo suplementados con 2,4D 0,1 mg/l (75%) y la combinación 2,4D 0,5 mg/l + BAP 0,1 mg/l (65%). El análisis estadístico aplicado no mostró diferencias significativas entre estos dos tratamientos pero si con los otros evaluados (figura 4).
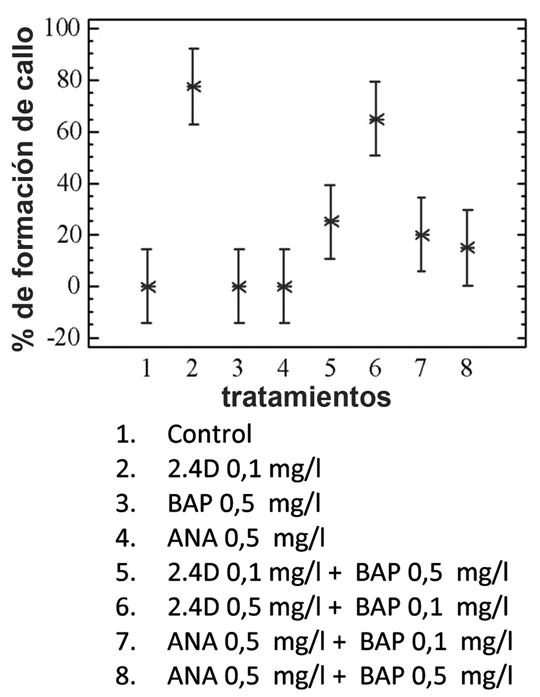
Figura 4. Influencia de diferentes concentraciones y combinaciones de 2,4-D, ANA y BAP en la inducción de callos a partir de explantes foliares de L. dulcis. El análisis de varianza (ANOVA) muestra que hay diferencias significativas entre los tratamientos, demostrando que el medio basal suplementado con 2,4-D a (0,1 mg/l) y con la combinación 2,4D (0,5 mg/l) + BAP 0,1 mg/l inducen una producción significativa de callo a partir de porciones de hojas.
Teniendo en cuenta que los porcentajes de inducción de callo en estos dos tratamientos no presentaron diferencias significativas, características como la friabilidad de los callos y coloración fueron los indicadores de respuesta utilizados para la selección.
Dado que los callos inducidos en los dos tratamientos seleccionados anteriormente exhibieron una coloración pardusca y una textura poco friable, se evaluó el uso de tiosulfato de plata y cambios de medio cada 20 días con el propósito de mejorar dichas características. Aunque en especies como Solanum tuberosum la coloración pardusca de los callos ha sido atribuida a la acumulación de etileno y solucionada en gran parte con la adición de tiosulfato de plata (STS) (Mollers et al. 1991, Hulme et al. 1992), en nuestro estudio no se encontraron diferencias en la pigmentación obtenida en los callos que se indujeron con STS y sin STS en el medio de cultivo. Sin embargo, cuando se renovó el medio de cultivo con una frecuencia de 20 días, se presentó un cambio significativo en la coloración de los callos, principalmente en el medio con 2,4D como única hormona (figura 5).
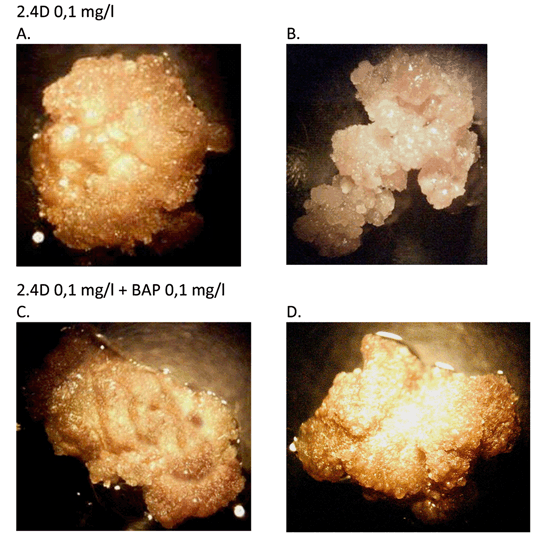
Figura 5. Características de los callos antes y después de iniciar la renovación del medio de cultivo cada 20 días. A y B. En el medio basal suplementado con 2,4 D 0,1 mg/l. C y D. En el medio basal suplementado con 2,4D 0,1 mg/l + BAP 0,1 mg/l
En la etapa de multiplicación de los callos, no se encontraron diferencias significativas entre los dos tratamientos evaluados, obteniéndose porcentajes del 80% de multiplicación. Después de cuatro pases cada 20 días, en el medio de cultivo con la combinación hormonal 2,4D 0,5 mg/l + BAP 0,1 mg/l, el callo continuó siendo compacto con una coloración café, diferenciándose significativamente de los multiplicados en el medio con 2,4D (0,1 mg/l), los cuales presentaron una coloración café clara y una textura suave, fácilmente disgregable. Por lo tanto, se seleccionó el medio de cultivo con 2,4D (0,1 mg/l) como el adecuado para el proceso de inducción y multiplicación, ya que la friabilidad de los callos y la coloración, son aspectos determinantes para el establecimiento de una suspensión celular.
En el estudio realizado para el establecimiento de una suspensión celular de Lippia dulcis, se logró incrementar el volumen de células sedimentadas desde 0,2 ml en el día cero a 3,0 ml el día 28, en el tratamiento con 2,4-D (0,5 mg/l) y Kinetina (0,1 mg/l). La viabilidad celular se mantuvo en un 80% y se evidenciaron células en división activa. A partir de este resultado se puede iniciar el trazado de la curva de crecimiento celular y realizar el análisis de presencia o no del metabolito de interés.
DISCUSIÓN
El desarrollo de plantas completas in vitro a partir de yemas apicales y laterales, está determinada, entre otros aspectos, por la formulación basal del medio de cultivo, los reguladores de crecimiento endógenos y exógenos, las condiciones de crecimiento (fotoperíodo y temperatura, entre los más importantes) y el genotipo. Aunque esta respuesta no siempre incluye la formación del vástago y raíz en el mismo momento, en este caso se presentó esta respuesta cuando se cultivaron ápices y nudos en medios de cultivo sin la presencia de reguladores de crecimiento, lo cual coincide con lo reportado para Lippia junelliana (Juliani et al. 1999). De igual manera, la mayor altura y número de nudos se logró en el medio basal MS libre de reguladores de crecimiento. No obstante, utilizando el mismo medio de cultivo para la propagación, en otras especies del género como L. alba, la mayor altura y número de brotes se obtuvo con BA (2 mg/l) como único regulador de crecimiento (Gupta et al. 2001), con la combinación BA (1 mg/l) /ANA (0,01 mg/l) para L filifolia (Pereira et al. 2006), y para L. micromera con la combinación AIA (0,1 mg/l)/BAP (2 mg/l) (Capote et al. 1999).La respuesta al cultivo in vitro es más influenciada por el genotipo que por cualquier otro factor. Por tanto, el medio y las condiciones del cultivo necesitan ser variadas frecuentemente de un género a otro o de una especie de planta a otra, e incluso variedades de plantas muy próximas pueden diferir en sus requerimientos de cultivo (Veitia et al. 1999).
En este estudio, tanto en el control como en los tratamientos que incluyeron reguladores de crecimiento, se logró el desarrollo plantas completas sin diferencia estadística en la altura y número de nudos en la etapa de establecimiento, sin embargo para la fase de multiplicación se marcaron diferencias significativas, con las mayores alturas y número de nudos para las plantas creciendo en el control y en el tratamiento con AIA. Teniendo en cuenta el balance auxina/citoquinina, y acorde con la revisión realizada por Collin y Edwards (1998), nuestros resultados sugieren que el contenido endógeno de auxina en esta especie está en una concentración apropiada para sustentar el desarrollo de plantas completas in vitro, ya que la adición exógena de AIA a 0,1 mg/l inhibió la formación de la raíz y promovió la formación de callo en la base del explante, sin embargo en ausencia de esta se formaron sistemas radiculares largos y vigorosos.
Con respecto a la respuesta obtenida en presencia del BAP (1 mg/l) en el medio de cultivo, se puede sugerir también un nivel endógeno de citoquinina adecuado para sustentar el desarrollo de plantas completas in vitro, ya que la adición exógena de ésta generó múltiples brotes sin la altura apropiada, posiblemente debido a su acción supresora de la dominancia apical y formación de nuevos brotes (Azcon y Talón 2000). Esto indica que en el caso de L. dulcis, la adición de hormonas al medio de cultivo, principalmente las citoquininas, es apropiada para la inducción de brotes pero va en detrimento de las características morfológicas de las plantas fuente de explante para otros procesos in vitro, por ejemplo para la obtención de hojas con el tamaño y vigor adecuados para la inducción de callos, fuente de inoculo para suspensiones celulares.
Con el propósito de inducir la formación de callo a partir de tejido foliar, se evaluaron diferentes tratamientos hormonales que incluyeron auxinas solas o en combinación con citoquininas. La inducción de tejido desdiferenciado en diferentes explantes generalmente requiere de una auxina, siendo la más frecuentemente utilizada 2,4-D a diferentes concentraciones, sin embargo, en muchos casos se hace necesario la combinación con una citocinina para romper el balance hormonal endógeno y estimular una mayor formación de callo (Urrea et al. 2001). Los discos de hoja de L. dulcis respondieron efectivamente tanto a la auxina sintética 2,4-D sola, como a su combinación con la citoquinina BAP, sin embargo la coloración y textura de los callos fueron determinantes en la selección del tratamiento hormonal a ser utilizado. Al realizar cambios frecuentes a medio fresco los callos cultivados en el medio con 2,4-D (0,1 mg/l) mejoraron su textura y coloración respecto a los que se multiplicaron en el medio con 2,4D (0,5 mg/l) + BAP (0,1 mg/l). Entre las causas del oscurecimiento de los tejidos in vitro esta la actividad de las oxidasas liberadas o sintetizadas cuando el tejido es manipulado (Pérez, 1998), no obstante la liberación de etileno durante el cultivo in vitro de callos y protoplastos ha sido un problema descrito también para algunos cultivares de papa (Urrea et al. 2001). En el primer caso una de las prácticas más comunes para contrarrestar el efecto de la oxidación fenólica es la inactivación, reducción de las enzimas fenolasas y la remoción de los compuestos fenólicos producidos, esta última incluye entre otros el cambio frecuente de medio de cultivo, el cual en esta investigación fue efectivo para mejorar tanto el color como la textura de los callos de L. dulis. De otro lado, el medio de cultivo tiene un efecto determinante en el desarrollo del callo, por lo que se debe optimizar, especialmente la concentración de las fitohormonas con énfasis en la relación auxina/citoquinina; normalmente una alta concentración de auxinas promueve la iniciación del callo (Collin y Edwards, 1998).
CONCLUSIONES
A pesar del alto poder edulcorante y medicinal de Lippia y los costos altos de manejo in vivo, son pocos los grupos de investigación que trabajan en la búsqueda de alternativas de producción. Los resultados obtenidos aquí demuestran la posibilidad de multiplicar las plantas de L. dulcis en medio exento de hormonas, disminuyendo así grandemente los costos de su manejo, especialmente con miras a la micropropagación clonal, eliminando así los efectos negativos que puedan ser causados por el uso de hormonas. Adicionalmente, se reporta un medio de cultivo adecuado para la inducción y multiplicación de callos a partir de explantes foliares, que incluye el empleo de un solo regulador de crecimiento a baja concentración, dejando fuera los efectos impredecibles que puede conllevar la combinación de diferentes hormonas. Adicionalmente, se encontró que es posible establecer y lograr el crecimiento de la suspensión celular cuando se emplea la combinación hormonal 2,4 D 0,5 mg/l + Kinetina 0,1 mg/l, lo cual es el punto de partida para el trazado de la curva de crecimiento celular y de producción del metabolito de interés.
AGRADECIMIENTOS
Al profesor Ramiro Fonnegra del Grupo de Estudios Botánicos de la U de Antioquia.
REFERENCIAS
1. Abe, Fumiko, Nagao T, Okabe H. 2002. Antiproliferative constituents in plants 9.1) aerial parts of Lippia dulcis and Lippia canescens. Biological & Pharmaceutical Bulletin, 25 (7): 920-922. [ Links ]
2. Azcon-Bieto J, Talón M. 2000. Fundamentos de fisiología vegetal. Barcelona (España): McGraw Hill. p.522. [ Links ]
3. Capote A, Fuentes V, Blanco N, Pérez O. 1999. Micropropagación y regeneración de plantas in vitro de oreganillo Lippia micromera Schau. in DC. Var. helleri (Brito). Revista del Jardín Botánico Nacional, XX:139-142. [ Links ]
4. Collin HA, Edwards S. 1998. Plant cell culture. Oxford: Bios Scientific Publishers. [ Links ]
5. Compadre CM, Hussain RA, López de Compadre RL, Pezzuto JM, Kinghorn DA. 1987. The intensely sweet sesquiterpene hernandulcin: isolation, sintesis, characterization, and preliminary safety evaluation. Journal of Agricultural and Food Chemistry, 35: 273-279. [ Links ]
6. Compadre CM, Pezzuto JM, Kinghorn AD. 1985. Hernandulcin: an intensely sweet compound discovered by review of ancient literature. Science, 227: 417-419. [ Links ]
7. Compadre CM, Robbins EF, Kinghoran AD. 1986. The intensely sweet herb, Lippia dulcis Trev.: Historical uses, field inquiries and constituents. Journal of Ethnopharmacology, 15 (1): 89-106. [ Links ]
8. De Block M. 1988. Genotype-independent leaf disc transformation of potato (Solanum tuberosum) using Agrobacterium tumefaciens. Theoretical and Applied Genetics, 76: 767-774. [ Links ]
9. Gupta SK, Khanuja SPS, Kumar S. 2001. In vitro micropropagation of Lippia alba. Current Science, 81: 206-210. [ Links ]
10. Hulme JS, Higgins ES, Shields R. 1992. An efficient genotype-independent method for regeneration of potato plants from leaf tissue. Plant Cell, Tissue and Organ Culture, 31: 161-167. [ Links ]
11. Julini H Jr, Koroch A, Julini H, Trippi V. 1999. Micropropagation of Lippia junelliana (Mold) Tronc. Plant Cell, Tissue and Organ Culture, 59: 175-179. [ Links ]
12. Kaneda N, Lee I, Gupta M, Soejarto DD, Kinghorn AD. 1992. (+)4ß-hydroxyhernandulcin, a new sweet sesquiterpene from the leaves and flowers of Lippia dulcis. Journal of Natural Products, 55 (8): 1136-1141. [ Links ]
13. Kinghorn AD, Ito Aiko, Kennelly E, Kim NC, Wetenburg. 1998. Studies on some edible and medicinal plants of mesoamerica. Proceedings of the Western Pharmacology Society, 41: 253-258. [ Links ]
14. Kinghorn AD, Soejarto DD. 2002. Discovery of terpenoid and phenolic sweeteners from plants. Pure and Applied Chemistry, 74 (7): 1169-1179. [ Links ]
15. Mollers C, Zhang JS, Wenzel G. 1991. The influence of silver thiosulfate on potato protoplast cultures. Plant Breeding, 108 (1): 12-18. [ Links ]
16. Masateru O, Morinaga H, Masuoka C, Ikeda T, Okawa M, Kinjo J, Nohara T. 2005. New Bisabolane-Type Sesquiterpenes from the Aerial Parts of Lippia dulcis. Notes. Chemical & Pharmaceutical Bulletin, 53 (9): 1175-1177. [ Links ]
17. Murashige T, Skoog F. 1962. A revised medium for rapid growth and bioassays with tobacco tissue cultures. Physiologia Plantarum 15: 473-497. [ Links ]
18. Paniego NB. Gullieti AM. 1996. Artemisin production by Artemisia annua L. –transformed organ cultures. Enzyme and Microbial Technology, 18: 526-530. [ Links ]
19. Pascual ME, Slowing K, Carretero E, Sánchez M, Villar A. 2001. Lippia: tradicional uses, chemistry and pharmacology: a review. Journal of Ethnopharmacology, 76: 201-214. [ Links ]
20. Pereira-Peixoto PH, Gonçalves-Salimena FR, Oliveira-Santos M de, Silva-Garcia L Da, Oliveira-Pierre PM de, Facio-Viccini L, Campos-Otoni W. 2006. In vitro propagation of endangered Lippia filifolia Mart. and Schauer ex Schauer. In Vitro Cellular & Developmental Biology, 42: 558-561. [ Links ]
21. Pérez JN. 1998. Propagación y mejora genética de plantas por biotecnología. Santa Clara (Cuba): Instituto de biotecnología de las plantas, Ed. p. 390. Pérez S, Meckes C, [ Links ]
22. Pérez C, Susunaga A, Zavala MA. 2005. Anti-inflammatory activity of Lippia dulcis. Journal of Ethnopharmacology, 102: 1-4. [ Links ]
23. Ramachandra-Rao S, Ravishankar GA. 2002. Plant cell cultures: chemical factories of secondary metabolites. Biotechnology Advances, 20: 101-153. [ Links ]
24. Sauerwein M, Flores HE, Yamazaki T, Shimomura K. 1991b. Lippia dulcis shoot cultures as a source of the sweet sesquiterpene hernandulcin. Plant Cell Reports, 9 (10): 663-666. [ Links ]
25. Sauerwein Martina, Yamazaki T, Shimomura K. 1991a. Hernandulcin in hairy root cultures of Lippia dulcis. Plant Cell Reports, 9 (10): 579-581. [ Links ]
26. Savitha B, Thimmaraju R. Bhagyalakshmi N, Ravishankar G. 2006. Different biotic and abiotic elicitors influence betalain production in hairy root cultures of Beta vulgaris in shake-flask and bioreactor. Process Biochemestry, 1 (4): 50-60. [ Links ]
27. Shinde AN, Malpathak N, Fulzele DP. 2009. Studied enhancement strategies for phytoestrogens production in shake flasks by suspension culture of Psoralea corylifolia. Bioresource Technology, 100: 1833-1839. [ Links ]
28. Souto FA, Echeverría M, Cárdenas O, Acuña M, Meléndez P, Romero L. 1997. Terpenoid composition of Lippia dulcis. Phytochemistry, 44 (6): 1077-1086. [ Links ]
29. Urrea AI, Veitía N, Bermúdez I. 2001. Selección in vitro de callos de papa (Solanum tuberosum ) var. Diacol Capiro empleando el filtrado crudo de Phytophthora infestans ( mont) De Bary. Actualidades Biológicas, 23 (74): 5-13. [ Links ]
30. Veitia N, García L, Clavero J, Urrea AI. 1999. Desarrollo de diferentes medios de cultivo para la formación de callos de papa. Revista del Centro Agrícola, III/99. [ Links ]
31. Young-Am Chae, Hee-Suk Yu, Ji-Sook Song, Hee-Kyung Chun, Sang-Un Park. 2000. Indigo production in hairy root cultures of Polygonum tinctorium Lour. Biotechnology Letters, 22: 1527-1530. [ Links ]
32. Zhao J, Davis LC, Verpoorte R. 2005. Elicitor signal transduction leading to production of plant secondary metabolites. Biotechnology Advances, 23: 283-333. [ Links ]
Recibido: febrero 2009;
aceptado: junio 2009.














