Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Actualidades Biológicas
Print version ISSN 0304-3584
Actu Biol vol.33 no.94 Medellín Jan./June 2011
ARTÍCULOS DE INVESTIGACIÓN
MICROPROPAGACIÓN E INDUCCIÓN DE ÓRGANOS DE ALMACENAMIENTO EN CURCUMA LONGA L.
MICROPROPAGATION AND INDUCTION OF STORAGE ORGANS IN CURCUMA LONGA L.
Aura I. Urrea-Trujillo1, Alejandra Canal-M.2, Zulma I. Monsalve-F.3
1 Docente. Instituto de Biología, Universidad de Antioquia. A. A. 1226. Medellín (Antioquia), Colombia. aurrea@matematicas.udea.edu.co.
2 Bióloga. Universidad de Antioquia. A. A. 1226. Medellín (Antioquia), Colombia. zmonsalve@matematicas.udea.edu.co.
3 Docente. Instituto de Biología, Universidad de Antioquia. A. A. 1226. Medellín (Antioquia), Colombia.
Recibido: noviembre 2010; aceptado: mayo 2011.
Resumen
Curcuma longa L. es una especie cuya composición química la hace atractiva al mercado, ya que además de los pigmentos, utilizados como colorante y medicinal, contiene cetonas y alcoholes que le dan sabor al rizoma, por tanto es utilizado como especia. La propagación de C. longa se realiza principalmente por vía asexual, con bajas tasas de propagación, además los rizomas son vulnerables a enfermedades, dificultando su almacenamiento. El cultivo de tejidos vegetales brinda entre otras alternativas, la producción de microrrizomas, facilitando el manejo en invernadero y campo, el transporte, intercambio y la conservación. El objetivo de este trabajo fue introducir y multiplicar in vitro plantas de C. longa, e inducir la formación de microrrizomas. Después de estandarizar el protocolo de desinfección, para los ápices establecidos se evaluó la altura y coeficiente de multiplicación como índice de respuesta a diferentes concentraciones de bencilaminopurina. Para la inducción de microrrizomas se usaron vitroplantas de 10 cm, evaluando la formación de estos, el número promedio y características morfológicas. Los resultados obtenidos sugieren que el medio MS con 2 mg/l de bencilaminopurina (BAP) es adecuado para producir buena cantidad y calidad de nuevas plantas. Condiciones de oscuridad y la concentración de sacarosa por encima de 60 g/l fueron factores determinantes en la inducción de los microrrizomas.
Palabras clave: Curcuma longa, fotoperiodo, microrrizoma, reguladores de crecimiento, Turmeric.
Abstract
One of the important characteristics of the plant species Curcuma longa L. is its chemical composition that makes it commercially attractive, because in addition to its pigments, which are used as food dyes or in medicines, it contains acetones and alcohols that give flavor to its rhizomes, making useful as a spice. Curcuma propagation is mainly conducted asexually, with low propagation rates; in addition, the rhizomes are susceptible to disease, making their storage difficult. Plant tissue culture offers, among other alternatives, microrhizome production, facilitating management in the greenhouse and field, transportation, exchange, and conservation. The goal of this project was to introduce and multiply C. longa plants in vitro, and induce microrhizome formation. After standardization of a disinfection protocol, the height and coefficient of multiplication of the established apexes were evaluated as response indeces to differing bencilaminopurine concentrations. Vitroplants of 10 cm were used to induce microrhizomes, and their formation, mean number, and morphological characteristics were evaluated. The results obtained suggested that MS medium with 2 mg/l bencilamonopurine (BAP) is adequate for producing a good quantity and quality of new plants. Conditions of total darkness and a sugar concentration above 60 g/l were key factors in the induction of microrhizomes.
Keywords: Curcuma longa, growth regulators, microrhizomes, photoperiod, turmeric.
INTRODUCCIÓN
La especie Curcuma longa L. es una planta monocotiledónea, herbácea, perenne y tropical perteneciente a la familia Zingiberaceae, originaria del sur de Asia y cultivada principalmente en Bangladés, China, India, Pakistán y Sri Lanka; siendo la India su principal exportador (Bailey 1949).
Sus rizomas tienen múltiples aplicaciones, entre las cuales se puede citar su uso en la industria de alimentos como especia saborizante, colorante y conservante; en medicina tradicional como anticancerígeno, antiinflamatorio, antioxidante, antiparasitario, antiviral, antiséptico, estomático, tónico y purificador de la sangre (Chattopadhyay et al. 2004, John et al. 1997), antibacterial, anticoagulante, antidiabético, antifibrótico, antifúngico, antimutagénico e hipocolesterolémico (Chattopadhyay et al. 2004, Scartezzini y Speroni 2000); también tiene usos industriales como aromatizante, en la elaboración de cosméticos, como ornamental, en la protección de cultivos, tintura natural, y más recientemente se ha evaluado, con mucho éxito, el potencial de sus extractos como controlador de plagas (resultados propios). Lo anterior, sin que se registren actividades tóxicas, mutagénicas o reacciones farmacológicas adversas a la fecha.
Estas aplicaciones son debidas a que la planta sintetiza compuestos polifenólicos, derivados sesquiterpénicos, alcoholes, cetonas y aceites esenciales volátiles, entre otros (Mau et al. 2003). Entre los polifenoles vale destacar el diferuloylmethano o curcumina, el cual es responsable de la mayoría de las acciones farmacológicas de la planta.
Sin embargo C. longa, se ve limitada ya que es una planta triploide básicamente estéril (2n = 3x = 63) (John et al. 1997), por lo cual solo puede ser propagada vegetativamente a través de rizomas; adicionalmente, su tasa de propagación es muy baja (de 5 a 10 veces en un año) y los rizomas son muy vulnerables al ataque de insectos y a enfermedades causadas por bacterias y hongos (distintas especies de Pythium), lo que hace que su almacenamiento sea complicado y se aumente el riesgo de dispersión de los patógenos. De igual forma, las enfermedades causadas por distintas especies de Colleotrichum son un problema para la conservación y almacenamiento de germoplasma de diferentes especies de Curcuma, principalmente en depósitos clónales (Nayak 2000).
Asociado a esto, las necesidades propias de su cultivo, tales como altitud (entre los 1.300 y 1.800 m) temperatura alta, agua abundante (1.000 mm mínimo de lluvia anual con irrigación complementaria) y suelos óptimos (rico en materia orgánica), hacen que su comercialización y su potencialidad en aplicaciones no sean tan efectivas y beneficiosas como se podría esperar. No sobra mencionar que el tipo y cantidad de metabolitos sintetizados por la planta varía dependiendo del lugar de origen, lo que implica que las condiciones de cultivo influyen grandemente en el control de las rutas metabólicas (Barrero y Carreño 1999).
Otro factor que limita el uso sostenible de la cúrcuma es su tiempo de ''maduración'', el cual fluctúa entre siete y nueve meses, esto hace que la recolección de rizomas no pueda ser efectuada sino a partir de los 10 meses posteriores a la siembra (Filho et al. 2000), alcanzando un porcentaje favorable solo a los 24 meses después de la siembra. Esto sin mencionar el efecto que la explotación continuada ha generado en las poblaciones de cúrcuma y que a la fecha no ha sido debidamente evaluado.
Las técnicas de cultivo de tejidos permiten la obtención de plantas sanas, en mayor cantidad, en menor tiempo y espacio, sin limitaciones referentes a las condiciones ambientales, facilitando el manejo del cultivo, optimizando la producción tanto de las plantas como de su contenido de metabolitos, facilitando y reduciendo costos de transporte y comercialización, entre otros; además, y no menos importante, la conservación de germoplasma.
Los estudios en el área de cultivo de tejidos in vitro de C. longa se han orientado principalmente a la propagación y a la generación de microrrizomas (Balachandran 1990, Cousins y Adelberg 2008, Dekkers 1991, Mrudul et al. 2001, Nadgauda et al. 1978, Salvi et al. 2001, Singh et al. 2011, Tyagi et al. 2004). No obstante, se requieren nuevas investigaciones que permitan obtener mejores resultados tanto en propagación vegetativa como en organogénesis y, obviamente, en la obtención de plantas completas.
La formación de rizomas in vitro de C. longa fue lograda por Mrudul et al. (2001) y Sunitibala et al. (2001) utilizando diferentes concentraciones de citoquininas y azúcar, lo mismo que diferentes fotoperiodos; Cousins y Adelberg (2008) evaluaron diferentes tiempos de exposición al medio de inducción de microrrizomas que contenía BA y/o metiljasmonato, en distintas concentraciones logrando la formación de estas estructuras en tiempos cortos (6 semanas) y largos (23 semanas). Estos resultados se han obtenido también en especies como C. amada (Nayak 2002), C. aromatica (Nayak 2000) y jengibre (Zingiber officinale; Sharma et al. 1995).
La producción de microrrizomas tiene ventajas comparativas con la producción in vitro de plantas. Las plantas micropropagadas necesitan aclimatización bajo condiciones de luz y humedad controladas por varios días, además del mantenimiento posterior en un invernadero hasta que sean plantadas en el suelo. Los microrrizomas, por su parte, pueden ser sembrados directamente en el suelo sin necesidad de aclimatización; además su almacenamiento y transporte es mucho más sencillo, facilitando así el intercambio de germoplasma (Mrudul et al. 2001). Por esto la obtención de microrrizomas mediante cultivo de tejidos es una alternativa para la propagación masiva de la especie y por lo tanto de los curcuminoides, de manera más fácil, rápida, económica y con menor incidencia de patógenos (Mrudul et al. 2001, Nayak 2000, 2002, Sunitibala et al. 2001).
En Colombia, el trabajo con C. longa se ha limitado a la propagación de rizomas mediante técnicas convencionales realizadas en pequeños cultivos comerciales con fines alimenticios y terapéuticos, localizados en Chigorodó, Chocó y Tolima, principalmente.
El presente estudio tiene como objetivo establecer las condiciones óptimas para la propagación in vitro e inducción de la formación de microrrizomas de Curcuma longa L., evaluando su coeficiente de multiplicación, y el efecto del fotoperiodo y reguladores de crecimiento sobre la formación de microrrizomas.
MATERIALES Y MÉTODOS
Material vegetal. Como fuente de explantes se usaron plantas de Curcuma longa L. regeneradas a partir de rizomas provenientes de Chocó, Colombia. Las brotes obtenidos fueron individualizados y mantenidos bajo condiciones de vivero hasta el desarrollo de las plantas, usando una mezcla tierra arena (2:1) previamente esterilizada. Cada 30 días se fertilizaron con las sales MS (Murashige y Skoog 1962) a la mitad de la concentración de su fórmula.
Desinfección y establecimiento in vitro. Las yemas apicales localizadas en la base del tallo fueron utilizadas como explante para los diferentes ensayos de desinfección. La sección basal de los tallos de seis centímetros de longitud fue lavada superficialmente con jabón quirúrgico y posteriormente enjuagadas con agua corriente repetidas veces. Luego, en condiciones asépticas, se evaluaron los siguientes protocolos de desinfección.
Protocolo 1: los explantes fueron sumergidos durante 15 minutos en hipoclorito de sodio al 2% adicionado con Tween 20, seguido por dos enjuagues con agua destilada estéril y la remoción de bordes y capas externas de tejido hasta un tamaño de yema de 2,5 cm aproximadamente. Estas yemas se sumergieron nuevamente en hipoclorito de sodio al 3% durante 10 minutos, finalmente se enjuagaron con agua destilada estéril hasta eliminar los restos de hipoclorito.
Protocolo 2: los explantes fueron tratados con el fungicida Manzate® a 100 mg/l durante 10 min, posteriormente se procedió con los pasos descritos en el protocolo 1.
Protocolo 3: los explantes fueron tratados como se describió en el protocolo 1, pero al final se realizaron cortes eliminando nuevamente el tejido externo hasta un tamaño aproximado de la yema de 1,5 cm. Estas yemas fueron sumergidas durante 10 a 15 s en una mezcla de hipoclorito al 3% y ácido acético al 5% en proporción 70:30, y finalmente se enjuagaron con agua destilada estéril hasta eliminar los restos de la mezcla biocida.
En todos los casos, los explantes fueron cultivados en el medio basal MS a pH 5,7 y gelificado usando gelrite a 1,8 g/l, a una temperatura de 24 ± 2 °C con un fotoperiodo de 16 h luz (28-35 μmol m-2 s-1) y 8 h oscuridad. Se estableció un tamaño de muestra de 15 yemas por tratamiento distribuidas individualmente en frascos de vidrio de 150 ml que contenían 25 ml del medio de cultivo, se realizaron tres repeticiones en cada protocolo. Como indicadores de respuesta se evaluaron: porcentaje de desinfección, tipo de contaminante, porcentaje de viabilidad y número de plantas con brotes.
Propagación in vitro. El medio de cultivo utilizado para la siembra de las yemas fue el medio basal MS, manteniendo las condiciones descritas anteriormente.
Los tratamientos evaluados para el establecimiento y la multiplicación, se describen a continuación. En todos los casos se usó el medio de cultivo basal MS suplementado con sacarosa (30 g/l) y gelrite (1,8 g/l), ajustando el pH a 5,7 antes de esterilizar en autoclave a 121 °C a 20 lb de presión por 15 min. Se evaluó el efecto en diferentes concentraciones (0,0, 2,0, 3,0 y 4,0 mg/l) de bencilaminopurina (BAP) sobre el coeficiente de multiplicación en las vitroplantas de 7 cm de longitud, establecidas como se describió anteriormente. El tamaño de muestra utilizado fue de 23 explantes por tratamiento, cada uno con cuatro réplicas. Como indicador del efecto se registró el número de brotes nuevos por explante a las cuatro semanas de iniciado el cultivo.
Formación de microrrizomas. Para la inducción de microrrizomas se evaluaron tres condiciones lumínicas y seis tratamientos de reguladores de crecimiento como se describe a continuación. En todos los casos se usaron vitroplantas de C. longa de 15 cm de longitud mantenidas en medio basal MS a pH 5,7 suplementado con BAP a 2,0 mg/l y sacarosa a 30 g/l, a temperatura de 25 ± 2 °C. Los reguladores de crecimiento evaluados fueron ácido naftalenacético (ANA), kinetina (KIN) y BAP; los medios se prepararon de la siguiente manera: medio 1, se mantuvo exento de reguladores; el medio 2, igualmente estuvo exento de reguladores, y se usó la mitad de la concentración de las sales basales MS; el medio 3, fue adicionado con ANA a 0,1 mg/l y KIN a 1,0 mg/l; el medio 4, fue adicionado con ANA a 0,1 mg/l y KIN a 1,0 mg/l en consistencia semisólida; el medio 5, fue adicionado con BAP a 5,0 mg/l; finalmente el medio 6, contenía BAP a 5,0 mg/l con 60 g/l de sacarosa. En el tratamiento en que se evaluó el estado semisólido del medio, el agente usado fue gelrite a 1,6 g/l.
Todos los medios descritos anteriormente fueron evaluados en distintas condiciones de luz, así: 0 h luz; 8 h luz-16 h oscuridad; y 16 h luz-8 h oscuridad.
En todos los casos, el tamaño de muestra fue de cinco vitroplantas por tratamiento y evaluado por duplicado. Cada 30 días las plantas se transfirieron a medio fresco de la misma composición y a los 90 días se registró la formación o no de microrrizomas, y el número y características morfológicas de los mismos.
Análisis estadísticos. Los datos obtenidos se procesaron estadísticamente mediante análisis de varianza simple (ANOVA). La determinación de grupos homogéneos y significativamente diferentes se llevó a cabo mediante la prueba de Student-Newman-Keuls con un nivel de confianza del 95%, usando el programa Statgraphics 5 plus.
RESULTADOS
Desinfección y establecimiento in vitro. Con la aplicación del protocolo 1, en el cual los explantes se sometieron al efecto desinfectante del hipoclorito de sodio en dos concentraciones diferentes (2 y 3%), a la acción surfactante del Tween 20 y la remoción de tejido externo hasta un tamaño de yema de 2,5 cm, no se logró disminuir la carga microbiana, el total de explantes se contaminaron principalmente con hongos y en algunos casos con bacterias (dato no mostrado).
Considerando los resultados anteriormente descritos, en el protocolo 2 se incluyó un tratamiento inicial con Manzate®; mientras que en el protocolo 3 se realizó una segunda eliminación de tejido externo hasta lograr un tamaño de yema de 1,5 cm seguido de la acción conjunta del hipoclorito de sodio y ácido acético.
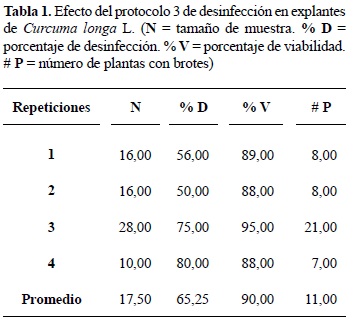
El tratamiento con el fungicida solo permitió obtener una proporción de desinfección del 30%, persistiendo tanto hongos como bacterias. Sin embargo, con el último tratamiento de desinfección, el porcentaje promedio obtenido fue de 65,25%, con fluctuaciones entre el 50 y 80%. Con respecto a la viabilidad, el promedio fue de 90% con una rango entre 88 y 95%. Finalmente, el número promedio de plantas con brotes llego a ser de 11 con un máximo de 21 plantas (tabla 1).
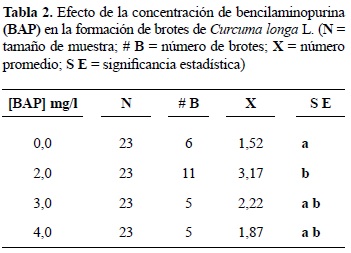
Propagación in vitro. Con el objetivo de obtener el mayor número de brotes por explante, se evaluaron distintas concentraciones de BAP. Paradójicamente, el medio sin BAP y los medios con concentraciones altas de este regulador de crecimiento no mostraron diferencias significativas entre ellos, logrando un número de brotes entre cinco y seis. En contraste, usando BAP a 2,0 mg/l se obtuvo el mayor número de brotes por explante (11 brotes; tabla 2), mostrando una diferencia estadísticamente significativa con respecto al control.
Es de anotar que las características morfológicas de las plantas desarrolladas usando 2,0 mg/l de BAP difieren de las demás, presentando mayor altura (6 ± 3 cm), mejor capacidad de formar raíces y mayor vigor de la planta.
Formación de microrrizomas. Para inducir la formación de microrrizomas se evaluaron medios con distintas características de reguladores de crecimiento, concentración de sacarosa y consistencia, en diferentes regímenes de fotoperiodo.
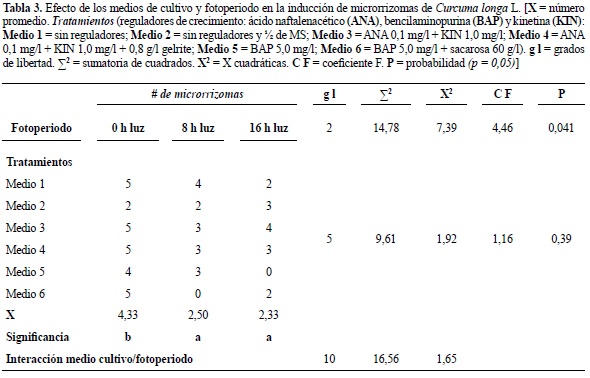
Cuando las plantas se cultivaron en ausencia de luz, no se detectó diferencias significativas en el número de microrrizomas, usando como referencia las características de los medios de cultivo. Una situación que se repitió en los demás fotoperiodos evaluados, salvo aquellos como el medio 5 con 16 h/luz y el medio 6 con 8 h/luz, en los que no se logró la formación de microrrizomas. No obstante, al comparar las condiciones de fotoperiodo, independientemente del medio de cultivo, se evidenció una diferencia estadísticamente significativa al mantener condiciones de ausencia de luz. Esto es, a 0 h/luz, en todos los medios de cultivo, se obtuvieron entre 2 y 5 microrrizomas con promedio de 4,33, en tanto que con los regímenes de luz de 8 y 16 h los promedios fueron de 2,50 y 2,33, respectivamente (figura 1; tabla 3).
DISCUSIÓN
Desinfección y establecimiento in vitro. Como es bien conocido, superar las dificultades de la etapa de desinfección es crucial para lograr avanzar en las siguientes etapas de la micropropagación, y el cultivo de tejidos en general. Es así como para conseguir una desinfección eficiente se deben considerar, entre otros, la procedencia del material vegetal, las condiciones de crecimiento, el tipo y concentración de los desinfectantes y sus posibles combinaciones con otro tipo de compuestos o prácticas.
En el presente estudio, se trabajó con plantas madre que se desarrollaron y mantuvieron bajo condiciones de vivero, donde no se tiene ningún control de los contaminantes ambientales a los cuales están expuestas las plantas. Teniendo esto en mente, es razonable suponer que el poco éxito de los tratamientos de desinfección empleados inicialmente fue debido a la carga infectiva portada por el material de inicio, la cual incluía, según la inspección visual del material, tanto
bacterias como hongos.
Es relevante anotar que aunque se usó hipoclorito de sodio, uno de los desinfectantes más ampliamente utilizados por sus propiedades biocidas sobre bacterias y hongos, en condiciones tan drásticas como 3% de concentración por 15 min, fue necesario hacer un pretratamiento con agentes antifúngicos y aun así no se logró el nivel de desinfección requerido.
En vista de los resultados anteriores, la pertinencia de emplear un tratamiento más fuerte se valida, aun a costa de sacrificar, en parte la viabilidad de los tejidos. En el presente caso, fue necesario recurrir a la acción combinada del hipoclorito de sodio con ácido acético (70:30). Como referencia para incluir este tratamiento en el estudio, se recurrió a resultados previos descritos en prácticas no reportadas por nuestro laboratorio. El ácido acético actúa bajando el pH de la solución, esto afecta a los microorganismos haciendo más efectiva la desinfección, sin descartar el impacto que pueda tener este en combinación con el hipoclorito de sodio sobre las proteínas de la pared y membrana celular, y por ende en la viabilidad de los microorganismos. Este tratamiento aunado a la remoción progresiva de capas superficiales del tejido, permitieron alcanzar porcentajes de desinfección superiores al 60%, lo cual a la luz de lo antes mencionado, hace factible considerar como un nivel muy adecuado para este material. No sobra resaltar que la viabilidad del tejido se mantuvo en un promedio del 90%.
Más aún, según los registros la aplicación de tratamientos efectivos, que incluyen tanto fungicidas como antibióticos, pueden tener repercusiones negativas dependientes del genotipo en la capacidad de regeneración del explante inicial y en la estabilidad genética del material vegetal resultante (Da Silva et al. 2003). En este caso, aunque no se han llevado a cabo pruebas específicas para asegurar su estabilidad genética, su capacidad de regeneración y sus características morfológicas y fisiológicas no se vieron afectadas. Las plantas alcanzaron una longitud superior a 15 cm, con raíces profusas, gruesas y largas; adicionalmente se pudo constatar la aparición de pequeños brotes.
Es de resaltar que en este protocolo de desinfección se obvia la utilización de cloruro de mercurio, el cual ha sido necesario para lograr éxito en la desinfección de tejidos del género Curcuma (Hoang et al. 2005, Mrudul et al. 2001, Nayak 2000, 2002, Singh et al. 2011, Tyagi et al. 2004).
La reducción del tamaño del explante, debida a la progresiva remoción de tejido, es un factor clave en el éxito de este protocolo de desinfección. Cuando se eliminaron capas de tejido hasta un tamaño de yema inferior a 1,0 cm la viabilidad es severamente afectada, de forma tal que todos los tejidos de este tamaño sufrieron un proceso de necrosamiento, el cual corresponde al 8,7%. Sin embargo, las yemas de mayor tamaño mantuvieron su capacidad regenerativa, el 95,7% de las plantas produjeron nuevos brotes.
Propagación in vitro. Desde mucho tiempo atrás es aceptado que las citoquininas actúan rompiendo la dominancia apical que ejercen los ápices meristemáticos en las plantas, lo cual se traduce en el aumento de la frecuencia de formación de yemas laterales y adventicias. Los resultados de este estudio son consistentes con esto, de forma tal que en el tratamiento control, exento de BAP, el número de brotes obtenidos fue el más bajo.
Llama la atención que al usar concentraciones mayores de BAP (superiores a 3,0 mg/l) el efecto observado en la formación de brotes se afecta, mostrando nuevamente resultados que no presentan diferencia significativa con el control sin el regulador. Es probable que este efecto sea debido a que el balance a favor de la formación de nuevos brotes sea alterado por el exceso mismo del BAP, se debe recordar que los efectos fisiológicos de las citoquininas son explicados por su interacción con las auxinas, y más aún, en el control de la expresión de los genes que codifican las citoquininas participan, entre otros, las citoquininas mismas (Segura 2008). Así, es de esperar que la adición de citoquinina exógena se comporte diferencialmente dependiendo del nivel endógeno tanto de las auxinas como de las citoquininas. Esto se ejemplifica en la gran disimilitud de las concentraciones de BAP reportadas para llegar a la óptima multiplicación de los brotes en C. longa (Cousins y Adelberg 2008, Naz et al. 2009, Singh et al. 2010, Tyagi et al. 2004).
Además del número de brotes formados, es importante considerar las características morfológicas de las plantas desarrolladas, entre las cuales se pueden destacar la altura, el grosor, la coloración y la formación o no de raíces. En el presente estudio, cuando se usaron 2,0 mg/l de BAP fue evidente que las características fenotípicas de las plantas obtenidas sobresalieron favorablemente entre los demás tratamientos evaluados (dato no mostrado).
De otro lado, es importante considerar que la formación de estructuras aéreas y raíces de manera simultánea es una cualidad altamente deseable para facilitar la propagación y el establecimiento ex vitro del material vegetal. En este sentido, los resultados obtenidos fueron altamente satisfactorios, ya que esta simultaneidad en el desarrollo organogénico evita el uso posterior de tratamientos hormonales para inducir la formación de raíces.
Formación de microrrizomas. Una de las características del proceso de inducción de órganos de reserva como tubérculos y rizomas es el engrosamiento de la base del tallo. La mayoría de plantas que se propagan vegetativamente presentan órganos capaces de acumular sustancias de reserva en sus parénquimas primarios y secundarios en un determinado momento del ciclo biológico. Estos órganos pueden ser los tallos, las raíces y las hojas. Algunos órganos de multiplicación, a la vez que acumulan sustancias de reserva, presentan hipertrofia radial de los órganos tuberizados que se convierte en órganos de almacén, y después de un periodo más o menos largo sirven para la multiplicación de la especie (Vázquez y Torres 2001).
Cabe mencionar trabajos que han descrito la formación de microrrizomas en diferentes especies de Curcuma, como por ejemplo: Cousins y Adelberg (2008), Hashemy et al. (2009), Mrudul et al. (2001) y Sunitibala et al. (2001) en C. longa; Nayak (2000) en C. aromática; y Nayak (2002) en C. amada.
Uno de los aspectos de importancia en la inducción de microrrizomas es la composición del medio de cultivo, particularmente la disponibilidad de nitrógeno (Agramonte 1999). Al reducir las sales MS a la mitad de su concentración (medio 2) se observó una clara reducción en el número de microrrizomas obtenidos. Si bien no hubo diferencia estadísticamente significativa en lo que respecta a la concentración de las sales MS, es importante resaltar que esta tendencia puede ser explicada por esa baja disponibilidad de nitrógeno. Adelberg (2010) advierte la importancia de la disponibilidad de nitrato y amonio, como fuentes de nitrógeno, en el incremento de biomasa y la multiplicación de yemas apicales en C. longa. Este mismo autor reporta que minerales como el fósforo, el azufre, el magnesio y el cobre son suplementos necesarios para la formación de órganos de almacenamiento.
En gran variedad de especies se ha demostrado que el nivel de sacarosa en el medio de cultivo influye significativamente la formación de órganos de almacenamiento in vitro (bulbos, cormos, tubérculos y rizomas; Adelberg y Cousins 2007, Mrudul et al. 2001, Nayak 2000, Sunitibala et al. 2001, Shirgurkar et al. 2001), ya que constituye la fuente de carbono y agente osmótico esencial para la formación de estas estructuras. Sin embargo, en estudios realizados comparando la sacarosa y el manitol en medios con potenciales osmóticos equivalentes, se encontró que solo la sacarosa promueve la formación de microtubérculos en papa (Martínez et al. 1991), órgano de almacenamiento. Más aún, es probable observar un efecto contrario, es decir de inhibición de la formación de los microrrizomas por un alto potencial osmótico (Mrudul et al. 2001, Sunitibala et al. 2001), lo cual puede ser debido a un fuerte impedimento estérico al desarrollo de estas estructuras. Demostrando que el efecto osmótico no es el inductor como sí lo es la disponibilidad de la fuente de carbono.
La formación de órganos de reserva también es afectada por el fotoperiodo, se ha reportado que periodos cortos de luz estimulan la formación de microrrizomas, sin embargo, no hay consistencia en los informes al respecto. Ejemplo de ello son las investigaciones realizadas por Mrudul et al. (2001) en C. longa, quienes reportan mejores resultados en la inducción de microrrizomas incubando en condiciones de total oscuridad. En contraste, tanto Hashemy et al. (2009) como Sunitabala et al. (2001), evaluando la misma especie, describen mejores resultados con un fotoperiodo de 8 h/luz. En otras especies del mismo género, como lo son C. aromática y C. amada, estudios de Nayak (2000, 2002) describen la inducción de microrrizomas en condiciones óptimas con 8 y 16 h/luz, respectivamente. En el presente estudio se determinó que la incubación en condiciones de oscuridad total potencian la formación de microrrizomas (en todos los medios de cultivo evaluados), apoyando el reporte de Mrudul et al. (2001), pero en contraste con lo reportado por Hashemy et al. (2009) y Sunitabala et al. (2001). La significancia de estos resultados tan contrastantes, no solo pueden ser debidos a la influencia que obviamente tiene el genotipo, sino también al efecto que pueden estar ejerciendo las condiciones de cultivo previas a los tratamientos de inducción de microrrizomas, particularmente la intensidad lumínica, y la composición y consistencia del medio de cultivo empleados en la etapa de multiplicación de las plantas a las cuales se inducirá la formación de microrrizomas, factores que no han sido correlacionados previamente para el género Curcuma.
Finalmente, a diferencia de los estudios previos (Adelberg 2010, Adelberg y Cousins 2007, Hashemy et al. 2009, Mrudul et al. 2001, Nayak 2000, Sunitibala et al. 2001, Shirgurkar et al. 2001), en nuestro estudio no se evidenció una diferencia significativa en el efecto de los reguladores de crecimiento evaluados sobre la formación de microrrizomas, lo cual refuerza la hipótesis de la marcada influencia de las condiciones de cultivo en las etapas previas a la inducción.
AGRADECIMIENTOS
Se agradece a los laboratorios de Fisiología Vegetal y Cultivo de Tejidos, Ingeniería Genética y Biología Molecular de Plantas; y al Instituto de Biología de la Facultad de Ciencias Exactas y Naturales de la Universidad de Antioquia.
REFERENCIAS
1. Adelberg J. 2010. Sucrose, water and nutrient use during stage II multiplication of two turmeric clones (Curcuma longa L.) in liquid medium. Scientia Horticulturae, 124: 262-267. [ Links ]
2. Adelberg J, Cousins M. 2007. Development of micro-and minirhizomes of turmeric, Curcuma longa L., in vitro. Acta Horticulture, 756: 103-108. [ Links ]
3. Agramonte D. 1999. Métodos biotecnológicos para la producción de semilla original de papa (Solanum tuberosum L.) [Tesis de doctorado]. [Santa Clara (Cuba)]: Instituto de Biotecnología de las Plantas, Universidad Central de las Villas. p. 96. [ Links ]
4. Bailey LH. 1949. Manual of cultivated plants most commonly grown in the continental United States and Canada. New York (U. S. A.): Macmillan Co. p. 1116. [ Links ]
5. Balachandran SM, Bhat SR, Chandel KPS. 1990. In vitro clonal multiplication of turmeric (Curcuma spp.) and ginger (Zingiber officinale Rosc.). Plant Cell Report, 8: 521-524. [ Links ]
6. Barrero M, Carreño R. 1999. Evaluación de los pigmentos de Curcuma cultivada en Venezuela. Agronomía Tropical, 49 (4): 491-504. [ Links ]
7. Chattopadhyay I, Biswas K, Bandyopadhyay U, Banerjee RK. 2004. Turmeric and curcumin: Biological actions and medicinal applications. Current Science, 87 (1): 44-53. [ Links ]
8. Cousins MM, Adelberg JW. 2008. Short-term and long-term time course studies of turmeric (Curcuma longa L.) microrhizome development in vitro. Plant Cell Tissue and Organ Culture, 93: 283-293. [ Links ]
9. Da Silva JA, Teixeira N, Duong T, Michio T, Seiichi F. 2003. The effect of antibiotics on the in vitro growth response of chrysanthemum and tobacco stem transverse thin cell layers (tTCLs). Scientia Horticulturae, 97: 397-410. [ Links ]
10. Dekkers AJ, Rao AN, Goh CJ. 1991. In vitro storage of multiple shoot cultures of gingers at ambient temperatures of 24-29 8C. Scientia Horticulturae, 47: 157-167. [ Links ]
11. Filho ABC, de Souza RJ, Trevizan-Braz L, Tavares M. 2000. Cúrcuma: planta medicinal, condimentar e de outros usos potenciais. Revisión bibliográfica. Ciência Rural (Santa Maria), 30 (1): 171-175. [ Links ]
12. Hashemy T, Maki H, Yamada Y, Kanako T, Syono K. 2009. Effects oh light and cytokinin on in vitro micropropagation and microrhizome production in turmeric (Curcuma longa L.). Plant Biotechnology, 26: 237-242. [ Links ]
13. Hoang N, Trong D, Ho Kwon T, Sik M. 2005. Micropropagation of zedoary (Curcuma zedoaria Roscoe) - a valuable medicinal plant. Plant Cell Tissue and Organ Culture, 81:119-122. [ Links ]
14. John CK, Nadgauda RS, Mascarenhas AF. 1997. Turmeric. En: Varios, editores. Tissue culture of economic plants. New Delhi (India): Center for Science and Technology of the Non-Aligned and Other Developing Countries. p. 191-209. [ Links ]
15. Martínez L, Stecco VL, Tizzio R. 1991. Potenciales osmóticos y tuberización in vitro de secciones de brotes y esquejes de papa. Turrialba, 41 (4): 515-519. [ Links ]
16. Mau J, Lai E, Wang N, Chen C, Chang C, Chyau C. 2003. Composition and antioxidant activity of the essential oil from Curcuma zedoaria. Food Chemistry, 82 (4): 583-591. [ Links ]
17. Mrudul VS, John CK, Nadgauda RS. 2001. Factors affecting in vitro microrhizome production in turmeric. Plant Cell Tissue and Organ Culture, 64: 5-11. [ Links ]
18. Murashige T, Skoog F. 1962. A revised medium for rapid growth and bioassays with tobacco tissue cultures. Physiology Plant, 15: 437-497. [ Links ]
19. Nadgauda RS, Mascarenhas AF, Hendre RR, Jagannathan V. 1978. Rapid multiplication of turmeric (Curcuma longa Linn.) plants by tissue culture. Indian Journal of Experimental Biology, 16: 120-122. [ Links ]
20. Nayak S. 2000. In vitro multiplication and microrhizome induction in Curcuma aromatica Salisb. Plant Grow Regulation, 32: 41-47. [ Links ]
21. Nayak S. 2002. High frequency in vitro production of microrhizomes of Curcuma amada. Indian Journal of Experimental Biology, 40 (2): 230-232. [ Links ]
22. Naz S, Illyas S, Javed S, Ali A. 2009. In vitro clonal multiplication and acclamitization of different varieties of tuurmeric (Curcuma longa L.) Pakistan Journal of Botany, 41 (6): 2807-2816. [ Links ]
23. Salvi ND, George L, Eapen S. 2001. Plant regeneration from leaf base callus of turmeric and random amplified polymorphic DNA analysis of regenerated plants. Plant Cell Tissue and Organ Culture, 66: 113-119. [ Links ]
24. Scartezzini P, Speroni E. 2000. Review on some plants of Indian traditional medicine with antioxidant activity. Journal of Ethnopharmacology, 71 (1-2): 23-43. [ Links ]
25. Segura J. 2008. Citoquininas. En: Azcón J, Talón M, editores. Fundamentos de fisiología vegetal. Barcelona (España): Editorial McGraw-Hill Interamericana. p. 421-443. [ Links ]
26. Sharma TR and Singh BM. 1995. In vitro microrhizome production in Zingiber officinale Rosc. Plant Cell Reports, 15: 274-277. [ Links ]
27. Shirgurkar MV, Jhon CK, Nadgauda RS. 2001. Factors affecting in vitro microrhizome production in turmeric. Plant Cell Tissue and Organ Culture, 64 (1): 5-11. [ Links ]
28. Singh S, Kuanar A, Mohanty S, Subudhi E, Nayak S. 2011. Evaluation of phytomedicinal yield potential and molecular profiling of micropropagated and conventionally grown turmeric (Curcuma longa L.). Plant Cell Tissue and Organ Culture, Plant Cell Tissue and Organ Culture, 104 (2): 263-269. [ Links ]
29. Sunitibala H, Damayanti M, Sharma GJ. 2001. In vitro propagation and rizhome formation in Curcuma longa. Cytobios, 2001 (105): 71-82. [ Links ]
30. Tyagi RK, Yusuf A, Dua P, Agrawal A. 2004. In vitro plant regeneration and genotype conservation of eight wild species of Curcuma. Biologia Plantarum, 48 (1): 129-132. [ Links ]
31. Vázquez E, Torres S. 2001. Capítulo 10. Reproducción, multiplicación vegetativa. En: Vásquez E, Torres S. Fisiología vegetal. La Habana (Cuba): Ed. Félix Varela. p. 391-403. [ Links ]