Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Actualidades Biológicas
Print version ISSN 0304-3584
Actu Biol vol.36 no.101 Medellín July/Dec. 2014
ARTÍCULOS DE INVESTIGACIÓN
Biomasa de rotíferos de dos embalses con diferentes estados tróficos (Antioquia, Colombia) y su relación con algunas variables limnológicas
Rotifer biomass of two reservoirs with different trophic states (Antioquia, Colombia) and its relationship with some limnological variables
Silvia L. Villabona-González1,2,3*, Robinson F. Buitrago-Amariles1,4, John J. Ramírez-Restrepo1,5, Jaime A. Palacio-Baena2,6
1 Grupo de Investigación en Limnología Básica y Experimental y Biología y Taxonomía Marina, Universidad de Antioquia. A. A. 1226. Medellín (Antioquia), Colombia.
2 Grupo de Investigación en Gestión y Modelación Ambiental, Universidad de Antioquia. A. A. 1226. Medellín (Antioquia), Colombia.
Correos electrónicos (*autor para correspondencia): 3 silvillabo81@gmail.com; 4 robultimate@hotmail.com; 5 johnra77@gmail.com; 6 japalaci@udea.edu.co.
Recibido: febrero 2014; aceptado: junio 2014.
Resumen
Se evaluó la variación de la biomasa de rotíferos en los ejes longitudinal y vertical de la zona fótica de los embalses La Fe y Riogrande II (Antioquia), Colombia, con diferentes estados tróficos, durante los periodos de alta y baja precipitación. Además, se analizó su relación con las variables temperatura, oxígeno disuelto, pH, transparencia, nutrientes y con la biomasa fitoplanctónica. La biomasa de rotíferos fue dominada por Asplanchna girodi De Geurne 1888, en los dos embalses y fue significativamente mayor en el embalse de menor trofía. Aunque la biomasa de rotíferos no mostró un gradiente longitudinal significativo, sí presentó zonación vertical dentro de la zona fótica, con mayor biomasa en el 10 y 1% de incidencia lumínica. Los patrones de variación de la biomasa total de rotíferos y de las especies dominantes estuvieron determinados principalmente por el ingreso de sólidos suspendidos en el embalse de mayor trofía y por la biomasa y la densidad del fitoplancton en el embalse con menos nutrientes. A diferencia de lo esperado, la biomasa de los rotíferos no fue favorecida por condiciones de mayor estado trófico, ya que el factor preponderante sobre la expresión de biomasa fue la calidad de los recursos alimenticios en cada embalse.
Palabras clave: Asplanchna girodi, biomasa, embalses, fitoplancton, rotíferos, sólidos suspendidos.
Abstract
Rotifers biomass was evaluated across longitudinal and vertical axes of the photic zone in the La Fe y Riogrande II reservoirs (Antioquia), Colombia, with different trophic states during periods of high and low precipitation. IN addition, its relationship with temperature, dissolved oxygen, pH, transparency, nutrient availability, and phytoplankton biomass was analyzed. In both reservoirs, rotifer biomass was dominated by Asplanchna girodi De Geurne, 1888, and it was significantly higher in the reservoir with a lower trophic state. Even though rotifers biomass did not exhibit a longitudinal gradient, a vertical zonation in the photic zone was documented, with the greatest biomass at 10% and 1% of light intensity. Patterns of variation in total rotifer biomass and in dominant species biomass appear to be determined primarily by the entry of suspended solids into the reservoir with the higher trophic state, and by phytoplankton biomass and density in the reservoir with lower nutrient levels. Contrary to expectations, rotifer biomass was not favored by increasing trophic state. The most important factor determining rotifer biomass was the quality of food resources in each reservoir.
Key words: Asplanchna girodi, biomass, phytoplankton, reservoirs, rotifers, suspended solids.
INTRODUCCIÓN
En los embalses tropicales los rotíferos juegan un rol fundamental, ya que normalmente predominan en riqueza y densidad en estos sistemas (Sendacz et al. 2006), presentan alto valor nutricional, un aspecto importante en las redes tróficas de los ambientes limnéticos (Ruttner-Kolisko 1977), y algunas especies son sensibles a cambios en la calidad del agua (Marneffe et al. 1998).
En general, los estudios sobre embalses tropicales han enfatizado la relación entre abundancia y composición del zooplancton y condiciones abióticas (Arcifa et al. 1992, Bini et al. 1997, Corgosinho y Pinto 2006, González et al. 2002, Guevara et al. 2009, Pinto-Coelho 1998, Sendacz 1984). Sin embargo, pocos estudios consideran la dinámica de la biomasa y su relación con variables ambientales (Rossa et al. 2007).
Existen diversas hipótesis acerca de la contribución de los rotíferos a la biomasa del zooplancton (Rossa et al. 2007, Vásquez y Rey 1992), el comportamiento de la biomasa en embalses con diferente estado trófico (Nagae 2007), las variaciones temporales (Andrew y Fitzsimons 1992, Bonecker et al. 2007, Sendacz et al. 2006) y los gradientes verticales (Dippolito 1988, Infante 1993) y longitudinales (Marzolf 1990, Monroy 2008). Es claro que la expresión de biomasa de los rotíferos está determinada por las características biológicas, físicas, hidráulicas y químicas particulares de cada embalse (Bonecker et al. 2007, Conde- Porcuna et al. 2002, González et al. 2011). En Colombia, solo se dispone de estudios sobre biomasa de zooplancton en los embalses Betania (Huila; Herrera 1993), La Fe (Antioquia; Estrada-Posada 1999), La Esmeralda (Boyacá; Monroy 2008) y Prado (Tolima; Guevara et al. 2009), por lo que en general, se carece de información sobre la biomasa de los rotíferos.
La pregunta del presente estudio es cómo varía la biomasa de rotíferos en la zona fótica de los embalses La Fe y Riogrande II (Antioquia), Colombia, a lo largo de los ejes longitudinal y vertical de cada embalse, y entre estos dos embalses durante los periodos de alta y baja precipitación. Si la biomasa de rotíferos en un embalse está determinada por los caudales y los materiales aportados por los tributarios, el estado trófico y la biomasa fitoplanctónica, entonces se prevé que los rotíferos presentan las máximas biomasas en la zona media y al 10% de incidencia lumínica, durante la época de menor precipitación en ambos embalses, y que la biomasa alcanza los mayores valores en el embalse Riogrande II, predominantemente eutrófico.
MATERIALES Y MÉTODOS
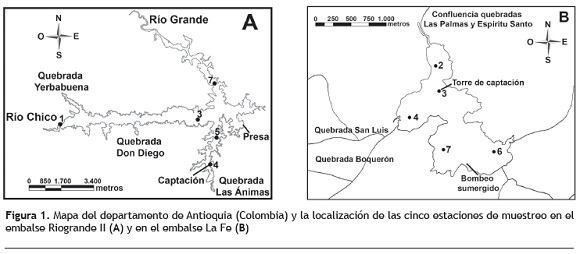
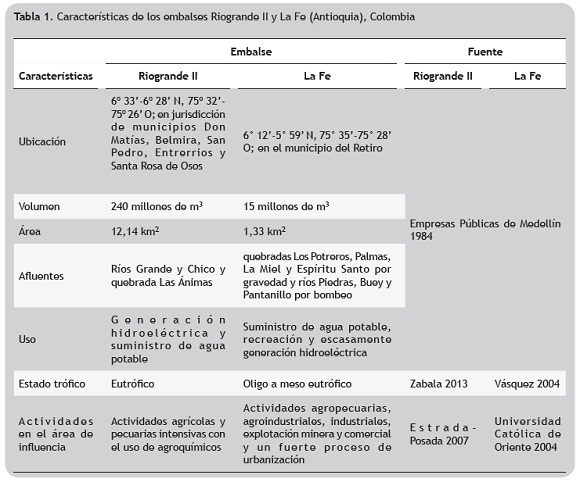
Área de estudio. Fueron establecidas cinco estaciones de muestreo en los embalses La Fe (2, 3, 4, 6, 7) y Riogrande II (1, 3, 4, 5, 7) (figura 1, tabla 1), durante el periodo de lluvias bajas: enero de 2011 para Riogrande II y febrero de 2011 para La Fe; y periodo de lluvias altas: octubre de 2011 para ambos embalses (tabla 2). Se tomaron muestras de zooplancton mediante arrastres verticales con una red de 40 μm de luz de malla para el análisis del biovolumen de las especies de rotíferos. Además, con un tamiz de 40 μm de luz de malla se filtraron 35 l de agua proveniente de tres profundidades (sub-superficie, a 10 y a 1% de incidencia lumínica) para calcular las densidades de los organismos. La numeración de las estaciones de muestreo sigue la codificación fijada por el programa ''Estudio de la problemática ambiental de tres embalses de empresas públicas de Medellín para la gestión integral y adecuada del recurso hídrico''.
Las muestras de agua para los análisis de biovolumen fueron preservadas en formaldehído al 4% (de Azevedo 2006) y para los análisis cuantitativos con solución transeau [seis partes de agua tres de alcohol etílico al 95% y una de formaldehído] en proporción 1:1. Todas las muestras fueron depositadas en la Colección de Limnología de la Universidad de Antioquia (CLUA 035), Medellín (Antioquia), Colombia. Para la nomenclatura taxonómica de las especies de rotíferos se siguió la de Segers (2007) y la clasificación de las especies las de: Fernando (2002), Kosté (1978), Kosté y Shield (1987), Segers (1995) y, Shield y Kosté (1992, 1993).
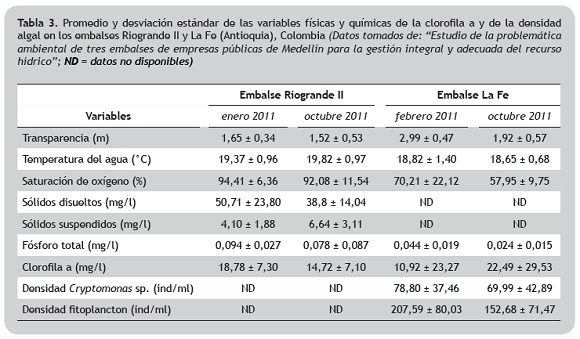
Los datos de las variables físicas y químicas, de la biomasa fitoplanctónica y de la densidad algal (disponible sólo en La Fe) fueron generados en el programa ''Estudio de la problemática ambiental de tres embalses de empresas públicas de Medellín para la gestión integral y adecuada del recurso hídrico'' (tabla 3) (Palacio et al. 2012a, b, Toro et al. 2012a, b). Debido a la disminución del nivel del agua en La Fe, no fue posible tomar las muestras en algunas estaciones de muestreo, principalmente a la profundidad de 1% de luz incidente.
El biovolumen de las especies de rotíferos se calculó con base en las fórmulas geométricas más semejantes a la forma del cuerpo de cada especie (Ruttner-Kolisco 1977). Se midieron aleatoriamente 30 individuos de las especies de rotíferos más abundantes en cada embalse, que constituyen hasta el 99% de la densidad total. Los valores de biovolumen fueron convertidos en peso húmedo, suponiendo que 106 μm3 equivalen a 1μg de peso húmedo (Bottrel et al. 1976) y el peso seco fue estimado como el 10% del peso húmedo (Pace y Orcutt 1981), excepto para las especies de Asplanchna (3,9%; Dumont et al. 1975).
Análisis estadístico. Para evaluar la significancia de las diferencias de biomasa total de rotíferos entre embalses se empleó la prueba de Kruskal y Wallis (Guisande et al. 2011). La significancia de las diferencias de biomasa entre las estaciones, profundidades y muestreos en cada embalse se evaluó mediante análisis de varianza ANOVA de una vía (Guisande et al. 2011), previa transformación de los datos con Ln. Cuando se encontraron diferencias significativas, se aplicó la prueba de Tukey (Guisande et al. 2011) para la comparación de las medias. Se realizaron análisis de regresión lineal simple entre la biomasa total de los rotíferos y las variables físicas y químicas y la clorofila a, y análisis de correlación entre la biomasa de Asplanchna girodi (De Geurne 1888), y las densidades de las especies dominantes del fitoplancton del embalse La Fe. Los análisis se realizaron con el paquete R.x64 2.15.2 (R Development Core Team 2008).
Para estimar la longitud del gradiente de la biomasa de los rotíferos se empleó un Análisis de Correspondencia Destendenciado (DCA, por sus siglas en inglés) por segmentos (Hill y Gauch 1980) con la biomasa de las especies dominantes y comunes (Sokal y Rohlf 1995).
De acuerdo con los resultados de este análisis, se decidió realizar una ordenación de gradiente directo por Análisis de Redundancia (RDA, por sus siglas en inglés) como el método más robusto para establecer las variables ambientales determinantes en los patrones de distribución de la biomasa de rotíferos.
Se utilizó la prueba de Monte Carlo (Leps y smilauer 2003) con 999 permutaciones para determinar la significancia de los predictores (< 0,05). Variables con inflación de la varianza (VIFs) > 20, fueron excluidas del análisis. Las ordenaciones se realizaron con el programa CANOCO versión 4.5 (Ter Braak y smilauer 2002).
RESULTADOS
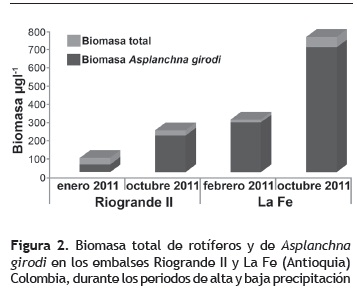
En el embalse La Fe, la biomasa de rotíferos tuvo en total 737,95 μg l-l en octubre de 2011 y 285,30 μg l-l en febrero de 2011, mientras que en Riogrande II la biomasa alcanzó solo 227,31 μg l-l en octubre de 2011 y 76,54 μg l-l en enero de 2011, valores significativamente menores a los encontrados en La Fe (Chi-cuadrado = 13,89, gl = 1, p = 0,0001). En los dos embalses, la biomasa total fue significativamente mayor en el periodo de máxima precipitación (Riogrande II: F = 4,53, gl = 1, p = 0,0425; La Fe: F = 5,86, gl = 1, p = 0,0322) (figura 2).
En los dos embalses y en los dos periodos climáticos, la especie Asplanchna girodi dominó en biomasa, con 55% de la biomasa total en el muestreo de lluvias bajas y 88% en el de lluvias altas en Riogrande II y con 96 y 93% en La Fe, respectivamente (figura 2).
Aunque el peso seco promedio de A. girodi fue mayor en Riogrande II (0,83 μg) que en La Fe (0,62 μg), la densidad alcanzó valores muy superiores en La Fe (tabla 4), especialmente en la profundidad del 10% de incidencia lumínica en la estación 2 en octubre de 2011, lo que influyó en el alto valor de biomasa allí registrado (554,31 μg l-l) (figura 3), el cual coincidió con el pico máximo de la densidad del alga Cryptomonas sp. (155,93 ind/ml). La biomasa de las otras 15 especies de rotíferos en Riogrande II (entre < 0,01 y 14%) y de 10 especies en La Fe fue baja (entre < 0,01 y 3%).
Aunque en ninguno de los dos embalses se encontraron diferencias significativas en la biomasa entre las estaciones de muestreo, en el embalse Riogrande II generalmente se encontró mayor biomasa en las estaciones 1 (entrada río Chico) y 7 (entrada río Grande) (figura 3).
En la zona fótica del embalse Riogrande II se encontraron los valores mínimos de biomasa en la sub-superficie durante los dos periodos climáticos, con valores medios de 3,53 μg l-l en el muestreo de bajas precipitaciones (enero) y de 6,92 μg l-l en el de altas precipitaciones (octubre). En contraste, la mayor biomasa se observó a la profundidad de 10% de incidencia lumínica, con valores medios de 8,07 μg l-l en enero y de 22,63 μg l-l en octubre (figura 3). El análisis de varianza mostró diferencias significativas en la biomasa entre las profundidades analizadas (F = 4,40, gl = 2, p = 0,02264).
Aunque en La Fe no se registraron diferencias significativas estadísticamente en la biomasa a través de la columna de agua en la zona fótica, la tendencia de los resultados no difiere de la señalada para el embalse Riogrande II. No obstante, la ausencia de significancia puede deberse a la falta de datos en las profundidades del 10 y del 1% de incidencia lumínica en algunas estaciones (figura 3).
Sólo la clorofila a influyó significativamente y de forma positiva sobre la biomasa total de los rotíferos en los dos embalses, mientras en Riogrande II también incideron los sólidos suspendidos sobre el valor de la biomasa de rotíferos; y en La Fe fueron importantes la turbidez y la temperatura del agua, pero esta última de forma negativa. Sin embargo, de acuerdo con los resultados de los análisis de regresión lineal, la relación entre la biomasa y todas estas variables fue leve (p < 0,05, R2 < 0,40). La biomasa de A. girodi se asoció positivamente (p = 0,046, R2 = 0,52) con la densidad de Cryptomonas sp., género que dominó el fitoplancton del embalse La Fe.
Los dos primeros ejes del DCA aportaron una varianza del 54,50% en Riogrande II y de 54,10% en La Fe. Las especies mostraron una longitud de gradiente de 1,83 desviaciones estándar (D. E.) en Riogrande II y de 1,58 D. E. en La Fe, ajustándose a un comportamiento lineal en ambos casos. De acuerdo con la prueba de Monte Carlo, el RDA fue significativo para todos los ejes canónicos en Riogrande II (F = 3,81, p = 0,0020, n = 29) y La Fe (F = 3,33, p = 0,0010, n = 22).
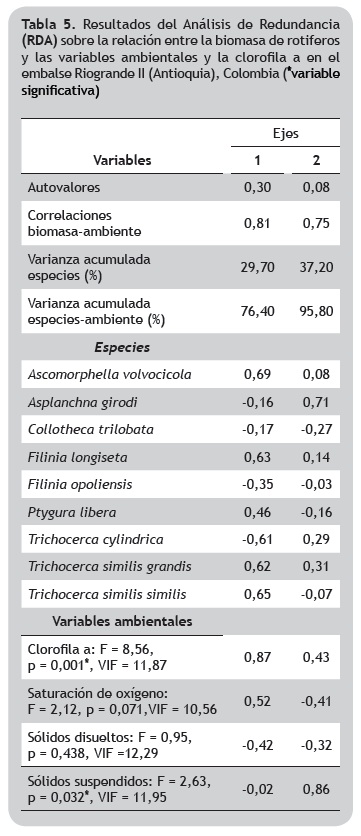
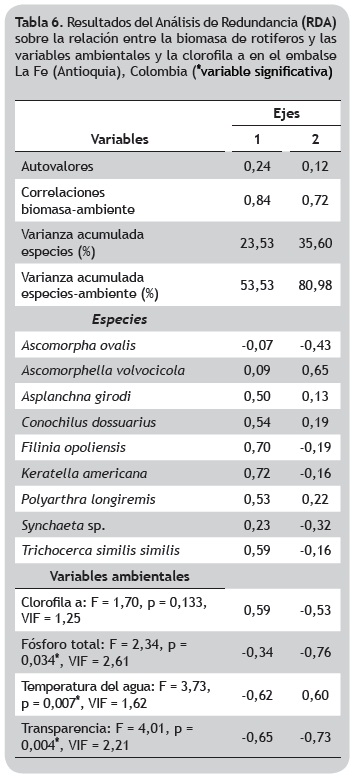
Los primeros dos ejes del RDA presentaron una suma de autovalores de 0,38 y explicaron el 95,80% del total de la varianza de los datos de la biomasa de rotíferos y el ambiente para Riogrande II, y el 80,98% para La Fe con suma de autovalores = 0,36. En ambos casos hubo alta correlación entre la biomasa de las rotíferos incluidos en el RDA y el componente ambiental (Riogrande II: 0,81 eje 1 y 0,75 eje 2; La Fe: 0,84 eje 1 y 0,72 eje 2; tablas 5 y 6).
Mientras en Riogrande II solamente la clorofila a y los sólidos suspendidos explicaron significativamente (p < 0,05) el comportamiento de la biomasa de los rotíferos, en La Fe estuvo asociado significativamente al fósforo total, la transparencia y la temperatura del agua. Sin embargo, en Riogrande II se incluyeron dentro del RDA variables como la saturación de oxígeno y los sólidos disueltos, y en La Fe, la clorofila a, que aunque no fueron significativas mostraron alto aporte a la varianza (figuras 4 y 5).
En el embalse Riogrande II, la biomasa de cinco de las especies de rotíferos analizadas, principalmente de Ascomorphella volvocicola (Plate, 1886) y Trichocerca similis similis (Wierzejski, 1893), se correlacionó positivamente en el primer eje de ordenación con las variables que reflejan la producción fitoplanctónica como la clorofila a y la saturación del oxígeno disuelto. En el segundo eje, la biomasa de A. girodi, especie que más aportó a la variación, estuvo determinada principalmente de forma positiva por los sólidos suspendidos y en menor medida, por la colorofila a y de forma negativa por la saturación de oxígeno y los sólidos disueltos. Este resultado, tiende a diferenciar el periodo de mayor precipitación (octubre) de la epoca más seca (enero) y la sub-superficie de las profundidades del 10 y del 1% de incidencia lumínica (figura 4, tabla 5).
En La Fe, las especies A. girodi, Filinia opoliensis (Zacharias, 1898), Keratella americana (Carlin, 1943) y T. similis similis, se relacionaron positivamente con la concentración de clorofila a, y negativamente con la transparencia y la temperatura del agua en el primer eje de ordenación. En el segundo eje, la biomasa de Ascomorpha ovalis (Carlin 1943) estuvo determinada principalmente por la concentración de fósforo total (figura 5, tabla 6).
No se encontró un patrón longitudinal claro para las estaciones de muestreo en los dos embalses que se asocie con alguna de las especies o de las variables ambientales analizadas.
DISCUSIÓN
Los resultados de esta investigación no apoyan la idea general de que en los embalses eutrofizados como Riogrande II se encuentra mayor cantidad de biomasa de rotíferos y no coinciden con lo registrado en la literatura para otros embalses tropicales, en los que la mayor biomasa de rotíferos se presenta en los sistemas acuáticos eutróficos, seguido de los mesotróficos y por último de los oligotróficos (Nagae 2007).
Particularmente, el patrón de variación de la biomasa de rotíferos en los dos sistemas estuvo determinado por la disponibilidad y calidad de alimento. En Riogrande II, la cantidad de material que ingresa al embalse se asoció positivamente con la biomasa, en particular de A. girodi, la especie dominante. Giraldo (2010) encontró en este embalse que A girodi tiene una estrategia trófica de forrajeo óptimo, lo que implica el consumo de los ítems de mayor disponibilidad y el máximo ahorro de energía (Begon et al. 2006).
En Riogrande II, el fitoplancton está constituido principalmente por varias especies del género Staurastrum (Palacio et al. 2012a), un ítem poco apetecible para el zooplancton debido a sus características morfológicas (Hansson y Tranvik 1996). De esta manera, es posible que en este embalse A. girodi prefiriera ítems probablemente muy abundantes y más apetitosos, como las bacterias y el detrito, pues en otros estudios se ha informado que hay especies de rotíferos que pueden ingerir partículas grandes de detritos, en las que las bacterias asociadas pueden formar agregados (Starkweather et al. 1979) y que además la materia orgánica en suspensión es un recurso trófico para el zooplancton (Arruda et al. 1983).
El fitoplancton del embalse La Fe, cuya mayor biomasa estuvo representada por Ceratium furcoides (Langhans, 1925) y Cryptomonas sp. (López-Muñoz, com. pers.), constituye un alimento más favorable para la proliferación de rotíferos. En este embalse, la biomasa algal se asoció positivamente con la mayoría de las especies de rotíferos, y la biomasa de la especie dominante, A girodi, mostró relación positiva con Cryptomonas sp., uno de los taxones más nutritivos para el zooplancton (Conde-Porcuna et al. 2004).
Aunque el género Asplanchna ha sido catalogado principalmente como omnívoro con preferencia alimenticia sobre rotíferos y cladóceros pequeños, Giraldo (2010) mostró que la gran diversidad trófica de A. girodi incluye el forrajeo sobre varias especies de algas.
La influencia de los recursos alimenticios se reflejó también en la variación temporal de la biomasa en los dos embalses que se incrementó en el periodo de mayor precipitación, en especial por el aporte de A. girodi. En Riogrande II, este aporte estuvo determinado significativamente por el mayor ingreso de sólidos suspendidos. En La Fe, por la mayor biomasa fitoplanctónica y aguas menos cálidas y más turbias durante el periodo de lluvias.
De acuerdo con el estudio de Infante (1993), durante el periodo de lluvias en un lago natural de Venezuela, el mayor caudal arrastra gran cantidad del material particulado adyacente a los afluentes, el cual es en parte de origen orgánico y favorece el transporte y desarrollo de bacterias.
Sendacz (1984) registró aumento de la producción primaria y de la biomasa zooplanctónica durante este periodo y Nagae (2007) argumentó que el menor tiempo de residencia del agua durante la época de mayor precipitación favorece el desarrollo de rotíferos oportunistas.
En este estudio, se rechaza la hipótesis que postula que mayores valores de biomasa serían hallados hacia la zona media de los embalses, y que según el modelo de Marzolf (1990), la distribución del zooplancton alcanzaría su máximo en esta zona por el balance entre las fuerzas hidrodinámicas (flujo y tiempo de residencia del agua) y la acumulación de los recursos que ingresan desde el río (nitrógeno y fosforo).
Sin embargo, el modelo corresponde a una situación ideal, pues de acuerdo con Kimmel et al. (1990), los tributarios y su descarga en los embalses agregan discontinuidad horizontal, y por tanto, estimulan nuevos agrupamientos del plancton en el eje horizontal en cortos periodos de tiempo y en estructuras de meso-escala (1-20 km), por lo tanto, la permanente reorganización del sistema en los embalses en función de la energía externa interrumpe las regularidades y descompone el eje horizontal en unidades heterogéneas en el espacio, a las que se agregan las comunidades de fitoplancton y zooplancton (Margalef 1983). En consecuencia, las zonas de un embalse usualmente son dinámicas, se expanden y se contraen en respuesta a los eventos de escorrentía en las cuencas, a las características de la densidad del flujo y a la operación de descarga del agua del embalse.
Aunque el fósforo total explicó el patrón de biomasa de algunas especies en La Fe, no hubo asociación clara con las diferentes estaciones del embalse, y la dinámica de la captación de los afluentes naturales y del agua importada que dividen el embalse en dos cuerpos de agua, norte y sur (Román-Botero 2011), no determinaron diferencias entre la biomasa de los rotíferos. Aunque en Riogrande II tampoco se encontraron diferencias estadísticas en el eje longitudinal, la biomasa tendió a ser mayor en las estaciones cercanas al ingreso de los tributarios, los cuales traen consigo alta concentración de sólidos suspendidos.
A pesar que en los dos embalses se encontró mayor acumulación de biomasa en las capas más profundas de la zona fótica (10 y 1% de incidencia lumínica), estas diferencias solo fueron significativas para Riogrande II, donde la biomasa, en especial de A. girodi, se asoció a mayores concentraciones de sólidos suspendidos en el 10 y 1% de incidencia lumínica. Por su parte, en la subsuperficie las mayores concentraciones de oxígeno y de sólidos disueltos favorecieron especies de poco aporte a la biomasa como es el caso de Collotheca trilobata (Collins, 1872) y Ptygura libera (Myers, 1934).
Dippolito (1988) concluyó que el comportamiento vertical de las poblaciones de rotíferos está ligado principalmente al pulso de las floraciones algales. En este sentido, se encontró que la biomasa de la mayoría de las especies de rotíferos en ambos embalses se asoció positivamente con la clorofila a, y que en el embalse La Fe, el fitoplancton tendió a concentrarse en el 10 y 1% de incidencia lumínica (Palacio et al. 2012b), lo que coincidió con mayor aporte de biomasa de rotíferos en estas profundidades.
De acuerdo con lo anterior, es posible que la luz que penetra hasta esta zona influya indirectamente la expresión de biomasa en los embalses La Fe y Riogrande II. En la subsuperficie, el exceso de luz y radiación solar puede afectar al zooplancton negativamente, debido a que allí pueden ser fácilmente visualizados por los depredadores, y a que algunas especies se ven afectadas fisiológicamente por el exceso de radiación. Masson et al. (2004) mostraron que la distribución vertical de la biomasa del zooplancton es función de su evasión a los depredadores potenciales y de ocupación de un ambiente físico y químico mejor.
En conclusión, los resultados no permitieron corroborar totalmente la hipótesis planteada, pues la biomasa de los rotíferos no estuvo determinada por el estado trófico de los embalses ni fue favorecida por las condiciones ecológicas propias del periodo de menor precipitación, ni por las condiciones de la zona media de estos embalses. No obstante, dentro de la zona fótica se encontró un gradiente vertical con biomasas mayores en las capas más profundas. La oferta trófica en cada embalse y la calidad del alimento fueron probablemente los factores más importantes en la regulación de la biomasa de los rotíferos en los embalses La Fe y Riogrande II, en especial de la especie dominante, A. girodi.
AGRADECIMIENTOS
Este trabajo se realizó gracias a la financiación de Empresas Públicas de Medellín, de los grupos GAIA y LimnoBasE y del laboratorio de biología de la regional de oriente de la Universidad de Antioquia (Medellín), Colombia. Agradecemos al programa ''Estudio de la problemática ambiental de tres embalses de empresas públicas de Medellín para la gestión integral y adecuada del recurso hídrico'', realizado conjuntamente entre los grupos de investigación de la Universidad de Antioquia: GAIA, GDECON y Productos naturales y el posgrado de recursos hidráulicos de la Universidad Nacional, Sede Medellín por facilitarnos los datos ambientales y por su invaluable colaboración en los muestreos. A Diego Chalarca y Agustín Moreno por la elaboración de los mapas y a Claudia Bonecker, Daniel Monroy, Santiago Gaviria y Patricia Pelayo por sus valiosos aportes al estudio.
REFERENCIAS
Andrew TE, Fitzsimons AG. 1992. Seasonality, population dynamics and production of planktonic rotifers in Lough Neagh. Northern Ireland. Hydrobiologia, 246 (2): 147-164. [ Links ]
Arcifa MS, Gomes EAT, Meschiatti AJ. 1992. Composition and fluctuations of the zooplankton of a tropical Brazilian reservoir. Archiv für Hydrobiologie Beiheft Ergebnisse der Limnologie, 123 (4): 479-495. [ Links ]
Arruda JA, Marzolf GR, Faulk RT. 1983. The role of suspended sediments in the nutrition of zooplankton in turbid reservoirs. Ecology, 64: 1225-1235. [ Links ]
Begon M, Townsend CR, Harper JL. 2006. Ecology: from individuals to ecosystems. 4th ed. Oxford (Inglaterra): Blackwell Publishing. p. 752. [ Links ]
Bini LM, Tundisi JG, Matsumura-Tundisi T, Mathes CE. 1997. Spatial variation of zooplankton groups in a tropical reservoir (Broa Reservoir, São Paulo State Brazil). Hydrobiologia, 357 (1-3): 89-98. [ Links ]
Bonecker CC, Nagae MY, Bletller MC, Machado LF, Lansac-Tôha FA. 2007. Zooplankton biomass in tropical reservoirs in southern Brazil. Hydrobiologia, 579 (1): 115-123. [ Links ]
Bottrell HH, Duncan A, Gliwicz ZM, Grygierek E, Herzig A, Hillbricht- Ilkowska A, Kurasawa H, Larsson P, Weglenska T. 1976. A review of some problems in zooplankton production studies. Norwegian Journal of Zoology, 24 (24): 419-456. [ Links ]
Conde-Porcuna JM, Ramos-Rodríguez E, Morales-Baquero R. 2004. El zooplancton como integrante de la estructura trófica de los ecosistemas lénticos. Revista Ecosistemas, 13 (2): 23-29. [ Links ]
Conde-Porcuna JM, Ramos-Rodríguez E, Pérez-Martínez C. 2002. Correlations between nutrient concentrations and zooplankton populations in a mesotrophic reservoir. Freshwater Biology, 47: 1463-1473. [ Links ]
Corgosinho PHC, Pinto-Coelho RM. 2006. Zooplankton biomass, abundance and allometric patterns along an eutrophic gradient at Furnas Reservoir (Minas Gerais, Brazil). Acta Limnologica Brasiliensia, 182: 213-224. [ Links ]
De Azevedo F. 2006. Relações ecológicas da riqueza, densidade, massa individual e biomassa das assembléias zooplanctônicas em lagoas fechadas da planície de inundação do alto rio Paraná (PR-MS) [Tesis de doctorado]. [Maringá (Brasil)]: Programa de Pós- Graduação Em Ecologia de Ambientes Aquáticos Continentais, Universidad de Maringá. p. 78. [ Links ]
Dippolito A. 1988. Distribución vertical y temporal de los rotíferos del embalse Cassaffousth (Córdoba, Argentina). Asociación de Ciencias Naturales del Litoral, 19 (2): 155-166. [ Links ]
Dumont HJ, Van De Velde I, Dumont S. 1975. The dry weight estimate of biomass in a selection of Cladocera, Copepoda and Rotifera from the plankton, periphyton and benthos of continental waters. Oecologia, 19 (1): 75-97. [ Links ]
Empresas Públicas de Medellín. 1984. Proyecto de aprovechamiento múltiple del río Grande. Medellín (Colombia). Medellín (Colombia): Empresas Públicas de Medellín. Declaración de Impacto Ambiental. [ Links ]
Estrada-Posada A. 1999. Variação espacial e temporal da comunidade zooplanctônica do Reservatório ''La Fé'', Antioquia, Colombia [Tesis de maestría]. [Sao Paulo (Brasil)]: Universidad de São Paulo. p. 78. [ Links ]
Estrada-Posada A. 2007. Variación de la estructura y la distribución del zooplancton en función de los gradientes longitudinales en el embalse Riogrande II, Antioquia Colombia [Tesis de doctorado]. [Medellín (Colombia)]: Instituto de Biología, Universidad de Antioquia. p. 83. [ Links ]
Fernando CH. 2002. A guide to tropical freshwater zooplankton: identification, ecology and impact on fisheries. Leiden (Países bajos): Backhuys Publishers. p. 291. [ Links ]
Giraldo M. 2010. Composición de la dieta del rotífero Asplanchna girodi (De Guerne, 1888) y su variación temporal y espacial en el embalse Riogrande II (Antioquia, Colombia). [Trabajo de pregrado]. [Medellín (Colombia)]: Instituto de Biología, Universidad de Antioquia. p. 80. [ Links ]
González E, Matos M, Peñaherrera C, Merayo S. 2011. Zooplankton abundance, biomass and trophic state in some venezuelan reservoirs. En: Atazadeh I, editor. Biomass and Remote Sensing of Biomass. [Internet]. Rijeka: InTech. Disponible en: http://www.intechopen.com/books/biomass-and-remote-sensing-of-biomass/zooplankton-abundance-biomass-and-trophic-state-in-somevenezuelan-reservoirs. [ Links ]
González EJ, Ortaz M, Matos ML, Mendoza J, Herrera CP, Carrillo V. 2002. Zooplancton de dos embalses neotropicales con distintos estados tróficos. Interciencia, 27 (10): 551-558. [ Links ]
Guevara G, Lozano L, Reinoso G, Villa F. 2009. Horizontal and seasonal patterns of tropical zooplankton from the eutrophic Prado Reservoir (Colombia). Limnologica, 39: 128-139. [ Links ]
Guisande C, Vaamonde A, Barreiro A. 2011. Tratamiento de datos con R, Statistica y SPSS. (España): Diaz De Santos. p. 978. [ Links ]
Hansson LA, Tranvik LJ. 1996. Quantification of invertebrate predation and herbivory in food chains of low complexity. Oecologia, 108: 542-551. [ Links ]
Herrera Y. 1993. Estudio del zooplancton del embalse de Betania, Huila. [Trabajo de pregrado]. [Bogotá (Colombia)]: Departamento de Biología, Universidad Nacional de Colombia. p. 73. [ Links ]
Hill MO, Gauch HG. 1980. Detrended correspondence analysis, an improvised ordination technique. Vegetation, 42: 47-58. [ Links ]
Infante A. 1993. Vertical and horizontal distribution of the zooplankton in a lake Valencia. Acta Limnologica Brasileira, 6: 97-105. [ Links ]
Kimmel BL, Lind OT, Paulson LJ. 1990. Reservoir primary production. En: Thornton KW, Kimmel BL, Payne FE, editores. Reservoir limnology: Ecological perspectives. Nueva York (E.U.A): Wiley. p. 133-193. [ Links ]
Kosté W, Shield RJ. 1987. Rotifera from Australian Inland Waters. II Epiphanidae and Brachionidae (Rotifera: Monogononta). Invertebrate Taxonomy, 1 (7): 949-1021. [ Links ]
Kosté W. 1978. Rotatoria. Die Rädertiere Mitteleuropas. Überordnung Monogononta. Berlin (Alemania): Gebrüder Bornträger. p. 673. [ Links ]
Leps J, smilauer P. 2003. Multivariate analysis of ecological data using CANOCO. New York (U. S. A.): Cambridge University Press. p. 283. [ Links ]
Margalef R. 1983. Limnología. Barcelona (España): Omega. p. 1010. [ Links ]
Marneffe Y, Comblin S, Thome JP. 1998. Ecological water quality assessment of the Butgenbach lake (Belgium) and its impact on the River Warche using rotifers as bioindicators. Hydrobiologia, 387/388: 459-467. [ Links ]
Marzolf GR. 1990. Reservoirs as environments for zooplankton. En: Thornton KW, Kimmel BL, Payne FE, editores. Reservoir limnology: Ecological perspectives. Nueva York (U. S. A.): Wiley. p. 195-208. [ Links ]
Masson S, Pinel-Alloul B, Dutilleul P. 2004. Spatial heterogeneity of zooplankton biomass and size structure in southern Québec lakes: variation among lakes and within lake among epi-, metaand hypolimnion strata. Journal of Plankton Research, 26 (12): 1441-1458. [ Links ]
Monroy JD. 2008. Determinación de la expresión del zooplancton (excepto protozoos) en función de las variables ambientales de un embalse tropical (La Esmeralda-Colombia) [Tesis de maestría]. [Bogotá (Colombia)]: Departamento de Ciencias Biológicas, Universidad de los Andes. p. 74. [ Links ]
Nagae MY. 2007. Estudos das assembléias de rotíferos em reservatórios do sudeste e sul do Brasil [Tesis de doctorado]. [Maringá (Brasil)]: Programa de Pós-Graduação Em Ecologia de Ambientes Aquáticos Continentais, Universidade Estadual de Maringá. p. 114. [ Links ]
Pace ML, Orcutt JD Jr. 1981. The relative importance of protozoans, rotifers and crustaceans in a freshwater zooplankton community. Limnology and Oceanography, 26 (5): 822-830. [ Links ]
Palacio-Baena J, Herrera-Loaiza N, López-Muñoz M, Palacio- Betancourt H, Rodríguez M. 2012 a. Limnoecología de los embalses Riogrande II, La Fe y Porce II. En: Estudio de la problemática ambiental de tres embalses de empresas públicas de Medellín ESP para la gestión integral y adecuada del recurso hídrico. Medellín (Colombia): Universidad de Antioquia y Universidad Nacional sede Medellín. Informe técnico semestral de avance embalse Riogrande II, junio-diciembre de 2011. p. 649. [ Links ]
Palacio-Baena J, Herrera-Loaiza N, López-Muñoz M, Palacio- Betancourt H, Rodríguez M. 2012 b. Limnoecología de los embalses Riogrande II, La Fe y Porce II. En: Estudio de la problemática ambiental de tres embalses de empresas públicas de Medellín ESP para la gestión integral y adecuada del recurso hídrico. Medellín (Colombia): Universidad de Antioquia y Universidad Nacional sede Medellín. Informe técnico semestral de avance embalse La Fe, junio-diciembre de 2011. p. 390. [ Links ]
Pinto-Coelho RM. 1998. Efects of eutrophication on seazonal patterns of mesozooplankton in a tropical reservoir: a 4-year study in Pampulha lake, Brazil. Freshwater Biology, 40 (1): 159-173. [ Links ]
R Development Core Team. 2009. R: a language and environment for statistical computing [Internet]. Vienna, Austria: R Foundation for Statistical Computing. Fecha de acceso: junio de 2014. Disponible en: http://www.r-project.org. [ Links ]
Román-Botero R. 2011. Caracterización espacio temporal de la estructura térmica de un embalse tropical poco profundo, abastecido parcialmente por bombeo [Tesis de maestría]. [Medellín (Colombia)]: Posgrado de Aprovechamiento de Recursos Hidráulicos, Universidad Nacional de Colombia, Sede Medellín. p. 136. [ Links ]
Rossa DC, Bonecker CC, Fulone LJ. 2007. Biomassa de rotiferos em ambientes dulceacuícolas: Revisão de métodos e factores influentes. Interciencia, 32 (4): 220-226. [ Links ]
Ruttner-Kolisko A. 1977. Suggestions for biomass calculations of plankton rotifers. Archiv für Hydrobiologie Beiheft Ergebnisse der Limnologie, 8: 71-76. [ Links ]
Segers H. 1995. The Rotifera: Lecanidae (Monogonota). En: Nogrady T, editor. Guides to the identification of the microinvertebrates of the continental waters of the world. 2nd ed. Belgica (Holanda): SPB Academic publishing bv. p. 4-203. [ Links ]
Segers H. 2007. Annotated checklist of the rotifers (Phylum Rotifera), with notes on nomenclature, taxonomy and distribution. Zootaxa, 1564: 1-104. [ Links ]
Sendacz S, Caleffi S, Santos-Soares J. 2006. Zooplankton biomass of reservoirs in different trophic conditions in the State of Sao Paulo, Brazil. Brazilian Journal of Biology, 66: 337-350. [ Links ]
Sendacz S. 1984. A study of the zooplankton community of Billings Reservoir São Paulo. Hydrobiologia, 113 (1): 121-127. [ Links ]
Shield RJ, Kosté W. 1992. Rotifera from Australian inland waters VIII. Trichocercidae (Monogononta). Royal Society of South Australia Inc, 116 (1): 1-27. [ Links ]
Shield RJ, Kosté W. 1993. Rotifera from Australian inland waters. IX. Gastropodidae, Synchaetidae, Asplanchnidae (Rotifera: Monogononta). Royal Society of South Australia Inc, 1 (7): 111-139. [ Links ]
Sokal RR, Rohlf FJ. 1995. Biometry: the principles and practice of statistics in biological research. 3rd ed. New York (U. S. A.): WH Freman and Company. p. 887. [ Links ]
Starkweather PL, Gilbert JJ, Frost TM. 1979. Bacterial feeding by the rotifer Brachionus calyciflorus: clearance and ingestion rates, behavior and population dynamics. Oecologia, 44 (1): 26-30. [ Links ]
Ter Braak CJF, smilauer P. 2002: CANOCO Reference Manual and CanoDraw for Windows. User's Guide: Software for Canonical Community Ordination (version 4.5). Ithaca (U. S. A.): Microcomputer Power. p. 500. [ Links ]
Toro M, Chalarca D, Grajales H, Moreno A. 2012 a. Nutrientes de los embalses Riogrande II, La Fe y Porce II. En: Estudio de la problemática ambiental de tres embalses de empresas públicas de Medellín ESP para la gestión integral y adecuada del recurso hídrico. Medellín (Colombia): Universidad de Antioquia y Universidad Nacional sede Medellín. Informe técnico semestral de avance embalse Riogrande II, junio-diciembre de 2011. p. 649. [ Links ]
Toro M, Chalarca D, Grajales H, Moreno A. 2012 b. Nutrientes de los embalses Riogrande II, La Fe y Porce II. En: Estudio de la problemática ambiental de tres embalses de empresas públicas de Medellín ESP para la gestión integral y adecuada del recurso hídrico. Medellín (Colombia): Universidad de Antioquia y Universidad Nacional sede Medellín. Informe técnico semestral de avance embalse La Fe, junio-diciembre de 2011. 390. [ Links ]
Universidad Católica de Oriente. 2004. Estudio ambiental y plan de manejo de las microcuencas abastecedoras de las plantas de potabilización de las Empresas Públicas de Medellín E. S. P. del Valle del Aburrá. Medellín: Unidad de gestión ambiental. p. 232. [ Links ]
Vásquez E, Rey J. 1992. Composition, abundance and biomass of zooplankton in Orinoco floodplain lakes, Venezuela. Annales de Limnologie - International Journal of Limnology, 28: 3-18. [ Links ]
Vásquez LF. 2004. Determinación de la dinámica del fósforo en el embalse La Fe, [Trabajo de pregrado]. [Medellín (Colombia)]: Instituto de Biología, Universidad de Antioquia. p. 99. [ Links ]
Zabala AM. 2013. Evaluación del estado trófico del embalse Riogrande II (Antioquia, Colombia) a través del comportamiento espacial y temporal de los nutrientes. [Trabajo de pregrado]. [Medellín (Colombia)]: Instituto de Biología, Universidad de Antioquia. [ Links ]