INTRODUCCIÓN
El tabaquismo es un problema de salud pública que reúne causas genéticas, psicológicas, sociales y fisiológicas; aunque es considerado por la Organización Mundial de la Salud la primera causa de muerte prevenible en los países desarrollados, el 80% de los fumadores habitan países de ingresos bajos o medios, en los cuales la edad de inicio del consumo es cada vez menor (entre 9−13 años) (OMS 2015).
Personas cada vez más jóvenes inician el consumo reiterado, reduciendo con esto su expectativa de vida y generando tolerancia a las sustancias que lo componen y provocando una dependencia que se manifiesta en la dificultad para abandonarlo (Pérez y Pinzón 2005, OMS 2013); por lo tanto, identificar los factores genéticos y no genéticos que se relacionan con la probabilidad de abandono, la edad de inicio y la cantidad de tabaco consumido, es fundamental para comprender la biología de la dependencia, mejorar los pronósticos y generar nuevas alternativas terapéuticas, las cuales podrían personalizarse, acorde con el genotipo, para minimizar los efectos secundarios (Chen y Bierut 2013).
En cuanto a los procesos biológicos asociados con el tabaquismo, se han identificado varios genes dentro de los cuales las subunidades del receptor de acetil colina nicotínico (nAChR) se describen entre los mejores candidatos de genotipos relacionados con el tabaquismo. El gen CHRNA5, que codifica la subunidad 5 alfa del nAChR, se relaciona con la sensación agradable durante la experiencia inicial al fumar; una de sus variantes, el SNP (polimorfismo de un solo nucleótido) rs680244, se asocia con los niveles de ARNm, incidiendo directamente en la cantidad de receptores, por lo que podría asociarse con la probabilidad de no abandonar el tabaco, tal como lo informan Chen y Baker (2014), Berrettini y Doyle (2012) y Li y Yoon (2010).
Por otro lado, el gen CYP2A6 codifica el citocromo P450 que cataliza el metabolismo de la nicotina en cotinina en el hígado y según Osorio (2010), posee variantes que están relacionadas con la velocidad con la cual es procesada la nicotina (Oscarson 2001); una de estas variantes es el SNP rs1801272, cuyo alelo A se presenta en personas que metabolizan más lentamente la nicotina, y por lo tanto, el número de cigarrillos que requieren para producir la misma sensación se altera; así, aquellos que presentan el genotipo lento tienen una tendencia a consumir menos cigarrillos por día y a tener menores niveles de nicotina en sangre según lo registran Osorio (2010) y Raunio (2001).
Durante el primer estudio poblacional de salud mental realizado en Itagüí (Torres et al. 2012), se encontró que la prevalencia anual del consumo de sustancias en adolecentes era del 12,4%, siendo el tabaco una de las más frecuentes y encontrándose que la edad promedio de inicio de su consumo es 12,4 años.
Considerando lo anterior, este estudio evaluó la asociación de la variante rs680244 del gen CHRNA5 y la variante rs6801272 del gen CYP2A6 con el hábito de fumar y la dependencia al tabaco en una muestra de la población de Itagüí, Colombia.
MATERIALES Y METODOS
Obtención de base de datos.
Durante el desarrollo del primer estudio poblacional de salud mental en Itagüí (Torres et al. 2012), cuyo objetivo fue conocer los trastornos mentales más prevalentes, se recopiló información entrevistando la población general, ubicada en los diferentes estratos socioeconómicos de las seis comunas del municipio de Itagüí (Colombia), utilizando el WorldnHealth Organizatión Composite International Diagnostic inter-view (versión CIDI-CAPI; WHO 2017); adicionalmente, se tomó muestra de saliva para análisis genético a un total de 896 personas entre los 13 y los 65 años, con el debido consentimiento informado o asentimiento en caso de menores de edad, previa aprobación del Comité de ética de la Universidad CES, y considerando el respeto y la protección a los derechos individuales.
El tamaño de muestra se calculó con base en la fórmula para la estimación de una proporción poblacional: n= Nz2p (1-p). d2(N-1)m+ z2p(1-p) donde: N es la población total, z: valor Z para un nivel de confianza del 99%, d: Precisión absoluta del 5% y p: 5.9% (prevalencia anual esperada para la depresión según Torres et al. 2012).
Obtención de un banco de ADN.
La extracción del ADN a partir de las 896 muestras de saliva se realizó con el kit comercial DNA Ora gene Genotek siguiendo el protocolo descrito por Torres et al. (2012). El protocolo de extracción incluyó el uso de resinas quelantes (chelex-100 BIO-RAD) (Armas y Capo 2011); las muestras de ADN se almacenaron a -20 °C.
Selección de casos y controles.
A partir de la base de datos obtenida del primer estudio poblacional de salud mental se detectaron 185 fumadores (143 habituales y 43 esporádicos), 110 exfumadores (personas que llevaban un año o más sin consumir cigarrillos) y del banco de ADN se seleccionaron 70 exfumadores, 70 fumadores y 140 controles pareados por sexo, edad (con una diferencia máxima de 5 años entre caso y control) y comuna mediante el paquete Matchit 2.4-20 de R (Ho et al. 2007). Para estimar el tamaño de la muestra se emplearon las frecuencias de los alelos de riesgo en población europea e hispana (Saccone et al. 2009, Verde et al. 2011) y el número de habitantes del municipio de Itagüí, con una potencia del 80% utilizando el software Epiinfo (Manocci et al. 2012) y se obtuvo un valor aproximado de 40 individuos para cada categoría.
Genotipificación.
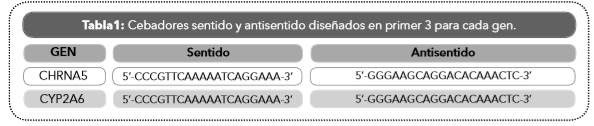
Los cebadores fueron diseñados usando el software PRIMER 3 v.04.0 (Koressaar 2007) (Tabla 1); se verificaron mediante PCR in silico (Fujita et al. 2010) y las enzimas de restricción se seleccionaron utilizando el programa NEBcutter (Vincze et al. 2003).
Se usó el protocolo de RFLPs propuesto por Verde et al. (2011). Las regiones seleccionadas se amplificaron mediante la reacción en cadena de la polimerasa (PCR) para las secuencias genéticas que contenían los SNPs rs680244 y rs6801272 (Tabla 1); los productos de amplificación se visualizaron mediante una lámpara de luz ultravioleta, tras su separación electroforética en gel de agarosa al 2% y tinción con bromuro de etidio. Posteriormente se sometieron los amplificados a digestión usando las enzimas SFaNI y HindIII respectivamente; finalmente, se resolvieron los genotipos en geles de agarosa al 2%; este proceso se repitió en aproximadamente el 20% de las muestras y se usaron controles negativos de extracción de ADN y PCR.
Análisis Estadístico
Análisis de datos no genéticos.
Entre los fumadores y exfumadores seleccionados previamente se calculó la proporción de sexos, la media y la desviación estándar para la cantidad de cigarrillos consumidos por día y la edad de inicio; adicionalmente se calculó mediante un Ji cuadrado la significancia para la proporción de sexos en fumadores y exfumadores con un nivel de confianza del 95%.
Análisis de datos genéticos.
Para el SNP rs680244 se calculó el equilibrio de Hardy Weinberg, las frecuencias alélicas y genotípicas mediante el software GENEPOP (Rousset 1995); se realizó un test de asociación alélica y genotípica calculando los OR, con intervalos de confianza del 95% y valores p (Cerda et al. 2013) para los grupos de fumadores vs exfumadores, fumadores vs controles de fumadores y exfumadores vs controles de exfumadores. Además, se evaluó la correlación con el número de cigarrillos por día y la edad de inicio mediante el software PLIK (Purcell et al. 2007)
RESULTADOS
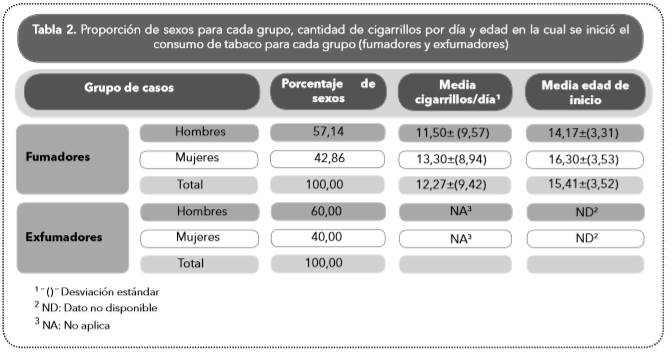
Mediante los análisis no genéticos no se observaron diferencias significativas en las proporciones de hombres y mujeres fumadores y exfumadores (p= 0,73); tampoco se determinaron diferencias entre sexos en relación con la cantidad de cigarrillos y la edad de inicio (Tabla 2).
Tabla 2 Proporción de sexos para cada grupo, cantidad de cigarrillos por día y edad en la cual se inició el consumo de tabaco para cada grupo (fumadores y exfumadores)
En cuanto a los resultados obtenidos para el SNP rs6801272 ubicado en el gen CYP2A6, la genotipificación de 110 individuos (30 fumadores, 33 exfumadores y 47 controles) evidenció, en todas las muestras analizadas, una banda de 587 pb correspondiente al genotipo TT; al establecer la homogeneidad genotípica en el 40% de las muestras se concluyó que el locus es monomórfico, por lo cual no se continuo con la genotipificación.
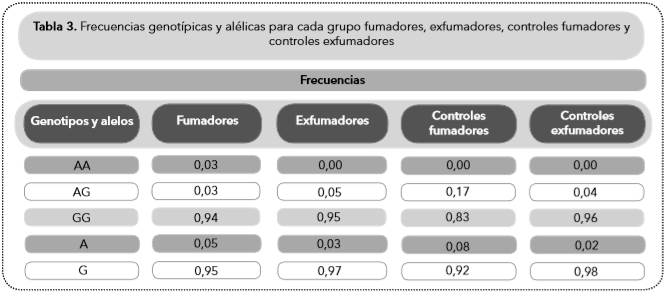
Para el SNP rs680244 se genotipificaron 183 individuos (33 fumadores, 57 exfumadores, 42 controles de fumadores, 51 controles de exfumadores) y se encontraron tres genotipos: AA, AG y GG; posteriormente se calculó la frecuencia alélica y genotípica en cada grupo. Se observó una mayor frecuencia del alelo A en fumadores y la presencia del genotipo AA solo en un individuo del grupo de fumadores (Tabla 3).
Tabla 3 Frecuencias genotípicas y alélicas para cada grupo fumadores, exfumadores, controles fumadores y controles exfumadores
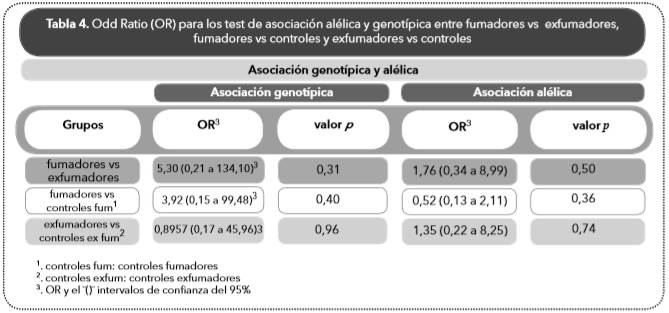
Al realizar los análisis genético−poblacionales, se encontró equilibrio de Hardy Weinberg para todos los datos con excepción de la categoría ‘casos fumadores´ (datos no mostrados). La revisión de la distribución de genotipos en función de las frecuencias alélicas demostró que si bien no se esperaba un genotipo homocigótico, dada la baja frecuencia del alelo de riesgo (0,05), este si fue detectado en este grupo. Al realizar el test de asociación genotípica y alélica no se obtuvieron resultados significativos para ninguna de las comparaciones entre fumadores, exfumadores y los respectivos controles (Tabla 4); también se encontró que no existe una correlación entre dicha variante y la cantidad de cigarrillos consumidos o la edad de inicio, ya que los coeficientes de determinación fueron 0,00 (p = 0,86) y 0,02 (p = 0,50) respectivamente.
DISCUSIÓN
No se encontró una diferencia significativa en la proporción de sexos en fumadores y exfumadores; la OMS (2010), durante un estudio realizado en 150 países, estableció que la proporción de sexos, aunque en la mitad de los países era de 40% hombres y 9% mujeres; en el otro 50% la diferencia no era significativa. Sumado a lo anterior, al compararse el porcentaje de fumadores habituales en la muestra de la población de Itagüí (15,96%), con los datos registrados por la OMS (2017) para diferentes países, encontramos que este valor es alto en relación con otros países, indicando una alta prevalencia del consumo de tabaco.
Dado que se ha establecido que la población de estudio presenta un 70% de ancestría europea (Duque et al. 2012), se esperaba encontrar para el SNP rs6801272 ambos alelos. Sin embargo, para América, el proyecto 1000 genomas registra una frecuencia del alelo T del 0,0072 (NCBI 2014), lo cual es congruente con los resultados de este estudio. La ausencia del alelo T pudo originarse por un efecto fundador ya que la población de Antioquia fue establecida por europeos, africanos y amerindios (Duque et al. 2012). Por otra parte, según Keyeux et al. (2000), los grupos indígenas son, desde el punto de vista genético, muy homogéneos o monomórficos, en relación con otras poblaciones, lo cual puede estar también reflejándose en estos hallazgos.
El alelo presente en la población de Itagüí codifica una enzima que procesa la nicotina más rápido en relación con la enzima en presencia del alelo A, que conlleva a un cambio aminoacídico de Leu por His en la posición 160, resultando en la inactividad enzimática; por tanto, los individuos podrían categorizarse como metabolizadores normales, es decir, los individuos con el genotipo GG procesan la nicotina más rápido respecto a los individuos que poseen el alelo A, así, la sensación producida por un cigarrillo es menos duradera comparada con los individuos que presentan el alelo mutante; se podría concluir que el genotipo GG, hallado en la población, conlleva a un consumo mayor de cigarrillos, según Osorio (2010) y Raunio (2001).
En cuanto al rs680244 se observó que aun cuando los intervalos de los OR no son significativos estos se encuentran más distribuidos hacia la derecha, indicando una posible asociación que no fue detectada en este estudio; es posible que al evaluarlo junto con otras variantes genéticas y no genéticas se modifique este resultado.
También se observó que la frecuencia del alelo A es más alta en fumadores que en el resto de grupos, siendo esto consistente con los estudios de Cerda et al (2013) y Chen y Bierut (2013) donde se relaciona el alelo A con una disminución en la probabilidad de abandono, debido a que incrementa el síndrome de abstinencia; no obstante, la frecuencia encontrada para este alelo es menor que la registrada para población hispana (0,26) (Ning et al. 2001) y para América (0,22) de acuerdo con el estudio de los 1000 genomas (NCBI 2014).
Es de resaltar que aun cuando el grupo de fumadores se encuentra fuera del equilibrio de Hardy Weinberg, el valor p es 0,045. Dicho resultado se debe al individuo homocigótico observado; aunque ante frecuencias alélicas bajas, como en este caso, se espera que el alelo se encuentre en forma heterocigótica (Kalmes y Huret 2001), esta única observación es insuficiente para determinar la asociación ya que las pruebas de ji cuadrado y exacta de fisher se ven afectadas por el número de observaciones según Pértega y Pita (2004), lo que explicaría la no obtención de diferencias entre los grupos de estudio.
Dado que las frecuencias para el SNP rs680244 son diferentes a las registradas por otros estudios, lo que puede deberse a que la muestra en este trabajo no fue tomada al azar si no bajo los criterios anteriormente expuestos, logrando modificar la distribución de los genotipos y alelos (Hedrick 2011).
Para futuras investigaciones se recomienda incluir la interacción con otros genes ya que una de las limitaciones de este estudio fue la cantidad de mutaciones que se pudieron evaluar; en fenotipos complejos pueden estar interactuando múltiples genes. Un gen que podría ser incluido sería SLC6A4 que codifica una proteína de membrana llamada DAT lo cual podría revelar si la variante evaluada en conjunto con otros genes está involucrada en el hábito de fumar (Pombo 2014, Schellekens 2012, Watanabe 2011).
CONCLUSIONES
Los resultados obtenidos permiten concluir que no existe diferencia en la proporción de hombres y mujeres que fuman o que abandonan el cigarrillo; además, se detectó un elevado consumo de cigarrillos en la población por lo cual es pertinente continuar realizando estudios de este tipo.
Adicionalmente, considerando los hallazgos para el SNP rs680244, se puede concluir que aun cuando los OR obtenidos no son significativos, aumentar el tamaño de la muestra y adicionar otros genes permitiría evaluar nuevas interacciones del gen CHRNA5 relacionadas con el hábito de fumar.