INTRODUCCIÓN
El aumento de las actividades agropecuarias y de zonas urbanas afectan directamente los ecosistemas riparios y acuáticos de Colombia y el mundo (Carvajal-Cogollo, 2008; Valdés, 2011). Esta intervención humana en el paisaje natural ha producido fenómenos como la degradación progresiva del hábitat, generando fragmentos de vegetación nativa rodeada de nuevos tipos de ambientes como cultivos, en un proceso conocido como fragmentación del ecosistema (Montenegro, 2009; Valdés, 2011; Williams-Linera, Manson, y Isunza, 2002). En los ecosistemas riparios y acuáticos, el proceso de fragmentación ha causado la pérdida de vegetación ribereña y cambios en la composición de macrófitas, alterando la entrada de energía alóctona al ecosistema acuático (Moulton, 2006; Neres-Lima et al, 2017). De manera similar, este proceso tiene un efecto particular en las áreas del bosque seco tropical (BST), afectadas por su importancia agrícola, a consecuencia de sus suelos llenos de nutrientes, causando su fragmentación, reducción y desertificación (Miles et al, 2006). Finalmente, este proceso de fragmentación ha impulsado la reducción en las áreas de BST en Colombia, que actualmente ocupan menos de 85.000 km2, cerca del 8% del territorio del país y menos del 10% de su área potencial (Gómez, Moreno, Andrade, y Rueda, 2016; Pizano y Garcia, 2014).
Al mismo tiempo, el proceso de fragmentación ha provocado alteraciones en los ambientes dulceacuícolas, promoviendo el cambio en la diversidad de macroinvertebrados y la capacidad de recuperación del hábitat (Feld et al, 2016; Firmiano et al, 2017). Esta modificación de la diversidad de los macroinvertebrados se relaciona con alteraciones en los procesos ecosistémicos como el mantenimiento de la energía de las redes alimentarias en los entornos acuáticos y riparios (Hepp y Santos, 2009; Johnson, Jin, Carreiro, y Jack, 2013). El orden Odonata está altamente implicado en este proceso energético, ya que algunas especies son muy dependientes de las condiciones ecológicas de las áreas acuáticas y las poblaciones de otros macroinvertebrados, lo que nos permite usarlo como medio para comprender los cambios que ocurren dentro de los ecosistemas acuáticos y riparios (Benke, Huryn, Smock, y Wallace, 1999; Corbet, 2004). De esta manera, la diversidad y la composición de odonatos pueden emplearse como indicadores del grado de perturbación en los ecosistemas acuáticos y riparios afectados por la fragmentación y la influencia antropogénica (Monteiro-Júnior, Couceiro, Hamada, y Juen, 2013). En los últimos años, muchos investigadores han promovido el uso de odonatos como indicadores de perturbaciones ambientales, especialmente en el Neotrópico (Monteiro-Júnior et al, 2013; Silva, De Marco, y Resende, 2010; Tognelli, Lasso, Bota-Sierra, Jiménez-Segura, y Cox, 2016). No obstante, en Colombia las investigaciones sobre Odonata se han centrado en estudios taxonómicos extensos, y aún faltan investigaciones que promuevan a los odonatos como una herramienta en la restauración y conservación ambiental (McGeogh, 1997; Palacino-Rodríguez, 2016).
En efecto, comprender los cambios en la biodiversidad ayuda a inferir el proceso de fragmentación y el grado de perturbación antropogénica dentro de los ecosistemas riparios y acuáticos, especialmente en zonas amenazadas como el BST. Por lo tanto, el objetivo de este artículo fue observar los cambios en la diversidad y la composición de Odonata en áreas con diferentes tipos de vegetación riparia, en cuatro periodos de un año, a lo largo de un arroyo ubicado en un remanente de BST en Paicol, Huila (Colombia). Además, se planteó la hipótesis de que existen diferencias significativas en la diversidad y la composición de Odonata, y que estas se relacionan con las diferencias en la vegetación riparia a lo largo del arroyo y los períodos de muestreo que corresponden a las temporadas de lluvia y sequía.
MATERIALES Y METODOS
Área de estudio
Los odonatos se muestrearon a lo largo del arroyo “La Avería”, localizado en el municipio de Paicol, departamento de Huila, Colombia. Paicol presenta una temperatura promedio de 27 °C, la precipitación media anual es de 1820 mm, con una estación seca entre los meses de marzo y agosto, y una estación húmeda comprendida entre septiembre y febrero (Instituto de Hidrología, Meteorología y Estudios Ambientales [IDEAM], 2016). El arroyo tiene una longitud total de 5 km aproximadamente, el flujo de agua nace dentro de un remanente conservado de BST y posteriormente cruza áreas donde el bosque seco ha sido perturbado por actividades humanas como los cultivos de arroz o la ganadería, para finalmente desembocar en el río Páez (Figura 1).
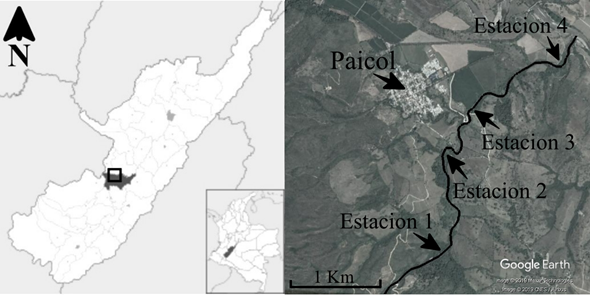
Figura 1 Área de estudio en el departamento del Huila, Colombia. Ubicación de las estaciones de muestreo en el arroyo La Avería.
Se definieron cuatro estaciones de muestreo a lo largo del arroyo separadas por una distancia de aproximadamente un km entre cada estación de muestreo. Se caracterizó la cubierta del dosel adyacente al arroyo con un muestreo e identificación de la vegetación utilizando la información taxonómica de Vargas (2015). La zona alta está cubierta por bosque nativo (Estación 1: 2°26'22,3''N y 75°46'31,4''W ± 822 m s. n. m.) correspondiente a parches preservados de BST interconectados entre ellos. La vegetación riparia en esta estación estuvo compuesta por grandes árboles y arbustos, entre lo que dominan: Clavija sp., Guadua angustifolia, Guarea guidonia, Machaerium capote, Pseudosamanea guachapele y Renealmia sp. La segunda estación de muestreo es una combinación de parches interconectados de bosque nativo y amplias áreas de cría de ganado (Estación 2: 2°26'51,2''N y 75°46'11,3''W ± 819 m s. n. m.); la vegetación a las orillas del arroyo consistió en una mezcla de diferentes plantas como Adiantum sp., Carludovica palmata, Cenchrus clandestinus y Selaginella sp. La tercera estación estaba dominada por arrozales a lo largo del arroyo, además de ser una zona de vertimientos de aguas residuales provenientes del centro urbano cercano (Estación 3: 2°26'31,8''N y 75°46'5,9''W ± 813 m s. n. m.). Esta estación presenta vegetación ribereña dominada por Cecropia sp., Piper spp. y macrófitas como Spathiphyllum sp. acompañando los arrozales. En la parte baja del arroyo, la última estación estuvo compuesta por áreas de cría de ganado bovino (Estación 4: 2°26'57,2''N y 75° 45'24,6''W ± 805 m s. n. m.) con campos de hierba de C. clandestinus y macrófitas como Cyperus sp. que fueron abundantes en toda la estación.
Muestreo
Se realizaron muestreos durante febrero, mayo, agosto y noviembre de 2016, para cubrir todo el ciclo de lluvias del área de estudio. Se midieron: conductividad (μs cm-1), oxígeno disuelto (mg L-1), sólidos suspendidos totales (mg L-1), pH, temperatura (°C) y caudal (m3 s-1), utilizando una sonda multiparamétrica marca HANNA®. Además, se determinaron las concentraciones (mg L-1) de amonio (NH4 +), nitrato (NO3 -) y fosfato (PO4 -3) mediante el análisis colorimétrico propuesto por API Freshwater Master Test Kit. Todas las variables fisicoquímicas e hidrológicas se midieron in situ tres veces por período de muestreo en cada punto de muestreo.
En cada estación se capturaron odonatos adultos por medio de redes entomológicas, en tres transectos lineales de 50 m, perpendiculares al arroyo. Por otro lado, se recolectaron larvas en etapas cercanas a la emergencia, para facilitar su posterior identificación, utilizando una D-net encerrada por un cilindro (diámetro 0,55 m) en 10 ubicaciones adyacentes a las macrófitas del arroyo, a 0,3 m de profundidad en tres transectos de 50 m en cada estación de muestreo por periodo de muestreo. El proceso de recolecta presentó un esfuerzo de muestreo de 90 min, para larvas y adultos por separado, para cada estación durante cada período de muestreo, eligiendo el momento con la mayor luz solar en el día. Consecutivamente, los organismos se identificaron taxonómicamente a nivel de especie, utilizando las claves disponibles para adultos (De Marmels, 2012; Garrison, 1994; Garrison y Ellenrieder, 2015; Garrison, Ellenrieder, y Louton, 2006; Leonard, 1977; May, 1998; Meurgey y Poiron, 2011; Ris, 1930; von Ellenrieder, 2003; Walker, 2015) y larvas (Belle, 1996; Limongi S, 1983; Novelo-Gutierrez, 2002; Novelo-Gutiérrez, 2005; Zloty, Pritchard, y Esquivel, 1993). Las identificaciones fueron corroboradas y verificadas por especialistas del orden Odonata, del grupo LAZOEA de la Universidad de los Andes, Bogotá-Colombia. Por último, los especímenes recolectados fueron dispuestos en el Museo La Salle en Bogotá, Colombia.
Análisis estadístico
Para definir cambios significativos en los datos fisicoquímicos, a lo largo de las estaciones y los periodos de muestreo, se utilizó un ANOVA (p < 0.05). Se calcularon las curvas de rango-abundancia de los organismos por estación y periodo de muestreo. Adicionalmente, con el software EstimateS Win v9.1 (Colwell et al, 2012) se estimó si el esfuerzo de muestreo fue efectivo utilizando una curva de rarefacción con la riqueza estimada, el estimador Jacknife de primer orden y el índice Estimador basado en la Cobertura de Abundancia (ACE); en este último índice se consideraron como especies raras a aquellas especies con cinco o menos individuos. Estos índices se usaron porque presentaron el estimador más preciso y menos sesgado en una comparación de varios procedimientos (Palmer, 1990). Posteriormente, se calculó la diversidad α, agregando adultos y larvas, por estación de muestreo y tiempo, utilizando el índice diversidad de Shannon-Wiener (H') en el programa PAST v3.14 (Hammer, Harper, y Ryan, 2001). Además de utilizar un ANOVA (p < 0.05) para encontrar diferencias significativas en la diversidad de los insectos de acuerdo con la estación y periodo de muestreo. Finalmente, para determinar la diversidad β entre la estación de muestreo y el tiempo, se usó un análisis de similitud y dendrogramas, a partir del índice de Jaccard, utilizando el algoritmo paired-group (Jackson y Somers, 1989).
Tabla 1 Lista de todas las especies de Odonata recolectadas en cada estación y mes de muestreo
| Especie | Adultos | Larvas | Estación | Mes |
|---|---|---|---|---|
| Aeshnidae | ||||
| Coryphaeschna viriditas Calvert, 1952 | 0 | 1 | 2 | Nov |
| Calopterygidae | ||||
| Hetaerina caja Drury, 1773 | 11 | 0 | 2, 4 | May, Nov |
| Hetaerina occisa Selys, 1853 | 26 | 19 | Todas | Todos |
| Coenagrionidae | ||||
| Acanthagrion kennedii Williamson, 1916 | 15 | 1 | 2, 3, 4 | Todos |
| Argia cupraurea Calvert, 1901 | 3 | 0 | 2 | May |
| Argia fissa Selys, 1865 | 1 | 0 | 1 | Ago |
| Argia oculata Selys, 1865 | 43 | 3 | Todas | Todos |
| Enallagma novaehispaniae Calvert, 1907 | 32 | 35 | 2, 3, 4 | Todos |
| Libellulidae | ||||
| Dythemis nigraMeurgey & Poiron, 2011 | 4 | 4 | Todas | Todos |
| Elasmothemis cannacrioides Calvert, 1906 | 0 | 3 | 2 | Feb, May |
| Erythrodiplax castanea Burmeister, 1839 | 11 | 2 | 3, 4 | Todos |
| Elga leptostyla Ris, 1909 | 0 | 3 | 1, 2 | Feb, Nov |
| Libellula herculea Karsh, 1889 | 1 | 1 | 1 | May, Nov |
| Macrothemis hemichlora Burmeister, 1839 | 5 | 23 | Todas | Todos |
| Perithemis mooma Kirby, 1889 | 16 | 5 | 2, 3, 4 | Todos |
| Gomphidae | ||||
| Erpetogomphus sabaleticus Williamson, 1918 | 0 | 4 | 1 | Todos |
| Total | 168 | 104 |
RESULTADOS
Se capturaron 272 especímenes, 168 adultos y 104 larvas, comprendidos en cinco familias y 16 especies en toda el área de estudio durante el año de recolección (Tabla 1). La curva de rango-abundancia mostró que la Estación 1 tuvo la menor abundancia de individuos (10 adultos y 10 larvas), mientras que la Estación 4 presentó la mayor abundancia de individuos con 82 adultos y 44 larvas; la Estación 2 exhibió la mayor riqueza, con 12 especies (Figura 2A). La mayoría de los individuos de Odonata fueron recolectados al comienzo de la estación húmeda, al igual que la mayor riqueza de especies se observó durante la época de noviembre a febrero (Figura 2B). Las especies más abundantes fueron Enallagma novaehispaniae (Calvert, 1907) con 67 individuos (32 adultos y 35 larvas) y Argia oculata (Selys, 1865) con 46 individuos (43 adultos y 35 larvas). Se considera que el esfuerzo de muestreo fue suficiente debido a que las curvas de acumulación de especies casi alcanzaron las asíntotas con los estimadores (Figura 3). Sin embargo, estas curvas de acumulación indican que, aun así, es posible encontrar algunas especies de Odonata que no fueron recolectadas en nuestro período de muestreo.
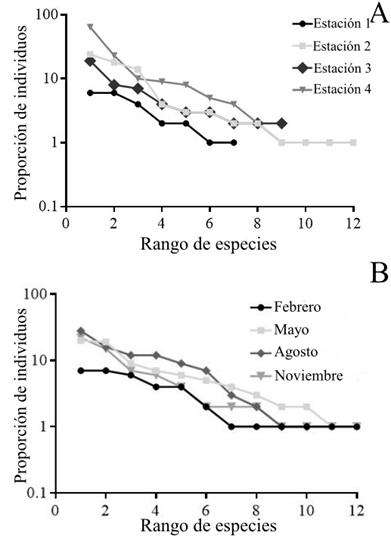
Figura 2 Abundancia de Odonata en cada Estación (A) y periodos (B) de muestreo en el arroyo La Avería en Paicol (Huila-Colombia).
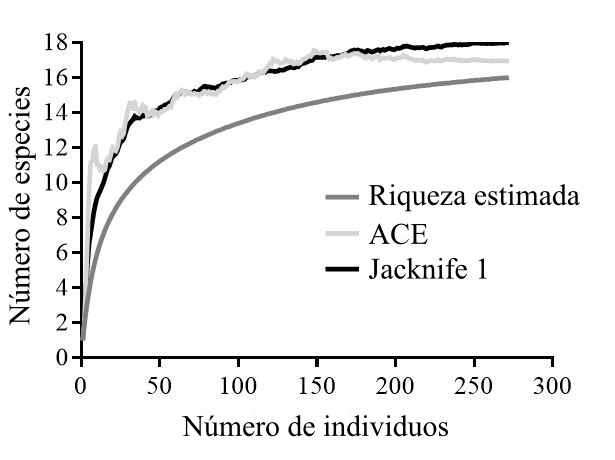
Figura 3 Curvas de acumulación de especies de Odonata en el arroyo La Avería, en Paicol (Huila-Colombia). Para el índice ACE se consideraron como especies raras aquellas con 5 o menos individuos recolectados.
El ANOVA (p < 0,05; F = 0,44) no mostró diferencias significativas en el índice de diversidad de Shannon-Wiener entre estaciones de muestreo y períodos. Sin embargo, la Estación 2 y el mes de febrero registraron la mayor diversidad durante todo el año de muestreo (Figura 4). Por otro lado, el índice de similitud de Jaccard expuso que las estaciones y períodos de muestreo no comparten las mismas especies, por lo que existen diferencias en la composición de especies de Odonata en cada estación y período de muestreo (Figura 5).
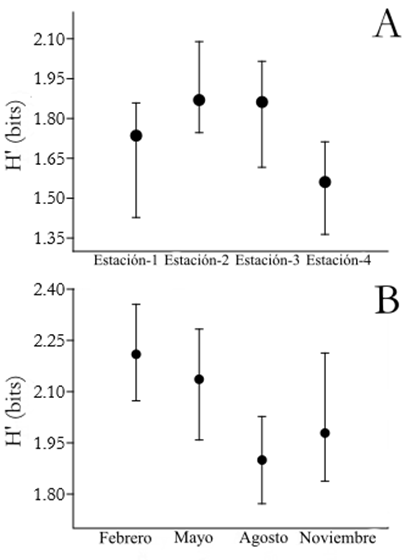
Figura 4 Variación en el índice de diversidad Shannon-Wiener (H') con el error estándar para los odonatos colectados, tanto adultos como larvas, por Estación (A) y periodo de muestreo (B).
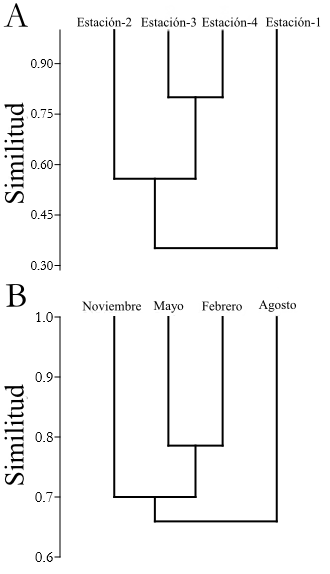
Figura 5 Especies de Odonata, tanto adultos como larvas, definidos de acuerdo a grupos de similitud por medio del índice de Jaccard y el algoritmo paired-group, entre las estaciones (A) y los períodos de muestreo (B).
Finalmente, se encontró una variación significativa en la conductividad y la concentración de nutrientes (NH4 + y NO3 -) (p < 0,05; F = 1,65) a lo largo del arroyo. Se observó un aumento de casi diez veces en la conductividad que cambió de 14 μs cm-1 en la Estación 1 a 144 μs cm-1 en la Estación 4 (Tabla 2). Los nutrientes también aumentaron: el amonio (NH4 +) aumentó de 0,06 a 0,31 mg dm-3, de la Estación 1 a la Estación 3 y el nitrato (NO3 -) aumentó de 0 a 10 mg L-1, a la Estación 4 (Tabla 2). En contraste, el fosfato (PO4 -3) no mostró diferencias significativas entre las estaciones de muestreo. Simultáneamente, las características fisicoquímicas variaron con el tiempo, el pH y la temperatura, mostrando diferencias significativas a lo largo del año (p < 0,05; F = 2,35). La temperatura cambió de un valor medio de 24,3 °C en la estación húmeda, a un máximo valor de 28,37 °C registrado en la estación seca, y el pH osciló entre 7,73 y 10,01, entre la estación seca y la lluviosa (Tabla 2).
Tabla 2 Promedio () y desviación estándar (SD) de los datos fisicoquímicos presentes en cada estación de muestreo (estación 1=áreas conservadas; estación 2, 3 y 4=áreas perturbadas) y tiempo, en el arroyo La Avería en Paicol (Huila). Tamaño de muestra (N) = 16
| Estación 1 | Estación 2 | Estación 3 | Estación 4 | Febrero | Mayo | Agosto | Noviembre | |||||||||
| Parámetro | | SD | | SD | | SD | | SD | | SD | | SD | | SD | | SD |
| Conductividad (µs cm-1) | 14 | 28 | 85.25 | 62.33 | 114.75 | 47.39 | 144 | 58.84 | 107 | 103.35 | 52.75 | 37.41 | 65.75 | 49.92 | 132.5 | 53.03 |
| Oxígeno disuelto (mg L-1) | 7.24 | 0.2 | 7.88 | 0.3 | 18.32 | 2.1 | 7.17 | 0.71 | 6.02 | 3.04 | 6.78 | 0.9 | 6.73 | 1.28 | 7.35 | 0.87 |
| SST (mg L-1) | 7 | 14 | 40 | 26.27 | 230 | 23.85 | 71.5 | 28.9 | 53.25 | 51.19 | 26.25 | 18.55 | 32.75 | 24.97 | 63.75 | 24.01 |
| pH | 6.98 | 0.49 | 7.59 | 1.13 | 31.12 | 1.52 | 7.63 | 1.29 | 7.55 | 0.14 | 6.74 | 0.38 | 6.77 | 0.4 | 8.92 | 1.24 |
| Temperatura (°C) | 24.82 | 0.86 | 25.38 | 1.13 | 103.27 | 2.1 | 25.1 | 1.2 | 26.71 | 1.26 | 23.85 | 0.26 | 24.6 | 0.22 | 25.95 | 0.51 |
| Caudal (m3 s-1) | 0.39 | 0.23 | 1.04 | 0.3 | 3.1 | 0.34 | 1.16 | 0.75 | 0.41 | 0.18 | 0.78 | 0.43 | 1.01 | 0.04 | 1.17 | 0.77 |
| NH4 + (mg L-1) | 0.06 | 0.13 | 0.19 | 0.13 | 12.5 | 1.75 | 0.31 | 0.13 | 1.19 | 1.89 | 1.06 | 1.96 | 1.13 | 1.92 | 0.31 | 0.13 |
| NO3 - (mg L-1) | 0 | 0 | 1.25 | 2.5 | 5 | 2.5 | 10 | 7.07 | 2.5 | 2.89 | 6.25 | 9.46 | 2.5 | 5 | 1.25 | 2.5 |
| PO4 -3 (mg L-1) | 0.13 | 0.25 | 0.25 | 0 | 2.75 | 0.38 | 1.31 | 0.85 | 0.94 | 0.77 | 0.56 | 0.52 | 0.69 | 0.9 | 0.19 | 0.13 |
DISCUSIÓN
La diversidad de los odonatos no cambió significativamente a lo largo de las estaciones ni los periodos de muestreo. Esto es causado por la alta tasa de dispersión y la movilidad en odonatos adultos que generan que las especies compartan diferentes puntos de muestreo (Altamiranda, 2009; Collins y McIntyre, 2015). Del mismo modo, el orden Odonata, tanto larvas como adultos, es un grupo de insectos que no tiene necesidad trófica directa por las macrófitas y plantas ribereñas, por lo que la estructura vegetal riparia no afecta significativamente la distribución de muchas especies de Odonata (Garzón y Realpe, 2009; González-Soriano, Noguera, Zaragoza-Caballero, y Ramírez-García, 2009). No obstante, observamos valores de diversidad más altos en la Estación 2 y la Estación 3, lo que concuerda con otras investigaciones en Colombia y en los trópicos, donde se registra una mayor diversidad de Odonata vinculada con la intervención antrópica (Altamiranda, 2009; Hernandez, Reece, y McIntyre, 2006; Novelo-Gutiérrez y Gómez-Anaya, 2009; Urrutia, 2005). Los valores más altos de diversidad de Odonata en entornos perturbados se asocian con una mayor abundancia de macrófitas, que proporcionan hábitats para la alimentación y la reproducción en especies con alta capacidad de dispersión y bajos requisitos ecológicos (Brix, 1997; Hernandez et al, 2006; Miserendino y Masi, 2010; Perron y Pick, 2019). En un caso similar, se registran los datos de diversidad más altos durante la estación húmeda (febrero). Estos valores de mayor diversidad están relacionados con la abundante oferta de hábitats y presas, como mosquitos y moscas, causados por más precipitaciones durante la temporada de lluvias (Ball-Damerow, M’Gonigle, y Resh, 2014; Janzen y Schoener, 1968; Vilela, Guillermo-Ferreira, y Del-Claro, 2016). Finalmente, se podría inferir que los parches de bosque de la zona estudiada son demasiado pequeños para albergar una comunidad madura de odonatos. Por esa razón, se recomienda extender el área y tiempo de muestreo en futuras investigaciones.
Se encontraron diferencias en la composición de Odonata entre estaciones y períodos de muestreo. Estos cambios se producen por el reemplazo vegetal en el bosque ripario nativo hacia sistemas de cultivos, arbustos y macrófitas, como se detalla a lo largo del arroyo (Monteiro-Júnior et al, 2013). Hay especies de Odonata adaptadas a áreas perturbadas (cultivos de arroz y áreas de ganado), como es el caso de Acanthagrion kennedii, Enallagma novaehispaniae, Erythrodiplax castanea, Hetaerina caja y Perithemis mooma, especies que prefieren áreas abiertas con una alta densidad de macrófitas, una característica registrada solo en las partes bajas del sistema lótico (Estaciones 3 y 4) (Altamiranda, 2009; Monteiro-Júnior et al, 2013; Rache-Rodríguez, 2015; Suhonen, Korkeamäki, Salmela, y Kuitunen, 2014). De igual manera, hubo cuatro especies que se encontramos a lo largo de todo el arroyo: Argia oculata, Dythemis nigra, Hetaerina occisa y Macrothemis hemichlora. Estas especies se caracterizan por una alta movilidad y ausencia de preferencias por el tipo de vegetación (Altamiranda, 2009; Renner, Périco, Schmidt-Dalzochio, y Sahlen, 2018; Simaika, Samways, y Frenzel, 2016).
Con respecto a los cambios significativos en las variables fisicoquímicas a lo largo del arroyo, se observó la influencia de los cultivos de arroz y el vertimiento de residuos urbanos en la Estación 3, que promueven el aumento de las variables de conductividad y nutrientes, especialmente amonio y nitrato (García-Velázquez y Gallardo, 2017; Ometo et al, 2000). Esta alteración en las características del agua podría estar relacionada con cambios en la distribución de macrófitas y la diversidad de larvas de Odonata a lo largo del arroyo (Brix, 1997; Kasangaki, Chapman, y Balirwa, 2008; Perron y Pick, 2019); sin embargo, en este estudio no se obtuvieron datos suficientes para explicar esta correlación.
En conclusión, dados los cambios en la riqueza y abundancia de Odonata entre estaciones de muestreo y períodos, se acepta en parte la hipótesis previamente planteada Estos cambios están causados por el cambio en la cobertura vegetal riparia que promueven la presencia de diferentes especies de Odonata a lo largo del arroyo. No obstante, la diversidad de Odonata no cambia a lo largo del arroyo, debido a que estos requisitos ecológicos no son tan relevantes en la distribución de estos insectos. Finalmente, consideramos este estudio como un paso preliminar para una mayor valoración ecológica en los ecosistemas acuáticos de Colombia, especialmente en las regiones BST donde el ecosistema ripario se ha estado fragmentado. Estos resultados resaltan la necesidad de más estudios de Odonata en los parches remanentes de BST en Huila y en Colombia.














