Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Caldasia
Print version ISSN 0366-5232On-line version ISSN 2357-3759
Caldasia vol.29 no.1 Bogotá Jan./June 2007
ESTUDIO DE LA VARIACIÓN MORFOLÓGICA DEL GONOPODO DE STRENGERIANA MANIFORMIS (BRACHYURA: PSEUDOTHELPHUSIDAE) MEDIANTE APLICACIÓN DE MORFOMETRÍA GEOMÉTRICA
Study of morphological variation of the gonopod of Strengeriana maniformis (Brachyura: Pseudothelphusidae) based on the application of geometric morphometry
MANUEL PEDRAZA
MARTHA R. CAMPOS
Universidad Nacional de Colombia, Departamento de Biología, mepedraza@unal.edu.co
Instituto de Ciencias Naturales, Universidad Nacional de Colombia, Apartado 7495, Bogotá, D.C., Colombia. mhrochad@unal.edu.co
RESUMEN
Se utiliza la morfometría geométrica para determinar la variación morfológica del primer gonopodo del macho en especímenes de Strengeriana maniformis. Se examinaron 35 machos de la colección de Crustáceos del Instituto de Ciencias Naturales y 9 machos de la colección del Museo de la Salle. El estudio morfométrico se centró en el ápice y el proceso mesial del gonopodo izquierdo; en su desarrollo se utilizaron algunos de los programas de la serie TPS: tpsUtil, tpsDig, tpsRelw, tpsRegr y el Palaeontological Statistics software package (PAST). El análisis permitió determinar que la parte más variable del gonopodo corresponde al proceso mesial, y la menos variable a la porción distal del lóbulo mesial. Se estableció que la variación en la forma del gonopodo es independiente del tamaño del espécimen y de la población a la cual pertenece. Se pudo descartar que la contaminación con metales pesados sea el agente causante de la variación.
Palabras clave. Cangrejos de agua dulce, gonopodo, morfometría geométrica.
ABSTRACT
In this paper geometric morphometry is used to determine the morphological variation of the male’s first gonopod in specimens of Strengeriana maniformis. 35 males from the Crustacean collection of the Instituto de Ciencias Naturales and 9 males of the Museum La Salle collection were examined. The morphometric study was centered in the apex and the mesial process of the left first gonopod using following programs of the TPS series: tpsUtil, tpsDig, tpsRelw, tpsRegr and the Palaeontological Statistics software package (PAST). The analysis allowed us to determine that the most variable portion of the gonopod corresponds to the mesial process, and the most constant is the distal portion of the mesial lobe. The study established that the morphological variation of the gonopod is independent of the size of the specimen and the population. The hypothesis that contamination with heavy metals causes the variation was rejected.
Key Words. Freshwater crabs, gonopod, geometric morphometry.
INTRODUCCIÓN
El primer par de gonopodos del macho es una estructura esencial para la determinación taxonómica de los cangrejos de agua dulce (Smalley 1964). Esta determinación se basa en la forma particular del gonopodo, el cual debe su especificidad a que funciona como un sistema de cerradura/llave en concordancia con la abertura genital de la hembra.
Los registros de variaciones a nivel del gonopodo son escasos. Para algunas especies de Neostrengeria Pretzmann, 1965, se encontraron variaciones morfológicas esencialmente a nivel del lólulo lateral, accesorio o del ápice que estaban definidas por un patrón poblacional (Campos 1994); mientras que en Microthelphusa racenisi Rodríguez, 1966, se lograron establecer cuatro patrones de variación del gonopodo, a nivel del proceso mesial y del canal espermático, los cuales estaban directamente relacionados con el tamaño de los ejemplares (Rodríguez 1982).
Al examinar machos adultos de Strengeriana maniformis Campos & Rodríguez 1993, se observaron variaciones morfológicas en el primer gonopodo, principalmente del proceso mesial, de tal forma que cada espécimen presenta una forma particular. Esto contrasta con los caracteres morfológicos del caparazón, las quelas y los pereopodos que son similares al holotipo.
Strengeriana maniformis se distribuye en la vertiente oriental de la cordillera Central desde Cajamarca, Tolima, que corresponde a la localidad típica, hasta Samaná, Caldas, en un rango altitudinal de 400 a 1750 m (Campos 2005). Muchos de los registros para la especie corresponden a regiones donde históricamente se ha realizado la explotación artesanal de oro, como es el caso del río La Miel en Samaná, Caldas. Con base en el informe del Ministerio del Medio Ambiente (2002), Caldas ocupa el segundo lugar después de Antioquia, con la mayor explotación de oro en Colombia. Esta explotación se caracteriza por ser artesanal, a través de la extracción fluvial. La extracción de oro implica la utilización de grandes cantidades de agua y de metales pesados como el mercurio y el cianuro en los procesos de la recuperación del oro. La aplicación de estos procesos conlleva a la disminución significativa de la calidad del agua en las regiones de explotación, al aumento de la cantidad de cargas orgánicas y químicas, metales pesados, grasas y aceites, que alteran las condiciones fisicoquímicas del agua, lo que repercute en los ecosistemas acuáticos y en la fauna asociada. En el caso del mercurio, se sabe que éste se incorpora a las fuentes de agua efectuando su bioacumulación en los organismos.
Algunos organismos, como los peces, poseen cierto grado de plasticidad fenotípica que les permite responder a los cambios ocurridos en el ambiente en el cual se desarrollan (O’ Reilly & Horn 2004). En nuestro caso, la contaminación con metales pesados del habitat natural de los cangrejos de la especie en estudio y los procesos subyacentes a esta contaminación, podría ser la causa de la variación morfológica observada en el gonopodo.
La morfometría hace referencia al estudio de la forma y del tamaño, y de como estas dos variables se relacionan entre sí (Astua de Moraes 2003). El desarrollo de las técnicas de captura y procesamiento de las imágenes digitales en las últimas décadas ha permitido estudiar con mayor exactitud la geometría de las estructuras y ha motivado el desarrollo de métodos estadísticos que permiten la combinación de las técnicas de análisis multivariado con métodos de observación directa de las formas biológicas (Cadrin & Fredland 1999).
Los avances de la morfometria geométrica con relación a la morfometria tradicional incluyen, la forma de medir la cantidad de diferencia entre las conformaciones (utilizando distancias procrustes), el desarrollo de métodos estadísticos especializados para el estudio de la conformación, y el desarrollo de nuevas técnicas para la representación gráfica de los resultados (MadlLeod & Forey 2002).
Actualmente, la morfometría es una herramienta utilizada en muchos campos de la investigación biológica, como en la medicina, para el estudio de enfermedades (Ghalaibeh et al. 2000, Singh & Thing 2003); en estudios ecológicos (Burgman et al. 1999, Dayton et al. 2005, Depecker et al. 2006) y en estudios filogenéticos (Dewel 1985, Claude et al. 2003, Manier 2004, Hendry et al. 2005). En crustáceos, Rosemberg (2001) estudió la variación en la forma de los quelipedos en especies de Uca Leach, 1814. Bermúdez (2001) utilizó esta técnica para realizar la caracterización poblacional de dos especies de la familia Galatheidae del caribe colombiano.
En el desarrollo de este trabajo se utilizaron los programas de la serie TPS desarrollados por J. Rohlf, los cuales se encuentran disponibles en: http://www.life.bio.sunysb.edu/morph/index.html. El objetivo central de este trabajo consistió en estudiar la dinámica en la variación del primer gonopodo de la especie Strengeriana maniformis y si esta variación está determinada por la contaminación de su medio natural.
MATERIALES Y MÉTODOS
Material biológico.
El estudio se basó en 44 machos de Strengeriana maniformis, 35 machos pertenecientes a la colección de Crustáceos del Instituto de Ciencias Naturales (ICN-MHN-CR) y 9 machos de la Colección del Museo de La Salle, Bogotá (MLS). Para cada espécimen se registraron la longitud (cl) y el ancho del caparazón (cb), en mm. Se examinaron el caparazón, las quelas y pereopodos de cada uno de los ejemplares a fin de determinar variaciones morfológicas con respecto al holotipo.
Material examinado.
COLOMBIA. Caldas: Manzanares, 1200 m alt., 24 Ene 1997, R. Casallas, 1 macho, cl 10.3 mm, cb 16.6 mm, ICN-MHN-CR 1662.— 1200 m alt., 24 Ene 1997, R. Casallas, 6 machos, el mayor cl 18.2 mm, cb 11.9 mm, el menor cl 13.4 mm, cb 8.6 mm, MLS 251.— Samaná. Km 18.3, carretera a Pensilvania, 1170 m alt., 24 Abr 1994, P. Ruíz, 1 macho, cl 12.0 mm, cb 21.2 mm, ICN-MHN-CR 1346.— Vereda La Miel, quebrada en carretera Cañaveral-Samaná, 600 m alt., 23 Abr 1994, M. R. Campos, 2 machos, cl 12.5 y 8.5 mm, cb 20.5 y 13.8 mm, ICN-MHN-CR 1342.— Vereda La Miel Alta, quebrada en carretera Cañaveral-Samaná, 700 m alt., 22 Abr 1994, M. R. Campos, 2 machos, cl 14.5 y 13.5 mm, cb 23.2 y 22.1 mm, ICN-MHN-CR 1338.— Vereda La Miel Alta, quebrada en carretera Cañaveral-Samaná, 1000 m alt., 21 Abr 1994, M. R. Campos, 10 machos, el mayor cl 14.0 mm, cb 25.4 mm, el menor cl 11.9 mm, cb 19.3 mm, ICN-MHN-CR 1337.— Vereda Marías, 1750 m alt., 23 Abr 1994, M. R. Campos, 1 macho, cl 10.8 mm, cb 18.4 mm, ICN-MHN-CR 1340.— Quebrada afluente del Rió La Miel, 1100 m, 24 May 1995, F. Montoya, 8 machos, el mayor cl 13.6 mm, cb 23.2 mm, el menor cl 9 mm, cb 14.6 mm, ICN-MHN-CR 1649.— Victoria. Vereda Canaan, quebrada en carretera Victoria-Samaná, 1100 m alt., 19 Abr 1994, M. R. Campos, 2 machos, cl 15.6 y 9.1 mm, cb 26.5 y 14.7 mm, ICN-MHN-CR 1333.— Vereda Hamburgo, quebrada en carretera Victoria-Cañaveral, 1100 m alt., 20 Abr 1994, M. R. Campos, 1 macho cl 14.5 mm, cb 23.2 mm, ICN-MHN-CR 1336.— Vereda San Mateo, quebrada en carretera Victoria-Cañaveral, 1050 m alt., 20 Abr 1994, M. R. Campos, 6 machos, el mayor cl 16. mm, cb 27.8 mm, el menor cl 10.2 mm, cb 16.5 ICN-MHN-CR 1335.
Tolima: Cajamarca, caño en carretera central, 1560 m alt., 3 Ago 1988, R. Sánchez, holotipo 1 macho, cl 20.2 mm, cb 32.5 mm, ICN-MHN-CR 0938.— Fresno, 1200 m, 2 May 1997, R. Casallas, 1 macho, cl 13.7 mm, cb 22.2 mm, ICN-MHN-CR 1663.— 1200 m, 2 May 1997, R. Casallas, 3 machos, el mayor cl 14.6 mm, cb 24.6 mm, el menor cl 8.9 mm, cb 10.2 mm, MLS 256.
Imágenes
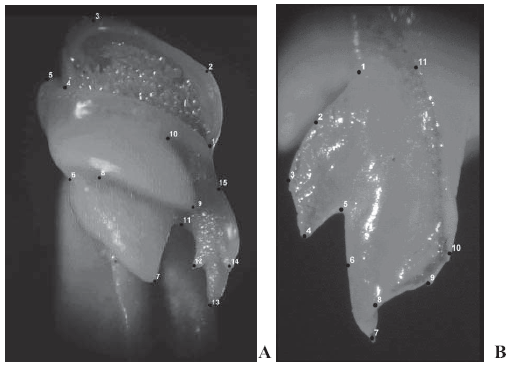
Las imágenes se obtuvieron por medio de fotografía digital. Las fotografías fueron tomadas a través del ocular de un estereoscopio Wild, Modelo 420, con una cámara SONY, DSC-P72. Por convención se utilizó el gonopodo izquierdo. De cada gonopodo se obtuvieron 2 imágenes: el ápice en vista cefálica, con una magnificación de 40x (Fig.1A) y el proceso mesial en vista cefalo-mesial, con una magnificación de 80x (Fig.1B).
Figura 1. Strengeriana maniformis Campos & Rodríguez, 1993. Gonopodo izquierdo, ICN-MHN-CR 1333 (1): A, ápice, vista cefálica; B, proceso mesial, vista cefalo-mesial.
Morfometría geométrica
A partir de las imágenes se seleccionó la ubicación de los puntos anatómicos de referencia (landmarks), teniendo en cuenta que describieran de la manera más precisa la estructura. Se seleccionaron 15 para el ápice (Fig.1A) y 11 para el proceso mesial (Fig.1B).
Para la digitalización de los landmarks se creó un archivo de imágenes con el programa tpsUtil, versión 1.34 (Rohlf 2005a), luego, se utilizó el programa tpsDig2, versión 2.04 (Rohlf 2005b), para ubicar cada uno de los puntos de referencia en las fotografías.
El análisis morfométrico se efectuó con el programa tpsRelw, versión 1.42 (Rohlf 2005c). Las configuraciones, definidas por los landmarks, son estandarizadas a un valor centroide unitario a fin de elimar las diferencias en los tamaños. Los efectos de la orientación son corregidos mediante la óptima superposición de todas las configuraciones, respecto a una de ellas, la cual se toma como referencia (MadlLeod & Forey, 2002).
El análisis generalizado de “procrustes” (GPA), a partir de una configuración consenso, produce un grupo de datos transformados en el que cada espécimen es alineado respecto a una conformación de referencia (MadlLeod & Forey 2002). Las distancias procrustes (la distancia mínima obtenida entre dos configuraciones) definidas por el GPA pertenecen a un espacio multidimensional con distancias geodésicas llamado “espacio de la forma de Kendall” (Rohlf & Slice 1990). Los métodos estadísticos tradicionales (métodos multivariados) presuponen distancias euclidianas. Para poder utilizar éstos métodos, es necesario realizar una proyección del espacio de la forma de Kendall a un espacio lineal tangente con distancias euclidianas (MadlLeod & Forey 2002).
Como resultado del análisis el programa TPS rewl, genera dos matrices una “U”, que contiene los componentes de la variación uniforme y otra matriz “W”, con los componentes de la variación no-uniforme. Estas variables son obtenidas a partir de la proyección tangente de las distancias en el espacio de la forma de Kendall (Rohlf & Slice 1990). El programa también nos permite obtener una matriz llamada “weight matrix” que reune la información de los componentes de conformación uniformes y no-uniformes, la cual se utiliza para realizar el análisis de componentes principales.
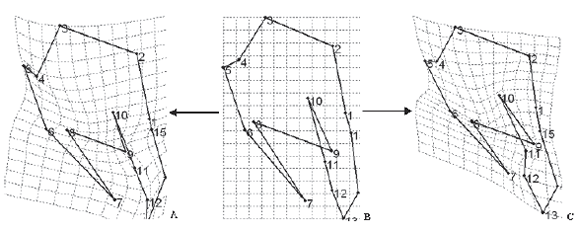
La técnica “torsión de placas delgadas” (Thing-plate splines) (Fig. 2 y Fig. 3), permite la visualización de las deformaciones parciales “partial warps” de los componentes no-uniformes. Esta técnica esta basada en el modelamiento físico de la torsión de una placa de metal, que se supone de un grosor despreciable, y cuantifica la energía que se necesitaría para deformar la placa de tal forma que sus landmarks coincidan con los de la configuración consenso (Bookstein 1991). Las gráficas obtenidas nos permiten identificar las regiones de mayor variación.
Figura 2. Strengeriana maniformis Campos & Rodríguez, 1993. Gonopodo izquierdo, ápice, vista cefálica. Representación gráfica de las deformaciones de los especímenes localizados en los extremos del eje del primer componente principal: A, ICN-MHN-CR 1337 (2); B, Configuración consenso; C, ICN-MHN-CR1346 (1).
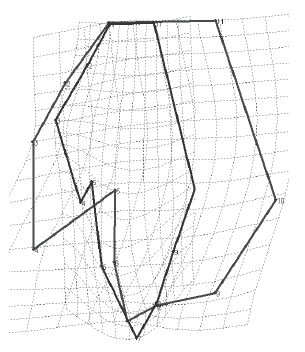
Figura 3. Strengeriana maniformis Campos & Rodríguez, 1993. Gonopodo izquierdo, proceso mesial, vista cefalo-mesial. Representación gráfica de las deformaciones de los especímenes localizados en los extremos del eje del primer componente principal: MLS 251 (6), ICN-MHN-CR1335 (1).
Análisis multivariado
Para la obtención de los componentes principales (CP) se utilizó el programa PAST, versión 1.40 (Hammer et al., 2001). Por medio del análisis de componentes principales (PCA) es posible encontrar nuevas variables ortogonales, sin correlación entre ellas, que explican la máxima variabilidad posible, a partir de un grupo de variables correlacionadas (Harlow 2005). También se analizó, mediante una prueba de regreción con el programa tpsRegr, versión 1.31 (Rohlf 2005d), si la conformación de la estructura del ápice del gonopodo estaba relacionada con su tamaño, es decir si el patrón de crecimiento del gonopodo respecto a la forma es isométrico.
RESULTADOS Y DISCUSIÓN
Análisis de las deformaciones.
La técnica de “torsión de placas delgadas” (Thing-plate splines), nos permitió obtener la representación gráfica de las deformaciones que presenta la configuración consenso, repecto a los especímenes localizados en los extremos del eje del primer componente principal. Por medio del análisis de estas gráficas se pudo determinar de forma cualitativa, como es la dinámica de la variación.
En el ápice, la región que presenta la mayor variación corresponde a la delimitada por los puntos de referencia 8 al 15 (Fig. 2). Esta región involucra dos estructuras, el lóbulo cefálico y el proceso mesial. Para el proceso mesial la variación se presenta tanto en el eje x como en el y, mientras que para el lóbulo cefálico se presenta preponderantemente en el eje x. Razón por la cual los cambios en la conformación de éste último no son tan drásticos como los observados para el proceso mesial. De esta forma las representaciones gráficas de la deformación, muestran que la región más susceptible de variación en la forma del gonopodo, corresponde al proceso mesial. Esto se corrobora con el porcentaje que cada landmark aporta a la variación total, ya que para el conjunto de puntos que describen el proceso mesial es de aproximadamente el 50%.
El lóbulo mesial (puntos 1 al 4) (Fig. 2 A-C), por otra parte, corresponde al área donde se genera la menor deformación, siendo casi nula sobre los puntos 2 y 3. La forma de esta estructura permanece prácticamente constante en todos lo especímenes.
La comparación de los especímenes localizados en los extremos del eje del primer componente principal (Fig 3), nos permitio establecer que el área delimitada por los puntos de referencia del 6 al 9, concentra la mayor variabilidad en la forma del proceso mesial. Al realizar observaciones detalladas de esta área en cada ejemplar, se pudieron establecer múltiples configuraciones que varían desde presentar 7 espinas hasta carecer completamente de ellas. Por lo tanto esta área se puede considerar como el región con mayor plasticidad dentro del gonopodo.
Análisis multivariado
El análisis de componentes principales, sobre las variables de conformación resultantes de la alineación, traslación y rotación de los puntos de referencia, tanto del ápice como del proceso mesial, mostraron los siguientes resultados: para el proceso mesial el primer componente principal (CP) explica el 22,8% de la variación, el segundo el 16,3% y el tercero el 13,1%. En estudios que involucran varias especies el mayor porcentaje de la variabilidad total, se explica en los primeros componentes principales (Rosemberg 2001, Bermúdez 2005, Depecker et al. 2006). En nuestro caso, la variación se encuentra dispersa en varios componentes principales. Esto debido al hecho de que los especímenes analizados pertenecen a una misma especie, de tal forma que la variación observada se dispersa al obtener las nuevas variables no correlacionadas u ortogonales.
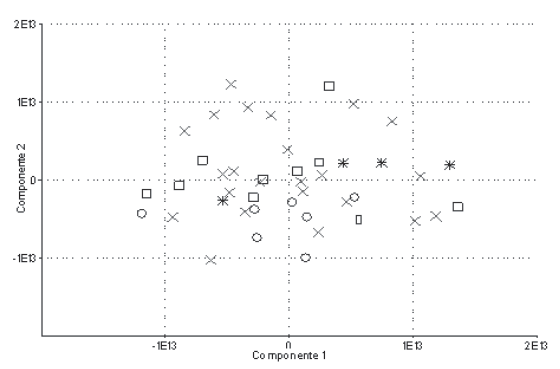
A partir del análisis de la variación del proceso mesial respecto a los componentes principales (CP), primero y segundo, se obtuvo una gráfica. Si se representa cada ejemplar por un símbolo de acuerdo a su procedencia, no se observa ningún tipo de agrupamiento entre los especímenes de la misma población (Fig. 4). Se concluye entonces que el cambio en la forma del proceso mesial no está asociado a la localidad. En la gráfica correspondiente al (CP) 1 vs. (CP) 3, tampoco fué posible distinguir algún tipo de agrupamiento.
Figura 4. Variación del proceso mesial respecto a los componentes principales (CP), primero y segundo, en los especímenes de Strengeriana maniformis Campos & Rodríguez, 1993. Cada ejemplar se representa por un símbolo de acuerdo a su procedencia: O = Manzanares, X = Samaná, □ = Victoria, = Cajamarca, ∗ = Fresno.
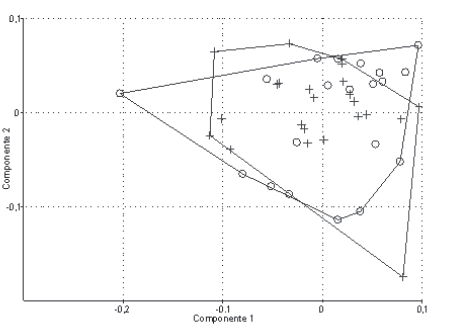
Al efectuar el análisis de componentes principales, para el ápice del gonopodo, los resultados fueron similares a los obtenidos para el proceso mesial. El primer (CP) explica el 23,9%, el segundo 17,3% y el tercero el 11,9% de la variación. Se analizó también si los especímenes provenientes de regiones donde hay explotación minera presentan un patrón de variación diferente a los provenientes de regiones donde no existe dicha explotación. En la Figura 5 se puede observar claramente que las variaciones en el ápice del gonopodo no están correlacionadas con las localidades, de tal forma que la contaminación generada por la explotación minera no es el factor responsable de la variación morfológica del gonopodo de Strengeriana maniformis.
Figura 5. Variación del proceso mesial respecto a los componentes principales (CP), primero y segundo, en los especímenes de Strengeriana maniformis Campos & Rodríguez, 1993. + = poblaciones con explotación minera, O = Poblaciones sin explotación minera.
Al realizar la prueba de regresión entre los componentes de conformación obtenidos para el ápice, y el tamaño centroide de cada ejemplar, se obtuvo un valor de p <0.01 (p = 0.0013), dado este valor se puede establecer que el desarrollo del ápice es independiente del tamaño del gonopodo. Tampoco se observo correlación entre el tamaño del espécimen y la forma de su gonopodo, como lo registrado para Microthelphusa racenisi Rodríguez, 1966 (Rodríguez 1982); de tal manera que el crecimiento del gonopodo es alométrico tanto para la forma (prueba de regresión), como para el tamaño.
CONCLUSIONES
Se encontró que el proceso mesial del gonopodo de la especie Strengeriana maniformis es la región donde se registra la mayor variación morfológica y que su porción distal es el área de mayor plasticidad. Mediante técnicas de morfometría geométrica se estableció que las variaciones morfológicas del primer gonopodo, en los especímenes de Strengeriana maniformis, no son causadas por la contaminación generada por la explotación minera en las regiones donde hay poblaciones de esta especie. En efecto, se estableció que estas variaciones son completamente independientes del lugar de procedencia.
De acuerdo con Dujardin (2002), la variación fenotípica es el resultado de la variación producida por el ambiente y los genes. Con base en nuestros resultados, se puede pensar que la variación morfológica del primer gonopodo de S. maniformis tiene un origen genético. Es necesario hacer nuevos muestreos con el fin de observar los patrones morfológicos del gonopodo en las nuevas generaciones.
AGRADECIMIENTOS
Los autores agradecen al Dr. Jorge Martínez del Departamento de Estadística de la Universidad Nacional de Colombia por su valiosa ayuda en la interpretación y el análisis de los resultados; a Adriana Bermúdez por su colaboración en la implementación de los programas y al Hermano Roque Casallas, del Museo La Salle por el préstamo del material.
LITERATURA CITADA
1. Astua de Moraes. D. 2003. A morfometria geometrica e a “revolução na morfometria”: localizando e visualizando mudanças na forma dos organismos. Bioletim. Año III. Número 3.
2. Bermúdez, A. 2005. Caracterización morfológica de las poblaciones de Agonida longipes y Munida flingi (Crustácea: Decapoda: Galatheidae) en el mar Caribe colombiano. Tesis de grado Maestría Biología Marina, Universidad Nacional de Colombia, Bogotá. [ Links ]
3. Burgman, M. A., D. A. Keit., F. J. Rohlf. & C. R. Tood. 1999. Probabilistic classification rules for setting conservation priorities. Biological Conservation 89: 227-231. [ Links ]
4. Campos, M. R. 1994. Diversidad en Colombia de los cangrejos del género Neostrengeria. Academia Colombia de Ciencias Exactas, Físicas y Naturales, Col. Jorge Álvarez Lleras No. 5: 1-144. [ Links ]
5. Campos, M. R. 2005. Freshwater crabs from Colombia a taxonomic and distributional study. Academia Colombia de Ciencias Exactas, Físicas y Naturales, Col. Jorge Álvarez Lleras No. 24: 1-364. [ Links ]
6. Campos, M. R. & G. Rodríguez. 1993. Three new species of Strengeriana from Colombia (Crustacea: Decapoda: Pseudothelphusidae). Proceedings of the Biological Society of Washington 106: 508 - 513. [ Links ]
7. Cardin, S. X. & K. D. Friedland.1999. The utility of imagen processing techniques for morphometrics analysis stock identification. Fisheries Research 43: 129-139. [ Links ]
8. Claude, J., E. Paradise., H. Tong & J. C. Auffray. 2003. A geometric morphometric assessment of the effects of environment and cladogenesis on the evolution of the turtle shell. Biological Journal of the Linnean Society 79: 485-501. [ Links ]
9. Dayton. G, Saenz. D, Baum. K, Langerhans. B, & Dewitt. T. 2005. Body saphe, burst speed and escape behavior of larval anurans. Oikos 111: 582 - 591. [ Links ]
10. Depecker, M., C. X. Berge Penin & S. Renous. 2006. Geometric morphometrics of the shoulder girdle in extant turtles (Chelonii). Journal of Anatomy 208:35-45. [ Links ]
11. Dewel, V. H. 1985. Insect morphometric. Annual Review of Entomology 30: 415-38. [ Links ]
12. Dujardin, J. P. 2002. PADwin_47: version 2, Unité de Recherches 062-Unité Mixte de Recherches UMR9926. Institut de Recherches pour le Développement (IDR, France). [ Links ]
13. Ghalaibeh, W. S., F. J. Rolhf., D. E. Slice & L. E. Delisi. 2000. A geometric morphometric assessment of change in midline brain structural shape following a first episode of Schizophrenia. Biological Psychiatry 48: 398-405 [ Links ]
14. Harlow, L. L. 2005. The essence of multivariable thinking basic themes and methods. Lawrence Erlbawn associates. New Jersey 152 -172. [ Links ]
15. Hammer, O., D. A. Harper & P. D. Ryan. 2001. Palaeontological statistics software package for education and data analysis (PAST). Palaeontología Electrónica. [ Links ]
16. Hendry, A. P., M. L. Kelly., M. T. Kinnison & D. N. Reznick. 2005. Parallel evolution on the sexes? Effects of predation and habitat features on the size and shape of wild guppies. Journal Compilation 2006. European Society For Evolutionary Biology. [ Links ]
17. Leach, W. E. 1814. Crustaceology. In Endingurgh Encyclopaedia, 7: 383 – 437, pl 221. Edingurgh.
18. Macleod, N. & P. Forey. 2002. Morphology, shape and phylogeny. Taylor and Francis, Icorporated. Florence, KY, 175-180. [ Links ]
19. Manier.M.K. 2004. Geographic variation in the long-nosed snake, Rhinocheilus lecontei (Colubridae): beyond the subspecies debate. Biological Journal of the Linnean Society 83: 65-85. [ Links ]
20. MINISTERIO DEL MEDIO AMBIENTE. 2002. Gestión minero ambiental para las regiones auríferas de Colombia Diagnostico y proyecciones. Ministerio del Medio Ambiente 17-38. [ Links ]
21. O’Reilly, K. M. & M. H. Horn. 2004. Phenotypic variation among populations of Atherinops affinis (Atherinopsidae) with insights from a geometric morphometric analysis. Journal of Fish Biology 64: 1117-1135.
22. Pretzmann, G. 1965. Vorläufiger Bericht über die Familie Pseudothelphusidae. Anzeiger der Österreichischen Akademie der Wissenschaften Mathematische Naturwissenschaftliche Klasse 1(1): 1-10. [ Links ]
23. Rodríguez, G. 1966. The freshwater crabs of the genus Pseudothelphusa from northern Venezuela and Trinidad (Brachyura, Potamonidae). Zoologische Mededelingen, Leiden 41: 111-135. [ Links ]
24. Rodriguez, G. 1982. Les crabes d’eau douce d’Amerique famille des Pseudothelphusidae. Orstom. Paris. 163-164.
25. Rohlf, J. M. & D. E. Slice. 1990. Extensions of the procrustes method for the optimal superimposition of landmarks. Systematic Zoology 39: 40-59. [ Links ]
26. Rohlf, J. F. 2005a. Tps Utility program version 1.33. Ecology and Evolution, SUNY at Stony Brook. [ Links ]
27. Rohlf, J. F. 2005b. Tps Dig, version 2,04. Ecology and Evolution, SUNY at Stony Brook. [ Links ]
28. Rohlf, J. F.2005c. Tps Relative warps version 1.42. Ecology and Evolution, SUNY at Stony Brook. [ Links ]
29. Rohlf, J. F. 2005d. Tps Regr version 1.31. Ecology and Evolution, SUNY at Stony Brook. [ Links ]
30. Rosemberg, M. S. 2001. Fiddler crab claw shape variation: a geometric morphometric analysis across the genus Uca (Crustacea: Brachyura: Ocypodidae). Biological Journal of the Linnean Society 75: 147-162. [ Links ]
31. Singh, S. D. & B. D. Thing. 2003. Effects of the headgear activator Teuscher appliance in the treatment of class II division 1 malocclusion: a geometric morphometric study. Orthod Craniofacial 6: 88-95 [ Links ]
32. Smalley, A. E. 1964. A terminology for the gonopods of the American River Crabs. Systematic Zoology 13: 28-31. [ Links ]
Recibido: 11/09/2006
Aceptado: 17/04/2007