Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Caldasia
Print version ISSN 0366-5232On-line version ISSN 2357-3759
Caldasia vol.34 no.1 Bogotá Jan./June 2012
JUAN CARLOS JARAMILLO-LONDOÑO
NÉSTOR JAIME AGUIRRE-RAMÍREZ
Grupo GAIA. Universidad de Antioquia, Grupo de Investigaciones y Mediciones Ambientales, Facultad de Ingenierías, Universidad de Medellín, Apartado 1983, Medellín, Colombia. jcjaramillo@udem.edu.co
Facultad de Ingeniería, Grupo GAIA, Universidad de Antioquia, Medellín, Colombia.
RESUMEN
Se evaluaron los cambios espaciales y temporales de los ensambles fitoplanctónicos y zooplanctónicos durante la época de menor nivel de agua en la Ciénaga de Ayapel. Se tomaron muestras integradas en toda la columna de agua, en seis estaciones de muestreo, siguiendo el eje longitudinal de la ciénaga en sentido norte-sur, y durante siete días continuos. Durante el período de estudio la ciénaga se comportó como un sistema de aguas blandas, alcalino, altamente turbio, con profundidad y transparencia reducidas, fuertemente mezclado y con diferencias notables a nivel espacial y una alta homogeneidad temporal de sus variables físicas, químicas y biológicas. Ambos ensambles presentaron homogeneidad temporal y diferencias espaciales. Las Cianobacteria representaron el 70% de la densidad total del fitoplancton principalmente Cylindropermopsis raciborskii y Planktolyngbya limnetica y el zooplancton por las formas inmaduras de los copépodos (nauplios principalmente) y rotíferos del género Brachionus.
Palabras clave. fitoplancton, zooplancton, ciénagas, Colombia.
ABSTRACT
The spatial and temporal changes of phytoplankton and zooplankton assemblages were evaluated during the period of low water level in the swamp Ciénaga de Ayapel. During seven continuous days, integrated water samples were taken throughout the water column along six sampling stations located north-south across the longitudinal axis of the swamp. During the study period, the swamp acted as a soft, alkaline water system, strongly mixed, with reduced depth and transparency, with noticeable differences in the spatial conditions, and witha high temporal homogeneity of the physical, chemical and biological variables. Both phytoplankton and zooplankton assemblages showed spatial differences and a high temporal homogeneity. Cyanobacteria represented 70% of the total density of phytoplankton, mainly Cylindropermopsis raciborskii and Planktolyngbya limnetica. Zooplankton was represented by the immature stages of copepods (mainly naiplii) and rotifers of the genus Brachionus.
Key words. Phytoplankton, zooplankton, swamp, Colombia.
Recibido: 07/12/2010
Aceptado: 15/04/2012
INTRODUCCIÓN
Las planicies de inundación son áreas que se inundan periódicamente debido al sobre flujo lateral de los ríos o por precipitación directa sobre la cuenca de drenaje, dando como resultado un ambiente fisicoquímico cambiante y dinámico, en el que la hidrología y los flujos de materiales condicionan la estabilidad y la diversidad de las comunidades allí presentes (Neiff et al. 1994, Neiff 1999, Mitsch & Gosselink 2000, Junk et al. 2010). Dependiendo del grado de conectividad de estos cuerpos de agua con los ríos, estos ambientes reciben agua durante las crecientes y durante los períodos secos vierten aguas al río contribuyendo a mantener sus niveles. Estos ciclos marcan estaciones muy definidas asociadas también a ciclos de producción, consumo y reproducción de los organismos que las habitan. Las variaciones estacionales del volumen de agua en el interior de estos sistemas están asociadas a la precipitación, a los flujos de aguas superficiales, subsuperficiales y subterráneos y a la evapotranspiración (Amoros & Roux 1988, Risser 1990, Vásquez & Rey 1993, Gopal 1994, Neiff et al. 1994, Ward & Stanford 1995, Bonecker & Lansac-Toha 1996, Junk 1997, Ramírez & Viña 1998, Middleton 1999, 2002, Junk & Wantzen 2003).
En Colombia, las planicies de inundación son regionalmente denominadas "ciénagas" y se definen como ecosistemas de poca profundidad (usualmente no sobrepasan los 6 m), están localizadas a alturas inferiores a 1000 metros sobre el nivel del mar, poseen una temperatura superior a los 25 °C y precipitaciones mayores a 2000 mm anuales. Colombia posee cerca de 1938 ciénagas que ocupan 4785 km2, cobertura que las sitúa como el principal sistema lenítico del país (Arias 1985). Se ubican como macrounidades geomorfológicas en los que predominan procesos de dinámica fluvial (erosión, depositación e inundación, entre otros), y a partir de los trabajos publicados por ecólogos y biogeógrafos en las últimas décadas, el concepto de planicie de inundación es manejado en el contexto del término "humedal", el cual ha demostrado ser inesperadamente fecundo y operativamente aceptable para los latinoamericanos (Neiff 1999).
El establecimiento de las diferentes comunidades acuáticas en las ciénagas y la naturaleza de las interacciones dependen de las condiciones hidrológicas, de la presencia de corrientes, del efecto del viento, de las condiciones ambientales y de las complejas relaciones dentro y entre los ensambles fitoplanctónicos y zooplanctónicos. Los cambios temporales de los ensambles planctónicos, sus patrones de distribución espacial y las interacciones tróficas entre ellos y con otras comunidades, constituyen uno de los conjuntos de características básicas para la comprensión de los procesos ecológicos de cualquier ambiente de aguas leníticas (Pinto-Coelho 1987). Las ciénagas pueden sufrir cambios profundos en sus condiciones limnológicas y con ello afectar a las comunidades biológicas que allí se encuentran presentes. Por ejemplo, el crecimiento del fitoplancton está estrechamente relacionado con el enriquecimiento por nutrientes, ese crecimiento puede disminuir drásticamente bajo los efectos del pastoreo intensivo, el cual depende de la composición del zooplancton, puesto que la naturaleza de la selección de alimento varía entre los taxones herbívoros (Officer et al. 1982, Havens 1991, Hily 1991, Mellina et al. 1995, Abdel-Aziz et al. 2006), el desarrollo del ensamble zooplanctónico no depende solamente de de la cantidad de alimento disponible sino también de la diferente calidad nutricional del fitoplancton del cual se alimenta (Brett et al. 2000, Ramos-Rodríguez & Conde-Porcuna 2003), a su vez el zooplancton puede transferir detritos y bacterias a niveles tróficos superiores y también participar activamente en el proceso de recirculación de los nutrientes para que estos sean aprovechados nuevamente por el fitoplancton (Macedo & Pinto-Coelho 2000, Mitsch & Gosselink 2000, Hunt & Matveev 2005, Tundisi & Matsumura-Tundisi 2008) y de esta manera regular la densidad y composición de los diferentes niveles tróficos de la comunidad (Donaghay et al. 1991; Torres et al. 2006). El presente trabajo pretende evaluar la variación espacial y temporal de los ensambles fitoplanctónicos y zooplanctónicos de la Ciénaga de Ayapel para un ciclo semanal durante la época de menor nivel del agua de la ciénaga.
ÁREA DE ESTUDIO
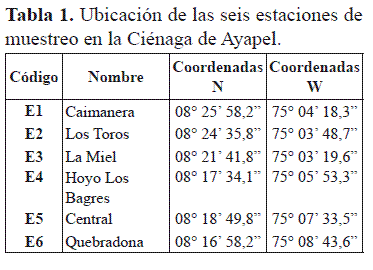
La ciénaga de Ayapel, está ubicada en jurisdicción del municipio del mismo nombre en el departamento de Córdoba (8° 19' Norte y 75° 6' Oeste), a 22 metros de altura sobre el nivel del mar, en la planicie caribeña del norte de Colombia. Forma parte del microsistema de humedales y zonas anegables de la Depresión Momposina y se constituye en el sistema cenagoso más grande e importante del sector de la región de La Mojana. La cuenca de la ciénaga se ubica entre los 20 y 150 metros sobre el nivel del mar y tiene un área de captación de aproximadamente 1500 km2. El territorio se ubica en una zona de bosque húmedo tropical (bh-T), con temperaturas promedio anuales superiores a los 25 °C. El régimen de precipitación se ve enmarcado por una época de lluvias de abril a noviembre y una época seca de diciembre a marzo. El promedio anual de lluvias fluctúa entre 2000 y 2500 mm (Aguirre et al. 2005, Rangel-Ch & Arellano 2010). Para el período en el que se desarrollo éste trabajo la precipitación fue de apenas 6 mm y la temperatura ambiental alcanzó los 30 °C. La Ciénaga de Ayapel posee unos elementos funcionales particulares, entre ellos están el régimen hidrológico del río San Jorge que penetra al norte por el caño Grande, la afluencia desde el costado oriental del caño Barro, por el sur la afluencia de la quebrada Quebradona y por el costado occidental la influencia del casco urbano del municipio de Ayapel. La ubicación de las estaciones de muestreo en la Ciénaga de Ayapel se muestra en la tabla 1.
Según Aguirre et al. (2005), la Ciénaga de Ayapel es un sistema somero y polimíctico cálido que presenta una fluctuación pronunciada del nivel del agua a lo largo del año. Ésta y todas las ciénagas vinculadas hidrológicamente a ella, cubren un área máxima en las condiciones extremas de aguas altas de 140 km2 y en el período histórico de mínima esta área se reduce a unos 20 km2. En términos de los promedios mensuales multianuales, la ciánaga varía desde 58 km2 (marzo-abril) hasta 128 km2 (septiembre-octubre) con un promedio anual de 106 km2. La amplia franja comprendida entre estos dos extremos presenta una dinámica contrastante que alterna un período seco de variable humedad disponible en el suelo, con un período en el cual la franja se convierte en una extensa y somera zona litoral de la ciénaga, con profundidades variables, donde emerge vegetación de gramíneas que se aprovechan para pastoreo de ganado o bien para el desarrollo de algunos cultivos transitorios.
MATERIALES Y MÉTODOS
Se seleccionaron seis estaciones de muestreo siguiendo un eje longitudinal de la ciénaga en sentido norte-sur en las que se tomaron muestras, diariamente y durante siete días continuos, de variables físicas y químicas y de plancton.
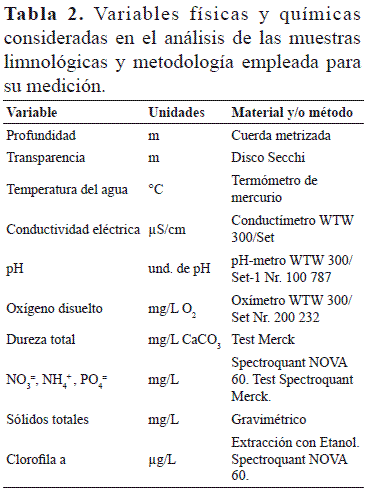
En cada una de las seis estaciones de muestreo se midieron diariamente, in situ: profundidad, transparencia, temperatura del agua, conductividad eléctrica, pH, oxígeno disuelto, y se tomaron muestras subsuperficiales en recipientes plásticos de 2 L para los análisis de dureza, nitratos, amonio, fosfatos, sólidos totales y clorofila a; las variables y los métodos empleados se presentan en la tabla 2.
Para tomar las muestras de plancton se construyó un tubo muestreador de PVC de 2 m de longitud y 10 cm de diámetro al que se le adaptó una llave de seguridad de 3 cm de diámetro en uno de sus extremos (Fig. 1). La muestra era colectada a lo largo de la columna de agua y para todos los casos incluyó la zona fótica completa. El fitoplancton se tomó introduciendo el tubo hasta una profundidad máxima de 2 m. El material colectado se filtró en una red cónica de 20 micras de abertura de malla, con un frasco vial de 50 mL atado en el extremo inferior de la misma, concentrando de esta manera el material filtrado; el volumen total filtrado fue de 20 L; el frasco colector se retiró y la muestra se fijó con una solución de lugol al 10% (concentración final), para su posterior identificación y conteo en el laboratorio.

Para la observación de las muestras se utilizó un microscopio invertido Leica DMIN provisto de reglilla ocular; la muestra de agua proveniente del campo se agitó y de ella se extrajo una alícuota de 1 mL que se depositó en una cámara de Sedgwick-Rafter para su conteo. Las observaciones se realizaron en un aumento de 400X y para calcular la densidad de organismos por mililitro se aplicó la expresión de Ros (1979). Las determinaciones de los taxones fitoplanctónicos se realizaron hasta el mayor nivel taxonómico posible.
El zooplancton se tomó introduciendo el tubo hasta una profundidad máxima de 2 m, el material recolectado se filtró en una red cónica de 64 micras de abertura de malla, con un frasco vial de 50 mL atado en el extremo inferior de la misma para concentrar el material filtrado; el volumen filtrado fue de 100 L; el frasco se retiró y la muestra se fijó con una solución de formalina al 4% (concentración final), para su posterior identificación y conteo en el laboratorio.
La observación de las muestras se realizó en un microscopio Leica DMLB, la muestra de agua proveniente del campo se agitó y de ella se extrajo una alícuota de 1 mL que se depositó en una cámara de Sedgwick-Rafter para su conteo.
La cámara fue contada en su totalidad y hasta completar un mínimo de individuos de 400, para garantizar una precisión del 90% (Edmonson & Winberg 1971, Pinto-Coelho 1987) en un aumento de 100X y se calculó la densidad de organismos por litro, la determinación de los taxa zooplanctónicos se realizó hasta el mayor nivel taxonómico posible.
A todas las variables se les aplicó un análisis de varianza (ANOVA) para establecer diferencias entre estaciones y campañas de muestreo. Para establecer relaciones entre las densidades fitoplanctónicas y zooplanctónicas se aplicó un análisis de correlación múltiple utilizando el Coeficiente de Correlación Lineal de Pearson (r). Estos análisis se realizaron usando el programa SYSTAT versión 11 (SYSTAT Software Inc., Point Richmond, California).
RESULTADOS
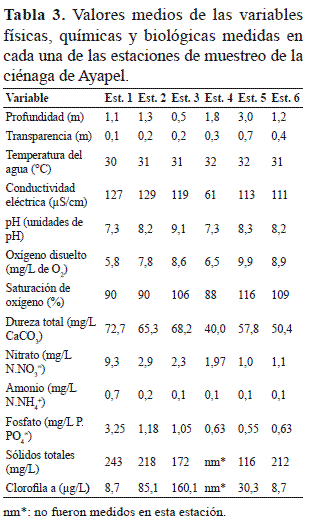
Los valores medios de las variables físicas, químicas y biológicas más importantes en cada una de las estaciones de muestreo de la ciénaga de Ayapel se muestran en la tabla 3. La profundidad en general fue baja, el mayor valor se encontró en la estación 5 y las demás estaciones presentaron valores cercanos a un metro; la transparencia del agua fue muy baja; el pH fue ligeramente alcalino; la conductividad eléctrica, los sólidos totales, los nitratos, amonios y fosfatos mostraron un ligero gradiente en sentido norte-sur, la estación 1 ubicada más al norte fue la que presentó los valores más altos y estos fueron disminuyendo gradualmente hacia la estación 6 ubicada hacia el extremo sur de la ciénaga.
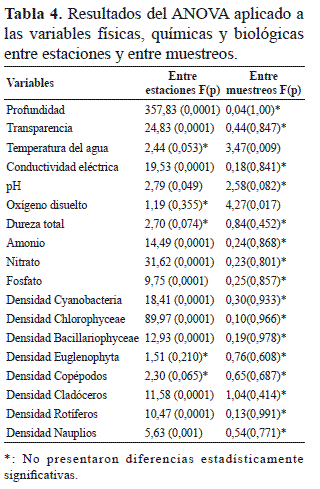
El análisis de varianza mostró diferencias entre estaciones para profundidad, transparencia, pH, conductividad, amonio, nitrato, fosfato, y para las densidades de cianobacterias, clorofíceas, bacilariofíceas, cladóceros, rotíferos y nauplios y entre muestreos para la temperatura del agua y el oxígeno disuelto (Tabla 4).
La tabla 5 muestra las morfoespecies del fitoplancton que alcanzaron las densidades más altas, en total se encontraron 74 morfoespecies, la mayoría de ellas perteneciente a las clorofíceas, cianobacterias y bacilariofíceas (31, 17 y 12 morfoespecies respectivamente), sin embargo, las densidades más altas fueron para las cianobacterias (70% de la densidad total correspondió a éste grupo) principalmente las especies Cylindrospermopsis raciborskii Woloszýnska (253 996 ind/mL) y Planktolyngbya limnetica Lemmerman (205 272 ind/mL).

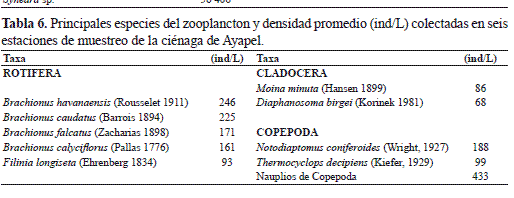
Las especies del zooplancton que alcanzaron las densidades más altas en la Ciénaga de Ayapel durante el momento del estudio se presentan en la tabla 6. En total se colectaron 35 especies, de las cuales 25 pertenecen al grupo de los rotíferos, este grupo fue el que alcanzó la mayor densidad (55% del total de individuos colectados), las formas inmaduras de los copépodos fueron las que alcanzaron las mayores densidades a lo largo de todo el muestreo (433 ind/L). Las especies con más altas densidades fueron: Brachionus havanaensis Rousselet (246 ind/L), B. caudatus Barrois (224 ind/L), B. falcatus Zacharias (171 ind/L) y B. calyciflorus Pallas (161 ind/L), Notodiaptomus coniferoides Wright (188 ind/L).
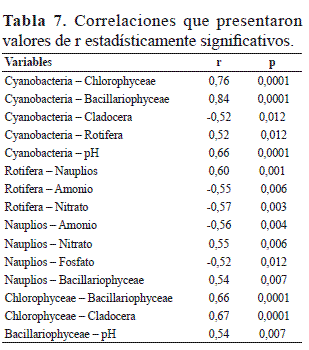
La tabla 7 muestra las correlaciones que presentaron valores de r estadísticamente significativos entre las densidades de los grupos fitoplanctónicos y zooplanctónicos y las variables físicas y químicas medidas.
Las cianobacterias presentaron correlaciones positivas con clorofíceas, bacilariofíceas, rotíferos y pH y negativas con los cladóceros. Por su parte las cloroficeas mostraron correlaciones positivas con bacilariofíceas y cladóceros. Las bacilariofíceas presentaron correlaciones positivas con nauplios y pH. Los rotíferos correlaciones positivas con los nauplios y negativas con las concentraciones de amonio y nitrato. Finalmente los nauplios mostraron correlación positiva con la concentración de nitrato y negativa con las concentraciones amonio y fosfato.
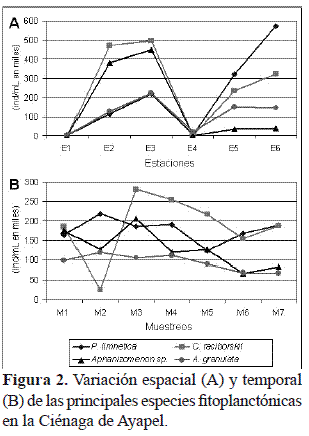
La figura 2A muestra la variación espacial de las principales especies fitoplanctónicas en la Ciénaga de Ayapel, las estaciones 1 y 4 fueron las que presentaron las densidades más bajas, para las estaciones 2 y 3 las especies C. raciborskii y Aphanizomenon sp fueron las que presentaron las densidades más altas, mientras que en las estaciones 5 y 6 las especies con mayor densidad fueron P. limnetica y C. raciborskii. Con respecto a la variación temporal (Fig. 2B) C. raciborskii presentó en general las mayores densidades (excepto para el muestreo 2) en el que esta especie alcanzó el valor más bajo y se observó un incremento de la especie P. limnetica.
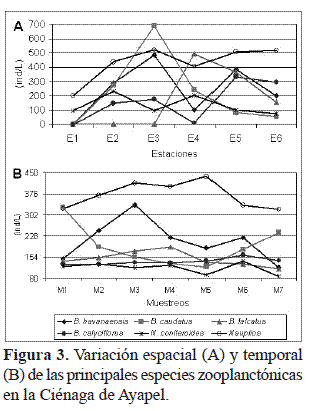
Con respecto a la variación espacial de las principales especies del zooplancton (Fig. 3A), se observó un incremento en las densidades de los organismos de la estación 1 a la estación 3, en la estación E4 disminuyen en general las poblaciones de rotíferos (excepto B. caudatus, cuya densidad aumentó) y se incrementó también la densidad del copépodo N. coniferoides, por su parte los nauplios mostraron en general las más altas densidades tanto espacial como temporalmente (Fig. 3B).
DISCUSIÓN
Durante el período de estudio la Ciénaga de Ayapel fue un sistema de aguas blandas, alcalino, altamente turbio, con profundidad y transparencia reducidas; altas concentraciones de sólidos totales y nutrientes; en donde la constante acción del viento sobre el espejo de agua ocasiona una mezcla continua y la resuspensión de los sedimentos del fondo, que en algunos casos puede involucrar a toda la columna de agua; con diferencias notables a nivel espacial y una homogeneidad temporal de sus variables físicas, químicas y biológicas.
El ensamble fitoplanctónico en la Ciénaga de Ayapel estuvo compuesto principalmente por especies del grupo de las cianobacterias, en su mayoría P. limnetica y C. raciborskii, estas especies mostraron diferencias a nivel espacial y homogeneidad a nivel temporal. Este predominio de cianobacterias en la Ciénaga de Ayapel también ha sido reportado previamente por Hernández-Atilano et al. (2008). Mur et al. (1999) reportan que estas especies poseen bajas tasas de crecimiento, sin embargo, sus poblaciones se ven compensadas por la baja herbivoría por parte del zooplancton y la alta capacidad de suspensión que presentan, lo que hace que las pérdidas por sedimentación sean muy bajas. Adicionalmente son tolerantes a deficiencias lumínicas (Padisák 1997, Reynolds et al. 2002), y en este sentido la Ciénaga de Ayapel es un ambiente propicio para su desarrollo debido a la gran cantidad de material en suspensión y la presencia de una zona fótica bastante reducida, que en la mayoría de los casos no supera el metro de profundidad.
En términos generales se ha reportado que muchas cianobacterias parecen menos comestibles para el zooplancton y peces comparadas con otros grupos de algas (Gilbert 1996, Reynolds 1998). Muchos filamentos algales que son simples y largos como el caso de C. raciborskii y P. limnética son ingeridos con facilidad por otros organismos y esto ayuda en la eficiencia de la alimentación de especies filtradoras (Gliwicz & Lampert 1990). Sin embargo, existen numerosos reportes de que las cianobacterias no son consumidas (Porter & Orcutt 1980, de Bernardi & Giussani 1990), que interfieren con el pastoreo (Gliwicz & Seidlar 1980) y que tienen un efecto negativo vía toxicidad (Paerl & Fulton 2006, Ibelings & Havens 2007). En el caso específico de C. raciborskii se reporta baja palatabilidad (Bouvy et al. 2001) lo que sugiere que además de su adaptabilidad ecológica, su población puede ser favorecida por una baja tasa de pastoreo comparada con otros grupos fitoplanctónicos más susceptibles herbivoría como por ejemplo las clorifíceas (Gragnani et al. 1999). En este sentido, aunque C. raciborskii alcanzó densidades de hasta 496 424 ind/mL en la ciénaga no constituye una buena oferta alimenticia, por lo que consideramos que posiblemente el bacteriplancton y los detritos serían los responsables del sostenimiento de la red trófica en este ecosistema.
El ensamblaje zooplanctónico en la Ciénaga de Ayapel estuvo conformado principalmente por rotíferos y formas inmaduras de copépodos; su composición presentó homogeneidad temporal y variaciones espaciales notorias. Los rotíferos que presentaron las mayores densidades correspondieron al género Brachionus, los cuales son considerados comunes en aguas tropicales (Fernando 2002). La contribución de este género en la riqueza zooplanctónica de la ciénaga coincide con lo encontrado por Caravalho (1983) en el Lago Grande en el Amazonas brasilero, Gavilán-Díaz (2000) en las ciénagas de Paredes, El Llanito y Chucurí en el Magdalena medio Colombiano y en trabajos previos realizados en la Ciénaga de Ayapel por Gallo-Sánchez et al. (2009) y Villabona-González et al. (2011).
Para Matsumura-Tundisi y Tundisi (2005), la dominancia de rotíferos puede estar relacionada con sus características oportunistas (especies r-estrategas, adaptadas a rápido crecimiento poblacional durante estaciones favorables cortas) y a su capacidad para aprovechar recursos alimenticios de baja calidad nutricional como detritos orgánicos (Gannon & Stemberger 1978, Infante 1982, Mangas & García 1991). Otro factor que contribuye al éxito de los rotíferos limnéticos es su plasticidad para adaptarse a diferentes fuentes alimenticias; esta característica, sumada a la baja presión de predación, por su pequeño tamaño, le proporcionan ventajas competitivas sobre los otros grupos zooplanctónicos (Dumont 1977). Este grupo juega un papel muy importante en la ciénaga, principalmente debido a su habilidad para filtrar bacterias y fitoplancton de pequeño tamaño, que son comunes en este ecosistema. También se destaca una alta densidad de formas larvales de copépodos, estos organismos son de gran importancia en la estructura de los ensambles zooplanctónicos en cuanto a su dinámica y aspectos tróficos. Mientras los nauplios y primeros estadios de desarrollo de los copepoditos del orden Cyclopoida son filtradores y predominantemente herbívoros, los últimos estadios de los copepoditos y los adultos tienen hábito raptorial y son predominantemente carnívoros (Neves et al. 2003). Y de acuerdo con Edmondson (1959), la alta proporción de formas inmaduras de copépodos son el resultado de la continua reproducción de estos organismos en regiones tropicales; la alta densidad de nauplios en relación con los copépodos adultos puede ser un indicador de una alta tasa de mortalidad durante las diferentes etapas de su desarrollo (Sartori et al. 2009). Un factor que podría estar determinando la proporción de formas jóvenes y adultos, es la intensidad de la predación y el balance entre la predación por invertebrados y vertebrados, puesto que los copépodos representan gran parte de los elementos alimenticios de peces jóvenes y adultos (Paggi & de Paggi 1990, Urabe 1990, Lansac-Tôha et al. 1991). Para la Ciénaga de Ayapel no se tiene información sobre el impacto de los peces sobre la comunidad zooplanctónica; sin embargo, la alta abundancia y la riqueza de especies de peces observada en la ciénaga es un importante factor que puede ser considerado en futuros estudios.
Las bajas densidades de cladóceros pueden ser consecuencia de la gran cantidad de sólidos presentes en el agua (Nogeira et al. 1999); ya que las partículas suspendidas pueden afectarles directamente por interferencia mecánica o indirectamente por la disminución de la luz (Paggi & de Paggi 1990). Sin embargo, el comportamiento alimenticio de estos organismos y otras interacciones biológicas en aguas turbias aún no está bien comprendido. Se ha considerado que los cladóceros son mejores competidores que los rotíferos porque son de mayor tamaño, son más eficientes filtrando su alimento, e interfieren mecánicamente con los rotíferos que son atrapados en su cámara branquial (Gilbert 1985, Jaramillo-Londoño & Pinto-Coelho 2010). En la Ciénaga de Ayapel los rotíferos son abundantes y los cladóceros son escasos, de acuerdo con Kirk (1991) esta escasez puede ser una consecuencia del descenso en la rata de ingestión de fitoplancton debido a la alta concentración de partículas inorgánicas suspendidas en la columna de agua.
AGRADECIMIENTOS
Los autores agradecen al Grupo de Investigación en Gestión y Modelación Ambiental-GAIA, de la Universidad de Antioquia por el apoyo económico para la realización de este trabajo y a CORPOAYAPEL por el apoyo logístico en la zona durante los muestreos, también agradecemos al grupo de evaluadores anónimos, quienes con sus sugerencias contribuyeron a mejorar el manuscrito.
LITERATURA CITADA
1. ABDEL-AZIZ, N.E., S.M. GHARIB & M.M. DORGHAM. 2006. The interaction between phytoplankton and zooplankton in a Lake-Sea connection, Alexandria, Egypt. International Journal of Oceans and Oceanography 1(1):151-165. [ Links ]
2. AGUIRRE, N., J. PALACIO, M. FLÓREZ, A. WILLS, O. CAICEDO, L.F. JIMÉNEZ, N. VILLEGAS, H. GRAJALES, C. PALACIO, M. TORO & J. VÉLEZ. 2005. Análisis de la relación río-ciénaga y su efecto sobre la producción pesquera en el sistema cenagoso de Ayapel, Colombia. Grupo GAIA. Universidad de Antioquia. Medellín. 419pp. [ Links ]
3. AMOROS, C. & A.L. ROUX. 1988. Interaction between water bodies within the floodplains of larger rivers: Functions and development of conectivity. Munstersche Geographische Arbeiten 29:125-130. [ Links ]
4. ARIAS, P. 1985. Las ciénagas en Colombia. Divulgación Pesquera. INDERENA (Bogotá). 22 (2, 3, 4):39-70. [ Links ]
5. BONECKER, C.C. & F.A. LANSAC-TÔHA. 1996. Community structure of rotifers in two environments of the upper river Parana floodplain-Brazil. Hydrobiologia 325:137-150. [ Links ]
6. BOUVY, M., M. PAGANO & M. TROUSSELLIER. 2001. Effects of a Cyanobacterial bloom (Cylindrospermopsis raciborskii) on bacteria and zooplankton communities in Ingazeira reservoir (northeast Brazil). Aquatic Microbial Ecology 25: 215–227. [ Links ]
7. BRETT, M.T., D.C. MULLER-NAVARRA & S. PARK. 2000. Empirical analysis of the effect of phosphorus limitation on algal food quality for freshwater zooplankton. Limnology and Oceanography. 45:1564-1575. [ Links ]
8. CARAVALHO, M.L. 1983. Efeitos da flutuação do nível da água sobre a densidade e composição do zooplancton em um Lago de várzea da Amazônia, Brasil. Acta Amazonica 13(5-6): 715-724. [ Links ]
9. DE BERNARDI, R. & G. GIUSSANI. 1990. Are blue-green algae a suitable food for zooplankton? An overview. Hydrobiologia 200: 29-41. [ Links ]
10. DONAGHAY, P., P. LISS, R. DUCE, D. KESTER, A. HANSON, T. VILLAREAL, N. TINDALE & D. GIFFORD. 1991. The role of episodic atmospheric nutrient inputs in the chemical and biological dynamics of oceanic ecosystems. Oceanography 4(2):62-70. [ Links ]
11. DUMONT, H.J. 1977. Biotic factors in the population dynamics of rotifers. Archiv fur Hydrobiologie. 8:98–122. [ Links ]
12. EDMONDSON, W.T. 1959. Freshwater Biology. 2ª ed. John Wiley. Nueva York. 1248 pp. [ Links ]
13. EDMONSON, W T. & G.C. WINBERG. 1971. A manual on methods for the assessment of secondary productivity in fresh waters. I. B. P. Handbook n°17. Blackwell Scientific Publications, Oxford, 385 p. [ Links ]
14. FERNANDO, C.H. 2002. A guide to tropical freshwater zooplankton. Identification, ecology and impacto on fisheries. Backhuys Publishers, Leiden. 291pp. [ Links ]
15. GALLO-SÁNCHEZ, L.J, N.J. AGUIRRE-RAMÍREZ, J.A. PALACIO-BAENA & J.J. RAMÍREZ-RESTREPO. 2009. Zooplancton (Rotifera y microcrustacea) y su relación con los cambios del nivel del agua en la ciénaga de Ayapel, Córdoba, Colombia. Caldasia 31(2): 339-353. [ Links ]
16. GANNON, J.E. & R.S. STEMBERGER. 1978. Zooplankton (especially crustaceans and rotifers) as indicators of water quality. Transactions of the American Microscopical Society. 97(1): 16-35. [ Links ]
17. GAVILÁN-DÍAZ, R.A. 2000. Limnologia comparativa de três lagoas Neotropicais da bacia do Magdalena Medio Santandereano, (Colombia), com ênfase no estudo da diversidade da comunidade zooplanctónica e sua relação com a dinâmica hidrológica do sistema regional. Tese (Doutorado). Universidade Federal de São Carlos, São Carlos, Brasil. [ Links ]
18. GILBERT, J.J. 1985. Competition between rotifers and Daphnia. Ecology 66: 1943-1950. [ Links ]
19. GILBERT, J.J. 1996. Effect of food availability on the response of planktonic rotifers to a toxic strain of the cyanobacterium Anabaena flos-aquae. Limnology and Oceanography 41: 1565-1572. [ Links ]
20. GLIWICZ, Z.M. & E. SEIDLAR. 1980. Food size limitation and algae interfering with food collection in Daphnia. Archiv fur Hydrobiologie 88: 155-177. [ Links ]
21. GLIWICZ, Z.M. & W. LAMPERT. 1990. Food thresholds in Daphnia species in the absence and presence of blue-green filaments. Ecology 71: 691-702. [ Links ]
22. GOPAL, B. 1994. The role of ecotones (transition zones) in the conservation and management of tropical inland waters. Mitteilungen Internationale Vereinigung fü r Theoretische und Angewandte Limnologie 24:17-25. [ Links ]
23. GRAGNANI, A., M. SCHEFFER & S. RINALDI. 1999. Top-down control of cyanobacteria: a theoretical analysis. American Naturalist 153: 59-72. [ Links ]
24. HAVENS, K.E. 1991. The importance of rotiferan and crustacean zooplankton as grazers of algal productivity in a freshwater estuary. Archiv fü r Hydrobiologie 122:1-22. [ Links ]
25. HERNÁNDEZ-ATILANO, E., N.J. AGUIRRE, J.A. PALACIO & J.J. RAMÍREZ. 2008. Variación espacio temporal de la asociación fitoplanctónicaen diferentes momentos del pulso hidrológico en la cienaga de Ayapel (Córdoba), Colombia. Actualidades Biológicas 30(88): 67-81. [ Links ]
26. HILY, C. 1991. Is the activity of benthic suspension feeders a factor controlling water quality in the Bay of Brest? Marine Ecology. Progress Series 69:203-210. [ Links ]
27. HUNT, R.J. & V.F. MATVEEV. 2005. The effect of nutrients and zooplankton community structure on phytoplankton growth in a subtropical Australian reservoir: an enclosure study. Limnologica. 35:90-101. [ Links ]
28. IBELINGS, B.W. & K.E. HAVENS. 2007. Cyanobacterial toxins: a qualitative meta-analysis of concentrations, dosage and effects in freshwater, estuarine and marine biota. Advances in Experimntal Medicine and Biology 619: 685-744. [ Links ]
29. INFANTE, A. 1982. Annual variations in abundance of zooplankton in Lake Valencia (Venezuela). Archiv fur Hydrobiologie 93: 194-208. [ Links ]
30. JARAMILLO-LONDOÑO, J.C. & R.M. PINTO-COELHO. 2010. Interaction between Hexarthra intermedia (Rotifera) and Bosmina longirostris (Cladocera): a case of opportunistic nutrition or interference competition?. Journal of Plankton Research 32(6): 961-966. [ Links ]
31. JUNK, W.J. 1997. General aspects of floodplain ecology with special reference to Amazonian floodplain. Ecological Studies. 126:3-20. [ Links ]
32. JUNK, W.J. & K.M. WANTZEN. 2003. The flood pulse concept: new aspects, approaches and applications an updates. Proceedings of the Second International Symposium on the Management of Large Rivers for Fisheries: 117-149. [ Links ]
33. JUNK, W.J., M.T.F. PIEDADE, F. WITTMAN, J. SCHONGART & P. Parolin. 2010. Amazonian flood plain forest: ecophysiology, biodiversity and sustainable management (Ecological studies). Springer. 632pp. [ Links ]
34. KIRK, K.L. 1991. Inorganic particles alter composition in grazing plankton: the role of selective feeding. Ecology 72: 915–923. [ Links ]
35. LANSAC-TÔHA, F.A., A.F. LIMA, N.S. HAHN & I.F. ADRIAN. 1991. Composição da dieta alimentar de Hypophthalmus edentatus Spix, 1982 (Pisces, Hypophthalmidae) no reservatório de Itaipu e no rio Ocoí. 1978. Revista Unimar, Maringá 13(2): 147-162. [ Links ]
36. MACEDO, C.F. & R.M. PINTO-COELHO. 2000. Diel variations in respiration, excretion rates and nutritional status of zooplankton from the Pampulha Reservoir, Belo Horizonte, M.G. Journal of Experimental Zoology. 286:671-682. [ Links ]
37. MANGAS, E. & H. GARCÍA. 1991. Seasonal fluctuations of zooplankton biomass in Lake Xólotlan (Managua). Hydrobiological Bulletin 24(2):157-162. [ Links ]
38. MATSUMURA-TUNDISI, T. & J.G. TUNDISI. 2005. Plankton richness in a eutrophic reservoir (Barra Bonita Reservoir, SP, Brazil). Hydrobiologia 542: 367-378. [ Links ]
39. MELLINA, E., J.B. RASMUSSEN & E.L. MILLS. 1995. Impact of Zebra mussels (Dreissena polymorpha) on phytoplankton cycling and chlorophyll in lakes. Canadian Journal of Fisheries and Aquatic Sciences. 52:2553-2579. [ Links ]
40. MIDDLETON, B.A. 1999. Wetland restoration, flood pulsing and disturbance dynamics. John Wiley & Sons, Nueva York. 389pp. [ Links ]
41. MIDDLETON, B.A. 2002. Flood pulsing in wetlands: restoring the natural hydrological balance. John Wiley & Sons, Nueva York. 308pp. [ Links ]
42. MITSCH, W.J. & J.G. GOSSELINK. 2000. Wetlands. Third Edition. John Wiley & Sons, Inc. New Cork. 920pp. [ Links ]
43. MUR, R.L., O.M. SKULBERG & H. UTKILEN. 1999. Cyanobacteria in the Environment. En: I. Chorus. & J. Bartram (ed). Toxic Cyanobacteria in Water: A guide to their public health consequences. St. Edmundsbury Press, Bury St. Edmunds, Suffolk. [ Links ]
44. NEIFF, J.J. 1999. El régimen de pulsos en ríos y grandes humedales de Sudamérica. En: Malvárez, A.I. (ed) Tópicos sobre humedales subtropicales y templados de Sudamérica. Oficina Regional de Ciencia y Tecnología de la UNESCO para América Latina y el Caribe. Montevideo. 229pp. [ Links ]
45. NEIFF, J.J., M.H. IRIONDO & R. CARIGNAN. 1994. Large tropical South American wetlands: a overview. Pp. 156-165. En: R.J. Naiman & H. Decamp (eds). The ecology and management of aquatic-terrestrial ecotones. Man and the biosphere series, vol. 4. The Parthenon Publ. Group Inc., Park Ridge. [ Links ]
46. NEVES, J.F., O. ROCHA, K. ROCHE & A.A. PINTO. 2003. Zooplankton community structure of two marginal lakes of the river Cuiabá (Mato Grosso, Brazil) with analysis of Rotifera and Cladocera diversity. Brazilian Journal of Biology 63(2): 329-343. [ Links ]
47. NOGUEIRA, M.G., R. HENRY & F.E. MARICATTO. 1999. Spatial and temporal heterogeneity in the Jurumirim Reservoir, São Paulo, Brazil. Lakes & Reservoirs: Research and Management. 4: 107–120. [ Links ]
48. OFFICER, C.B., T.J. SMAYDA & R. MANN. 1982. Benthic filter feeding: A natural eutrophication control. Marine Ecology. Progress Series. 9:203-210. [ Links ]
49. PADISÁK, J. 1997. Cylindrospermopsis raciborskii (Woloszynska) Seenayya et Subba Raju, an expanding, hightly adaptive cyanobacterium: worldwide distribution and review of its ecology. Archiv fur Hydrobiologie Supplement 4:563–593. [ Links ]
50. PAERL, H.W. & R.S. FULTON III. 2006. Ecology of harmful cyanobacteria. En: Graneli, E. & J.T. Turner (eds), Ecology of Harmful Algae. Springer-Verlag, Berlin: 95–109. [ Links ]
51. PAGGI, J.C. & S.J. DE PAGGI. 1990. Zooplancton de ambientes lóticos e lênticos do Rio Paraná Médio. Acta Limnologica Brasiliensia 3: 685-719. [ Links ]
52. PINTO-COELHO, R.M. 1987. Fluctuações sazonais e de curta duração na comunidade zooplancônica do lago Paranoá, Brasília-DF, Brasil. Revista Brasilera de Biologia 47(1/2): 17-29. [ Links ]
53. PORTER, K.G. & J.D. ORCUTT JR. 1980. Nutritional adequacy, manageability, and toxicity as factors that determine the food quality of green and blue-green algae for Daphnia. En: Kerfoot, W.C. (ed.), Evolution and Ecology of Zooplankton Communities. University Press of New England, Hanover, NH: 268–281. [ Links ]
54. RAMÍREZ, A. & G. VIÑA. 1998. Limnología Colombiana: Aportes a su conocimiento y estadísticas de análisis. Fundación Universidad de Bogota. Jorge Tadeo Lozano, Bogotá D.C. 294 pp. [ Links ]
55. RAMOS-RODRÍGUEZ, E. & J.M. CONDE-PORCUNA. 2003. Nutrient limitation on a planktonic rotifer: life history consequences and starvation resistance. Limnology and Oceanography 48:933-938. [ Links ]
56. RANGEL-CH, J.O. & H. ARELLANO. 2010. Clima. En: Rangel-Ch., J.O. (ed), Colombia Diversidad Biótica IX: Ciénagas de Córdoba. Biodiversidad, Ecología y Manejo ambiental. Instituto de Ciencias Naturales. Bogotá. 818 pp. [ Links ]
57. REYNOLDS, C.S. 1998. What factors influence the species composition of phytoplankton in lakes of different trophic status?. Hydrobiologia 369/370: 11-26. [ Links ]
58. REYNOLDS, C.S., V. HUSZAR, C. KRUK, L.N. FLORES & S. MELO. 2002. Towards a functional classification of the freshwater phytoplankton. Journal of Plankton Research 24(5): 417-428. [ Links ]
59. RISSER, P.G. 1990. The ecological importance of land-water ecotones. Pages 7-21. In: Naiman, R. J. & H. Decamps. (Eds.). The ecology and management of aquatic-terrestrial ecotones. Man and the biosphere series, vol. 4. The Parthenon Publ. Group Inc., Park Ridge. [ Links ]
60. ROS, J.D. 1979. Prácticas de Ecología. Barcelona: Ediciones Omega, SA. [ Links ]
61. SARTORI, L.P., M.G. NOGEIRA, R.HENRY & E.M. MORETTO. 2009. Zooplankton fluctuations in Jurumirim Reservoir (São Paulo, Brazil): a three-year study. Brazilian Journal of Biology 69(1):1-18. [ Links ]
62. TORRES, G., C. PALACIOS, T. CALDERÓN & S. RECALDE. 2006. Interacción del fitoplancton y zooplancton y sus condiciones oceanográficas durante el verano austral 2004 (Isla Greenwich-Antártica). Revista Tecnológica ESPOL. 19(1):153-160. TUNDISI, J.G. & T. MATSUMURA-TUNDISI. 2008. Limnologia. Oficina de Textos. Sao Paulo. 632pp. [ Links ]
63. URABE, J. 1990. Stable horizontal variation in the zooplankton community structure of a reservoir maintained by predation and competition. Limnology and Oceanography 35: 1703–1717. [ Links ]
64. VASQUEZ, E. & J. REY. 1993. Rotifer and cladoceran zooplankton assemblages in lakes on the Orinoco River floodplain (Venezuela). Verhandlungen Internationale Vereinigung fü r Theoretische und Angewandte Limnologie. 25:912-917. [ Links ]
65. VILLABONA-GONZÁLEZ, S.L., N.J. AGUIRRE-R. & A.L. ESTRADA-P. 2011. Influencia de las macrófitas sobre la estructura poblacional de rotíferos y microcrustáceos en un plano de inundación tropical. Revista de Biología Tropical. 59(2):853-870. [ Links ]
66. WARD, J. V. & J.A. STANFORD. 1995. Ecological connectivity in alluvial river ecosystems and its disruption by flow regulation. Regulated Rivers: Research and Management. 11:105-119. [ Links ]