Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Caldasia
Print version ISSN 0366-5232
Caldasia vol.34 no.2 Bogotá July/Dec. 2012
JOSÉ MONTALVA
BENJAMÍN CASTRO
JUAN LUIS ALLENDES
Instituto de Ecología y Biodiversidad, Facultad de Ciencias, Laboratorio de Sistemática Vegetal, Universidad de Chile, Santiago, Chile. montalva.jose@gmail.com
Facultad de Ciencias, Laboratorio de Ecología Terrestre, Universidad de Chile, Santiago, Chile.
RESUMEN
Se describe por primera vez la biología de nidificación y los estados inmaduros de Megachile semirufa (Hymenoptera: Megachilidae: Dasymegachile) a grandes alturas (3000 m) en el centro de Chile.
Palabras clave. Apoidea, Dasymegachile, Abejas corta hojas, alto andinas, estados inmaduros, Hymenoptera, nidificación, Megachilidae.
ABSTRACT
Nesting biology and immature stages (eggs, larvae predefecant, prepupae and pupae) of M. semirufa are described for first time (Hymenoptera: Megachilidae: Dasymegachile) from high altitudes (3000 m) in Central Chile.
Key words. Apoidea, Dasymegachile, leafcutter bees, high Andean, Hymenoptera, immature stages, nesting, Megachilidae.
Recibido: 14/07/2011
Aceptado: 08/06/2012
INTRODUCCIÓN
El género Megachile se distribuye en todo el mundo presentando más de 1500 especies descritas (Raw 2007, Michener 2007). Estas abejas se caracterizan por ser solitarias, tener escopa ventral bien desarrollada, la cabeza grande, con mandíbulas de bordes agudos, las cuales utilizan para cortar hojas y/o pétalos de plantas, que usan en la construcción de las celdas (Stephen et al. 1969, King 1984, Williams et al. 1986, Rozen 1987, Genaro 1996, Paini 2004, Michener 2007, Rozen & Soliman 2007). Este grupo también presenta una relativa importancia, porque algunas especies aceptan nidos artificiales y han sido empleadas como polinizadores de plantas de interés agrícola (King 1984, Durante et al. 2006). Dentro del género se encuentra el subgénero Dasymegachile, el cual posee alrededor de 20 especies descritas, distribuidas principalmente en el extremo sur del cordón montañoso de los Andes, abarcando los países de Argentina, Bolivia, Chile y Perú (Durante et al. 2006). Recientemente Durante et al. (2006) hicieron una revisión taxonómica del grupo, aportando también datos de distribución de las especies descritas. La biología de estas abejas es poco conocida; los únicos antecedentes existentes son para la especie Megachile saulcyi Guérin-Menéville, 1844 (Claude 1926, Michener 1953).
En el presente trabajo estudiamos la biología de nidificación y describimos los estados inmaduros de Megachile semirufa Sichel, 1867, una especie nativa de Chile y Argentina que se encuentra desde los 35°S a los 51°S, asociada principalmente a zonas de alta-montaña (Toro 1986, Durante & Abrahamovich 2003, Durante et al. 2006).
MATERIALES Y MÉTODOS
La recolección de las muestras se realizó entre los meses de enero y mayo del año 2008 y febrero del 2009 en el sector de La Parva ubicada entre los 3000 y 3400 m.s.n.m. (33° 19' Sur; 70° 16' Oeste) a 70 kilómetros al este de Santiago (Figura 1). El sector se caracteriza por poseer un clima de alta montaña con precipitaciones en forma de nieve (400-900 mm) durante los meses de invierno, la temperatura media anual bordea los 3° C y durante los meses de verano las temperaturas medias bordean los 7° C. Las muestras se separaron por nido en bolsas plásticas y se llevaron al laboratorio, en donde fueron observadas bajo microscopio estereoscópico, midiéndose el largo y el diámetro de las celdas, el diámetro de los opérculos de cada celda, el largo y el diámetro de los capullos y la longitud de los estados inmaduros.
Los caracteres y la terminología utilizada en la descripción de los estados inmaduros está basada en las propuestas de Stephen et al. (1969), King (1984), Mcginley (1989), Michener (1953, 1954, 2007) y Rozen & Soliman (2007). Los ejemplares fueron depositados en la Colección del Museo Nacional de Historia Natural (Chile), en la Colección del Instituto de Entomología de la Universidad Metropolitana de Ciencias de la Educación (Chile) y en la colección personal del primer autor (JM).
RESULTADOS
Área de nidificación
El sitio de nidificación se disponía en formaciones aisladas, siendo abejas completamente solitarias. Los nidos se formaban en hileras de celdas; a diferencia de lo que se ha descrito para otras especies chilenas del género M. semirufa no utiliza ni galerías abandonadas por otros insectos, ni construye sus propias galerías. Sus nidos se disponían principalmente bajo rocas planas, las cuales quedaban bajo una capa de nieve durante el invierno.
Celdas: estructura de forma cilíndrica, terminada con la base redondeada, ápice truncado con una longitud x = 15 ± 1,3 mm; (n = 42) y un diámetro de x = 7,4 ± 0,7 mm (n=42). Presenta opérculo, el cual es casi plano, pero con una leve curvatura hacia el interior, éste se encontraba constituído por una agregación de entre tres a cinco hojas de forma circular cuyo diámetro es de x = 8 ± 0,04 mm (n=32). Las celdas están compuestas solamente por hojas, a diferencia de otras especies del género las cuales también utilizan pétalos, éstas se encuentran cortadas y sobrepuestas, levemente sedimentadas. Su orientación es paralela a las rocas y su disposición es en tándem de cuatro a seis celdas unidas.
Descripción de los estados inmaduros
Huevo (Fig. 2) Aspecto general: Presenta una forma cilindro ovalada levemente curvado cuyo largo es x = 3,5±0,5mm (n= 4), de color blanquecino semitransparente. El huevo se encontraba insertado diagonalmente en la masa de polen en la periferia de la celdilla y se disponía hacia el centro de ésta.
Descripción de las larvas
Fueron identificados tres diferentes estadios larvales, que presentaban diferencias en la morfología y en la disposición que presentaban éstas dentro de la celdilla.
Primer estadio larval (Fig. 3) Aspecto general: Cuerpo vermiforme, ápoda y flácida de x = 4,9±0,3 mm de longitud (n=12). Tegumento semitransparente, con bajo grado de esclerotización, al igual que el aparato bucal. Los individuos en esta etapa se ubican sobre la masa de polen, con la sección anterior de su cuerpo introducida en el recurso. Es posible distinguir presencia de polen al interior de los individuos.
Larva pre-defecante (Fig. 4) Aspecto general: Cuerpo eruciforme ápodo y de contextura turgente de x = 8,8±0,2 mm de longitud (n=24). Cuerpo claramente segmentado. Aparato bucal desarrollado, apertura del salivario esclerotizada. Mandíbulas esclerotizadas. Las larvas en este estadio se encontraron con la región anterior apuntando hacia la base de la celdilla (contra opérculo). Junto a ellas se encontraban resto del recurso alimenticio.
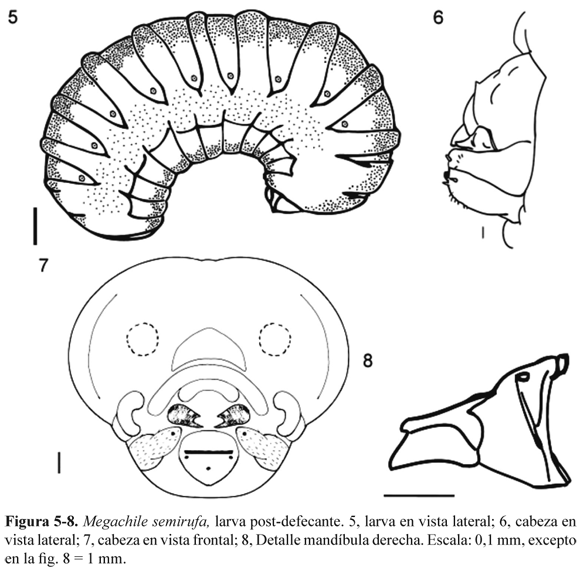
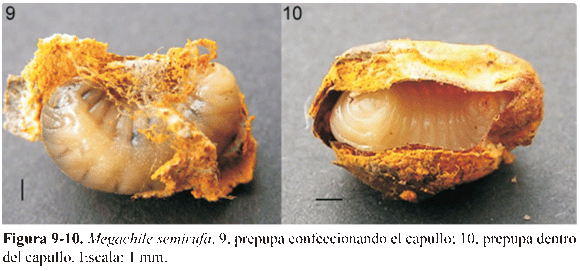
Larva Post-defecante o prepupa (Fig. 5-10). Aspecto general: Cuerpo eruciforme, ápodo y flácido de x = 9,4±0,2 mm de longitud (n=32), con protuberancias dorsolaterales, ventrolaterales y líneas intrasegmentales marcadas, las cuales se van pronunciando progresivamente a medida que se acerca la pupación; ausencia de tubérculos. La coloración varía de blanquecina a marrón. Presentan diez pares de espiráculos, de tamaño moderado, levemente pigmentados, los cuales se ubican en cada segmento, todo el tegumento posee abundantes setas pequeñas a excepción de la cabeza. Ano ubicado en la porción media del último segmento.
Cabeza: (Fig.6-7) Forma acorazonada, claramente mucho más angosta a la altura de las articulaciones mandibulares, pequeño tamaño en comparación al cuerpo 1,4 ± 0,15 mm de largo (n=9) por 1,7 ± 0,16 mm de diámetro (n=9), coloración blanco amarillenta, levemente esclerotizada. Prognata, alveólos antenales ubicados sobre la línea media superior de la cara, bandas parietales marcadas, ocelos ausentes, ojos compuestos muy levemente marcados, papila antenal poco pronunciada, labro poco desarrollado, sutura epistomal visible, clípeo cóncavo de lados convergentes hacia el extremo distal; mandíbula moderadamente corta, robusta, bidentada, diente externo más largo que el interno (Fig. 8), fuertemente esclerotizadas, de color café oscuro; apertura del salivario esclerotizada, transversal y muy amplia; palpos labiales y maxilares escasamente esbozados (Fig. 6, 7). Las maxilas densamente espiculadas. Presencia de protuberancia bajo la apertura del salivario.
La disposición de los individuos en esta etapa del desarrollo es con la cabeza hacia el opérculo.
Capullo. Aspecto general: Estructura ovoide, extremadamente coriácea, de color café. Longitud 12±1,1 mm (n= 50) diámetro 6,2 ± 0,6 mm (n= 50), el cual está compuesto de muchas capas de seda (Fig. 10). El capullo generalmente se encuentra rodeado por polen residual y las heces producidas por la larva. Los desechos se encuentran en mayor abundancia en las regiones cercanas al opérculo y disminuye a medida en que el espacio entre el capullo y la pared de la celdilla es menor.
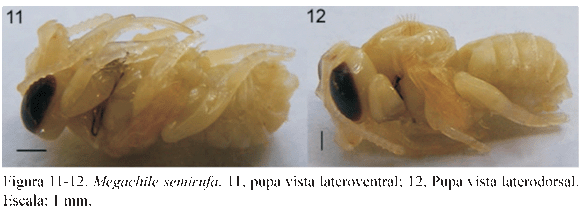
Pupa (Fig.11, 12). Se obtuvo un individuo en estado de pupa a partir de la crianza de larvas en condiciones ambientales. La pupa correspondió a un macho de coloración amarilla pálida de 11mm de longitud corporal. Presencia del pupario; esbozos alares cubiertos por el pupario al igual que los tres pares de patas. Mesosoma presenta pilosidad anaranjada incipiente. Metasoma con bandas de pelos anaranjados en la zona distal de los tergos I-V. Espinas alargadas en el interior de todas las coxas. Espiráculos conspicuos esclerosados de coloración café.
Cabeza: acorazonada, vértex con tubérculos al costado de los ocelos; ojos compuestos café; antenas desarrolladas; glosa desarrollada.
DISCUSIÓN
El estudio de la nidificación en abejas resulta relevante para la comprensión de la biología e historia natural de las especies estudiadas. En este sentido, el presente estudio contribuye a la comprensión de la nidificación en el grupo Dasymegachile, el cuál contaba con pocos antecedentes (Claude 1926, Michener 1953). Claude Joseph en su trabajo "Investigaciones biológicas sobre los Himenópteros de Chile" (1926) describe la biología de nidificación de M. saulcyi, siendo hasta ahora la única especie del subgénero estudiada (Claude 1926, Michener 1953). Uno de los aspectos relevantes de la biología de nidificación de M. saulcyi, es que esta especie usa galerías en el suelo o en murallas, además de reutilizar nidos abandonados de Sphecidos y Eumenidos (Claude 1926, Michener 1953, Raw 2007), esto difiere de lo que hemos descrito para M. semirufa en el presente trabajo. En el aspecto ecológico, son escasos los estudios que han abordado el tema de nidificación en abejas en ambientes altoandinos (Chiappa & Castro 2006, González & Chávez 2004). La forma en la cual nidifica M. semirufa en la zona estudiada podría deberse a una adaptación específica a este ambiente. De acuerdo a Mani (1968) microambientes bajo rocas generan condiciones de humedad y poca variación en la temperatura, lo cual se presenta como un refugio para insectos de alta montaña, lo que podría estar asociado a la elección del sitio de nidificación por parte de la abeja.
Es necesario dejar claro que M. semirufa presenta una amplia distribución en el sur de Sudamérica. El presente estudio está restringido a la localidad de La Parva, por lo que no se descarta que pueda existir variación en los rasgos estudiados, especialmente los de carácter ecológico, entre diferentes poblaciones de la especie.
AGRADECIMIENTOS
Al Dr. Víctor González (USDA, Utah State University, USA) y a los revisores anónimos que nos aportaron valiosas sugerencias y comentarios al manuscrito. También agradecemos a Cristhopher Guerra y Leah S. Dudley por su ayuda en los trabajos de campo.
LITERATURA CITADA
1. Chiappa, E. & R. Castro. 2006 Comportamiento de nidificación comunal y de abastecimiento de Protandrena evansi Ruz y Chiappa (Hymenoptera: Adrenidae: Panurginae) en Farellones, Región Metropolitana, Chile. Acta Entomológica Chilena 30: 7-14. [ Links ]
2. Claude, J.F. 1926. Recherches biologiques sur les Hyménoptères du Chile (Melliferes). Annales des Sciences Naturelles, Zoologie 9: 114-268. [ Links ]
3. Durante, S.P. & A.H. Abrahamovich. 2003. Megachile (D.) semirufa Sichel (Hymenoptera, Megachilidae): Redescription and first Argentinean records. Transactions of the American Entomological Society129: 309-314. [ Links ]
4. Durante, S.P, A.H. Abrahamovich & M. Lucia. 2006. El subgénero Megachile (Dasymegachile) Mitchell con especial referencia a las especies Argentinas (Hymenoptera: Megachile). Neotropical Entomology 35:791-802. [ Links ]
5. Genaro, J.A. 1996. Plantas usadas por abejas del género Megachile para construir las celdillas de sus nidos (Hymenoptera: Megachilidae). Caribbean Journal of Science 32: 365-368. [ Links ]
6. González, V.H. & F. Chávez. 2004. Nesting Biology of a New High Andean Bee, Anthophora walteri Gonzalez (Hymenoptera: Apidae: Anthophorini). Journal of the Kansas Entomological Society 77 (4): 584-592. [ Links ]
7. King, J. 1984. Inmature stages of some Megachilidae (Hymenoptera: Apoidea). Journal of the Australian Entomological Society 23: 51-57. [ Links ]
8. Mani, M.S. 1968. Ecology and biogeography of high altitude insects. The Hague. Nevada. [ Links ]
9. McGinley, R.J. 1989. A catalog and review of immature Apoidea (Hymenoptera). Smithsonian Contribution Zoology. Washington DC. [ Links ]
10. Michener, C. 1953. Comparative morphological and systematic studies of bee larvae with a key to the families of hymenopterous larvae. University Kansas Science Bulletin 35: 987-1102. [ Links ]
11. Michener, C. 1954. Observations on the pupae of bees. Pan-Pacific Entomologist 30: 63-70. [ Links ]
12. Michener, C. 2007. The Bees of the World. Johns Hopkins University Press, Baltimore MD, 2nd Edition. [ Links ]
13. Paini, D. 2004. Nesting biology of an Australian resin bee (Megachile sp.; Hymenoptera: Megachilidae): a study using trap nests. Australian Journal of Entomology 43:10-15. [ Links ]
14. Raw, A. 2007. An Annotated Catalogue of the Leafcutter and Mason Bees (Genus Megachile) of the Neotropics. Zootaxa 1601: 1-127. [ Links ]
15. Rozen, J. 1987. Nesting Biology of the Bee Ashmeadiella holtil and Its Cleptoparasite, a New Species of Stelis (Apoidea: Megachilidae). American Museum Novitates 2900:1-10. [ Links ]
16. Rozen, J. & M. Soliman. 2007. Investigations on the biologies and immature stages of the cleptoparasitic bee genera Radoszkowskiana and Coelioxys and their Megachile hosts (Hymenoptera, Apoidea, Megachilidae, Megachilini). American Museum Novitates. 3573: 1-43. [ Links ]
17. Stephen, W.P., G.E. Bohart & P.F. Torchio. 1969. The biology and external morphology of bees. Oregon State University Agricultural Experiment Station. [ Links ]
18. Toro, H. 1986. Lista preliminar de los ápidos chilenos. (Hymenoptera: Apoidea). Acta Entomológica Chilena 13:121-132. [ Links ]
19. Williams, H.J., M.R. Strand, S.B. Vinson, G.W. Elzen & S.J. Merritt. 1986. Nesting behavior, nest architecture, and use of Dufour's gland lipids in nest provisioning by Megachile integra and M. mendica mendica. Journal of the Kansas Entomological Society 59:588-597. [ Links ]