Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista de la Academia Colombiana de Ciencias Exactas, Físicas y Naturales
Print version ISSN 0370-3908
Rev. acad. colomb. cienc. exact. fis. nat. vol.35 no.134 Bogotá Jan./Mar. 2011
ZOOLOGÍA
1 Grupo de Herpetología, Eco-Fisiología & Etología, Departamento de Biología. Universidad del Tolima. Ibagué, Colombia. Correo electrónico: marceh415@hotmail.com
2 Grupo de Herpetología, Eco-Fisiología & Etología, Departamento de Biología. Universidad del Tolima. Ibagué, Colombia. Correo electrónico: mhbernal@ut.edu.co
Resumen
Este trabajo evalua la tolerancia al pH del agua en embriones y renacuajos de cuatro especies de anuros Colombianos bajo condiciones de laboratorio. De acuerdo con los valores DL50, E. pustulosus fue la especie más sensible para sustancias básicas como ácidas, mientras que R. granulosa fue la más tolerante a sustancias ácidas y R. marina a las sustancias básicas. H. crepitans presentó tolerancias intermedias al pH. Entre los embriones y renacuajos no se encontró una diferencia significativa en la respuesta al pH, pero en todas las especies hubo una mayor tolerancia al hidróxido de sodio y al ácido clorhídrico en comparación con el hidróxido de amonio y el ácido acético, respectivamente.
Palabras clave: Anuros, embriones, renacuajos, pH, tolerancia, DL50.
Abstract
In this work we evaluated the aquatic pH tolerance of embryos and tadpoles of four anuran Colombian species under laboratory conditions. According to the LC50 values, E. pustulosus was the most sensitive species to acid and basic pH while R. granulosa was the most tolerant to acid and R. marina to basic pH. H. crepitans had an intermediate pH tolerance. We did not find a significant difference in the pH tolerance between embryos and tadpoles but they were always more tolerant to hydrochloric acid and sodium hydroxide than acetic acid and ammonium hydroxide, respectively.
Key words: Anurans, embryos, tadpoles, pH, tolerance, LC50.
Introducción
La extinción y el declive de las poblaciones de anfibios es actualmente un fenómeno bien conocido (Blaustein & Wake, 1990; Stuart et al. 2004; Wake & Vredenburg, 2008). La alteración del hábitat, la contaminación ambiental y la aparición de enfermedades infecciosas están entre las causas más importantes de esta disminución (Young et al., 2004). Sin embargo, los cambios en el pH del medio acuático donde se reproducen y desarrollan la mayoría de los anfibios también han sido considerados como un posible factor contribuyente a esta problemática (Freda, 1986).
Cambios en el pH de las aguas pueden ser generados por diversas sustancias agrícolas, industriales y domésticas. Incluso, compuestos presentes en el aire como el dióxido de azufre pueden constituirse en contaminantes del agua a través de su precipitación en forma de lluvia ácida (Battarbee, 1991). Existe numerosa documentación internacional, y hasta el momento ninguna en Colombia, en donde se ha estudiado el efecto del pH sobre la sobrevivencia de los anfibios. Por ejemplo, los efectos letales y subletales de pH ácidos sobre los anfibios han sido resumidos por Freda (1986) y Pierce (1985). En estos trabajos se ha mencionado que la disminución de las poblaciones de anfibios en Europa y Norteamérica es en gran parte debida a la contaminación ácida de los cuerpos de agua. Por otra parte, en Rusia se han reportado pH básicos de 9.5 en cuerpos de agua cercanos a vertimientos industriales y a estos cambios del pH se les ha atribuido la altas mortalidades de los anfibios de estas zonas (Fominykh, 2008). Adicional a estos efectos letales, también se han reportado efectos subletales de la acidez sobre los embriones y larvas de anfibios, principalmente afectando su desarrollo embrionario, crecimiento, habilidad de forrajeo o de evadir predadores (Pierce, 1985).
Los anfibios son organismos que se caracterizan por su dependencia de los cuerpos de agua, por tener un ciclo de vida complejo, y por poseer una gran sensibilidad fisiológica ante las condiciones ambientales (Duellman & Trueb, 1994). Todos estos factores hacen que sean uno de los grupos más afectados por las alteraciones de su entorno y, en consecuencia, son considerados como importantes bio-indicadores ambientales (Wells, 2007). Sin embargo, diferentes especies parecen ser más sensibles que otras ante los cambios del entorno, como los generados por el pH, e incluso entre diferentes estadios de desarrollo (Grant & Licht, 1993; Green & Peloquin, 2008), ya que se ha encontrado que los embriones son más sensibles al pH que las larvas (Pierce, 1985), aunque estos datos deben ser confirmados con más especies. Por lo tanto, en este trabajo se reporta la tolerancia de embriones y renacuajos de cuatro especies de anuros colombianos al ser expuestos a cambios en el pH ácido y básico del agua donde se desarrollan y se compara su tolerancia de acuerdo con su estadio de desarrollo.
Materiales y métodos
Las especies sometidas a experimentación en este trabajo fueron: Hypsiboas crepitans (Wied-Neuwied, 1824), Engystomops pustulosus (Cope, 1864), Rhinella marina (Linneaus, 1758) y Rhinella granulosa (Spix, 1824). Los embriones de estas especies se colectaron en diferentes sitios en el departamento del Tolima: Hypsiboas crepitans y Engystomops pustulosus en la vereda Potrerillo, municipio de Coello, Rhinella marina en el corregimiento de Payandé, municipio de San Luis, y Rhinella granulosa en el municipio de Ibagué. En cada una de las zonas muestreadas se registró el nivel de oxígeno, con un oxímetro portátil (Hanna HI 8043), y la temperatura y el pH de las aguas con un medidor portátil de pH y temperatura (Hanna HI 8314). La temperatura en campo durante las horas de muestreo presentó un promedio de 24°C, un nivel de oxígeno de 6,62 mg/L y un pH entre 6,0 y 8,05.
Durante las salidas de campo se colectaron entre dos y tres posturas por cada especie, las cuales fueron transportadas al laboratorio de Herpetología de la Universidad del Tolima. Allí, con la ayuda de un estereoscopio ZOOM 2000 (Leyca) se observó el estadío de los embriones, para iniciar los experimentos con embriones en estadio 10 y renacuajos en estadio 25, según la clasificación hecha por Gosner (1960).
Para las pruebas de tolerancia al pH, diez embriones y diez renacuajos de cada especie fueron expuestos separadamente, con su réplica, a cada uno de cuatro tratamientos de pH ácidos y básicos, más el control (agua), en recipientes de vidrio de 2-L, con un litro de agua previamente declorada por aireación. Los tratamientos con el pH ácido fueron: 3,5, 4,5, 5,5 y 6,5, ajustados con ácido clorhídrico (HCl), para una serie de experimentos, y con ácido acético (CH3COOH), para otra serie de experimentos; los pH básicos fueron: 8,5, 9,5, 10,5 y 11,5 ajustados con hidróxido de sodio (NaOH) e hidróxido de amonio (NH4OH) para las dos series de experimentos. Estas sustancias químicas fueron escogidas por su uso común doméstico e industrial y porque han sido generalmente utilizadas en trabajos sobre la tolerancia al pH en anfibios. El agua de los recipientes de vidrio fue renovada cada 24 horas y el pH fue ajustado cada doce horas para mantenerlo dentro de un rango de variación de 1,0. Los experimentos se realizaron en un salón del laboratorio con aire acondicionado a una temperatura promedio de 24.26°C, y un régimen de 12:12 horas luz-oscuridad controlada con un temporizador. El nivel promedio de oxígeno en los tratamientos fue de 7,36 mg/L. Durante el tiempo de experimentación los individuos no fueron alimentados. Las observaciones generales y el registro de los datos de mortalidad se llevaron a cabo a las 12, 24, 36 y 48 horas una vez iniciada las pruebas. A las 48 horas se terminaron los experimentos y se determinó la tolerancia al és del índice de la dosis medial letal (DL50).
Análisis estadístico
Para el análisis de los datos se utilizó el programa estadístico Probit (Versión 1.5 SAS Institute), mediante el cual se obtuvo la dosis media letal (DL50) y los intervalos de confianza al 95%. La dosis media letal es el valor estimado de letalidad del 50% de los animales expuestos a los tratamientos. También, se utilizó la prueba pareada de Wilcoxon (Zar, 1996) para comparar en cada especie los valores DL50 entre los embriones y renacuajos (comparación ontogénica) expuestos separadamente tanto a pH ácidos como básicos. Igualmente, se utilizó esta prueba para comparar pareadamente en los embriones y renacuajos de cada especie la respuesta entre los ácidos acético y clorhídrico, y óxido de sodio e hidróxido de amonio.
Resultados
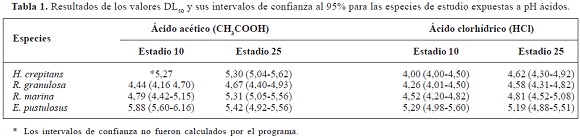
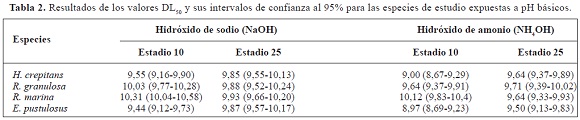
Las cuatro especies de estudio presentaron rangos de tolerancia a pH ácidos, DL50, entre 4,0 y 5,88; y para pH básicos entre 8,97 y 10,31 (Figuras 1 y 2). De acuerdo con los valores DL50, E. pustulosus fue la especie más sensible a los cambios del pH, tanto para sustancias básicas como ácidas (Tablas 1 y 2), mientras que R. granulosa fue la más tolerante frente a sustancias ácidas y R. marina ante sustancias básicas. Por su parte, los intervalos de confianza al 95% (p < 0,05) muestran que sólo los embriones de E. pustulosus fueron más sensibles que los embriones de las otras especies ante las dos sustancias ácidas (ácido clorhídrico y ácido acético) y que los embriones de R. marina y R. granulosa ante las dos sustancias básicas (hidróxido de sodio e hidróxido de amonio) (Tablas 1 y 2).
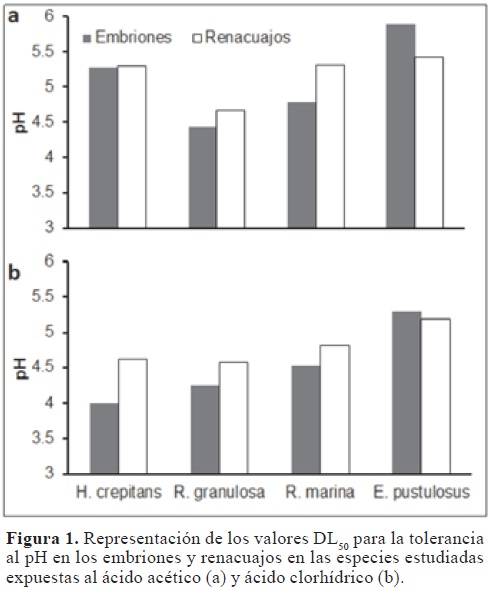
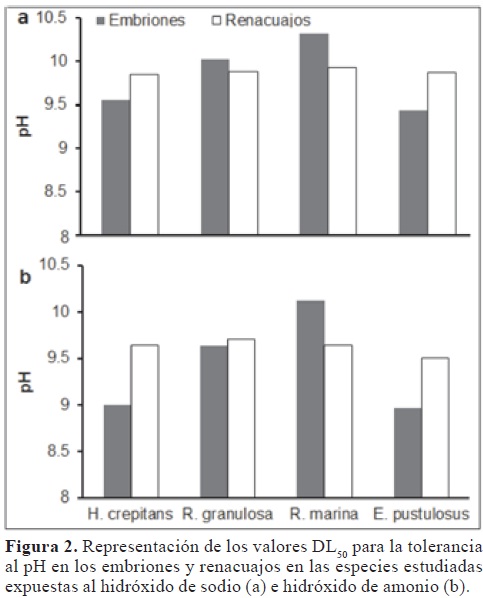
Contrastando los valores DL50 entre los embriones y los renacuajos (comparación ontogénica), con respecto de las sustancias ácidas y básicas, independientemente, no se encontró una diferencia significativa (Prueba de Wilcoxon, P > 0,05, para todos los casos). Pero interesantemente, en los embriones y renacuajos de todas las especies se observó una mayor tolerancia al hidróxido de sodio y al ácido clorhídrico, en comparación con el hidróxido de amonio y ácido acético, respectivamente (Prueba de Wilcoxon, P < 0,05, para todos los casos). Como observaciones generales se detectó que los embriones y renacuajos expuestos a pH extremos, tanto ácidos como básicos, presentaban rápidamente el desprendimiento de sus membranas externas y una muerte repentina. También, se observó un retraso en el desarrollo de los embriones y nados erráticos en los renacuajos que sobrevivieron al ser expuestos a pH menores a 5,5 o mayores a 7,5. Finalmente, los embriones y renacuajos expuestos a un pH que no generaron malformaciones aparentes continuaron su desarrollo normal, de acuerdo con las observaciones que se les siguió hasta quince días después
Discusión
Los anfibios se caracterizan por su gran sensibilidad ante las condiciones ambientales. También, porque la mayoría de las especies dependen de fuentes de agua para la reproducción y el desarrollo de sus embriones y renacuajos. Así, las variables que afecten estos cuerpos de agua pueden ser críticas para la sobrevivencia de los anfibios, particularmente en sus primeros estadíos de desarrollo (Duellman & Trueb, 1994; Wells, 2007). En este trabajo se comprueba que los cambios drásticos y repentinos en el pH del agua pueden generar altas mortalidades en los anuros, en tanto que cambios leves (no muy lejanos al pH neutro) pueden generar efectos subletales como anormalidades embrionarias, retrasos en el desarrollo embrionario, provocar malformaciones y nados erráticos en los renacuajos, lo que posteriormente puede reflejarse en mortalidades.
Entre las cuatro especies de estudio se observó que los embriones de E. pustulosus fueron los más sensibles a los cambios en el pH (Tablas 1 y 2). Luego, de manera general, le siguió H. crepitans y finalmente R. marina y R. granulosa. Rasanen et al. (2003) afirman que los diferentes rangos de tolerancia a pH ácidos se pueden explicar por la variación en la estructura y composición de las cápsulas de los huevos. Esto podría estar en concordancia con nuestros resultados en el sentido que las especies con una membrana externa protectora alrededor de sus huevos, tales como R. marina y R. granulosa, fueron más tolerantes al pH en comparación con H. crepitans y E. pustulosus, cuya capa protectora embrionaria es mucho más delgada. Particularmente, los huevos H. crepitans son puestos sobre la superficie del agua a manera de una película delgada, mientras que los de E. pustulosus son protegidos por un nido de espuma (Duellman & Trueb, 1994), el cual fue removido durante los experimentos de este trabajo.
En las cuatro especies de estudio los valores DL50 para los dos estadios ontogénicos comparados intra-específicamente, embriones Vs renacuajos, fueron ligeramente diferentes y contradictorios. Trabajos previos han reportado que los anuros en los primeros estadios de desarrollo embrionario son más sensibles ante los cambios del pH del agua circundante que en una etapa tardía o larvaria (Freda, 1991). Sin embargo, nuestros resultados no concuerdan con estos reportes. Es posible que esta diferencia se pueda deber a alguna variación inter-especifica, atribuida a la capacidad de las especies en cada estadío ontogénico para regular la pérdida de iones a través de la membrana celular (Frisbie & Wyman, 1992; Lehtinen & Skinner, 2006). Así, dado que los embriones de E. pustulosus fueron los más sensibles a los cambios en el pH, queda por establecer si hay alguna correlación entre esta sensibilidad y la capacidad de regulación iónica de acuerdo con el modo reproductivo y la calidad del agua donde se reproducen las especies de anfibios.
Los renacuajos de las cuatro especies expuestas a diferentes rangos de pH y que lograron sobrevivir presentaron un desarrollo posterior normal. Esto concuerda con otros estudios en anfibios que muestran que los renacuajos expuestos a pH ácidos no letales son capaces de alcanzar su metamorfosis (Freda, 1991). Sin embargo, Brady & Griffiths (1995), también han demostrado que los embriones de las salamandras Triturus helveticus y Triturus vulgaris incubados bajo condiciones de acidez (pH 5,5) presentan un desarrollo más lento. Nuestras observaciones en los embriones expuestos a condiciones de acidez cercanas a la DL50 mostraron esta misma tendencia, pero dado que no se cuantificó esta información es un trabajo que queda por realizar, incluyendo el estudio de otros efectos subletales, tales como la capacidad de desempeño locomotor en renacuajos y los efectos sobre su tamaño y tasa de crecimiento. Freda & Dunson (1984), trabajando con renacuajos, indican que la exposición a pH ácidos letales (2,5-3,5) provoca la pérdida excesiva de iones de sodio y cloro, y que la muerte se produce cuando los niveles de sodio alcanzan el 50% de su contenido inicial. Para el caso de los embriones, se considera que la muerte a pH bajos se debe principalmente a un efecto selectivo que conduce a la constricción de las membranas extraembrionarias (Dunson & Connell, 1982).
En este estudio se utilizaron cuatro compuestos químicos (dos básicos y dos ácidos) para mantener los valores de los pH experimentales. Estos compuestos son ampliamente usados a nivel industrial y doméstico, y fácilmente pueden llegar directa o indirectamente a los cuerpos de agua donde se reproducen los anuros y desarrollan sus embriones. Para las sustancias básicas se empleó hidróxido de sodio, correspondiente a una base fuerte, e hidróxido de amonio, como una base débil. Interesantemente, durante los experimentos con estas sustancias, se encontró que los embriones y renacuajos de las cuatro especies en todos los casos presentaron una mayor tolerancia al hidróxido de sodio que al hidróxido de amonio, e igualmente una mayor tolerancia al ácido clorhídrico en comparación con el ácido acético (Figuras 1 y 2). Por lo tanto, los cambios en el pH de las aguas tienen un efecto letal sobre los anuros, pero la tolerancia al pH puede estar estrechamente ligada con la naturaleza química del ácido o la base y, en este trabajo, los ácidos y bases débiles fueron más letales que los ácidos y bases fuertes a un mismo valor de pH. Así, estos resultados abren la posibilidad de realizar más experimentos con otras sustancias químicas y especies, para verificar en que medida la tolerancia a un determinado pH depende del tipo de la sustancia química que lo genere y cuál es la sensibilidad de los anfibios antes estas sustancias. Esto podría resultar de mucho interés para la comunidad científica, ya que hay numerosos trabajos en los que se reportan los efectos independientes e interactivos del pH con otros factores ambientales y cuyos resultados podrían ser diferentes de acuerdo con la sustancia química que se utilice para mantener los pH experimentales.
Agradecimientos
A Ana María Leiva, Mónica Gutiérrez, Angélica Beltrán y Gloria Palma, por el apoyo en el desarrollo de esta investigación. Este trabajo fue parcialmente patrocinado por el fondo de investigaciones de la Universidad del Tolima a través del proyecto 120107.
Bibliografía
Battarbee, R. W. 1991. Acid-rain and acid waters. Nature 350:285- 285. [ Links ]
Blaustein, A. R. & Wake, D. B. 1990. Declining amphibian populations: A global phenomenon. Trends in Ecology and Evolution 5:203-204. [ Links ]
Brady, L. D. & Griffiths, R. A. 1995. Effects of pH and aluminium on the growth and feeding behaviour of smooth and palmate newt larvae. Ecotoxicology 4:299-306. [ Links ]
Dunson, W. A. & Connell, J. 1982. Specific inhibition of hatching in amphibian embryos at low pH. Journal of Herpetology 16:314-316. [ Links ]
Duellman, W. E. & Trueb, L. 1994. Biology of Amphibians. Johns Hopkins University Press. Baltimore. [ Links ]
Freda, J. 1986. The influence of acidic pond water on Amphibians - A Review. Water Air and Soil Pollution 30:439-450. [ Links ]
_____. 1991. Long-term monitoring of amphibian populations with respect to the effects of acid deposition. Water, Air and Soil pollution 55:445-462. [ Links ]
_____ & Dunson, W.A. 1984. Sodium balance of amphibian larvae exposed to low environmental pH. Physiological Zoology 57:435-443. [ Links ]
Frisbie, M. P. & Wyman, R. L. 1992. The effect of environmental pH on sodium balance in the red-spotted newt, Notophthalmus viridescens. Archives of Environmental Contamination and Toxicology 23:64-68. [ Links ]
Fominykh, A. S. 2008. An Experimental Study on the Effect of Alkaline Water pH on the Dynamics of Amphibian Larval Development. Russian Journal of Ecology 39:145-147. [ Links ]
Grant, K. & Licht L. 1993. Acid tolerance of anuran embryos and larvae from Central Ontario. Journal of Herpetology 27:1-6. [ Links ]
Green L. & J. E. Peloquin. 2008. Acute toxicity of acidity in larvae and adults of four stream salamander species (Plethodontidae). Environmental Toxicology and Chemistry 27:2361-2367. [ Links ]
Gosner, K. L. 1960. A simplified table for staging anuran embryos and larvae with notes on identification. Herpetologica 16:183- 190. [ Links ]
Lehtinen R. & Skinner, A. 2006. The enigmatic decline of Blanchard's Cricket Frog (Acris crepitans Blanchardi): A test of the habitat acidification hypothesis. Copeia pp. 159-167. [ Links ]
Pierce, B. A. 1985. Acid tolerance in Amphibians. Bioscience 35:239-243. [ Links ]
Rasanen, K., Laurila A. & Merila, J. 2003. Geographic variation in acid stress tolerance of the moor frog, Rana arvalis. II. Adaptive maternal effects. Evolution 57:363-371. [ Links ]
Stuart, S. N., Chanson, J. S., Cox, N. A., Young, B. E., Rodriguez, A. S. L. , Fischman, D. L. & Walter, R. W. 2004. Status and trends of amphibian declines and extinctions worldwide. Science 306:1783-1786. [ Links ]
Wake, D. B. & Vredenburg, V. T. 2008. Are we in midst of the sixth mass extinction?. A view from the world of amphibians. Proceedings of the National Academy of Sciences 105:11466-11473. [ Links ]
Young, B. E., Stuart, S.N. , Chanson, J. S., Cox, N. A. & Boucher, T. M. 2004. Disappearing Jewels. The status of new world amphibians. Arlington, V.A: Natureserve. [ Links ]
Wells, K. D. 2007. The Ecology and Behavior of Amphibians. The University of Chicago Press. Chicago. [ Links ]
Zar, J. H. 1996. Biostatistical Analysis, 3rd edition. Prentice Hall. New Jersey. [ Links ]
Recibido: febrero 10 de 2011. Aceptado para su publicación: febrero 28 de 2011.













