Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista de la Academia Colombiana de Ciencias Exactas, Físicas y Naturales
Print version ISSN 0370-3908
Rev. acad. colomb. cienc. exact. fis. nat. vol.35 no.136 Bogotá July/Sept. 2011
QUÍMICA ANALÍTICA
1 Departamento de Química, Facultad de Ciencias, Universidad Nacional de Colombia. A.A. 14490. Bogotá-Colombia.
2Departamento de Ingeniería Química, Facultad de Ingeniería, Universidad Nacional de Colombia, Bogotá-Colombia.
3 Departamento de Química, Universidad de los Andes, Bogotá-Colombia.
*Autor que recibirá la correspondencia. Tel.: 3165000 Ext. 14448. Fax: 3165220. Correo electrónico:fparadaa@unal.edu.co.
Resumen
Mediante extracción con fluidos supercríticos-EFS se obtuvieron extractos de rizomas de jengibre (Zingiber officinale), con CO2 a diferentes condiciones de presión y temperatura. Adicionalmente, mediante extracción soxhlet se obtuvieron extractos lipofílicos. Los rendimientos de extracción fueron determinados y los extractos obtenidos se analizaron mediante cromatografía de gases acoplada a espectrometría de masas (CG-EM). La EFS permitió obtener extractos libres de solvente, alcanzando un rendimiento de 1.51% a 17.9 MPa y 40 ºC. por CG-EM se lograron identificar más de treinta componentes presentes en los extractos, algunos de los cuales le imparten el aroma característico al jengibre y poseen importantes tipos de actividad biológica.
Palabras clave: extracción con fluidos supercríticos, CO2 supercrítico, Zingiber officinale, jengibre.
Abstract
Extracts from ginger rhizomes (Zingiber officinale) were obtained by supercritical fluid extraction- SFE, with CO2 at different conditions of temperature and pressure. Additionally, lipophilic extracts were obtained by soxhlet extraction. The extracts were analyzed by gas chromatography-mass spectrometry (GC-MS) and there were determined the respective extraction yields. With SFE was possible to obtain solvent free extracts, they were enriched with aroma impact compounds and with important biological activity compounds, reaching an extract yield of 1.51% to 17.9 MPa and 40 ºC. Over thirty components present in the extracts were identified by GC-MS.
Key words:Supercritical fluid extraction, supercritical CO2, Zingiber officinale, ginger.
Introducción
La creciente demanda mundial por productos naturales en fresco o procesados, o por productos terminados que contengan componentes naturales, es una oportunidad para nuestro país, dadas las ventajas comparativas que éste posee. En esa dirección, el procesamiento de especies y plantas aromáticas puede constituir una posibilidad para aumentar el nivel de exportaciones no tradicionales, dada la demanda mundial que existe por productos vegetales del trópico, por sus delicadas y exóticas características sensoriales. Dicha posibilidad se acentúa al aumentar el conocimiento sobre nuestros recursos naturales, tal cual ha ocurrido con algunas frutas tropicales (Duque & Morales, 2005).
El jengibre (Zingiber officinale) es una planta nativa de Asia, cultivada en numerosas partes del mundo incluyendo el oeste de la India, Jamaica y África. Esta planta ha sido introducida a Colombia, actualmente existen algunos cultivos tecnificados y es una de las plantas medicinales comercializadas y avaladas por la OMS (Duque, 2000). Debido a que el aceite esencial que se obtiene del rizoma es un producto con un alto valor agregado, continuamente se buscan nuevas y mejores técnicas de extracción que conduzcan a mejorar la calidad y los rendimientos en la obtención de dicho aceite.
El aceite esencial y la oleorresina obtenidas del jengibre son de gran interés para el sector alimenticio y la medicina, debido a diferentes propiedades asociadas a su consumo tales como capacidad antioxidante (Stoilova et al., 2007; Taghizadeh et al., 2007), anticáncer (Shukla & Singh, 2007), antiespasmódico y antidiarreico (World Health Organization, 1999), entre otras. Estas características son debidas a algunas sustancias químicas presentes en dicho material vegetal, tales como los gingeroles. Adicionalmente, el aceite esencial de jengibre se compone de otros grupos de sustancias como monoterpenos y sesquiterpenos, responsables de las correspondientes características sensoriales (Gong et al., 2004). El aceite esencial de jengibre es obtenido tradicionalmente por destilación con arrastre de vapor o extracción soxhlet (Vásquez et al., 2001). Estos procesos no son costosos pero pueden inducir transformaciones de algunos componentes del aceite (degradación térmica y oxidativa); por otra parte, los extractos obtenidos con solventes orgánicos contienen residuos que contaminan los alimentos y las fragancias en los que se empleen.
A diferencia de las técnicas tradicionales, la extracción con fluidos supercríticos (EFS) permite obtener extractos libres de solventes, manteniendo las propiedades organolépticas del material vegetal de partida, sin ocasionar contaminación sobre el medio ambiente (Herrero et al., 2010). Teniendo en cuenta lo anterior, el objetivo planteado en esta investigación fue obtener extractos de jengibre libres de solvente, empleando un equipo de EFS diseñado y construido en nuestro grupo de investigación, el cual permite utilizar dióxido de carbono supercrítico (CO2 SC) como solvente, y comparar los extractos obtenidos por EFS con los correspondientes obtenidos mediante extracción tradicional con solventes (soxhlet).
Materiales y métodos
Materiales y muestra
Los rizomas de jengibre fueron adquiridos en un mercado local. Las muestras fueron cortadas y secadas a 30 ºC. El CO2 (99.9% de pureza) fue proporcionado por INGEGAS-Bogotá. Se emplearon solventes orgánicos grado analítico, los cuales fueron previamente destilados.
Obtención de extractos
Extracción soxhlet: Dos muestras vegetales (10.0 g) puestas en dedales de papel, fueron sometidas a extracción soxhlet durante 1.0 h, por separado, empleando nhexano (Sox1) y éter etílico (Sox2), respectivamente. Una vez obtenidos los extractos, éstos fueron secados, concentrados, pesados y refrigerados hasta su análisis.
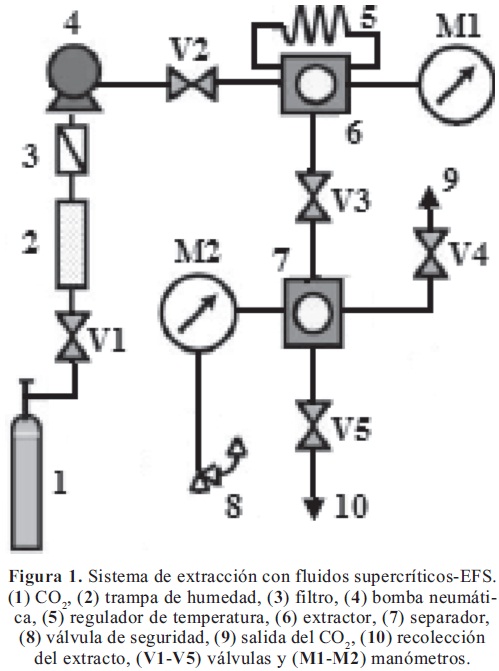
Extracción con fluidos supercríticos: La EFS a partir del rizoma de jengibre fue realizada utilizando el sistema de extracción presentado en la figura 1. Dicho sistema fue construido por nuestro grupo de investigación, empleando en su totalidad acero inoxidable 316 y permite realizar extracción por lotes en modalidad estática (Nivia et al., 2007). El equipo mencionado está conformado por (1) cilindro de CO2, (2) trampa de humedad, (3) filtro, (4) bomba neumática (HASKEL® modelo AGT-7/30, CA. USA), (5) regulador de temperatura (WATLOW serie SD 31, MI, USA, ± 1.0 °C) con termocupla tipo K, (6) celda de extracción de 50.0 mL, (7) separador de 40.0 mL, (8) válvula de seguridad, (9) salida del CO2, (10) recolección del extracto, (V1-V5) válvulas de aguja (WHITEY series SS- 1VS4 y SS-1VR4, OH, USA) y (M1 -M2) manómetros (BOURDON HAENNI, Vendôme cedex, France, 70 MPa). El procedimiento de extracción consistió en ubicar la muestra (10.0 g por cada ensayo) en la celda de extracción y ponerla en contacto, durante 1.0 h en modo estático, con el CO2 SC a las condiciones de extracción (EFS1 40 ºC/13.8 MPa; EFS2 40 ºC/17.9 MPa; EFS3 40 ºC/20.7 MPa; EFS4 50 ºC/13.8 MPa; EFS5 50 ºC/17.9 MPa; EFS6 50ºC/20.7 MPa). Pasado el tiempo de extracción se abrió V3, permitiendo la despresurización de la celda de extracción y posterior recolección del extracto por apertura de V5. Finalmente los extractos fueron pesados y refrigerados hasta su análisis.
Análisis de los extractos por CG-EM.
El análisis de los extractos obtenidos se realizó en un cromatógrafo de gases HP 6890 GC-System, equipado con una columna HP-5 (30 m, 0.25 mm, 0.25 µm). Se usó un programa de temperatura de 50 ºC por 4 minutos, y una rampa de 2 ºC/min hasta alcanzar 280 ºC. La temperatura en el inyector y en la línea de transferencia hacia el detector fue de 230 ºC. Se empleó helio como gas portador, a una velocidad de 1.7 mL/min. Las muestras fueron inyectadas en modo split-less. La energía de ionización fue 70 eV (Martínez et al., 2007). Los compuestos fueron identificados de acuerdo al criterio cromatográfico (índices de Kovats, I.K., consultados en el sitio web del National Institute of Standards and Technology, NIST) y al criterio espectral (espectros de masas).
Resultados
Los extractos de jengibre obtenidos por soxhlet mostraron rendimientos de 1.58 y 2.79% (empleando n-hexano y éter etílico, respectivamente); de acuerdo al análisis por CG-EM de dichos extractos, éstos presentaron residuos de los solventes empleados, lo cual les confirió a cada uno el aroma del solvente respectivo. La mayoría de compuestos identificados en dichos extractos fueron terpenos, lo cual coincide con los reportes encontrados en literatura (Martínez et al., 2007). En el extracto Sox1 se detectó un total de 37 compuestos, de los que se identificaron 22 (52%, porcentaje relativo por normalización de áreas), siendo los mayoritarios decanal, β-burboneno y linoleato de etilo; por otra parte, se logró detectar 41 constituyentes en el extracto Sox2, de los que se identificaron 25 (78%), determinando como mayoritarios al α-zingibereno, β-sesquifelandreno, citral y α-farneseno (Tabla 1).
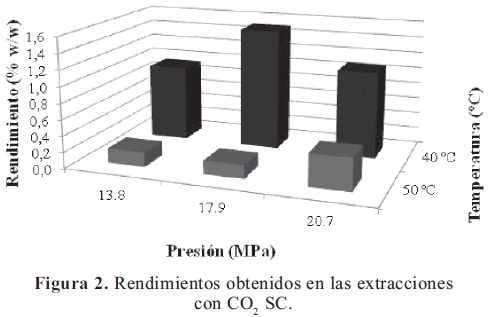
Respecto a los extractos obtenidos con CO2 SC, en la figura 2 se presenta el rendimiento en extracto obtenido bajo las diferentes condiciones de extracción. Es importante señalar que la totalidad de dichos extractos estuvieron exentos de solventes y presentaron un aroma intenso y característico. Con relación al efecto de la temperatura sobre el rendimiento de extracción, se observó que el incremento de ésta generó una disminución en la cantidad de extracto obtenido; a 40 ºC se obtuvieron los mejores rendimientos (1.51% a 17.9 MPa; 1.08% a 20.7 MPa; 0.95% a 13.8 MPa), los que contrastaron con los obtenidos a 50 ºC (0.40% a 20.7 MPa; 0.18% a 13.8 MPa; 0.17% a 17.9 MPa), lo cual puede deberse a la disminución en la densidad del CO2 SC al aumentar la temperatura. Respecto a la influencia de la presión, no se observó un comportamiento claro (mientras que a 40 ºC se observó un máximo a 17.9 MPa, a 50 ºC se presentó un mayor rendimiento a 20.7 MPa).
En los extractos obtenidos con CO2 SC se lograron identificar 34 compuestos (tabla 1), principalmente aldehídos y alcoholes terpénicos, tales como: citronelal, citral, linalol, borneol, á-terpineol, nerol, ladol, a-bisabolol y longipinocarveol. Los componentes mayoritarios en cada uno de los extractos obtenidos fueron: en el extracto EFS1 el transnerolidol, en EFS2 citral y nerol, en EFS3 b-sesquifelandreno y a-farneseno, en EFS4 linoleato de etilo y limoneno, en EFS5 zingerona y a-terpineol y en EFS6 docosano y zingerona. Contrasta la ausencia de a-farneseno, bsesquifelandreno, trans-nerolidol, hedicariol, trujopseno y ladol en los extractos obtenidos a 50 ºC, con la presencia de cantidades importantes de a-zingibereno en EFS4, de óxido de humuleno y zingerona en EFS5 y EFS6, así como de gingerol en EFS6. Tanto la zingerona como el gingerol, compuestos típicos del aceite esencial y la oleorresina de jengibre, son ampliamente reconocidos por sus propiedades antioxidantes (Stoilova et al., 2007; Burdock, 1995; Pfeiffer et al., 2006).
Discusión
En general, la composición de los extractos obtenidos en este trabajo empleando CO2 SC es relativamente similar, sin embargo existen diferencias considerables respecto a la concentración relativa de cada uno de los compuestos identificados, algo que también se evidencia al comparar dichos extractos con los obtenidos por soxhlet. Respecto a algunos de los compuestos señalados anteriormente, vale la pena resaltar que el α-zingibereno, α-farneseno, β- sesquifelandreno, linalol, borneol y nerol son compuestos asociados al aroma del rizoma de jengibre; adicionalmente, debido a su importancia medicinal y alimenticia es importante destacar la presencia de α-zingibereno, α-farneseno y β-sesquifelandreno en algunos extractos (Stoilova et al., 2007; Bhupesh et al., 1996). por otra parte, la zingerona y el gingerol, se asocian al sabor pungente y picante de jengibre (Shukla & Singh, 2007; Bhupesh et al., 1996).
Conclusiones
De las técnicas evaluadas en la obtención de aceite esencial a partir de rizoma de jengibre (Z. officinale), se evidenció que la EFS, empleando como solvente CO2 SC, presentó los mejores resultados respecto a cantidad y composición de los extractos obtenidos; adicionalmente ésta es una metodología selectiva y amigable con el ambiente que permitió la obtención de extractos libres de solventes. De los parámetros evaluados en las EFS las condiciones experimentales asociadas al mayor rendimiento fueron 40 ºC y 17.9 MPa (EFS2), con un 1.51% en extracto. Sin embargo, los extractos EFS5 y EFS6 resultaron muy interesantes por contener cantidades importantes de compuestos con actividad antioxidante y sabor pungente (característico del jengibre), tales como la zingerona y el gingerol.
Agradecimientos
Los autores agradecen a la Universidad Nacional de Colombia, por la financiación del presente estudio.
Referencias
Bhupesh R, Motonobu G, Tsutomu H. 1996. Extraction of Ginger oil with supercritical carbon dioxide: experiments and modelling. Ind. Eng. Chem. Res. 35:607-612. [ Links ]
Burdock G. 1995. Fenaroli's Hanbook Of Flavor Ingredients, CRC PRESS. Florida, USA.
Duque A. [ Links ] 2000. Encuesta Nacional de Plantas Medicinales y Aromáticas una Aproximación al Mercado de las PMyA en Colombia. Instituto de Investigación de Recursos Biológicos Alexander von Humboldt. [ Links ]
Duque C, Morales AL. 2005. El Aroma Frutal de Colombia. Editorial Unibiblos, Bogotá, Colombia.
Gong F, [ Links ] Fung Y, Liang Y. 2004. Determination of volatile components in Ginger using gas chromatography-mass spectrometry with resolution improved by data processing techniques. J. Agric. Food Chem. 52:6378-6383. [ Links ]
Herrero M, Mendiola JA, Cifuentes A, Ibañez E. 2010. Supercritical fluid extraction: Recent advances and applications- Review. J. Chromatogr. A 1217:2495-2511.
Martí [ Links ]nez J, Monteiro R, Rosa P, Marques M, Meireles A. 2003. Multicomponent model to describe extraction of Ginger oleoresin with supercritical carbon dioxide. Ind. Eng. Chem. Res. 42:1057-1063. [ Links ]
Nivia A, Castro H, Parada F, Rodríguez I, Restrepo P. 2007. Aprovechamiento integral de la guayaba (Psidium guajava L.): I. Obtención de extractos a partir de semillas utilizando como solvente CO2 supercrítico. Sci. Tech. 33:120-123.
Pfeiffer E, [ Links ] Heuschmid F, Kranz S, Metzler M. 2006. Microsomal hydroxylation and glucuronidation of [6]-gingerol. J. Agric. Food Chem. 54:8769-8774. [ Links ]
Shukla Y, Singh M. 2007. Cancer preventive properties of ginger: a brief review. Food Chem. Toxicol. 45:683-690.
Stoilova I, [ Links ] Krastanov A, Stoyanova A, Denev P, Gargova, S. 2007. Antioxidant activity of a ginger extract (Zingiber officinale). Food Chem. 102:764-770. [ Links ]
Taghizadeh A, Shirpoora A, Farshid A, Saadatian R, Rasmi Y, Saboory E, Ilkhanizadeh B, Allameh A. 2007. The effect of ginger on diabetic nephropathy, plasma antioxidant capacity and lipid peroxidation in rats. Food Chem. 101:148-153.
Vá [ Links ]squez O, Alba A, Marreros J. 2001. Extracción y caracterización del aceite esencial de jengibre (Zingiber officinale). Rev. Amaz. Inv. Alim. 1:38-42. [ Links ]
World Health Organization. 1999. Monographs on Selected Medicinal Plants. World Health Organization. Geneva, Switzerland. [ Links ]
Recibido: julio 27 de 2011. Aceptado para su publicación: agosto 30 de 2011.













