Introducción
La demanda biológica de oxígeno es una estimación semicuantitativa de los requerimientos de oxígeno que tienen las aguas residuales domésticas. Esta prueba se utiliza frecuentemente como criterio de calidad de vertimientos domésticos e industriales, así como para medir la eficiencia de los sistemas de remoción de carga orgánica, en las plantas de tratamiento de aguas residuales, (Eaton, Clesceri, Rice, Greenberg, 2005; Dogan, Sengorur, Koklu, 2009).
Existen básicamente dos métodos estándar para medir la DBO, el método de incubación a cinco días, y el método respirométrico, (Eaton, et al., 2005). El primero, mide la carga orgánica de las muestras, en función de la cantidad de oxígeno requerido para su oxidación biológica, por parte de microoorganismos biodegradadores, en cinco días, bajo condiciones cuidadosamente controladas (Li, et al., 2016) y, el segundo, en función del descenso de la presión causado por el consumo de oxígeno de la muestra, en un sistema x cerrado. Existen también otros métodos que han venido desarrollándose durante los últimos veinte años (Calderon, 2007) que apuntan fundamentalmente a tres objetivos. El primero, agilizar el tiempo de duración de los análisis, que en el método tradicional es de cinco días; el segundo, mejorar sustancialmente la reproducibilidad de las mediciones y, el tercero, simplificar el procedimiento de medición y las áreas de trabajo (Jouanneau, et al., 2014).
Los avances de la investigación en este campo apuntan hacia el desarrollo de metodologías de análisis basadas en bio-sensores, que detectan la bio-luminiscencia producida por la utilización de una fuente de carbono, en el uso de celdas de combustible microbiano que generan una corriente eléctrica proporcional a la metabolización microbiana y en el uso de bio-sensores electroquímicos que determinan la actividad metabólica del sistema, mediante la medición del potencial redox de un mediador o intermediario que se adiciona al sistema, generalmente, el hexacianoferrato de potasio III, K3Fe(CN)6, ( Li, et al., 2016; Liu, et al., 2016).
En este estudio se explora la posibilidad de encontrar una correlación entre la DBO de una muestra de agua residual doméstica y su generación de bióxido de carbono, durante el proceso de incubación, con el propósito de aportar en el mejoramiento de la reproducibilidad de las mediciones y de la simplificación del procedimiento y de las áreas de trabajo.
El estudio utiliza botellas comerciales de color ámbar y 500 ml de capacidad nominal para incubar las muestras; captura el bióxido de carbono generado por la metabolización aeróbica de la materia orgánica, en la fase acuosa, mediante un buffer concentrado y, determina posteriormente por titulación con una base fuerte, la cantidad de CO2 generado durante la incubación de las muestras.
Materiales y métodos
Reactivos. Los reactivos se prepararon según metodología descrita en Standard Methods for examination of water and wastewater’ (Eaton, et al., 2005).
Procedimientos. Todas las mediciones de oxígeno disuelto realizadas en éste estudio, fueron hechas por volumetría, según el método 4500-O C, Azide Modification, del Standar Methods for Examination of Water and Wastewate’.
Todas las mediciones de acidez realizadas en este estudio, fueron hechas por titulación de una alícuota de 100 ml de muestra, blanco o patrón, con solución estándar de NaOH 0,025 N, en presencia de fenolftaleína.
El estudio de las relaciones existentes entre la DBO de una muestra de agua residual doméstica y la correspondiente acidez producida durante el proceso de incubación de las muestras, se realizó en dos etapas. En una primera etapa se observó el comportamiento entre estas dos variables, utilizando como muestras de trabajo, soluciones patrón de glucosa-glutámico. En una segunda etapa, se utilizaron muestras de agua residual doméstica (ARD), provenientes del influente de la Planta de Tratamiento de Aguas Residuales El Salitre, facilitadas por la Empresa de Acueducto y Alcantarillado de Bogotá, Colombia, durante el año 2013.
Relaciones acidez/DBO en soluciones patrón de glucosa-glutámico. En esta primera etapa se utilizaron como muestras de análisis, soluciones patrón de glucosa-glutámico, por la ventaja que ofrece para el estudio de las variables en cuestión, el trabajo sobre muestras con valor de DBO perfectamente conocido.
En este sentido, se pesaron 450 mg de glucosa y 450 mg de ácido glutámico, anhidros y se disolvieron con agua destilada hasta un volumen total de 1000 ml. La DBO teórica de esta solución stock es de 600 mg O2/l (Eaton, et al., 2005). A partir de dicha solución se prepararon, 500 ml de cada una las soluciones patrón, abajo indicadas, con el objeto de observar la acidificación producida durante la incubación, a diferentes rangos de concentración:
Serie rango bajo: 20, 40, 60, 80 y 100 mg O2/l
Serie rango medio: 40, 80, 120, 160 y 200 mg O2/l
Serie rango alto: 100, 200, 300, 400 y 500 mg O2/l
Para los ensayos de rango bajo de concentración, se utilizó 1,0 ml de solución buffer concentrada, por cada 500 ml de muestra o blanco. Para los ensayos de rango medio, 2,0 ml y para los ensayos de rango alto, 3,0 ml. Todas las muestras y blancos se inocularon con 0,5 ml del efluente de una planta de tratamiento de aguas residuales, por cada 500 ml de muestra o blanco.
En este estudio, las muestras se incubaron en botellas comerciales de color ámbar y 500 ml de capacidad nominal, provistas de tapa y contratapa plásticas, que garantizan un cierre hermético.
Dentro de cada ensayo, cada muestra se incubó por duplicado, en alícuotas de 200 ml, para rangos de concentración bajo y medio y, en alícuotas de 100 ml, para rango alto de concentración. A cada una de las botellas se le incorporó un agitador magnético de aproximadamente 3,0 cm de longitud y, posteriormente, se tapó cada botella herméticamente.
En cada serie de ensayos, las botellas se colocaron sobre la plancha de agitación magnética de un equipo Oxitop® IS 12 y, posteriormente, se incubaron a 20 ± 1 °C durante cinco días, con una variación de más o menos 4 horas.
Luego de los cinco días de incubación, se retiraron las muestras de la incubadora y se tituló una alícuota de 100 ml de cada una de las muestras, con NaOH estándar 0,025 N, en presencia de fenolftaleína. Las titulaciones se realizaron con bureta digital y apoyo de agitación magnética, tomando como punto final de la titulación, la permanencia en la mezcla reaccionante, de un tinte rosado, durante más de 10 segundos. Por último, se realizaron los cálculos de las titulaciones y se expresó la acidez obtenida, como miligramos de carbonato de calcio por litro de muestra. De acuerdo con la hipótesis de trabajo, muestras con altos valores de DBO, deberían corresponder con altos valores de acidez y viceversa.
Relaciones acidez/DBO en aguas residuales domésticas. El estudio de las relaciones entre la acidez y la DBO, en aguas residuales domésticas, se realizó sobre muestras provenientes del influente de la Planta de Tratamiento de Aguas Residuales El Salitre, facilitadas por la Empresa de Acueducto y Alcantarillado de Bogotá, durante el 2013.
El procedimiento consistió en recoger un galón de muestra y trasladarla al Laboratorio de Aguas de la Facultad del Medio Ambiente y Recursos Naturales, de la Universidad Distrital Francisco José de Caldas, e iniciar los ensayos, antes de transcurridas cuatro horas, después del muestreo.
Ya en el laboratorio, la muestra se homogenizó por agitación mecánica durante varios minutos y luego se filtró sobre un lecho de algodón.
La muestra así tratada se dividió en dos porciones. Una de ellas se utilizó para la medición de la DBO5, por el método estándar de incubación a cinco días, (Eaton, et al., 2005) y, la otra, se tomó como solución stock, para preparar a partir de ella, por dilución con agua de dilución, una serie de soluciones patrón, cuya concentración se calculó posteriormente, a partir del resultado experimental obtenido para la DBO5, por el método estándar de incubación a cinco días.
Cada dilución de la muestra, de agua residual doméstica, se incubó por duplicado en botellas comerciales de color ámbar y 500 ml de capacidad nominal, provistas de cierre hermético, de manera semejante a como se procedió con las soluciones patrón de glucosa y ácido glutámico.
Resultados y discusión
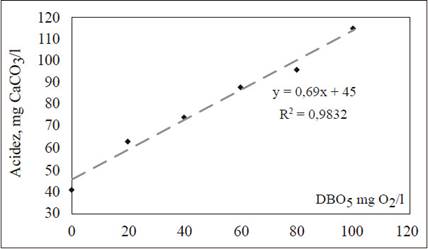
Relaciones acidez vs DBO en muestras de glucosa-glutámico, rango bajo. Los resultados obtenidos para el estudio de las relaciones acidez vs DBO en muestras artificiales de glucosa y ácido glutámico, para rangos bajo y medio de concentración, se muestran en las Figuras 1 y 2, respectivamente. Estos resultados se refieren a la acidez de las muestras, medida después del periodo de incubación de cinco días. En esta primera etapa, no se midió la acidez inicial de las muestras.
Nótese que en ambas gráficas, se obtiene como resultado, una inequívoca relación lineal entre la DBO de la muestra y su acidez, después de la incubación. Así lo indica el coeficiente de correlación lineal, superior, en ambos casos, al 95 %. Ensayos semejantes, realizados en condiciones semejantes, arrojan los mismos resultados. Sin embargo, las variables de la recta, pendiente y corte con el eje ‘Y’, cambian cuando se cambia la cantidad de buffer aplicado.
Las Figuras 1 y 2, sugieren que es posible medir la DBO de una muestra, no solo en función del consumo de oxígeno, durante la incubación de las muestras, sino también, en función de la acidez que genera, la metabolización aerobia de la materia orgánica contenida en la muestra. No obstante, estos ensayos, por sí solos, no son contundentes, por cuanto se debe tener en cuenta que estas muestras, contienen cantidades proporcionales de ácido glutámico. Es decir, que la pendiente de las líneas rectas, en estas figuras, podría darse, no solo por la acidez producida en la metabolización de la materia orgánica, sino también, por la concentración creciente del ácido glutámico, en las muestras. En síntesis, la tendencia es lineal pero el resultado no es concluyente. Es por esto que es necesario, trabajar en una segunda etapa, con muestras reales de agua residual doméstica.
Relaciones acidez vs DBO en agua residual doméstica. Los resultados obtenidos para el estudio de las relaciones acidez vs DBO en muestras de agua residual doméstica, se presentan separadamente en cuatro ensayos diferentes. En los dos primeros, se presentan también los resultados experimentales obtenidos en la medición de la DBO, por el método estándar de incubación a cinco días, mientras que en los dos últimos, se presentan solo las relaciones entre las variables estudiadas.
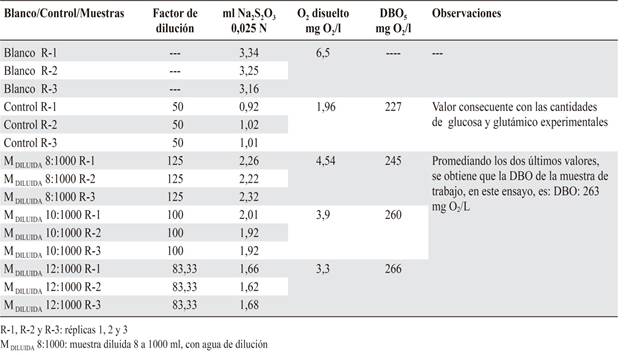
Ensayo 1: acidez vs DBO en agua residual doméstica. La muestra de agua residual doméstica, tratada según lo indicado anteriormente, se dividió en dos porciones. Con una de ellas se midió la DBO5, por el método estándar de incubación a cinco días, Tabla 1, y, con la otra, se realizaron las pruebas de acidez, antes y después del proceso de incubación, Tabla 2.
El valor de DBO obtenido en la Tabla 1, 263 mg O2/l, se tomó como valor verdadero para calcular los valores de DBO de la Tabla 2, en la cual se comparan los valores de DBO, con los correspondientes valores de acidez, medidos, antes y después del proceso de incubación de las muestras.
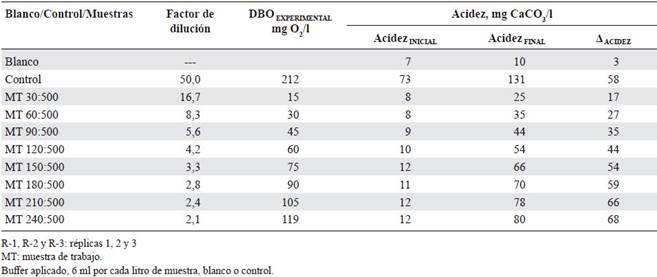
Se destacan tres hechos relevantes en la Tabla 2. El primero es el alto valor inicial de la acidez en la solución control que, téngase en cuenta, contiene ácido glutámico. El segundo es el valor casi constante de la acidez inicial en las muestras, para cualquier concentración de DBO y, el tercero, un valor creciente de acidez final, que se corresponde con una concentración creciente de DBO.
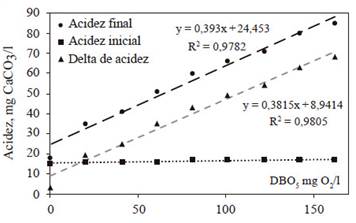
En la Figura 3 se grafican los resultados de acidez vs DBO, correspondientes a la Tabla 2. En ella se observa una relación lineal entre la DBO de las muestras y el valor de la acidez final, relación que se caracteriza en este ensayo, por un coeficiente de correlación lineal superior al 98 %. Obsérvese que al graficar el delta de acidez (acidez final menos acidez inicial) contra la DBO de las muestras, la linealidad se mantiene. Este hecho sugiere que es posible medir la DBO de una muestra, de agua residual doméstica, en función del valor de su acidez final, esto es, que no es necesario medir la acidez inicial, por cuanto ésta corresponde a un valor prácticamente constante, que no depende de su valor de DBO, sino, más bien, de su naturaleza ácida o básica.
Ensayo 2: acidez vs DBO en agua residual doméstica. Las Tablas 3 y 4 muestran los resultados obtenidos para un ensayo semejante al anterior, en el que se mantuvieron las mismas condiciones experimentales, pero se trabajó con una muestra diferente, proveniente de la misma fuente. Análogamente al primer ensayo, la Tabla 3 muestra los datos obtenidos en la medición de la DBO, por el método estándar de incubación a cinco días y la Tabla 4, los valores de acidez inicial y final, obtenidos para diluciones graduales de la muestra de trabajo.
El valor de DBO obtenido en la Tabla 3, se utilizó para calcular los valores de DBO de las muestras diluidas, que se muestran en la Tabla 4.
Nótese cómo, los mismos hechos relevantes observados en la Tabla 2, se presentan también en la Tabla 4: Un alto valor inicial de acidez en la solución control, un valor más o menos constante de acidez inicial en las muestras, y un valor creciente de acidez final, que se corresponde con una concentración creciente de DBO.
En la Figura 4 se grafican los resultados de acidez vs DBO, correspondientes a la tabla 4. Obsérvese que aunque cambian las pendientes, −de 0,66 para la acidez final en el primer ensayo, a 0,59 para la acidez final en el segundo− la linealidad se mantiene y los coeficientes de correlación lineal, escasamente disminuyen en 1%. Para efectos prácticos, el comportamiento de la relación existente entre las variables estudiadas, es el mismo, pues las diferencias entre uno y otro ensayo, caen dentro de las variaciones del error experimental, particularmente si se tiene en cuenta, que en el método estándar de incubación a cinco días, las diferencias aceptadas pueden llegar hasta el 25%, (Eaton, et al., 2005).
Finalmente, la correspondencia entre la DBO de la muestra y la acidez producida durante la incubación, se da tanto para la acidez final como para el delta de acidez, lo cual corrobora la posibilidad de simplificar la medición de DBO, mediante una sola medición de la acidez, al final de la prueba.
Este hecho se puede comprobar calculando con cualquiera de las ecuaciones del ensayo 1, −acidez o delta de acidez− los valores de DBO en el ensayo 2, a partir de la acidez final o del delta de acidez. Mientras se trabaje dentro del rango de concentración coincidente −de 20 a 80 mg O2/ l− las desviaciones obtenidas son inferiores al 10 % y, lo que es más importante, siempre inferiores al 25 %, que es la desviación máxima aceptada para el método estándar.
A modo de ejemplo, si mediante la ecuación Y = 0,6679X + 16,951, obtenida en el ensayo 1, se calcula la DBO de la muestra correspondiente a la acidez final de 54, obtenida en el ensayo 2, se llega al siguiente resultado: DBO experimental 60 mg O2/l y DBO calculado, 55,5 mg O2/l’.
Ensayos 3 y 4: acidez vs DBO en agua residual doméstica. En estos dos últimos ensayos, se realiza un procedimiento experimental semejante al descrito anteriormente, la única diferencia con respecto a los anteriores, es la concentración del buffer, que pasó, de 6,0 ml por litro, en los primeros ensayos a 4,0 ml por litro, para blancos, patrones y muestras, en estos últimos dos ensayos.
En general, en este estudio se realizaron ensayos variando la cantidad de buffer, entre 2 y 5 ml, por cada 500 ml de blanco, muestra o patrón. Sin embargo, para las muestras de agua residual estudiadas, cuyos rangos de DBO variaron aproximadamente entre 20 y 150 mg O2/l, los mejores resultados se obtuvieron con dosificaciones de 2-3 ml de buffer, por cada 500 ml de blanco, muestra o patrón.
La Tabla 5 y la Figura 5, corresponden al ensayo 3, en el cual, la DBO de la muestra, medida por el método estándar de incubación a cinco días, dio como resultado el valor de 218 mg O2/l. Con este resultado se calcularon los valores de DBO que aparecen registrados en la Tabla 5.
Obsérvese que el resultado es muy semejante al obtenido en los ensayos 1 y 2 y que la única diferencia consiste en la reducción de los deltas de acidez. Así, por ejemplo, en éste ensayo, un delta de acidez de 54, se corresponde con una DBO de 122 mg O2/l, mientras que en los ensayos 1 y 2, éste delta se correspondía con una DBO de aproximadamente 77 mg O2/l.
La Figura 5 muestra claramente que las tendencias se mantienen, tanto para la acidez final como para el delta de acidez. El paralelismo entre las rectas de interés es prácticamente idéntico y el valor de la acidez inicial de las muestras también. Por otra parte, los coeficientes de correlación lineal, escasamente cambian.
De cualquier modo, se debe tener presente, que si bien la reducción de la cantidad de buffer aplicado a los blancos, muestras y patrones, permite que los incrementos de acidez se relacionen cada vez más estrechamente con el metabolismo de la materia orgánica contenida en la muestra, una cantidad de buffer demasiado ajustada a la cantidad de acidez generada por el metabolismo, reduce también la posibilidad de atrapar el bióxido de carbono en la fase acuosa. Por esta razón, no es conveniente utilizar la misma concentración de buffer, que se utiliza en el método estándar de incubación a cinco días.
En la Tabla 6 y la Figura 6, se muestran los resultados correspondientes al ensayo 4. En este ensayo la DBO medida por el método de incubación a cinco días, dio como resultado, el valor de 203 mg O2/l. Con este valor se calcularon las DBO que aparecen registradas en la Tabla 6. Obsérvese la similitud gráfica y tabulada obtenida en estos dos ensayos, ambos realizados con la misma cantidad de buffer concentrado.
Al igual que en los dos primeros ensayos, se pueden calcular, con las ecuaciones del ensayo 3, los valores de DBO del ensayo 4 y viceversa, con discrepancias inferiores al 10%. La concordancia entre los valores de DBO calculados y los experimentales, reflejan las bondades de una posible medición de DBO, en función de la acidez generada durante la incubación de las muestras.
Por último, vale la pena tener presente que el propósito de este estudio era averiguar mediante experimentación, si existía o no, una relación entre las variables DBO y acidez generada durante la incubación y, adicionalmente, determinar el tipo de relación existente, entre dichas variables, en caso de encontrarse. Es por esto que durante la experimentación se determina primero la DBO de la muestra de trabajo, por el método estándar. Conocer ese valor, nos permite asociar la acidez producida, con un valor fiable de DBO.
Sin embargo, puesto que cada ensayo se realiza con una muestra diferente, no es posible obtener aún, una relación precisa entre la DBO expresada en mg O2/l y la DBO expresada en mg CaCO3/l. Ese es el objetivo de la segunda fase de este estudio, que se realiza actualmente con soluciones patrón de glucosa-glutámico y que se proyectará también a muestras reales de agua residual doméstica.
Conclusiones
La acidez producida durante el metabolismo aerobio de la materia orgánica presente en una muestra de agua residual doméstica, es directamente proporcional a su carga orgánica o DBO.
La acidez producida durante la metabolización de la materia orgánica contenida en una muestra de agua residual doméstica, se puede atrapar dentro de la fase acuosa, mediante la adición de un buffer concentrado y cuantificar posteriormente, por titulación con una base fuerte.
La DBO de las aguas residuales domésticas, puede medirse por cuantificación de la acidez producida durante el metabolismo de la materia orgánica contenida, con ventajas comparativas, en relación con el método estándar de incubación a cinco días.
La medición de la DBO, de las aguas residuales domésticas, en función de la acidez producida durante la incubación de las muestras, reduce o elimina la necesidad de diluir las muestras y simplifica la operatividad de la medición, en relación con el método estándar de incubación a cinco días.