Introducción
Uno de los principales problemas de la agricultura en muchas regiones de Colombia es la acidez de los suelos. Específicamente en la zona cafetera del país una alta proporción de las muestras de suelos analizadas en las últimas tres décadas revela limitaciones debido a la acidez (Sadeghian, 2016). En estas condiciones se incrementa la solubilidad del aluminio intercambiable (Al3+), disminuye la disponibilidad de calcio (Ca2+) y magnesio (Mg2+), y se reduce la solubilidad de fósforo (P) y la actividad de los microorganismos del suelo con consecuencias en el crecimiento de las plantas (Havlin, et al., 2017; Raij, 2011; Zapata, 2014).
La acidez del suelo puede corregirse con la aplicación de cales (carbonates, óxidos e hidróxidos de Ca y Mg) (Caires, 2010; Raij, 2011; Sousa, et al., 2007). En este sentido, el requerimiento de cal se define como la cantidad de material de encalado necesario para cambiar el pH del suelo o el contenido de Al3+ a partir de la condición inicial hasta alcanzar el nivel óptimo para el crecimiento de la planta (McLean, 1982; Soil Science Society of America - SSSA, 2008).
Se han propuesto diversos procedimientos para estimar dichos requerimientos en diferentes tipos de suelos, pero no existe un consenso sobre el tema, bien sea porque se sobreestiman las cantidades necesarias o se subestiman (Pagani & Mallarino, 2011) dada la naturaleza propia de los suelos y su variabilidad en propiedades físicas y químicas, las cuales generan diferencias en el comportamiento de la acidez. Por ejemplo, el poder tampón, que puede incrementarse con el aumento de la capacidad de intercambio catiónico (CIC) y la materia orgánica del suelo, y las fuentes de la acidez que pueden ser de origen biogénico o antropogénico (Havlin, et al., 2017; Zapata, 2004). Lo anterior ha sido corroborado por Sadeghian y Díaz-Marín (2020) para algunos de los suelos de la zona cafetera de Colombia. Así, para una misma región es posible encontrar el uso de diferentes métodos con el fin de alcanzar recomendaciones más precisas (Sims, 1996).
Algunas de las propuestas para estimar los requerimientos de cal de los suelos recurren a algoritmos basados en investigaciones de campo, en tanto que otras se sustentan en pruebas de laboratorio. En las primeras se emplean criterios como la neutralización de Al3+ (Kamprath, 1970), el porcentaje de saturación de bases (Cochrane, et al., 1980; Raij, 1991), la neutralización de Al3+ y el incremento de Ca2+ + Mg2+ (Álvarez & Ribeiro, 1999), y el aumento del pH, Ca2+ y Mg2+ en el caso del café (Sadeghian, 2008). Las técnicas de laboratorio, por su parte, incluyen el empleo de cales o reactivos alcalinizantes para elevar el pH hasta el valor deseado según las exigencias del cultivo. Tradicionalmente, en estas se han utilizado tres enfoques generales para determinar el requerimiento de cal: i) la incubación del suelo, ii) el uso de una solución tampón y, iii) la titulación directa con una base (Godsey, et al., 2007). El método más ampliamente aceptado es el de incubación, ya que permite resultados más próximos a los obtenidos en los experimentos de campo (Viscarra & McBratney, 2001; Sims, 1996; Alley & Zelazny, 1987). De aquí que muchos investigadores consideren este método como el referente o patrón al evaluar las nuevas metodologías o modelos de estimación (Teixeira, et al., 2020; McFarland, et al., 2020). La incubación es un método semidestructivo en el que las condiciones del suelo determinan la cinética de reacción de la neutralización de la acidez. Consiste en la mezcla de dosis crecientes de cal con el suelo a capacidad de campo durante 30 a 60 días, tiempo después del cual se mide el pH o el Al3+ (Cabrales, et al., 2018). La incubación, a pesar de ser el método ideal, resulta poco práctica debido al tiempo que se requiere, lo que ha impulsado la formulación de otras alternativas más prácticas.
En cuanto a los métodos basados en el uso de soluciones tampón propuestos por Woodruff (1948), Shoemaker, et al. (1961), Adams & Evans (1962), y Mehlich (1976), entre otros, aunque son más rápidos que la incubación, requieren el uso de reactivos como el p-nitrofenol, el cromo hexavalente y el bario, los cuales generan problemas de salud y seguridad, además de añadir costos para la disposición final de los residuos (Sikora, 2006). El método de titulación directa, por su parte, es destructivo y acelera el equilibrio a través de la agitación de la muestra. Consiste en adicionar una solución de hidróxido de calcio (Ca(OH)2) a la muestra de suelo mezclada con agua en una relación de 1:1, con lo que el equilibrio en el pH se logra aproximadamente en 30 min, es decir, el lapso en el que el valor del pH del suelo alcanza un valor constante (Liu, et al., 2004, Kissel, et al, 2007). El estudio de las titulaciones directas inició con Dunn (1943), quien con este método pronosticó el requerimiento de cal en suelos ácidos enfocándose en el tiempo de equilibrio de la reacción entre el suelo y la base, para el cual propuso 4 días. Sin embargo, el método seguía considerándose dispendioso en términos de tiempo, razón por la que se evaluó una titulación directa con 30 min como el intervalo de tiempo entre adiciones de la solución de Ca(OH)2 (Liu, et al., 2004). Desde entonces se han hecho estudios para medir aún más rápidamente el requerimiento de cal, incluso con una sola adición de Ca(OH)2 (Liu, et al., 2005), midiendo el pH inicial de la muestra y adicionando una sola cantidad de base; a partir de la curva de titulación obtenida, que se asume como lineal, se obtiene la cantidad de cal necesaria para elevar el pH a los valores requeridos. Entre los trabajos relacionados se pueden citar los de Aitken, et al. (1990) en Queensland (Australia), Alabi, et al. (1986) en Nebraska (Estados Unidos), Edmeades, et al. (1985) en Nueva Zelanda, Godsey, et al. (2007) en Kansas (EUA), Owusu-Bennoah, et al. (1995) en Ghana, Ssali, et al. (1981) en Kenya y Tunney, et al. (2010) en Irlanda.
En los últimos años se han desarrollado estudios en el Centro Nacional de Investigaciones de Café (Cenicafé), con el fin de determinar los requerimientos de cal de suelos de la zona cafetera de Colombia con base en el método de incubación (Sadeghian, et al., 2019; Sadeghian & Díaz-Marín, 2020). Sin embargo, este resulta ser un procedimiento largo y dispendioso, razón por la que en el presente trabajo se propuso evaluar el método de titulación directa con Ca(OH)2 como alternativa más rápida a la incubación para determinar dichos requerimientos.
Materiales y métodos
Maestreo, preparación y caracterización de suelos
En 25 localidades con lotes sembrados de café en la zona cafetera de Colombia, seleccionados previamente por las condiciones de acidez del suelo (pH < 5,5), se tomaron muestras de aproximadamente 10 kg a 20 cm de profundidad que luego se llevaron a Cenicafé en el municipio de Manizales (Caldas).
Las muestras se secaron en estufa a 40 °C, se pasaron por un tamiz No. 10 (abertura de 2 mm) y luego se analizaron las siguientes propiedades físicas y químicas (Tabla 1): pH, materia orgánica, calcio (Ca2+), magnesio (Mg2+), potasio (K+) y sodio (Na+), aluminio intercambiable (Al3+), CIC, fósforo (P), azufre (S), hierro (Fe), manganeso (Mn), zinc (Zn), cobre (Cu) y boro (B), así como su textura: arcilla (Ar), limo (L) y arena (A).
Tabla 1 Propiedades químicas y textura de las muestras de suelo analizadas
| Suelo | Departamento | Orden | pHa | Nb | MOc | Kd | Cad | Mgd | Nad | Ale | CICf | Pg | Sh | Fei | Mni | Zni | Cui | Bh | Arj | Lj | Aj | Textura |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| % | cmolc kg-1 | mg kg-1 | % | |||||||||||||||||||
| 1 | Meta | Entisol | 4,0 | 0,26 | 5,8 | 0,23 | 0,39 | 0,17 | 0,02 | 2,9 | 18 | 12 | 15,0 | 515 | 13 | 1,3 | 7,0 | 0,10 | 36 | 27 | 36 | FAr |
| 2 | Meta | Entisol | 4,1 | 0,34 | 8,0 | 0,12 | 0,09 | 0,12 | 0,01 | 1,5 | 19 | 102 | 19,6 | 336 | 25 | 2,1 | 23,3 | 0,09 | 34 | 31 | 34 | FAr |
| 3 | Meta | Entisol | 4,0 | 0,22 | 4,7 | 0,20 | 0,38 | 0,16 | 0,01 | 3,0 | 18 | 3 | 24,0 | 475 | 21 | 1,0 | 2,6 | 0,13 | 40 | 28 | 32 | FAr |
| 4 | Meta | Entisol | 3,6 | 0,27 | 6,1 | 0,21 | 0,24 | 0,18 | 0,02 | 3,6 | 15 | 44 | 18,6 | 810 | 28 | 1,3 | 6,1 | 0,29 | 31 | 17 | 52 | FArA |
| 5 | Meta | Entisol | 3,7 | 0,27 | 6,2 | 0,15 | 0,15 | 0,12 | 0,02 | 4,6 | 18 | 15 | 15,1 | 1495 | 7 | 0,9 | 8,5 | 0,15 | 41 | 20 | 39 | Ar |
| 6 | Meta | Entisol | 3,8 | 0,21 | 4,6 | 0,19 | 0,21 | 0,12 | 0,01 | 3,4 | 14 | 64 | 14,6 | 497 | 24 | 1,4 | 4,4 | 0,56 | 33 | 22 | 45 | FArA |
| 7 | Risaralda | Andisol | 4,5 | 0,46 | 11,6 | 0,83 | 1,84 | 0,46 | 0,01 | 1,3 | 26 | 28 | 23,3 | 162 | 31 | 12,4 | 2,5 | 0,44 | 25 | 25 | 50 | FArA |
| 8 | Risaralda | Inceptisol | 4,5 | 0,17 | 3,6 | 0,25 | 1,56 | 0,58 | 0,03 | 3,9 | 18 | 2 | 18,7 | 86 | 122 | 1,2 | 6,0 | 0,00 | 55 | 34 | 11 | Ar |
| 9 | Cauca | Andisol | 4,6 | 0,70 | 21,6 | 0,27 | 1,69 | 0,47 | 0,04 | 1,6 | 39 | 12 | 5,5 | 758 | 22 | 6,3 | 4,3 | 0,34 | 24 | 35 | 41 | F |
| 10 | Cauca | Andisol | 5,3 | 0,58 | 16,2 | 0,58 | 5,71 | 2,24 | 0,04 | 0,3 | 33 | 12 | 4,8 | 168 | 22 | 8,8 | 5,5 | 0,49 | 28 | 31 | 41 | FAr |
| 11 | Cauca | Andisol | 4,8 | 0,66 | 19,4 | 0,27 | 1,00 | 0,30 | 0,03 | 1,4 | 39 | 12 | 3,0 | 149 | 14 | 4,1 | 4,8 | 0,33 | 26 | 32 | 42 | F |
| 12 | Caldas | Andisol | 4,3 | 0,46 | 11,6 | 0,07 | 0,22 | 0,09 | 0,05 | 1,2 | 26 | 30 | 20,0 | 165 | 9 | 2,7 | 5,9 | 0,35 | 21 | 27 | 52 | FArA |
| 13 | Caldas | Andisol | 4,6 | 0,46 | 11,8 | 0,09 | 0,16 | 0,07 | 0,04 | 1,0 | 26 | 36 | 16,8 | 183 | 7 | 2,9 | 26,0 | 0,39 | 20 | 29 | 51 | F |
| 14 | Santander | Inceptisol | 4,0 | 0,45 | 11,4 | 0,50 | 1,80 | 0,38 | 0,03 | 6,7 | 27 | 17 | 5,3 | 991 | 6 | 2,2 | 2,0 | 0,46 | 67 | 19 | 15 | Ar |
| 15 | Santander | Molisol | 5,2 | 0,21 | 4,6 | 0,16 | 4,17 | 0,81 | 0,06 | 0,2 | 12 | 9 | 5,3 | 358 | 108 | 2,7 | 2,1 | 0,39 | 19 | 23 | 59 | FA |
| 16 | Santander | Inceptisol | 4,5 | 0,34 | 8,2 | 0,16 | 1,39 | 0,15 | 0,06 | 2,5 | 19 | 6 | 3,0 | 704 | 4 | 2,4 | 1,7 | 0,42 | 44 | 25 | 30 | Ar |
| 17 | Nariño | Andisol | 5,2 | 0,38 | 9,3 | 0,54 | 1,60 | 0,35 | 0,06 | 1,1 | 19 | 14 | 4,3 | 159 | 16 | 2,2 | 8,9 | 0,49 | 20 | 24 | 56 | FA |
| 18 | Huila | Inceptisol | 4,8 | 0,29 | 6,7 | 0,43 | 1,13 | 0,49 | 0,01 | 1,1 | 10 | 43 | 5,4 | 244 | 22 | 2,6 | 1,0 | 0,44 | 13 | 18 | 69 | FA |
| 19 | Huila | Inceptisol | 4,6 | 0,28 | 6,4 | 1,07 | 4,69 | 1,58 | 0,03 | 1,6 | 22 | 28 | 9,2 | 409 | 17 | 5,7 | 4,0 | 0,42 | 31 | 26 | 43 | FAr |
| 20 | Huila | Molisol | 4,4 | 0,28 | 6,4 | 0,88 | 1,74 | 0,66 | 0,03 | 1,3 | 16 | 12 | 11,2 | 558 | 14 | 5,7 | 12,5 | 0,48 | 33 | 16 | 51 | FArA |
| 21 | Huila | Inceptisol | 4,7 | 0,32 | 7,6 | 0,25 | 2,73 | 1,85 | 0,08 | 0,9 | 19 | 4 | 11,2 | 396 | 38 | 3 | 5,5 | 0,07 | 49 | 20 | 30 | Ar |
| 22 | Quindío | Andisol | 5,1 | 0,28 | 6,4 | 0,25 | 2,07 | 0,44 | 0,03 | 0,5 | 18 | 24 | 16,3 | 135 | 9 | 2,7 | 3,2 | 0,18 | 13 | 22 | 65 | FA |
| 23 | Quindío | Andisol | 4,7 | 0,33 | 7,9 | 0,25 | 1,59 | 0,30 | 0,03 | 1,0 | 19 | 66 | 16,3 | 146 | 4 | 0,9 | 1,1 | 0,26 | 15 | 21 | 64 | FA |
| 24 | Antioquia | Inceptisol | 4,1 | 0,16 | 3,3 | 0,12 | 0,20 | 0,12 | 0,03 | 4,3 | 13 | 9 | 13,8 | 156 | 15 | 6,1 | 2,7 | 0,41 | 40 | 40 | 20 | Ar |
| 25 | Antioquia | Andisol | 4,2 | 0,47 | 12,1 | 0,16 | 0,07 | 0,16 | 0,02 | 4,0 | 28 | 3 | 18,3 | 559 | 7 | 2,2 | 2,1 | 0,50 | 54 | 22 | 24 | Ar |
a Potenciométrico (H2O, 1:1); b Calculado: %N=0,016 + 0,0453(%MO)-0,00063(%MO)2; c Materia orgánica según método Walkley-Black; d Ac. amonio 1,0 M pH=7,0 extractante; e KCl 1,0 M extractante; f Ac. amonio 1,0 M pH=7,0; g Bray II extractante; h Fosfato monocálcio extractante; i EDTA 0,01 M y Ac. amonio 1,0 M extractante; j Método de Bouyucos (Carrillo, 1985).
Para determinar el requerimiento de cal por el método de titulación con Ca(OH)2, las muestras se secaron a 40 °C y se pasaron por el tamiz No. 10 (apertura de 2 mm). Con el método de incubación, el cual se consideró como patrón, las muestras se secaron al aire y se pasaron por una zaranda (apertura de 10 mm), con el fin de eliminar terrones grandes buscando que las muestras fueran lo más parecidas posibles a la realidad de campo.
Método de incubación con cal
Se pesó un volumen de 0,184 dm3 (decímetro cúbico) de cada muestra de suelo y se trasvasó a una matera plástica que luego se incubó durante 45 días con dosis equivalentes a 0,00; 1,25; 2,50; 5,00 y 10,00 g dm-3 de una cal dolomita (CaCO3.MgCO3) que contenía 34 % de CaO y 16 % de MgO, con un poder de neutralización de 102 %, una eficiencia granulométrica de 91 % y un poder relativo de neutralización total de 92 %. Las muestras se dispusieron por triplicado en el laboratorio de la Disciplina de Suelos de Cenicafé utilizando un diseño completamente aleatorio, y se regaron cada cuatro a cinco días con agua tipo II (conductividad<1 cm-1) para mantener la humedad a un 60 o 70 % de su máxima capacidad de retención. Al finalizar el tiempo de incubación, las muestras se secaron, se pesaron y se midió el pH. Con base en el volumen de las materas, el peso de suelo que ocupaba dicho volumen y la equivalencia de CaCO3.MgCO3 a CaCO3, se hizo la conversión de unidades de dosis de dolomita en g dm-3 a CaCO3 en g kg-1 de suelo (Anexo 1,https://www.raccefyn.co/index.php/raccefyn/article/view/1405/3158). La ecuación 1 describe las reacciones químicas que ocurren en el proceso de incubación y las especies formadas (Havlin, et al., 2017; Espinosa & Molina, 1999):
Método de titulación directa con Ca(OH) 2
Haciendo el procedimiento por triplicado, se agregó una muestra de 25 g de cada suelo a un tubo plástico de polipropileno de 250 mL con tapa de rosca; posteriormente, se adicionaron 25 mL de agua tipo II. La mezcla se agitó durante 30 min en un agitador horizontal marca Bioblock Scientific a 150 mot1 min-1 y se midió el pH; se adicionaron después los siguientes volúmenes de Ca(OH)2 0,02 M hasta alcanzar valores de pH superiores a 6,0: 2, 4, 8, 16, 32 y 64 mL. El intervalo de tiempo para cada adición de la solución de Ca(OH)2 fue de 30 min; la suspensión del suelo se agitó constantemente durante la titulación y la medición del pH entre cada intervalo de tiempo, según lo descrito por Liu, et al. (2004). Según la concentración de la solución de Ca(OH)2, las equivalencias de los pesos moleculares y el peso de suelo evaluado, se hizo la conversión de unidades de dosis de Ca(OH)2 en mL g-1 de suelo a CaCO3 en g kg-1 de suelo (Anexo 2,https://www.raccefyn.co/index.php/raccefyn/article/view/1405/3159). La ecuación 2 describe la reacción química que ocurre en el proceso de titulación y las especies formadas (Havlin, et al., 2017; Espinosa & Molina, 1999).
Análisis estadístico
Se evaluaron diferentes modelos de regresión para describir los cambios del pH con cada método de laboratorio en función de los tratamientos; para ello fue necesario expresar las dosis de dolomita y Ca(OH)2 en unidades de CaCO3 (g kg-1 de suelo). Para el análisis de la bondad del ajuste y la selección de los mejores modelos, se utilizaron el coeficiente de determinación (R2) y su variante ajustada (R2 aj) y la raíz del cuadrado medio del error (RCME) (Kaplan & Kemal, 2018).
Este procedimiento permitió seleccionar dos modelos: el lineal (y=a+bx) y el exponencial (y=a+b(1-e-cx)). Una vez obtenidas las ecuaciones para cada método y suelo, se estimaron las dosis necesarias para alcanzar el pH de 5,5, definido como óptimo para el cultivo de café en las condiciones de Colombia (Sadeghian, 2016). Posteriormente, se compararon los valores promedio de los dos métodos mediante la prueba t de Student (p<0,05) y se hizo un análisis de regresión múltiple con el fin de establecer la relación entre las diferencias de las dosis de CaCO3 para alcanzar el pH 5,5 según los métodos evaluados y las propiedades químicas y la textura de las muestras de suelo evaluadas (Tabla 1). El grado de acuerdo entre el método de incubación y el método de titulación ajustado se midió mediante la prueba de Bland-Altman. Para el procesamiento estadístico se utilizaron los programas SigmaPlot 10.0 (2006), Statgraphics Centurion XV 15.2.14 (2007) y SAS 9.4 (TS1M5).
Resultados y discusión
En la figura 1 se presentan los cambios del pH en respuesta a los tratamientos en cada uno de los suelos evaluados. En el método de incubación los incrementos del pH se ajustaron a la función exponencial creciente de la forma y=a+b(1-e-cx), en la cual las tasas tienden a reducirse con el aumento de las dosis equivalentes de CaCO3, en tanto que en el método de titulación los incrementos del pH por unidad de CaCO3 suministrada fueron mayores y se ajustaron a la función lineal y=a+bx. Como se discutirá más adelante, este resultado se relaciona con la diferencia en la solubilidad y con la reactividad de la caliza dolomítica y el hidróxido de calcio. Como consecuencia, en el método de titulación se requirió de una menor cantidad de agente alcalinizante para alcanzar el pH de 5,5.
Con el propósito de ilustrar las variaciones entre los dos métodos evaluados con mayor detalle, a manera de ejemplo, en la figura 2 se presentan los cambios del pH en función de las dosis equivalentes de CaCO3 y las dosis requeridas para alcanzar el pH de 5,5 para la muestra de suelo 1.
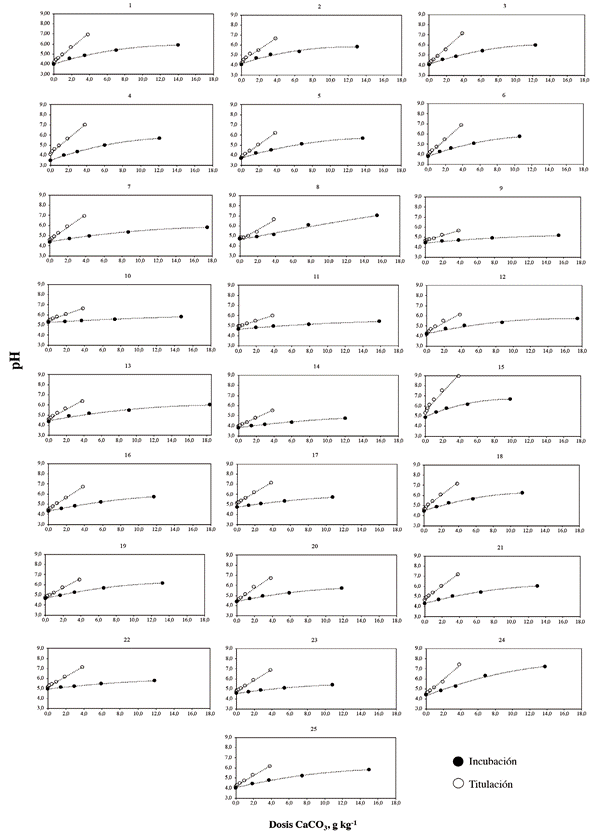
Figura 1 Cambios del pH del suelo en función de dosis equivalentes de CaCO3 registrados en los métodos de titulación e incubación para 25 muestras de suelo de la zona cafetera de Colombia
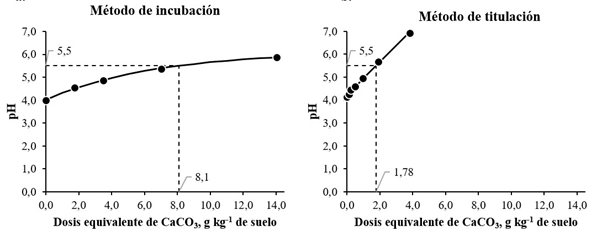
Figura 2 Cambios del pH del suelo en función de dosis equivalentes de CaCO3 registrados en los métodos de incubación (a) y titulación (b) para la muestra de suelo 1
En las tablas 2 y 3 se consignan las ecuaciones y los respectivos parámetros estadísticos que se tuvieron en cuenta como criterios de bondad de ajuste de los modelos seleccionados en cada uno de los métodos. Tanto los altos coeficientes de determinación (R2) y de determinación ajustados (R2 aj), como los menores valores de la raíz del cuadrado medio del error (RCME) y la significación de los parámetros de las ecuaciones (p<0,05), muestran que los modelos exponencial y lineal presentaron buen ajuste y lograron describir adecuadamente los resultados de los métodos de incubación y titulación, respectivamente.
Tabla 2 Ecuaciones y estadísticos asociados con el modelo exponencial obtenidos para el método de incubación
| Suelo | Ecuación | R2 | R2 aj | RCME |
|---|---|---|---|---|
| 1 | ŷ=4,0125+2,1047(1-e(-0,1514x)) | 0,994 | 0,993 | 0,330 |
| 2 | ŷ=4,0957+1,7747(1-e(-0,2195x)) | 0,989 | 0,988 | 0,051 |
| 3 | ŷ=4,0744+2,3385(1-e(-0,1413x)) | 0,996 | 0,996 | 0,014 |
| 4 | ŷ=3,4942+2,7822(1-e(-0,1258x)) | 0,994 | 0,993 | 0,020 |
| 5 | ŷ=3,7133+2,3994(1-e(-0,124x)) | 0,990 | 0,989 | 0,020 |
| 6 | ŷ=3,775+2,5087(1-e(-0,1405x)) | 0,988 | 0,986 | 0,025 |
| 7 | ŷ=4,3832+1,7575(1-e(-0,0945x)) | 0,997 | 0,996 | 0,006 |
| 8 | ŷ=4,618+12.3193(1-e(-0,0141x)) | 0,980 | 0,977 | 0,117 |
| 9 | ŷ=4,4153+0,962(1-e(-0,0924x)) | 0,974 | 0,971 | 0,010 |
| 10 | ŷ=5,2522+1,0314(1-e(-0,0518x)) | 0,951 | 0,945 | 0,008 |
| 11 | ŷ=4,6448+1,0525(1-e(-0,0787x)) | 0,984 | 0,982 | 0,013 |
| 12 | ŷ=4,1807+1,6072(1-e(-0,1607x)) | 0,983 | 0,981 | 0,045 |
| 13 | ŷ=4,4048+1,8045(1-e(-0,1088x)) | 0,981 | 0,979 | 0,063 |
| 14 | ŷ=3,827+1,4534(1-e(-0,0825x)) | 0,968 | 0,964 | 0,009 |
| 15 | ŷ=4,907+1,9483(1-e(-0,2285x)) | 0,978 | 0,975 | 0,035 |
| 16 | ŷ=4,308+2,1449(1-e(-0,0939x)) | 0,959 | 0,954 | 0,007 |
| 17 | ŷ=4,7354+1,5004(1-e(-0,0956x)) | 0,983 | 0,981 | 0,012 |
| 18 | ŷ=4,4488+2,1767(1-e(-0,1485x)) | 0,996 | 0,995 | 0,031 |
| 19 | ŷ=4,6552+1,9316(1-e(-0,1139x)) | 0,992 | 0,991 | 0,012 |
| 20 | ŷ=4,4029+1,7188(1-e(-0,1196x)) | 0,989 | 0,987 | 0,020 |
| 21 | ŷ=4,3059+2,202(1-e(-0,1159x)) | 0,996 | 0,995 | 0,027 |
| 22 | ŷ=4,9458+1,2327(1-e(-0,0916x)) | 0,981 | 0,979 | 0,015 |
| 23 | ŷ=4,5475+1,2159(1-e(-0,1087x)) | 0,993 | 0,992 | 0,006 |
| 24 | ŷ=4,3207+4,4687(1-e(-0,077x)) | 0,988 | 0,986 | 0,089 |
| 25 | ŷ=4,0306+2,2512(1-e(-0,1026x)) | 0,994 | 0,993 | 0,024 |
Todos los parámetros del modelo fueron significativos (p>0,05), con excepción de a y b en el suelo 8 y b en el suelo 10.
Tabla 3 Ecuaciones y estadísticos asociados al modelo lineal obtenidos para el método de titulación
| Suelo | Ecuación | R2 | R2 aj | RCME |
|---|---|---|---|---|
| 1 | ŷ=4,2198+0,7184x | 0,996 | 0,995 | 0,056 |
| 2 | ŷ=4,3615+0,6037x | 0,979 | 0,977 | 0,113 |
| 3 | ŷ=4,1885+0,76x | 0,998 | 0,998 | 0,038 |
| 4 | ŷ=4,1817+0,7431x | 0,998 | 0,997 | 0,042 |
| 5 | ŷ=3,7853+0,632x | 0,997 | 0,997 | 0,044 |
| 6 | ŷ=3,974+0,7549x | 0,998 | 0,998 | 0,037 |
| 7 | ŷ=4,6099+0,6224x | 0,996 | 0,995 | 0,053 |
| 8 | ŷ=4,619+0,495x | 0,969 | 0,967 | 0,109 |
| 9 | ŷ=4,6471+0,2626x | 0,993 | 0,992 | 0,022 |
| 10 | ŷ=5,4545+0,3119x | 0,969 | 0,966 | 0,057 |
| 11 | ŷ=4,919+0,28x | 0,996 | 0,996 | 0,021 |
| 12 | ŷ=4,3799+0,4776x | 0,971 | 0,969 | 0,104 |
| 13 | ŷ=4,6371+0,4669x | 0,984 | 0,983 | 0,074 |
| 14 | ŷ=3,978+0,4047x | 0,997 | 0,997 | 0,019 |
| 15 | ŷ=5,5398+0,9274x | 0,972 | 0,969 | 0,177 |
| 16 | ŷ=4,4937+0,5832x | 0,998 | 0,997 | 0,025 |
| 17 | ŷ=5,1188+0,5296x | 0,997 | 0,997 | 0,023 |
| 18 | ŷ=4,7123+0,6572x | 0,991 | 0,991 | 0,075 |
| 19 | ŷ=4,7766+0,4654x | 0,993 | 0,992 | 0,040 |
| 20 | ŷ=4,4699+0,6125x | 0,979 | 0,978 | 0,096 |
| 21 | ŷ=4,7372+0,6435x | 0,997 | 0,997 | 0,040 |
| 22 | ŷ=5,1526+0,5155x | 0,999 | 0,999 | 0,019 |
| 23 | ŷ=4,7606+0,547x | 0,998 | 0,998 | 0,028 |
| 24 | ŷ=4,4361+0,7457x | 0,992 | 0,991 | 0,085 |
| 25 | ŷ=4,212+0,516x | 0,994 | 0,994 | 0,049 |
Todos los parámetros del modelo fueron significativos (p>0,05).
En el método de incubación el incremento del pH puede ocurrir de manera proporcional (lineal) (McFarland, et al., 2020) o decreciente (exponencial asintótico); en este sentido, Sadeghian & Díaz-Marín (2020), Castro & Munévar (2013) y Castro, et al. (2006) reportaron para las condiciones de Colombia dos tendencias y relacionaron esta diferencia con las propiedades físicas y químicas de los suelos. Asimismo, Uchida & Hue (2000) y Bailey, et al. (1989) describieron en suelos de Hawaii y de Irlanda, respectivamente, respuestas en su mayoría exponenciales en las que, debido a las diferencias entre suelos, los primeros recomiendan preferiblemente determinar los requerimientos de cal para cada tipo de suelo. Por lo general, en las curvas de incubación las tasas del incremento del pH se reducen con el aumento de las dosis sin sobrepasar un pH de 7,0, ya que el material encalante, el cual suele ser cal agrícola, dolomita o una mezcla de ambas (Teixeira, et al., 2020; Castro & Munévar, 2013), posee baja solubilidad y reduce sustancialmente su capacidad de reacción cuando el pH supera dicho valor. En este caso, el aumento de este parámetro está limitado por la velocidad a la que los hidrogeniones (H+) se neutralicen, de modo que, para que continúe la reacción de disociación del carbonato (proceso en el que se da la formación a ácido carbónico), debe haber H+ en la solución del suelo (ecuación 1) (Havlin, et al., 2017; Espinosa & Molina, 1999).
En cuanto al método de titulación, se confirmó lo descrito por Magdoff & Bartlett (1985) y Weaver, et al. (2004) en cuanto a que las curvas de titulación son aproximadamente lineales en un rango de pH de 4,5 a 6,5. Por esta razón, en este método Liu, et al. (2004) y Liu, et al. (2005) sugieren una sola adición de hidróxido de calcio y un tiempo de reacción de 30 min para determinar los requerimientos de cal en suelos ácidos. Con este procedimiento se obtiene una ecuación lineal partiendo de un punto inicial (pH original del suelo) para llegar a un punto final con la adición de 3 mL Ca(OH)2. Cabe aclarar que en estos trabajos se comparó el método de titulación directa con incubación aplicando una solución de hidróxido de calcio por 4 a 5 días, tiempo en el que el pH alcanzó estabilidad sin que se hiciera mezclado durante el proceso, lo que se denomina titulación con incubación.
En cuanto al tiempo requerido para las mediciones, en el método de incubación se necesitaron 50 días, en tanto que en el de titulación fueron necesarios 5 días. Cabe señalar que los períodos indicados tienen en cuenta el tiempo de preparación de la muestra, es decir, los procesos de secado y tamizado, así como la medición del pH posterior a la incubación en el método de incubación.
Comparación de los métodos
Dado que los modelos matemáticos que explican las variaciones del pH en función de las dosis de CaCO3 son diferentes, se puede afirmar que los métodos evaluados no son homogéneos o análogos. Es decir, que con el método de titulación no es posible obtener los mismos resultados que con el de incubación o, por lo menos, no de manera directa (Tabla 4). Lo anterior se pone de manifiesto en la diferencia significativa que presentaron los dos métodos objeto de estudio al estimar las dosis de cal necesarias para alcanzar un valor de pH igual a 5,5 (prueba t al 5 %). En las muestras de suelo 9 y 14 no fue posible determinar las dosis equivalentes de CaCO3 requerida en el método de incubación, debido a que las curvas obtenidas no alcanzaron este valor de pH (Figura 1). En el caso de la muestra 15, usando el método de titulación no se necesitó adicionar cal para aumentar el pH, lo que se explicaría por su valor de pH cercano a 5,5. Como lo revelan estos resultados, el método de titulación subestimó los requerimientos de cal para neutralizar la acidez del suelo hasta alcanzar el nivel óptimo en el cultivo de café comparado con el método de referencia. Los hallazgos concuerdan con los reportes de Godsey, et al. (2007), quienes encontraron que las valoraciones por titulación generalmente subestiman, incluso cuando se deja un tiempo de equilibrio de siete días (Baker & Chae, 1977). Algunas de las discrepancias expuestas en los estudios se han explicado con el argumento de que los resultados son inherentes al tipo de suelo y que los métodos se han desarrollado para suelos de zonas específicas (Godsey, et al., 2007). En este sentido, Bailey, et al. (1989) y Farhoodi & Coventry (2008) concuerdan en que se debe discriminar la respuesta del material para encalado según el tipo de suelo, de allí la importancia de calibrar los requerimientos de cal con base en las características propias de los suelos locales o regionales (Godsey, et al., 2007). Se destaca que en este estudio se incluyeron muestras de suelo con propiedades físicas y químicas contrastantes procedentes de diversas áreas de la zona cafetera colombiana que tenían desde un pH muy ácido (3,6) hasta valores adecuados para el café (5,3); materia orgánica muy baja (3 %) y con niveles altos (22 %); Ca de 0,07 a 5,71 cmolc kg-1; Mg de 0,07 a 2,24 cmolc kg-1; K de 0,07 a 1,07 cmolc kg-1; Al3+ de 0,2 y 6,7 cmolc kg-1; CIC de 10 a 39 cmolc kg-1; P de 2 a 102 mg kg-1; S de 3 a 24 mg kg-1; Fe de 86 a°1495 mg kg-1; Mn de 4 a 122 mg kg-1; Zn de 0,9 a 12,4 mg kg-1; Cu de 1 a 26 mg kg-1, y B de 0,09 a 0,56 mg kg-1 (Tabla 1). Dichas variaciones se relacionan tanto con el origen de los suelos como con su manejo. En cuanto al origen, se resalta la representación de los principales órdenes de la zona cafetera: Inceptisol (60,7 %), Andisol (17,6 %), Entisol (10,5 %) y Molisol (8 %) (Federación Nacional de Cafeteros de Colombia - FNC & Instituto Geográfico Agustín Codazzi - IGAC, 2017).
Tabla 4 Dosis equivalentes de CaCO3 estimadas con los métodos de incubación y titulación para alcanzar un valor de pH de 5,5
| Suelo | Método | |
|---|---|---|
| Incubación | Titulación | |
| x=f(y :5,5) | x=f(y : 5,5) | |
| Dosis CaCO3, g kg-1 suelo | ||
| 1 | 8,10 | 1,78 |
| 2 | 7,14 | 1,89 |
| 3 | 6,66 | 1,73 |
| 4 | 10,15 | 1,77 |
| 5 | 11,01 | 2,71 |
| 6 | 8,28 | 2,02 |
| 7 | 10,68 | 1,43 |
| 8 | 5,27 | 1,78 |
| 9 | - | 3,25 |
| 10 | 5,30 | 0,15 |
| 11 | 21,27 | 2,08 |
| 12 | 10,70 | 2,35 |
| 13 | 8,58 | 1,85 |
| 14 | - | 3,76 |
| 15 | 1,59 | -0,04 |
| 16 | 8,64 | 1,73 |
| 17 | 7,45 | 0,72 |
| 18 | 4,44 | 1,20 |
| 19 | 5,05 | 1,55 |
| 20 | 8,50 | 1,68 |
| 21 | 6,74 | 1,19 |
| 22 | 6,52 | 0,67 |
| 23 | 14,07 | 1,35 |
| 24 | 3,98 | 1,43 |
| 25 | 10,31 | 2,50 |
Los resultados del estudio difieren de lo descrito por Kissel, et al. (2007), quienes proponen que el método de titulación se realice con dos mediciones de pH únicamente, una adición de hidróxido de calcio y un tiempo de equilibrio de 30 minutos. En este sentido, Thompson, et al. (2010) demostraron que el equilibrio en el pH del suelo después de la adición del hidróxido de calcio y de una agitación por 20 segundos se alcanzó después de 84 h. No obstante, con una relación calculada experimentalmente se recomienda la titulación en un tiempo de 30 minutos, tal como en el presente estudio. Además, se debe resaltar que en los trabajos de Liu, et al. (2004) y Kissel, et al. (2007) se empleó la prueba de incubación con una solución de Ca(OH)2 por 3 a 5 días como estándar de comparación, en tanto que en este se empleó una incubación con cal dolomita por 45 días, lo que puede explicar parte de las diferencias encontradas.
Las variaciones en las dosis de cal entre el método de incubación y el de titulación pueden obedecer al tipo de material de encalado, la forma de aplicación y el tiempo de reacción. En el método de incubación se empleó dolomita incorporada en forma sólida a un volumen de suelo, y la mezcla se mantuvo durante 45 días. En contraste, en el método de titulación se empleó una solución de hidróxido de calcio, la cual se adicionó a una mezcla de suelo y agua. En tanto que la cal dolomita reacciona en presencia de acidez y humedad y en el proceso se da formación a iones hidroxilo (OH-), los cuales causan el aumento del pH (ecuación 1), la solución de hidróxido de calcio ya los tiene disponibles, así que el aumento del pH se alcanza más rápidamente (ecuación 2). Vale la pena destacar, sin embargo, que en cada método se tuvo en cuenta el tiempo necesario para alcanzar el equilibrio en el pH del suelo.
Es importante tener presente que la medición del pH en el método de titulación se efectúo a los 30 minutos de cada adición de la solución de Ca(OH)2, en tanto que el procedimiento establecido para la medición de dicho parámetro en un análisis de suelos recomienda hacerlo pasada una hora.
Regresión múltiple
Debido a las diferencias significativas detectadas entre los valores promedio de los dos métodos, se buscó una expresión matemática que permitiera obtener una aproximación significativa a las dosis requeridas de cal a partir de los resultados logrados con cada método evaluado. Para ello se calculó la diferencia entre las dosis de CaCO3 obtenidas con los dos métodos para alcanzar el valor de pH de 5,5. Posteriormente, se hizo una regresión múltiple que explicara estas diferencias en función de las propiedades medidas en el análisis de suelos (Tabla 1). El análisis de regresión múltiple generó una ecuación con la que se puede obtener un valor de corrección para el método de titulación con base en las propiedades químicas y la textura del suelo, el cual se debe sumar a la dosis determinada para el respectivo ajuste:
ŷ = 17,1184 + 7,81886MO - 217,177N + 0,0624708P + 7,50119K - 4,4739Mg + 0,203864S + 0,471334Al + 120,771Na - 0,0289981Mn - 0,131875Cu- 8,61187B - 0,265682L
La ecuación obtenida tiene un R2 de 0,97 y R2 ajustado de 0,94, con un marcado nivel de significación en todos los parámetros (p<0,05). A continuación se presenta un ejemplo de la aplicación de dicha ecuación para la muestra de suelo 1, en cuyo caso el requerimiento de cal por el método de titulación fue de 1,78 g CaCO3 kg-1 (Tabla 4). Los valores de las variables incluidas en la ecuación se encuentran en la tabla 1:
ŷ = 17,1184 + 7,81886*5,8 - 217,177*0,26 + 0,0624708*12 + 7,50119*0,23 -4,4739*0,17 + 0,203864*15+ 0,471334*2,9 + 120,771*0,02 - 0,0289981*13 -0,131875*7 - 8,61187*0,10 - 0,265682*27
ŷ = 5,22.
El resultado obtenido se suma a la dosis obtenida en el método de titulación. Así, la dosis necesaria para alcanzar un pH de 5,5 es igual a 1,78 g CaCO3 kg-1 + 5,22 g CaCO3 kg-1 = 7,00 g CaCO3 kg-1 de suelo.
Estos resultados corroboran lo descrito por Teixeira, et al. (2020) para estimar los requerimientos de cal. Para ello es necesario conocer algunas propiedades físicas y químicas de los suelos relacionadas con la resistencia al cambio de pH (capacidad de buffer). Entre las características de los suelos que han sido combinadas en modelos matemáticos para predecir los requerimientos se encuentran el pH y la materia orgánica (Edmeades, et al., 1985), la CIC y el porcentaje de saturación de bases (Quaggio, et al., 1985), el pH, el Al3+, las bases intercambiables y el carbono orgánico (Hochman et al., 1995), el pH, la textura, el contenido de materia orgánica y la CIC (Alatas, et al., 2005), la materia orgánica, el hierro extraíble y el contenido de arcillas (Curtin & Trolove, 2013) y el pH, la materia orgánica y el nivel de acidez potencial (Teixeira, et al., 2020). En cuanto a la titulación con Ca(OH)2, Owusu-Bennoah, et al. (1995) correlacionaron los requerimientos de cal con la materia orgánica, el Al3+ y el contenido de arcillas cuando el método se desarrolló en 72 horas. Así, se evidencia que la metodología evaluada puede ser efectiva para suelos de la zona cafetera de Colombia, sin que necesariamente sea aplicable en otras regiones debido a las diferencias en las características de los suelos de cada zona, lo que es determinante en la forma de cambiar el pH de un suelo.
En la figura 3 se observa la alta correlación entre las dosis de cal obtenidas en el método de incubación y las generadas con el de titulación una vez corregidas. Las muestras de suelo 9 y 14 no se incluyeron en el análisis dado que no alcanzaron valores de pH de 5,5, razón por la que el análisis se hizo con 23 muestras.
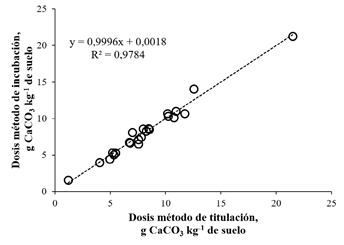
Figura 3 Requerimientos de CaCO3 determinados por el método de titulación ajustado a través de la regresión múltiple en función de los requerimientos de cal obtenidos mediante el método de incubación (n=23)
El grado de acuerdo entre los métodos, medido con la prueba de Bland-Altman, permitió obtener un diagrama de dispersión (Figura 4) que en el eje de las ordenadas presenta las diferencias entre los métodos de medición y en el eje de las abscisas, la media. Este análisis indica que el 95 % de las magnitudes de las diferencias entre los métodos se encontró dentro de un rango de diferencias de -1 y 1 dosis de CaCO3 (g kg-1 suelo), lo cual indica que los dos métodos son consistentes, es decir, que pueden usarse indistintamente, dado que hay un nivel de discrepancia permitido en este tipo de determinaciones. Como resultado, el ajuste realizado al método de titulación lo equiparó con el método de incubación para determinar los requerimientos de cal en suelos con problemas de acidez en la zona cafetera colombiana.
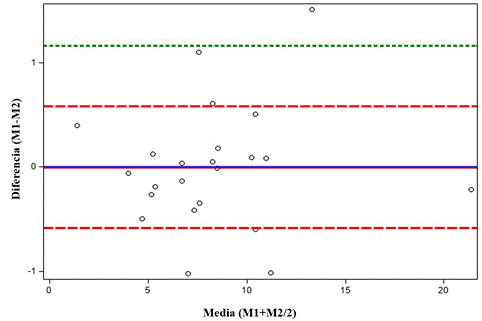
Figura 4 Análisis de concordancia de la diferencia entre el método de incubación (M1) y el método de titulación ajustado (M2) versus la media de las dos mediciones
Los resultados del estudio evidenciaron que el método de titulación para medir los requerimientos de cal puede emplearse en suelos de la zona cafetera colombiana si se hace un ajuste basado en la caracterización química y de la textura de las muestras. Se resalta que, como consecuencia de la naturaleza química de los suelos, el método de titulación pudo ajustarse mediante una expresión matemática.
Conclusiones
El método de titulación con Ca(OH)2 para determinar los requerimientos de cal fue más rápido que el de incubación con caliza dolomítica (CaCO3.MgCO3); sin embargo, este método subestimó dichos requerimientos para los suelos de la zona cafetera de Colombia. Por ello, las dosis obtenidas con este método no pudieron aplicarse directamente para definir dichos requerimientos.
Se halló una ecuación que permitió aproximar los valores de tales requerimientos obtenidos con la titulación a aquellos calculados mediante la incubación. Esta ecuación explicó el 94 % de la variación total y contiene las siguientes propiedades químicas y físicas del suelo: materia orgánica, N, P, K, Mg, S, Al, Na, Mn, Cu, B y limos. El valor generado por esta expresión matemática correspondió a un factor de corrección que se debe sumar a los valores obtenidos con el método de titulación.















