Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Colombia Médica
On-line version ISSN 1657-9534
Colomb. Med. vol.38 no.1 Cali Jan./Mar. 2007
Glucosa-6-fosfato deshidrogenasa (G6PD). Respuesta de los hematíes y otras células humanas a la disminución en su actividad
Javier Fernando Bonilla, M.D., M.Sc.1, Magda Carolina Sánchez, Lic. Quim.2, Lilian Chuaire, M.Sc.3
- 1. Profesor Asistente, Facultad de Medicina y Facultad de Rehabilitación, Universidad del Rosario, Bogotá, Colombia. e-mail:mailto:jfbonill@urosario.edu.co
- 2. Profesora Asistente, Facultad de Medicina, Universidad del Rosario, Bogotá, Colombia. e-mail: mcsanche@urosario.edu.co
- 3. Profesora Principal, Facultad de Medicina, Universidad del Rosario, Bogotá, Colombia. e-mail: lchuaire@urosario.edu.co
- Recibido para publicación julio 12, 2005 Aceptado para publicación enero 4, 2007
- 2. Profesora Asistente, Facultad de Medicina, Universidad del Rosario, Bogotá, Colombia. e-mail: mcsanche@urosario.edu.co
RESUMEN
La glucosa-6-fosfato deshidrogenasa (G6PD) es la primera enzima de la vía pentosa fosfato y la principal fuente intracelular de nicotidamina adenina dinucleótido fosfato reducido (NADPH), compuesto comprometido en diversos procesos fisiológicos,por ejemplo defensa antioxidante (sobre todo células como los eritrocitos), modulación del crecimiento endotelial, eritropoyesis, vascularización y fagocitosis. La deficiencia de G6PD es la enzimopatía ligada al cromosoma X más común en el ser humano. Si bien se puede presentar en cualquier tipo de célula, su carencia absoluta es incompatible con la vida. Según la OMS, en el mundo hay más de 400 millones de personas afectadas por la deficiencia de la enzima, y paraColombia calculan una prevalencia de la deficiencia severa entre 3% y 7%, pero no se conocen los datos relativos a las alteraciones leves y moderadas, que también tienen efectos clínicos. El presente artículo revisa los aspectos biomoleculares más importantes de la enzima, su clasificación de acuerdo con la actividad y la movilidad electroforética,y también se mencionan algunos aspectos clínicos relacionados con la alteración de su actividad.
Palabras clave: Ultraestructura; Fisiología; Genética; Epidemiología; Deficiencia de glucosa-6-fosfato deshidrogenasa; Eritrocitos; Anemia hemolítica congénita.
Todos los organismos vivientes, sean levaduras o protozoos, plantas o animales, expresan la enzima glucosa-6-fosfato deshidrogenasa (G6PD)1.
Aunque la G6PD se encuentra en el citoplasma de todas las células de los mamíferos, en los glóbulos rojos su deficiencia es más evidente, quizá porqueestas células viven durante largo tiempo sin núcleo y porque contienen proteasas que degradan la enzima mutante en mayor grado de lo que hacen las proteasas de otros tejidos1.
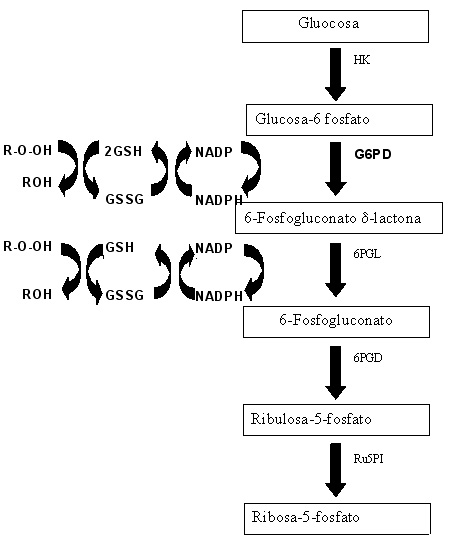
Como el eritrocito es una célula transportadora de oxígeno por excelencia sus mecanismos de defensa frente al estrés oxidativo hacen parte del mantenimiento de éste en circulación. Estos mecanismos de defensa dependen en gran parte del suministro metabólico de la forma reducida de NADP (NADPH + H+). Debido a las características metabólicas particulares de estas células, tan sólo las dos primeras reacciones de la vía de las pentosas (también llamada de la hexosa monofosfato) tienen la capacidad de generar NADPH + H. Estas son primero, la conversión de glucosa-6-fosfato en ácido-6-fosfoglucónico y segundo, la conversión de este intermediario en ribulosa-5-fosfato con desprendimiento de CO2. Las dos reacciones son secuenciales y en ambas el NADP es reducido. Mientras que la primera es catalizada por la enzima G6PD, la segunda lo es por la 6-fosfogluconato deshidrogenasa. Mediante la producción del NADPH los eritrocitos reducen el glutatión oxidado a glutatión reducido proceso catalizado por la enzima glutatión reductasa, una flavoproteína con FAD. A su vez el glutatión reducido retira el peróxido de hidrógeno, H2O2, del eritrocito en una reacción catalizada por la glutatión peroxidasa. Esta reacción es importante, porque el H2O2puede disminuir la esperanza de vida de los eritrocitos al incrementar la velocidad de la oxidación de la hemoglobina a metahemoglobina2 (Figura 1).

La deficiencia de G6PD provoca daño oxidativo irreversible y muerte celular3. La vida media de 60 días de la enzima refleja paso a paso la edad de los glóbulos rojos. Así, a mayor edad, la actividad de algunas enzimas disminuye, pues los eritrocitos son incapaces de sintetizar nuevas moléculas proteicas. Por este motivo, los reticulocitos tienen una actividad enzimática cinco veces mayor que la de los glóbulos rojos senescentes4 y deben ser separados antes de efectuar la determinación de la actividad de la enzima.
Estructura. La enzima glucosa-6-fosfato deshidrogenasa (E.C. 1.1.1.49; D-glucosa-6-fosfato: NADP oxidoreductasa)5 está presente en todas las células. En los eritrocitos se encuentra en sus formas dimérica y tetramérica. El monómero tiene un peso molecular de 59,256 daltons y consta de 515 aminoácidos. La actividad catalítica sólo se inicia cuando se establece una asociación en estado de equilibrio entre las formas dimérica y tetramérica6. Tal asociación requiere de la presencia de NADP, ligado fuertemente por la enzima7,8, lo que hace que NADP desempeñe un papel dual, tanto de componente estructural como de coenzima9-11. En 1967, Luzzatto12 postuló por lo menos dos sitios de unión del NADP a la enzima, con un estado de transición de baja a alta afinidad cuando aumenta la concentración de NADP, lo que significa que existen dos posibles formas de la enzima, de acuerdo con su afinidad por el NADP. Estas condiciones podrían variar en caso de aparición de un inhibidor competitivo del NADPH. La baja constante de disociación para el NADPH sugiere que la reacción puede ser un controlador muy eficiente, a manera de retro-alimentador, que regularía la actividad enzimática. Estos hechos permitieron establecer que la relación de concentración NADP/NADPH es un mecanismo regulador de la actividad de la G6PD y por tanto de la vía hexosa monofosfato (HMP) en el hematíe.
Función. La importancia de la G6PD radica en la trascendencia de los procesos celulares en los que participa, a saber: Génesis de NADPH, efectuada a partir de los dos primeros pasos de la vía hexosa monofosfato. El NADPH participa en la biosíntesis reductora del colesterol y de los ácidos grasos, así como también en la síntesis del óxido nítrico (NO). Por otra partese requiere para la actividad de la metahemoglobina reductasa y para el mantenimiento del nivel de glutatión reducido (GSH). NADPH y GSH son los responsables del potencial redox efectivo para proteger del estrés oxidativo tanto a los grupos sulfhidrilo de la membrana celular, como a las enzimas y a la hemoglobina que compromete la supervivencia del eritrocito3.
Otras funciones, que muestran la trascendencia de esta enzima en la vida celular son:
-
Regulación de la actividad de la proteína KU, implicada en reparar el DNA tras el daño que causan las radiaciones. La intervención de la G6PD se efectúa a través del ciclo de las pentosas y consiste en facilitar la unión de KU -con residuos de cisteína reducidos- al ADN en proceso de reparación13.
-
Desarrollo temprano del embrión. Cuando hay una deficiencia severa de G6PD en los tejidos extraembrionarios, el desarrollo de la placenta se detiene y se produce la muerte del embrión14.
-
Supervivencia del feto durante la transición de la hemoglobina fetal a la forma adulta. Aquí la G6PD impide el daño oxidativo debido a la generación de especies reactivas de oxígeno a partir de la hemoglobina adulta14,15.
-
Fagocitosis en células blancas. La deficiencia severa de esta enzima provoca una reducción de la generación de NADPH, lo que trae como resultado una disminución de la producción deH2O2, y por tanto la actividad microbicida del neutrófilo está afectada, y así mismo la respuesta inflamatoria16. Aunque las características clínicas de la deficiencia severa son semejantes a las de la enfermedad granulomatosa crónica (EGC), su aparición ocurre, a diferencia de esta última, hacia las etapas de vida más avanzadas17,18. La EGC constituye un modelo fundamental para investigar la composición y la activación del sistema microbicida de las células fagocíticas, en especial de los neutrófilos. Esta entidad se debe a un defecto profundo en la explosión respiratoria que acompaña a la fagocitosis de todas las células mieloides (neutrófilos, eosinófilos, monocitos, macrófagos). La explosión respiratoria genera la conversión catalítica del oxígeno molecular en el anión superóxido que da lugar a la formación de H2O2, de ácido hipocloroso y de radicales hidroxilo. Estos derivados del oxígeno juegan un importante papel en la reacción microbicida contra bacterias y hongos19,20.
-
Modulación del factor de crecimiento endotelial vascular que regula la angiogénesis. El NADPH se utiliza como cofactor de la óxido nítrico sintetasa endotelial (eNOS). Así, el óxido nítrico requerido para la modulación del crecimiento y la migración endotelial durante el crecimiento vascular, se mantiene en un nivel adecuado17.
-
La mayoría de los genes capaces de reducir el riesgo contra ciertas infecciones como la malaria se expresan en el glóbulo rojo, lo que se considera como un meca-nismo genético y/o evolutivo de defensa, como en el caso de los genes que expresan la G6PD21.
Deficiencia. La deficiencia de G6PD aún prevalece como el más común de todos los defectos enzimáticos heredables22,23 y clínicamente significativos, no sólo en el campo de la hematología, sino también de la biología humana24 y se caracteriza por una amplia heterogeneidad bioquímica y genética.
La deficiencia de la G6PD ha sido el prototipo, dentro de las anemias hemolíticas, debida a una enzimopatía como anormalidad primaria del eritrocito. De igual manera es un ejemplo de anemia hemolítica debido a una inter-acción entre causas extracelulares e intracelulares, ya que la hemólisis en la mayoría de los casos es disparada por agentes exógenos25.
La hemólisis de los hematíes deficientes ocurre como consecuencia del aumento en la susceptibilidad al daño oxidativo, debido a la incapacidad de las células para reducir de forma normal el NADP a NADPH. En presencia de agentes oxidantes, la producción de NADPH a través de la vía HMPse estimula múltiples veces, de modo que los niveles de NADPH y de GSH se mantienen estables. Estos eventos obedecen a la sobre-expresión de G6PD26. El mecanismo exacto en el incremento de la sensibilidad al daño oxidativo, facilitador de la hemólisis, no es claro aún. Sin embargo, existe un significativo volumen de información sobre el favismo, mayor que el disponible acerca de los diferentes medicamentos que lo pueden producir. En las habas existen sustancias como la devicina y el isouramil, que producen oxidación irreversible de GSH y de otros grupos de proteínas unidas por grupos -SH. Esto favorece en el hematíe no sólo un desequilibrio electrolítico, sino también la unión por entrecruzamiento de las membranas y microvesiculización, eventos acompañados por un aumento en la concentración de calcio en el eritrocito27.
La deficiencia de G6PD se produce por diversos mecanismos genéticos como deleciones, mutaciones puntuales y sustituciones que afectan la transcripción, procesamiento o estructura primaria de la enzima, lo que funcionalmente lleva a una disminución de la actividad enzimática o pérdida de afinidad por el sustrato. Hay otros factores que influyen sobre la actividad de la enzima. Así, en un estudio cuyo objetivo era determinar la posible relación entre la actividad de la enzima G6PD y la hipoxia, se encontró que la hipoxia favorecía una disminución en su actividad27,28.
Variantes. La deficiencia franca de G6PD se identificó inicialmente a mediados del siglo pasado, en norteamericanos de raza negra, en el curso de investigaciones llevadas a cabo sobre el efecto hemolítico de la primaquina19. En la actualidad el medicamento continúa como agente causal de la deficiencia en soldados iraquíes con malaria29.
Desde mediados del siglo pasado, se aceptó que el defecto metabólico primario en sujetos susceptibles a la hemólisis secundaria a medicamentos o al consumo de habas (Vicia faba), corresponde a una baja actividad de la G6PD en los eritrocitos30. Si bien está claramente definida la asociación entre la deficiencia de G6PD y la anemia hemolítica no inmune y no esferocítica22, también es evidente su correlación con la hemólisis debida a medicamentos, a alimentos y a otros eventos como procesos infecciosos, situación que Vulliamy et al.31 han destacado como el más importante desencadenante de hemólisis. Hacia 1958, Gross et al.30, por un lado y Szeinberg et al.22 por otro, determinaron que la deficiencia enzimática tenía una base hereditaria y sugirieron que estaba ligada al sexo.
La caracterización bioquímica ha permitido identificar no menos de 442 variantes de la deficiencia de la enzima. Alrededor de 299 fueron descritas mediante métodos utilizados por el grupo experto de la Organización Mundial de la Salud (OMS). Por otra parte, se documentaron 60 mutaciones o combinaciones, todas de naturaleza puntual, si se tiene en cuenta que la deficiencia total es incompatible con la vida23.
De acuerdo con su nivel de actividad las variantes de la enzima se agruparon en cinco clases23, que son:
Clase 1: Deficiencia de la enzima con anemia crónica hemolítica no esferocítica (CNSHA).
Clase 2: Deficiencia enzimática severa (menos de 10%, por ejemplo, la forma mediterránea).
Clase 3: Deficiencia enzimática moderada (10%-60%, por ejemplo, la forma africana).
Clase 4: Deficiencia enzimática leve o ausente (60%-100%).
Clase 5: Actividad enzimática por encima de lo normal.
La variante clase 1 es una forma rara y severa, asociada con la anemia hemolítica no esferocítica crónica. De aparición esporádica, sus casos se consideran únicos31. En regiones como los continentes africano y asiático y la cuenca mediterránea existe una alta frecuencia de las diferentes variantes de la deficiencia enzimática, mientras que en China y Japón la frecuencia es baja23.
En las poblaciones mediterráneas la deficiencia enzimática es mucho más severa y frecuente que en la población de raza negra norteamericana32, donde el defecto se identificó en los hematíes. En contraste, éste fue hallado en varios tipos celulares diversos, obtenidos en individuos sensibles italianos y de raza judía33. Con respecto a la frecuencia de la deficiencia severa, es notoria la variación entre las distintas poblaciones. Así, entre los americanos de raza negra, la frecuencia del gen de la deficiencia enzimática es de 0.10% a 0.11%34 con 15% de actividad enzimática respecto a la normal35. Como ejemplo de una frecuencia elevada de la deficiencia, se puede citar a los judíos kurdos en quienes alcanza, en su forma mediterránea, un valor igual a 0.7%36. La forma mediterránea es una variante cuya frecuencia de polimorfismo tiene una actividad menor a 10%. En ella, la mutación se presenta en el aminoácido 188, con sustitución de fenilalanina (Phe) por serina (Ser)37.
En Arabia Saudita la variante más frecuente es la mediterránea, con frecuencias que oscilan entre 0% y 0.4% en hombres y 0% y 0.2% en mujeres. Es posible que la alta prevalencia en mujeres obedezca a una disomía uniparental o bien, a la alta consanguinidad existente o a que el cromosoma X que contiene el gen normal sea el que se inactiva durante la impronta genética38.
En latinoamérica se han descrito algunas variantes de la enzima. En México por ejemplo, se identificaron 18, que son también de común aparición en otras regiones como el continente africano, el sur de Europa y el sudeste asiático39. Mientras que en México la frecuencia de la deficiencia estuvo entre 0.4% y 4.1%, en Cuba fue 4.9% con una prevalencia de la variante A-, y 7% para la variante A+40. Para países como Colombia, la frecuencia calculada por la OMS para las variantes fenotípicamente asociadas con la deficiencia severa (clase 2, con actividad menor de 10%) es entre 3% y 7%23. Sin embargo, en 103 individuos de sexo masculino, donantes del Banco de Sangre de la Cruz Roja Colombiana y en apariencia sanos, se halló una frecuencia de actividad subnormal (<60%) de aproximadamente 19.4%. Este estudio se hizo entre junio y octubre de 2003, mediante la aplicación de la técnica cualitativa de Beutler E (Palomino F. 2003. Universidad Nacional de Colombia. Comunicación personal).
Otra clasificación compara la movilidad electroforética de lasdiversas variantes con la enzima normal B, siendo la variante A-, presente en individuos de raza negra con baja actividad enzimática, más rápida en un pH alcalino que la enzima normal, en contraste, la variante de los sujetos deficientes mediterráneos se mueve a una velocidad normal37.
Otra variante común, A+, tiene una actividad normal y se encuentra en más o menos 20% de los norteamericanos de raza negra. Esta variante es electroforéticamente más rápida que la B, hecho explicable si se tiene en cuenta que la sustitución de asp (aminoácido neutro) por asn (aminoácido ácido) en la posición 126 modifica la carga eléctrica de la enzima, lo que se refleja en una movilidad electroforética más rápida37.
La variante A- se encuentra en cerca de 11% de la población negra norteamericana. No obstante, su frecuencia es mayor en la población del África negra subsahariana. La actividad enzimática de esta variante corresponde a 5% y 15% de la normal, disminución debida a la presencia de dos sustituciones, no de una como ocurre en la variante A+. Una de esas sustituciones es idéntica a la que aparece en la variante A+ y la otra, única para esta variante, obedece al cambio de val por met en la posición 6841.
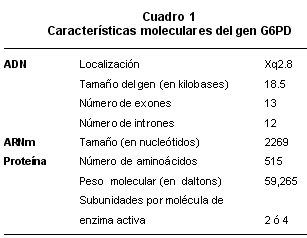
Genética. A la enzima G6PD la codifica un gen presente en la región terminal del brazo largo del cromosoma X, (Xq28), menos de 2 centi-Morgan al gen del factor VIII. En los hombres, la condición hereditaria ligada a X determina su carácter hemicigótico, lo que significa que hay un solo alelo, debido a la ausencia del locus homólogo. También hay mujeres homocigotas en poblaciones cuya frecuencia de la deficiencia de G6PD es alta. Las mujeres heterocigotas son portadoras aunque pueden desarrollar ataques hemolíticos. El gen de la G6PD se ha ubicado en la parte distal del brazo largo, tiene 18 Kb de largo y consta de 13 exones42 (Cuadro 1).
La región del gen que codifica para la proteína comprende 12 segmentos, con un promedio de tamaño entre 12 y 236 bp y un intrón presente en la región no traductora 5. En muchas líneas celulares, el extremo mayor 5 del ARNm de la G6PD se localiza a una distancia de 177 bp «upstream» del codón de iniciación de la transcripción43,44. Aunque las mutaciones se extienden a lo largo de la región codificadora del gen, existen unas pocas (4 de 56) que dan origen a la forma más severa de deficiencia de la enzima, esto es, la que se encuentra asociada con CNSHA (clase 1) en los 160 aminoácidos del extremo N-terminal. No obstante, no hay ninguna que cause formas moderadas de deficiencia (clases 2 y 3) en los 48 aminoácidos del extremo C-terminal. Muchas variantes en esta región exhiben movilidades electroforéticas anormales y son particularmente inestables cuando la concentración de NADP es baja. Esto se debe a que esta región codifica para el dominio de unión al NADP45.
En la variante A- se presenta una sustitución idéntica a la A+, aunque hay una segunda sustitución en el nucleótido 202 G---> A del exón 4, lo que provoca el cambio val por met, acompañado por inestabilidad de la enzima in vivo. Así, la diferencia entre las formas A y B corresponde al aminoácido que ocupa la posición 126, presumiblemente como resultado de un empalme alternativo o «splicing» de considerable heterogeneidad entre los diferentes cADNs de la G6PD41.
Manifestaciones clínicas. Casi todas las personas que cursan con la deficiencia de G6PD son usualmente asintomáticas y sólo se manifiesta la enfermedad cuando ingieren drogas o químicos que desencadenan la hemólisis masiva intravascular. La expresión clínica entonces resulta de la interacción de las propiedades moleculares de cada variante de G6PD y de factores exógenos. Se han descrito diferentes síndromes clínicos asociados con la deficiencia de esta enzima que incluyen:
Hemólisis inducida por fármacos. Clásicamente, luego de la ingestión de ciertos agentes como sulfamidas, antipiréticos, nitrofuranos y medicamentos antimaláricos, como la primaquina y cloroquina, el paciente desarrolla fiebre, orina de color negro, ictericia y anemia. La necrosis tubular aguda puede complicar el episodio hemolítico severo, sobre todo en las enfermedades subyacentes del hígado, como hepatitis. El mantenimiento del flujo renal adecuado de la sangre, por diuresis alcalina forzada, puede prevenir esta complicación. En estos casos con flujo renal comprometido de la sangre según lo evidenciado por la salida baja de la orina, la transfusión es lo ideal con el propósito de eliminar las células rojas dañadas que bloquean la microcirculación y puede también evitar la complicación renal. En algunos pacientes, la coagulación intravascular diseminada (DIC) puede complicar la hemólisis intravascular masiva y necesitar el tratamiento apropiado45.
Hemólisis inducida por infección. La infección es quizá la causa más común en quienes sufren deficiencia de G6PD. El mecanismo de hemólisis inducida por infecciones no es bien conocido; una explicación puede ser que la generación de H2O2 por los neutrófilos polimorfonucleares puede provocar una disminución en la cantidad de glutatión reducido, cuya función es eliminar del glóbulo rojo la acumulación de metabolitos que oxidan a los grupos sulfhidrilos formados por el estrés oxidativo, por lo que disminuye la capacidad protectora de la célula. Por otra parte, la activación de los neutrófilos interviene directamente en la peroxidación de los lípidos de la membrana y provoca de forma directa la destrucción de la célula46. La severidad y las consecuencias clínicas están influidas por muchos factores que incluyen la administración simultánea de medicamentos oxidantes, los niveles de hemoglobina previos, la función hepática y la edad47.
Favismo. Se reconoce desde la antigüedad; los pacientes presentan un cuadro clínico similar al inducido por fármacos, que se desencadena dentro de las 24 y 48 horas siguientes a la ingesta de habas. Se caracteriza por la presencia de un cuadro de hemólisis aguda luego de ingerir habas, sin embargo, no todos los individuos con deficiencia de G6PD presentan hemólisis cuando comen habas48.
Los síntomas del favismo se desarrollan pocas horas después de la ingestión. Los más comunes son náuseas, vómitos, malestar y vértigo. A estos síntomas les sigue una hemólisis aguda donde, a menudo, el recuento de eritrocitos cae por debajo de 1.0 x 1012/l. En la mayoría de los glóbulos rojos aparecen cuerpos de Heinz. Están presentes la hemoglobinemia y la hemoglobinuria. Los síntomas por lo general cesan luego de 2 a 6 días49,50.
Anemia hemolítica crónica no esferocítica. Las variantes de clase I, se caracterizan por este hallazgo, debido al grado tan severo de deficiencia enzimática. La hemólisis es sólo parcialmente intravascular y se puede acompañar de cálculos biliares y esplenomegalia. Sin embargo, existe una variabilidad en las manifestaciones asociadas con este tipo de anemia crónica47,50,51. En la literatura hay informes de casos donde describen anemia hemolítica crónica y una causa, aunque rara, es la deficiencia de G6PD52.
Preeclampsia. Entidad al parecer asociada en forma parcial con una peroxidación lipídica de la membrana plasmática del sincitiotrofoblasto. De ahí que las mujeres con alguna alteración en la actividad de la G6PD pueden tener serias dificultades en la reducción del GSSG a GSH y así presentar alteraciones en la defensa antioxidante53.
De otro lado es interesante señalar cómo la deficiencia de G6PD (variante A-) se asocia con aumento en la resistencia a la infección por Plasmodium falciparum en la región subsahariana de África. Esto indica que hay una fuerte respuesta adaptativa frente a esta invasión del hematíe54.
CONCLUSIONES
Si se tiene en cuenta que Colombia ha sido asiento de múltiples migraciones provenientes de África y Europa, es necesario llevar a cabo estudios que evalúen el rango de actividad de la G6PD, así como sus posibles variantes en esta región. El conocimiento obtenido podrá complementar los hallazgos efectuados en otras latitudes y por tanto derivará en un mejor diagnóstico, enfoque y tratamiento de las enfermedades asociadas con la hemólisis y la oxidación, como anemia, diabetes, hipertensión arterial y cáncer entre otras. Por otro lado, este conocimiento se podrá aplicar en el área de la fisiología del ejercicio, donde, a causa del estrés oxidativo, pueden ocurrir desde hemólisis hasta la muerte súbita del deportista.
En vista de los crecientes hallazgos sobre la participación en ciertas entidades patológicas, así como en la comprensión de procesos evolutivos de la especie humana, la determinación de la actividad de esta enzima es una prioridad para poblaciones como la colombiana donde sólo se tienen datos extrapolados por la OMS.
En distintas partes del mundo surgen diferentes técnicas que intentan favorecer la determinación rápida con alta sensibilidad y especificidad de la actividad de esta enzima55,56, sin embargo, para Colombia sólo se han hecho algunas determinaciones de grupo pequeños (datos sin publicar) pero hay grupos de trabajo en ciertas universidades, como la Universidad del Rosario en Bogotá, que pronto empezarán a dar resultados sobre la prevalencia de esta alteración en el metabolismo de tipo hereditario.
REFERENCIAS
1. Beutler E. Selectivity of proteases as a basis for tissue distribution of enzymes in hereditary deficiencies. Proc Natl Acad Sci USA 1983; 80: 3767-3768. [ Links ]
2. Grimes A. The hexose monophosphate pathway. In: Human red cell metabolism. Capítulo 8. Londes: Editorial Blackwell Scientific Publications;1980. 192-201.
3. van Wijk R, van Solinge WW. The energy-less red blood cell is lost-erythrocyte enzyme abnormalities of glycolysis. Blood 2005; 10: 1604-1622. [ Links ]
4. Arese P, De Fiora A. Pathophysiology of hemolysis in glucose-6-phosphate dehydrogenase deficiency. Semin Hematol 1990; 27: 1-40. [ Links ]
5. IUPAC. The International Union of Pure and Applied Chemistry. Actualizada 30 de enero de 2007 (fecha de acceso 5 de febrero de 2007). URL disponible en: http://www.iupac.org/ [ Links ]
6. Kirkman HN, Hendrickson EM. Glucose 6-phosphate dehydrogenase from human erythrocytes. II. Subactive states of the enzyme from normal persons. J Biol Chem 1962; 237: 2371-2376. [ Links ]
7. Chung A, Langdom R. Human erythrocyte glucose-6-phosphate dehydrogenase. I. Isolation and properties of the enzyme. J Biol Chem 1963; 238: 2309-2316. [ Links ]
8. Chung AE, Langdon RG. Human erythrocyte glucose-6-phosphate dehydrogenase II. Enzyme-coenzyme interrelationship. J Biol Chem 1963; 238: 2317-2324. [ Links ]
9. Marks PA, Tsutsui EA. Human glucose-6-P dehydrogenase: studies on the relation between antigenicity and catalytic activity. The role of TPN. Ann NY Acad Sci 1963; 103: 902-914. [ Links ]
10. Canepa L, Ferraris AM, Miglino M, Gaetani GF. Bound and unbound pyridine dinucleotides in normal and glucosa-6-phosphate dehydrogenase-deficient erythrocytes. Biochim Biophys Acta 1991; 1074: 101-104. [ Links ]
11.Bonsignore A, Cancedda R, Nicolini A, Damiani G, Deflora A. Metabolism of human erythrocyte glucose-6-phosphate dehydrogenase. VI. Interconversion of multiple molecular forms. Arch Biochem Biophys 1971; 147: 493-497. [ Links ]
12. Luzzatto L. Regulation of the activity of glucose-6-phosphate dehydrogenase by NADP+ and NADPH. Biochim Biophys Acta 1967; 146: 18-25. [ Links ]
13. Iraimoud S, Sttamato T, Mauldin S, Biaglow J et al. Mutation in the glucose 6 phosphate deshydrogenase gene leads to inactivation of Ku DNA end binding during oxidative Stress. J Biol Chem 2002; 277: 9929-9935. [ Links ]
14. Longo L, Vanegas O, Patel L, Rosti V, Li H, Waka J. et al. Maternally transmitted severe glucose 6 phosphate dehydrogenase deficiency is an embryonic lethal. EMBO J 2002, 21: 4229-4239. [ Links ]
15. Prchal JT. G6PD activity is essential for definite erythropoiesis. Blood 2004; 104: 2997. [ Links ]
16. Wilmanski J, Villanueva E, Deitch EA, Spolarics Z. Glucose-6-phosphate dehydrogenase deficiency and the inflammatory response to endotoxin and polymicrobial sepsis. Crit Care Med 2007; 35: 510-518. [ Links ]
17. Leopold J, Walker J, Scribner, Voetsch B, Zhang Y, Losclazo A, et al. Glucose-6-phosphate dehydrogenase modulates vascular endothelial growth factor-mediated angiogenesis. J Biol Chem 2003; 278: 32100-32106.
18. Chollet S, Gougerot M. Hereditary polymorphonuclear neutrophil deficiencies. Transfus Clin Biol 2000; 7: 533-539. [ Links ]
19.Beutler E. The hemolytic effect of primaquine and related compounds. A review. Blood 1959; 14: 103-139. [ Links ]
20. van Bruggen R, Bautista J, Petropoulou Th, de Boer M, van Zwieten R, Gómez-Gallego F, et al. Deletion of leucine 61 in glucose-6-phosphate dehydrogenase leads to chronic nonspherocytic anemia, granulocyte dysfunction, and increased susceptibility to infections. Blood 2002; 100: 1026-1033. [ Links ]
21. Tishkoff S, Varkonyi R, Cahinhinan L, Abbes S, Argyroupoulos G, Destro-Bisol G, et al. Haplotype diversity and linkage disequilibrium at human G6PD: recent origin at alleles that confer malarial resistance. Science 2002; 293: 455-462. [ Links ]
22. Szeinberg A, Sheba C, Adam A. Enzymatic abnormality in erythrocytes of a population sensitive to Vicia faba or hemolytic anemia induced by drugs. Nature 1958; 181: 181-183. [ Links ]
23. WHO Working Group. Glucose-6-phosphate dehydrogenase deficiency. Bull WHO 1989; 67: 601-611. [ Links ]
24. Beutler E. G6PDH deficiency. Blood 1994; 84: 3613-3636. [ Links ]
25. Luzzatto L. Glucose 6-phosphate dehydrogenase deficiency: from genotype to phenotype. Hematology 2006; 91: 1303-1305. [ Links ]
26. Salvemini F, Franze A, Lervolino, Filosa S, Salzano S, Ursini M. Enhanced glutathione levels and oxidoresistance mediated by increased glucosa-6-phosphate dehydrogenase expression. J Biol Chem 1999; 274: 2750-2757. [ Links ]
27. Turrini F, Naitana A, Mannuzzu L, Pescarmona G, Arese P. Increased red cell calcium adenosine triphosphatase, and altered membrane proteins during Fava bean hemolysis in glucose-6-phosphate dehydrogenase-deficient (Mediterranean variants) individuals. Blood 1985; 66: 302-305. [ Links ]
28. Torres K, Tuero I, Colarossi A. Efecto de la hipoxia sobre la actividad de la enzima G6PD en eritrocitos. Facultad de Ciencias y Filosofía. Departamento de Bioquímica y Biología Molecular, Universidad Peruana Cayetano Heredia. Lima , Perú; 2001. Memorias del XII Jornada Científica Alberto Cazorla Talleri. [ Links ]
29. Carr M, Fandre MN, Oduwa FO. Glucose-6-phosphate dehydrogenase deficiency in two returning Operation Iraqi Freedom soldiers who developed hemolytic anemia while receiving primaquine prophylaxis for malaria. Mil Med 2005; 170: 273-276. [ Links ]
30. Gross R, Hurwitz R, Marks P. A hereditary enzymatic defect in erythrocyte metabolism: glucose-6-phosphate dehydrogenase deficiency. J Clinic Invest 1958; 37: 1176-1184. [ Links ]
31. Vulliamy T, Kaeda J, Ait C. Clinical and haematological consequences of recurrent G6PD mutations and a single new mutation causing chronic nonspherocytic haemolytic anaemia. Br J Haematol 1998; 101: 670-675. [ Links ]
32. Marks P, Banks J, Gross R. Genetic heterogeneity of glucose-6-phosphate dehydrogenase deficiency. Nature 1962; 194: 454-459. [ Links ]
33. Szeinberg A, Sheba C, Adam A. Selective occurrence of glutathione instability in red blood corpuscles of the various Jewish tribes. Blood 1958; 13: 1043-53. [ Links ]
34. Heller P, Best W, Nelson R, Becktel J. Clinical implications of sickle-cell trait and glucose-6-phosphate dehydrogenase deficiency in hospitalized black male patients. N Engl J Med 1979; 300: 1001-1005. [ Links ]
35. Jaffé E. The reduction on methemoglobin in erythrocytes of a patient with congenital methemoglobinemia, subjects with erythrocytes glucose-6-phosphate dehydrogenase deficiency, and normal individuals. Blood 1963; 21: 561-572. [ Links ]
36. Oppenheim A, Jury C, Rund D, Vulliamy T, Luzzatto L. G6PD Mediterranean accounts for the high prevalence of G6PD deficiency in Kurdish Jews. Hum Gen 1993; 91: 293-296. [ Links ]
37. Beutler E. Glucose-6-phosphate dehydrogenase: New perspectives. Blood 1989; 73: 1397-1401. [ Links ]
38. Warsy A, Mohsen A. G6PD deficiency, distribution and variants in Saudi Arabia: an overview. Ann Saudi Med 2001; 21: 174-177. [ Links ]
39. Vaca G, Arámbula E, Monsalvo A, Medina C, Nuñez C, Sandoval L, et al. Glucose-6-phosphate dehydrogenase (G-6-PD) mutations in Mexico: four new G-6-PD variants. Blood Cells Mol Dis 2003; 31: 112-120. [ Links ]
40. Estrada M, Gutiérrez A, Palacios B, Pérez G, Rovira A, Vives J. Estudio bioquímico y molecular de la glucosa-6-fosfato deshidrogenasa en Cuba. Rev Cubana Hematol Inmunol Hemoterapia 1995; 2: 1-5. [ Links ]
41. Hirono A, Beutler E. Molecular cloning and nucleotide sequence of cDNA for human glucose-6-phosphate dehydrogenase variant A (-). Proc Natl Acad Sci USA 1988; 85: 3951-3954. [ Links ]
42. Persico M, Viglietto G, Martini G, Toniolo D, Paonessa G, Moscatelli C, et al. Isolation of human glucose-6-phosphate dehydrogenase (G6PD) cDNA clones: primary structure of the protein and unusual 5´non-coding region. Nucl Acid Res 1986; 14: 2511-2522. [ Links ]
43. Takizawa T, Huang IY, Ikuta T, Yoshida A. Human glucose-6-phosphate dehydrogenase: primary structure and cDNA cloning. Proc Natl Acad Sci USA 1986; 83: 4157-4161. [ Links ]
44. Martini G, Toniolo D, Vulliamy T, Luzzatto L, Dono R, Viglietto G, et al. Structural analysis of the X-linked gene encoding human glucose 6-phosphate dehydrogenase. EMBO J 1986; 5: 1849-1855. [ Links ]
45. Hirono A, Kuhl W, Gelbart T. Identification of the binding domain for NADP+ of human glucose-6-phosphate dehydrogenase by sequence analysis of mutants. Proc Nat Acad Sci USA 1989; 86: 10015-10017. [ Links ]
46. Mehta A, Mason P, Vulliamy T. Glucose-6-phosphate dehydrogenase deficiency. Clin Haematol 2000; 13: 21-38. [ Links ]
47. van Bruggen R, Bautista JM, Petropoulou T, de Boer M, van Zwieten R, Gómez-Gallego F, et al. Deletion of leucine 61 in glucose-6-phosphate dehydrogenase leads to chronic nonspherocytic anemia, granulocyte dysfunction, and increased susceptibility to infections. Blood 2002; 100: 1026-1030. [ Links ]
48. Mehta A, Mason P, Vulliamy T. Glucose-6-phosphate dehydrogenase deficiency. Clin Haematol 2000; 13: 21-38. [ Links ]
49. Dalal B, Kollmannsberger C. Drug-induced haemolysis and methaemoglobinaemia in glucose 6-phosphate dehydrogenase deficiency. Br J Haematol 2005, 129: 291-296. [ Links ]
50. Acosta T, Nuñez D, Suárez M. Anemia hemolítica por deficiencia de G6PD y estrés oxidativo. Rev Cubana Invest Biomed 2003; 22: 186-191. [ Links ]
51. Beutler E. Discrepancies between genotype and phenotype in hematology: an important frontier. Blood 2001; 98: 2597-2602. [ Links ]
52. Hundsdoerfer P, Vetter B, Kulozik A. Chronic haemolyticanaemia and glucose-6 phosphate dehydrogenase deficiency. Case report and review of the literature. Acta Haematol 2002; 108: 102-105. [ Links ]
53. Abdulhadi N. Glucose 6-phosphate dehydrogenase (G6PD) deficiency is a posible risk factor for the development of preeclampsia. Med Hypotheses 2004; 62: 780-782. [ Links ]
54. Saunders M, Slatkin M, Garner C, Hammer M, Nachman M. The extent of linkage desequilibrium caused by selection on G6PD in humans. Genetics 2005; 171: 1219-1229. [ Links ]
55. Gurbuz N, Aksu T, Van Noorden C. Biochemical and cytochemical evaluation of heterozygote individuals with glucose-6 phosphate dehydrogenase deficiency. Acta Histochem 2005; 107: 261-267. [ Links ]
56. Tagarelli A, Piro A, Bastone L, Condino F, Tagarelli G. Reliability of quantitative and qualitative tests to identify heterozygotes carryng severe or mild G6PD deficiency. Clin Biochem 2006; 39: 183-186. [ Links ]











 text in
text in