Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Colombia Médica
On-line version ISSN 1657-9534
Colomb. Med. vol.38 no.2 Cali Jan./Mar. 2007
Semliki Forest Virus: un vector viral con múltiples aplicaciones
Luis Felipe Henao, Biol1,2, Fabián Cortés, Bact2,3, María Cristina Navas2,4, M.Sc., D.Sc.
1. Biólogo, Universidad de Antioquia, Medellín, Colombia. e-mail: lfelipehc@hotmail.com
2. Grupo de Gastrohepatología, Facultad de Medicina, Universidad de Antioquia, Medellín, Colombia.
3. Estudiante de Maestría, Corporación Ciencias Básicas Biomédicas, Universidad de Antioquia, Medellín, Colombia. e-mail: fabiancortesm@yahoo.com
4. Profesora Asociada, Grupo de Gastrohepatología, Facultad de Medicina, Universidad de Antioquia, Medellín, Colombia. e-mail: mcnavasn@gmail.com
Recibido para publicación mayo 31, 2005 Aceptado para publicación abril 16, 2007
RESUMEN
Se han utilizado los alfavirus como vectores de expresión, entre estos se encuentra el Semliki Forest virus (SFV), que es un virus envuelto, el cual, además de replicarse en el citoplasma, tiene la propiedad de expresar por separado las proteínas estructurales de las no estructurales, permitiendo un mayor control de la expresión. Los vectores derivados del SFV pueden tener una gama amplia de aplicaciones. Se pueden obtener altos títulos virales para la expresión eficiente de proteínas en diferentes líneas celulares. Pueden infectar un espectro amplio de células de mamíferos, así como de tejidos. Son prometedores para ser usados en la terapia génica como vehículos para el envío de genes específicos in vivo o in vitro, tanto en la terapia contra el cáncer como en la neuronal, especialmente cuando sólo sea necesaria una expresión a corto plazo. Sus aplicaciones en la producción de vacunas profilácticas o terapéuticas, es otro aspecto estudiado; se ha demostrado la generación de respuestas inmunes importantes contra diferentes enfermedades virales y tumorales. El desarrollo de nuevos vectores no citopáticos, de otros regulados por temperatura, así como también de otros con replicación persistente; permitirán la prolongación de la expresión. Debido a estas nuevas ventajas y a las ya conocidas, gradualmente se podrían ampliar los usos para los vectores derivados del SFV a medida que se controlen sus efectos no deseados.
Palabras clave: Virus de los bosques de Semliki; Transducción genética; Expresión génica.
Semliki Forest Virus: a viral vector with multiple applications
SUMMARY
Recently, Alphavirus have been used as expression vectors, among these, Semliki Forest virus (SFV), an enveloped virus, besides replicating itself in the cytoplasm, has the property to express structural proteins separately from nonstructural proteins, allowing a greater expression control. Vectors derived from SFV can have a broad range of applications. High viral titers can be obtained to efficiently express proteins in different cell lines. They can infect a wide spectrum of mammalian cells, as well as tissues. They are promising to be used on gene therapy as vehicles for specific gene delivery in vivo or in vitro, as much as in therapy against cancer as neuronal therapy, especially when a short term expression is necessary. Another studied aspect is SFV vectors applications in prophylactic or therapeutic vaccine production; the generation of important immune responses against different viral and tumor diseases is still been discussed. Development of new non-cytopathic vectors, temperature-regulated vectors, as well as others with persistent replication, will allow prolongation of expression. Due to these new advantages and to others already known, uses for vectors derived from SFV could be extended gradually, as long as undesired effects are controlled.
Keywords: Semliki forest virus; Transduction genetic; Gene expression.
El uso de vectores para la producción de proteínas heterólogas se conoce como sistemas de expresión. La expresión génica en cultivos de células de mamíferos está limitada por la pobre eficiencia en la transfección, un limitado rango de células hospederas, y la complejidad de los sistemas de expresión. Los virus recombinantes son la herramienta más eficiente para la producción de proteínas en células eucariotes superiores. Los sistemas virales disponibles a nivel comercial o en desarrollo para investigaciones biomédicas se basan principalmente en los adenovirus (AV), virus adeno asociados (VAA), retrovirus (RV), lentivirus (LV), herpesvirus (HV) y vaccinia virus (VV), los cuales permiten la expresión heteróloga en células de mamíferos, y los baculovirus (BV) en células de insectos. Estos sistemas tienen ventajas y limitaciones, el tiempo de expresión, el tipo celular que infectan, el riesgo de bioseguridad1-5.
Los alfavirus han emergido como una herramienta útil en la producción rápida y eficiente de proteínas heterólogas. El género Alfavirus pertenece a la familia Togaviridae, estos virus se replican tanto en células de vertebrados como de invertebrados. El virus Sindbis y el Semliki Forest Virus (SFV, de sus siglas en inglés; el virus del bosque Semliki, de su traducción al español) son ampliamente conocidos como modelos de estudios a nivel de biología molecular y celular. Ambos han sido considerados como excelentes sistemas de expresión debido a que sus genomas se autoamplifican y sólo requieren de la maquinaria traduccional del hospedero para replicarse6.
En esta revisión se describen ampliamente las propiedades de un vector viral poco conocido en Colombia que puede tener importantes aplicaciones médicas a corto o mediano plazo. Se pretende hacer una revisión en la cual se presentan tanto los posibles beneficios como los posibles problemas del uso del SFV para la salud humana.
BIOLOGÍA MOLECULAR Y CICLOREPLICATIVO DEL SFV
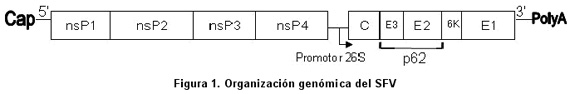
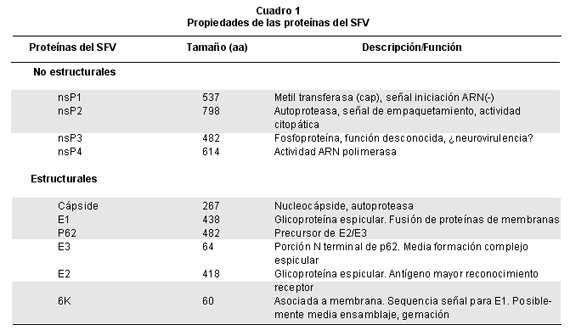
El SFV es un virus envuelto de un tamaño de 70 nm. Su genoma consta de ARN de cadena simple con polaridad positiva (ARN+) de aproximadamente 11.5 kilobases, codifica para 9 proteínas, 4 no estructurales (nsP1-4) y 5 estructurales (Cápside, p62[E3,E2], 6K, E1) (Figura 1), y es autoamplificable (se replica y transcribe sin la ayuda de proteínas celulares). En el Cuadro 1 se describen las propiedades de las proteínas del SFV7.
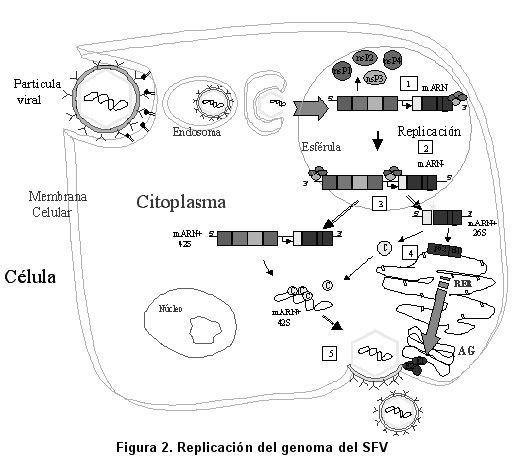
La partícula viral madura del SFV contiene una sola copia de ARN en una cápside icosahédrica (nucleocápside) formada por 240 proteínas de la cápside (C), rodeada por una bicapa lipídica (envoltura) que contiene 80 heterotrímeros de las glicoproteínas E1, E2 y E3 (espículas)8, se adhiere a la superficie celular por medio de las proteínas de la espícula (E2), penetrando la célula por un proceso de endocitosis dependiente de receptor. La fusión de la envoltura viral y la membrana endosomal, mediada por E1, permite la liberación de la nucleocápside, que es descapsidada, con la posterior salida del genoma viral al citoplasma celular9.
En el citoplasma, el ARN genómico del SFV sirve inicialmente como ARNm. Después, se traducen los dos tercios 5 del ARN viral a una poliproteína, que luego es cortada en 4 proteínas no estructurales que forman el complejo replicasa requerido para la replicación del ARN. El complejo inicia la replicación de cadenas completas de ARN con polaridad negativa (ARN-) en el extremo 3 del ARN genómico, las cuales en el curso de la infección generan múltiples copias de ARN+ genómico (42S). Las cadenas negativas también sirven como molde para la síntesis de un ARN subgenómico (26S), que corresponde al último tercio del genoma y que codifica las proteínas estructurales, gracias al reconocimiento del promotor 26S inmediatamente anterior a los genes estructurales (promotor 26S). Esta región subgenómica es traducida a una poliproteína precursora que es cortada cotraduccionalmente por la función autoproteasa de la C, generando la proteína de la C y el complejo de las glicoproteínas de la espícula (p62, 6K, E1). La proteína de la C reconoce una señal de encapsidación que está en la región codificadora para nsP2 y junto con el ARN+ completo constituye la nucleocápside, mientras que el complejo espicular es translocado cotraduccionalmente al retículo endoplasmático rugoso (ER) y las glicoproteínas son dirigidas a la membrana plasmática (MP) a través del complejo de Golgi, donde p62 es cortada a su forma madura E2 y E3. En la MP se da el proceso de gemación que es necesario para que el virus adquiera la bicapa lipídica, formándose la partícula viral infecciosa que sale al medio extracelular10,11(Figura 2).
SISTEMAS DE EXPRESIÓN DERIVADOS DEL SFV
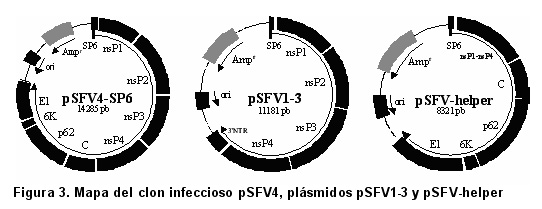
El sistema original de expresión del SFV utiliza un plásmido en el que el promotor bacteriófago SP6 se encuentra corriente arriba del ADN copia (ADNc, sintetizado a partir del ARNm) del genoma del SFV, con el que se construyó el plásmido pSFV4, que sirve para producir transcritos completos para replicación en células animales7 (Figura 3).
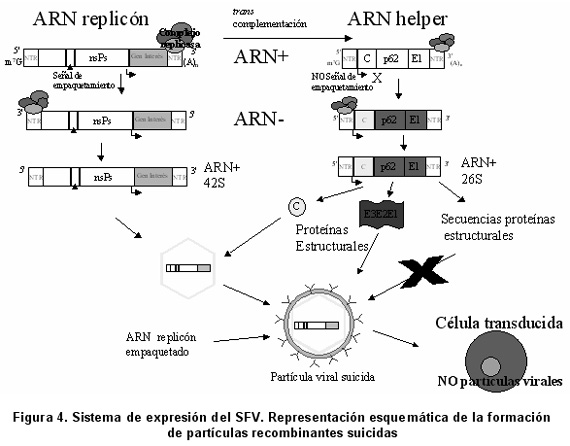
Para la producción de proteínas heterólogas, el SFV utiliza dos plásmidos subclonados a partir del ADNc del genoma del SFV. El primero es el vector replicón, pSFV1-3, en el cual un gen heterólogo (insertado en un sitio de policlonación) reemplaza la secuencia que codifica las proteínas estructurales virales, pero conserva el promotor subgenómico 26S que permite una alta expresión de la proteína heteróloga. Para la producción de las partículas recombinantes, el vector replicón es transcrito in vitro a ácido ribonucleico (ARN) y luego cotransfectado por electroporación o lipofección en células de mamíferos in vitro con el transcrito correspondiente al vector helper (pSFV-helper), que proporciona las secuencias de las proteínas estructurales en trans al vector replicón, aunque carece de la secuencia que codifica las proteínas no estructurales necesarias para la replicación viral, donde es amplificado. Se generan grandes cantidades de la proteína requerida a partir de la región subgenómica, hasta un millón de copias por ciclo. Las partículas que se generan in vivo contienen un genoma defectuoso (sólo contiene el ARN replicón) y aunque son capaces de replicarse, no producen partículas de novo, garantizando la bioseguridad del sistema. Cuando tales partículas recombinantes (partículas suicidas) se usan para transducir células animales, sólo el complejo de replicación y la proteína heteróloga son expresados7 (Figura 4).
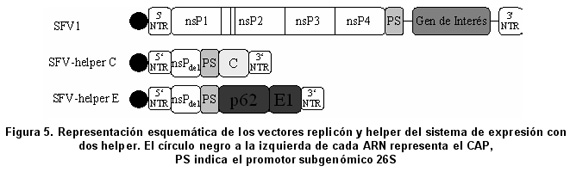
Se desarrollaron varias estrategias para evitar la posible formación de partículas virales silvestres durante el empaquetamiento, debido a la recombinación entre los dos tipos de ARN o al co-empaquetamiento: vectores helper (pSFV-helper-2) con mutaciones puntuales en p62, permitiendo la obtención de partículas con capacidad infecciosa limitada12; el empaquetamiento de ARN recombinante del SFV es un sistema de dos ARN helper, uno que expresa la proteína de la cápside (pSFV-helper-C) y otro que expresa las glicoproteínas virales (pSFV-helper-E)13 (Figura 5), el cual luego fue modifcado para lograr altos niveles de expresión de las glicoproteínas virales (similares a los de la cápside), se introdujo la secuencia «Cenh» antes de p62 y la secuencia que codifica la proteasa 2A del virus de la fiebre aftosa (FMDV, de sus siglas en inglés) entre éstas, para generar un sitio proteolítico, dando origen a los plásmidos pSFV-helper-S13.
Otra estrategia diseñada con el fin de mejorar la estabilidad genética del vector y evitar la síntesis de partículas virales silvestres fue la clonación de un gen heterólogo en el plásmido que contiene los genes del complejo de replicación sin la posterior co-transfección del vector «helper». Una limitante de esta estrategia fue lograr la expresión sostenida del gen de interés, para tal efecto EGFP fue insertado entre los genes nsP3 y nsP4, y flanqueado por duplicaciones del sitio de reconocimiento de la proteasa nsP2 (la unión nsP3/4), y aunque la replicación fue menos eficiente comparado con el virus silvestre, hubo cambios menores en el fenotipo y aumento en la estabilidad genética del gen reportero, luego de varios pases en el modelo in vivo14.
Avances en el desarrollo de vectores basados en el SFV. Aunque los vectores basados en el SFV tienen una amplia gama de aplicaciones, tienen características, que hasta cierto punto, limitan su uso. Los niveles extremadamente altos de expresión génica obtenidos a partir de vectores del SFV, no son comparables con los niveles fisiológicos15.
La alta toxicidad de los vectores para las células hospederas puede, de cierto modo, limitar la expresión de proteínas reporteras debido a la apoptosis inducida por la replicación viral. Este efecto limita los estudios sobre la cinética de expresión y las vías de transducción de señal15. Por esta razón, se han desarrollado novedosos vectores menos citotóxicos con alta expresión génica, basados en el SFV, como el SFV(PD), al que se le indujeron mutaciones en nsP215,16. También se ha diseñado un vector no citopático con tres mutaciones puntuales en nsP2, el SFV(PDE153), que ha demostrado tener un fenotipo sensible a la temperatura en células BHK y neuronas, en las que a una temperatura de 31°C induce niveles altos de expresión de proteínas. Este vector puede ser útil para aplicaciones en neurobiología, porque in vivo a mayor temperatura infecta preferentemente interneuronas y a menor temperatura células piramidales, en las que normalmente genera expresión génica el vector silvestre, permitiendo abordar temas como el control de la actividad de la red neuronal por medio de la actividad interneuronal17.
Otra característica de los vectores del SFV, la naturaleza transitoria de la expresión, es un impedimento si se desea una expresión duradera15. Se obtuvo un vector con una mutación puntual en nsP2, mediante la transfección de células BHK con replicones del SFV con mutaciones al azar en los genes no estructurales, que permitía una expresión más prolongada. Este vector se caracterizó por una replicación persistente y una muy baja citotoxicidad; puede ser de particular interés para prolongar estudios de expresión in vivo a nivel neuronal18. Los vectores basados en Alfavirus generalmente muestran una marcada preferencia por infectar neuronas.
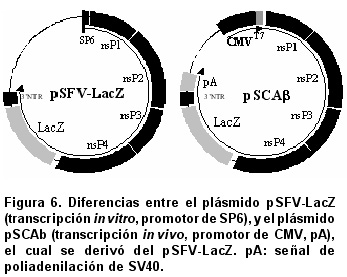
Para evitar la etapa de la transcipción in vitro, la cual es costosa y requiere de condiciones especiales para su manejo, se han diseñado vectores de ADN que permiten la transcripción in vivo (ADN/ARN) llamados pSCA. Se reemplaza el promotor SP6 por el enhancer/promotor inmediatamente temprano del citomegalovirus (CMV), dependiente de la ARN polimerasa II, el cual va a conducir la transcripción in vivo a partir del ADNc del vector19 (Figura 6).
APLICACIONES DEL SFV
El amplio rango de hospederos, la infección eficiente de células eucariotes, indispensable para las modificaciones postraduccionales de la proteína de interés y la capacidad para producir un alto nivel de proteínas, utilizando la maquinaria celular casi que exclusivamente para este propósito, hacen del SFV un vector muy eficiente; además, tiene otras ventajas como la replicación del ARN en el citoplasma, una relativa alta capacidad de clonación (4-7 kb) y efecto citopático tardío (72-96 horas), por lo que se utiliza para la expresión de diversas proteínas, nucleares, citoplasmáticas, de membrana y secretadas, en diversos estudios de biología molecular e incluso en la producción comercial de diferentes productos génicos; los vectores del SFV también se han comenzado a usar para el desarrollo de vacunas y para la terapia génica8,15,20.
Expresión de proteínas recombinantes. En el último decenio se han utilizado para expresar de manera eficaz diferentes proteínas de mamíferos, permitiendo la producción de numerosos receptores funcionales15 y la adaptación de la tecnología del SFV en cultivos de células en suspensión; ha facilitado la producción de grandes cantidades de receptores para posibles usos en la generación de medicamentos15,21. Por medio de vectores del SFV también se han expresado, muchas veces de manera eficaz y funcional, diferentes proteínas virales22-26. Henao et al.27 usó el sistema de expresión del SFV para expresar de manera eficaz proteínas heterólogas, como la proteína verde fluorescente (GFP), en la línea de hepatoma humano HepG2. También se han realizado ensayos para la expresión de la proteína Core del virus de la hepatitis C; sin embargo, se observó en los diferentes ensayos una diferencia marcada en el nivel de expresión de esta proteína viral comparado con el nivel de expresión de GFP. Están en curso estudios adicionales para determinar si un efecto tóxico está implicado en la baja eficiencia del sistema de expresión para la proteína Core del VHC.
El uso del SFV permite estudiar las propiedades de proteínas implicadas en mecanismos de patogénesis. Yepes et al.28, utilizando el SFV para la expresión transitoria de la proteína Core del VHC en células HepG2, logró determinar cambios en la expresión diferencial de ARN mensajero en células transducidas vs. no transducidas.
Por otra parte, la transferencia de genes al tejido nervioso es una poderosa herramienta para analizar la función de ciertas proteínas en el sistema nervioso central. El SFV induce una expresión transgénica rápida en neuronas con un alto nivel de expresión29.
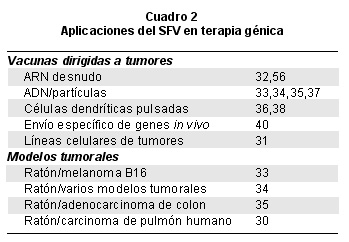
Aplicaciones en terapia génica. Son llamativas las posibles aplicaciones del SFV en terapia contra el cáncer, pues se ha visto que puede inducir apoptosis en líneas de glioma y gliosarcoma de rata30 y en líneas de tumores de próstata humana31. Se ha demostrado que la preinmunización con ARN de un replicón del SFV como un modelo de antígeno tumoral, pudo proteger ratones contra el reto tumoral o inducir la reducción de tumores32. Incluso, en varios estudios en que se investigó la eficacia terapéutica antitumoral del SFV, se encontró que en ratones vacunados con partículas recombinantes del SFV para el antígeno tumoral P815A (rSFV/E-P1A) o para las subunidades p40 y p35 de IL-12 (rSFV/IL12) se indujo la regresión de tumores, con el efecto restringido a la zona del tumor33,34, además de la inhibición de la metástasis en ratones con carcinogénesis avanzada35 y se planea usar vectores del SFV que expresan IL-12 encapsulados en liposomas en ensayos clínicos (Fase I y II) para el tratamiento de diferentes tumores. También se usan células dendríticas pulsadas con IL-18 unida al SFV e IL-12 contra ratones B16 para generar respuestas inmunológicas antitumorales36.
Los vectores del SFV se usan además en estrategias de inmunización en contra del cáncer cervical, que está asociado con el virus del papiloma humano (VPH), usando constructos con los oncogenes E6 y E7 del VPH en ratones, generando fuertes respuestas inmunes y efectos antitumorales importantes37. Un constructo de ADN basado en el SFV que codifica para la proteína de fusión E7-BCL-xL al ser transfectado en células dendríticas induce inmunidad antitumoral específica de antígeno38.
Los ensayos in vivo demuestran que los vectores basados en el SFV inducen una respuesta efectiva en modelos antitumorales, sin efectos colaterales detectables39.
La transferencia de genes por medio de vectores virales, también se usa para inhibir efectos nocivos en lesiones vasculares. Previamente se había informado de la especificidad in vitro de un vector basado en el SFV por las células no endoteliales a nivel cardiovascular1. Se demostró la capacidad de un vector recombinante del SFV para transferir de manera selectiva genes in vivo a células de aorta de rata con lesiones vasculares, por medio de sitios de unión específicos para el SFV en las células del tejido dañado, demostrando que este vector puede realizar una infección en células específicas en un mismo tipo de tejido40.
Una aplicación de especial interés es el uso potencial del SFV en el tratamiento de desórdenes del sistema nervioso central (SNC) dado su marcado neurotropismo. La esclerosis múltiple es una enfermedad autoinmune del SNC ampliamente estudiada en modelos murinos. Recientemente, y mediante el uso de un clon infeccioso avirulento que portaba el gen TGF-alfa1, se logró la replicación del vector en el SNC de animales de experimentación y la expresión local de TGF-alfa1, llevando a la disminución del proceso patogénico. Estos resultados soportan la utilización del SFV en la inmunomodulación de procesos inflamatorios autoinmunes del SNC41.
Estudios comparativos con vectores de adenovirus, sugieren considerar al SFV como un vector alternativo para potenciales estudios en terapia génica, ya que la cinética de expresión fue más eficiente y con un nivel de citotoxicidad similar1,42.
Diferentes características de los vectores del SFV, como el que no se integren al ADN cromosómico, los hacen una herramienta promisoria para respuestas inmunes seguras contra tumores, lo que podría facilitar la tera-pia génica contra el cáncer39.
En el Cuadro 2 se citan estudios sobre las aplicaciones del SFV en terapia génica.
Producción de vacunas. Los vectores basados en el SFV se han considerado como candidatos potenciales para la generación de vacunas. La inoculación intravenosa de partículas recombinantes del SFV o de ARN desnudo (implica mayor bioseguridad por la rápida degradación de éste) o vectores de ADN (inducen un mayor nivel en la respuesta inmune, por su alto nivel de replicación y de expresión de proteínas, comparados con los plásmidos de ADN convencional) o partículas virales que expresaban antígenos de diferentes virus como el de la influenza o de flavivirus, llevaron a unos niveles altos y específicos de respuesta inmune y/o a la protección contra el reto viral en ratones y chimpancés43-48. En diferentes estudios, macacos inmunizados fueron protegidos contra retos letales con cepas virulentas de retrovirus, demostrando disminución de la carga viral y generando respuestas inmunes; aunque no fueron protegidos contra la infección viral, sí se demostró la exitosa infección con los SFVs recombinantes por la inducción de anticuerpos específicos o por la activación de células Th específicas luego de la inmunización con SFV25,49-52. Recientemente, se usaron en estrategias de vacunación con múltiples vectores contra retrovirus53.
Otra línea de importancia en la generación de vacunas basadas en ácidos nucleicos es el virus de la hepatitis C (VHC). Como las terapias existentes tienen beneficios limitados y son costosas, el desarrollo de una vacuna para el VHC representa una prioridad54. En varios estudios se obtuvieron respuestas inmunes celulares específicas contra la proteína no estructural 3 (NS3) del VHC después de la inmunización con diferentes vectores recombinantes del SFV, con el propósito de generar vacunas terapéuticas con inmunógenos del virus (NS3)55,56, aunque no fue suficiente el uso del SFV para generar respuestas inmunes robustas en macacos a menos que la vacunación fuera reforzada con vectores de adenovirus57. Por otro lado, se ha puesto en duda la capacidad de inducción de una respuesta inmune específica contra las proteínas Core y E2 del VHC utilizando partículas recombinantes y vacunas de ADN derivadas del SFV, en un estudio en el que no se obtuvo una respuesta detectable de anticuerpos contra estos antígenos58.
Aunque resultados preliminares en ratones y pollos indican que la persistencia de las vacunas basadas en partículas del SFV es de menos de 7 días y su dispersión es muy limitada a partir del sitio de inoculación, vacunas basadas en ADN demostraron persistencia a largo plazo y una dispersión rápida y generalizada59, pero la utilidad del SFV como medio de vacunación puede verse disminuida por los efectos citotóxicos que aún se presentan en los modelos murinos en los que se ha probado60.
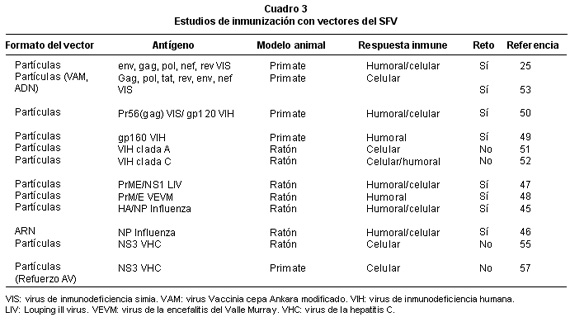
En el Cuadro 3 se citan los estudios de inmunización de animales con vectores del SFV.
Otras aplicaciones. Los vectores del SFV pueden tener aplicaciones en enfermedades degenerativas, como la de Creutzfeldt-Jakobs, el síndrome Gerstmann-Straussler-Scheinker y el insomnio fatal familiar, las cuales son causadas por priones; con vectores de ARN y ADN y partículas recombinantes del SFV se han generado anticuerpos contra estos61.
De otra parte, ratones que sobreviven a la infección con la cepa avirulenta del SFV, presentan desmielinación causada por el virus. La infección experimental de ratones con la cepa avirulenta del SFV, ha permitido su uso como modelo de enfermedades desmielinantes en humanos tales como la esclerosis múltiple, observándose cierta importancia de las células Th1 en la inmunidad protectora62.
Otra aplicación importante, puede ser la generación de líneas celulares diagnósticas que se puedan utilizar para agilizar el tiempo de detección de virus en muestras clínicas. Tal acercamiento ya se ha hecho con replicones del virus Sindbis cuya expresión es regulada por promotores del herpesvirus (HV), por lo que el replicón sólo expresa proteína reportera en respuesta a la infección de la línea celular con el HV63. Aprovechando el rápido sistema de expresión del SFV se podrían producir grandes cantidades de proteína reportera, que es fácilmente cuantificada y comparada con un estándar de referencia. Estas líneas también podrían ser útiles para determinar los títulos de las preparaciones de partículas virales, lo que facilitaría la comercialización de este tipo de vectores virales.
CONCLUSIONES
Los vectores basados en el SFV tienen a su favor la producción de virus de una manera fácil y abundante, el rango de hospederos y el envío de genes. Sin embargo, en su forma actual muestran un claro patrón de expresión transitorio. La naturaleza transitoria de la expresión génica mediada por el SFV se ha considerado a menudo como una desventaja. Es necesario analizar si los nuevos vectores con replicación persistente pueden extender sustancialmente la duración de la expresión y permitir el uso de los vectores para una expresión persistente. Pero la expresión transitoria puede ser ventajosa en ciertas áreas como la terapia génica, donde una expresión corta es suficiente y adecuada, lo que unido a su capacidad para infectar de forma específica neuronas y otras células in vivo lo hacen atractivo para estas aplicaciones. Además, la administración del vector en la forma de ARN desnudo con una vida media relativamente corta y sin capacidad de integración cromosómica aumenta considerablemente la bioseguridad del vector. El SFV se usa extensivamente para generar fuertes respuestas inmunes en animales, y aunque están por discutirse los resultados de estudios que indican que no se generan respuestas inmunogénicas contra el SFV después de repetidas dosis, su uso potencial para la producción de vacunas podría centrase a nivel antitumoral.
AGRADECIMIENTOS
Algunos de los resultados presentados en esta revisión corresponden a un proyecto financiado por el Instituto Colombiano para el Desarrollo de la Ciencia y la Tecnología «Francisco José de Caldas» (COLCIENCIAS) proyecto Cod. 1115-04-10228 y el Comité para el Desarrollo de la Investigación de la Universidad de Antioquia (CODI).
REFERENCIAS
1. Roks AJ, Pinto YM, Paul M, Pries F, Stula M, Eschenhagen T, et al. Vectors based on Semliki Forest virus for rapid and efficient gene transfer into non-endothelial cardiovascular cells: comparison to adenovirus. Cardiovasc Res 1997; 35: 498-504. [ Links ]
2. Fotaki ME, Pink JR, Mous J. Tetracycline-responsive gene expression in mouse brain after amplicon-mediated gene transfer. Gene Ther 1997; 4: 901-908. [ Links ]
3. Paterna JC, Moccetti T, Mura A, Feldon J, Büeler H. Influence of promoter and WHV post-transcriptional regulatory element on AAV-mediated transgene expression in the rat brain. Gene Ther 2000; 7: 1304-1311. [ Links ]
4. Mountain A. Gene therapy: the first decade. Trends Biotechnol 2000; 18: 119-128. [ Links ]
5. Wu N, Ataai MM. Production of viral vectors for gene therapy applications. Curr Opin Biotechnol 2000; 11: 205-208. [ Links ]
6. Schlesinger S. Alphavirus expression systems -promises and problems. ASM News 1999; 65: 688-695. [ Links ]
7. Liljeström P, Garoff H. A new generation of animal cell expression vectors based on the Semliki Forest virus replicon. Biol Technology 1991; 9: 1356-1361. [ Links ]
8. Liljeström P, Garoff H. SFV expression systems. Technical manual. Huddinge: Novum Research Center; 1993. [ Links ] 31 pp.
9. Wahlberg JM, Bron R, Wilschut J, Garoff H. Membrane fusion of Semliki Forest virus involves homotrimers of the fusion protein. J Virol 1992; 66: 7309-7318. [ Links ]
10. Lu YE, Kielian M. Semliki forest virus budding: assay, mechanisms, and cholesterol requirement. J Virol 2000; 74: 7708-7719. [ Links ]
11. Kujala P, Ikaheimonen A, Ehsani N, Vihinen H, Auvinen P, Kaariainen L. Biogenesis of the Semliki Forest virus RNA replication complex. J Virol 2001; 75: 3873-3884. [ Links ]
12. Berglund P, Sjoberg M, Garoff H, Atkins GJ, Sheahan BJ, Liljeström P. Semliki Forest virus expression system: production of conditionally infectious recombinant particles. Biol Technology 1993; 11: 916-920. [ Links ]
13. Smerdou C, Liljeström P. Two-Helper RNA System for Production of Recombinant Semliki Forest Virus Particles. J Virol 1999; 73: 1092-1098. [ Links ]
14. Tamberg N, Lulla V, Fragkoudis R, Lulla A, Fazakerley JK, Merits A. Insertion of EGFP into the replicase gene of Semliki Forest virus results in a novel, genetically stable marker virus. J Gen Virol 2007; 88 (Pt 4): 1225-1230. [ Links ]
15. Lundstrom K, Schweitzer C, Richards JG, Ehrengruber MU, Jenck F, Mülhardt C. Semliki Forest virus vectors for in vitro and in vivo applications. Gene Ther Mol Biol 1999; 4: 23-431. [ Links ]
16. Lundstrom K, Abenavoli A, Malgaroli A, Ehrengruber MU. Novel Semliki Forest virus vectors with reduced cytotoxicity and temperature sensitivity for long-term enhancement of transgene expression. Mol Ther 2003; 7: 202-209. [ Links ]
17. Lundstrom K, Rotmann D, Hermann D, Schneider EM, Ehrengruber MU. Novel mutant Semliki Forest virus vectors: gene expression and localization studies in neuronal cells. Histochem Cell Biol 2001; 115: 83-91. [ Links ]
18. Perri S, Driver DA, Gardner JP, Sherrill S, Belli BA, Dubensky TWJr, et al. Replicon vectors derived from Sindbis virus and Semliki forest virus that establish persistent replication in host cells. J Virol 2000; 74: 9802-9807. [ Links ]
19. DiCiommo DP, Bremner R. Rapid, high level protein production using DNA-based Semliki Forest virus vectors. J Biol Chem 1998; 273:18060-18066. [ Links ]
20. Colmenero P, Berglund P, Kambayashi T, Biberfeld P, Liljeström P, Jondal M. Recombinant Semliki Forest virus vaccine vectors: the route of injection determines the localization of vector RNA and subsequent T cell response. Gene Ther 2001; 8: 1307-1314. [ Links ]
21. Lundstrom K, Michel A, Blasey H, Bernard AR Hovius R, Vogel H, et al. Expression of ligand-gated ion channels with the Semliki Forest virus expression system. J Recept Signal Transduct Res 1997; 17: 115-126. [ Links ]
22. Torresi J, Meanger J, Lambert P, Li F, Locarnini SA, Anderson DA. High level expression of the capsid protein of hepatitis E virus in diverse eukaryotic cells using the Semliki Forest virus replicon. J Virol Methods 1997; 69: 81-91. [ Links ]
23. Kehm E, Goksu MA, Knopf CW. Expression analysis of recombinant herpes simplex virus type 1 DNase. Virus Genes 1998; 17: 129-138. [ Links ]
24. Nilsson M, von Bonsdorff CH, Weclewicz K, Cohen J, Svensson L. Assembly of viroplasm and virus-like particles of rotavirus by a Semliki Forest virus replicon. Virology 1998; 242: 255-265. [ Links ]
25. Giraud A, Ataman-Onal Y, Battail N, Piga N, Brand D, Mandrand B, et al. Generation of monoclonal antibodies to native human immunodeficiency virus type 1 envelope glycoprotein by immunization of mice with naked RNA. J Virol Methods 1999; 79: 75-84. [ Links ]
26. Greive SJ, Webb RI, Mackenzie JM, Gowans EJ. Expression of the hepatitis C virus structural proteins in mammalian cells induces morphology similar to that in natural infection. J Viral Hepat 2002; 9: 9-17. [ Links ]
27. Henao LF, Yepes JO, Álvarez CM, Bálcazar N, Navas MC. Expresión de la proteína verde fluorescente y proteína Core del Virus de la hepatitis C en la línea de hepatoma HepG2 mediante el sistema de expresión del Semliki Forest Virus. Acta Biol 2004; 25: 23-29. [ Links ]
28.Yepes JO, Gunturiz ML, Henao LF, Navas MC, Balcázar N, Gómez LA. Presentación diferencial de ARN mensajeros e identificación del gen selenocisteína liasa en células de carcinoma hepatocelular con expresión transitoria de la proteína core del virus de la hepatitis C. Biomedica 2006; 26: 194-205. [ Links ]
29. Ehrengruber MU, Lundstrom K, Schweitzer C, Heuss C, Schlesinger S, Gahwiler BH. Recombinant Semliki Forest virus and Sindbis virus efficiently infect neurons in hippocampal slice cultures. Proc Natl Acad Sci USA 1999; 96: 7041-7046. [ Links ]
30. Murphy AM, Morris-Downes MM, Sheahan BJ, Atkins GJ. Inhibition of human lung carcinoma cell growth by apoptosis induction using Semliki Forest virus recombinant particles. Gene Ther 2000; 7: 1477-1482. [ Links ]
31. Hardy PA, Mazzini MJ, Schweitzer C, Lundstrom K, Glode LM. Recombinant Semliki forest virus infects and kills human prostate cancer cell lines and prostatic duct epithelial cells ex vivo. Int J Mol Med 2000; 5: 241-245. [ Links ]
32. Ying H, Zaks TZ, Wang RF, Irvine KR, Kammula US, Marincola FM, et al. Cancer therapy using a self-replicating RNA vaccine. Nat Med 1999; 5: 823-827. [ Links ]
33. Colmenero P, Chen M, Castaños-Vélez E, Liljestrom P, Jondal M. Immunotherapy with recombinant SFV-replicons expressing the P815A tumor antigen or IL-12 induces tumor regression. Int J Cancer 2002; 98: 554-560. [ Links ]
34. Chikkanna-Gowda CP, Sheahan BJ, Fleeton MN, Atkins GJ. Regression of mouse tumours and inhibition of metastases following administration of a Semliki Forest virus vector with enhanced expression of IL-12. Gene Ther 2005; 12: 1253-1263. [ Links ]
35. Rodríguez-Madoz JR, Prieto J, Smerdou C. Semliki forest vírus vectors engineered to express higher IL-12 levels induce efficient elimination of murine colon adenocarcinomas. Mol Ther 2005; 12: 153-163. [ Links ]
36. Yamanaka R, Tsuchiya N, Yajima N, Honma J, Hasegawa H, Tanaka R, et al. Induction of an antitumor immunological response by an intratumoral injection of dendritic cells pulsed with genetically engineered Semliki Forest virus to produce interleukin-18 combined with the systemic administration of interleukin-12. J Neurosurg 2003; 99: 746-753. [ Links ]
37. Daemen T, Riezebos-Brilman A, Regts J, Dontje B, van der Zee A, Wilschut J. Superior therapeutic efficacy of alphavirus-mediated immunization against human papilloma virus type 16 antigens in a murine tumour model: effects of the route of immunization. Antivir Ther 2004; 9: 733-742. [ Links ]
38. Kim TG, Kim CH, Won EH, Bae SM, Ahn WS, Park JB, et al. CpG-ODN-stimulated dendritic cells act as a potent adjuvant for E7 protein delivery to induce antigen-specific antitumour immunity in a HPV 16 E7-associated animal tumour model. Immunology 2004; 112: 117-125. [ Links ]
39. Yamanaka R. Alphavirus vectors for cancer gene therapy. Int J Oncol 2004; 24: 919-923. [ Links ]
40. Loot AE, Henning RH, Deelman LE, Tio RA, Schoen P, Wilschut JC, et al. Semliki Forest virus is an efficient and selective vector for gene delivery in infarcted rat heart. J Mol Cell Cardiol 2004; 37: 137-142. [ Links ]
41. Vaha-Koskela MJ, Kuusinen TI, Holmlund-Hampf JC, Furu PT, Heikkila JE, Hinkkanen AE. Semliki Forest virus vectors expressing transforming growth factor beta inhibit experimental autoimmune encephalomyelitis in Balb/c mice. Biochem Biophys Res Commun 2007; 355: 776-781. [ Links ]
42. Wahlfors JJ, Zullo SA, Loimas S, Nelson DM, Morgan RA. Evaluation of recombinant alphaviruses as vectors in gene therapy. Gene Ther 2000; 7: 472-480. [ Links ]
43. Zhou X, Berglund P, Zhao H, Liljeström P, Jondal M. Generation of cytotoxic and humoral immune responses by nonreplicative recombinant Semliki Forest virus. Proc Natl Acad Sci USA 1995; 92: 3009-3013. [ Links ]
44. Malone JG, Bergland PJ, Liljestrom P, Rhodes GH, Malone RW.Mucosal immune responses associated with polynucleotide vaccination. Behring Inst Mitt 1997; 98: 63-72. [ Links ]
45. Berglund P, Fleeton MN, Smerdou C, Liljeström P. Immunization with recombinant Semliki Forest virus induces protection against influenza challenge in mice. Vaccine 1999; 17: 497-507. [ Links ]
46. Vignuzzi M, Gerbaud S, van der Werf S, Escriou N. Naked RNA immunization with replicons derived from poliovirus and Semliki Forest virus genomes for the generation of a cytotoxic T cell response against the influenza A virus nucleoprotein. J Gen Virol 2001; 82: 1737-1747. [ Links ]
47. Fleeton MN, Liljeström P, Sheahan BJ, Atkins GJ. Recombinant Semliki Forest virus particles expressing louping ill virus antigens induce a better protective response than plasmid-based DNA vaccines or an inactivated whole particle vaccine. J Gen Virol 2000; 81: 749-758. [ Links ]
48. Colombage G, Hall R, Pavy M, Lobigs M. DNA-based and alphavirus-vectored immunisation with prM and E proteins elicits long-lived and protective immunity against the flavivirus, Murray Valley encephalitis virus. Virology 1998; 250: 151-163. [ Links ]
49. Berglund P, Quesada-Rolander M, Putkonen P, Biberfeld G, Thorstensson R, Liljestrom P. Outcome of immunization of cynomolgus monkeys with recombinant Semliki Forest virus encoding human immunodeficiency virus type envelope protein and challenged with a high dose of SHIV-4 virus. AIDS Res Hum Retroviruses 1997; 13: 1487-1495. [ Links ]
50. Notka F, Stahl-Hennig C, Dittmer U, Wolf H, Wagner R. Accelerated clearance of SHIV in rhesus monkeys by virus-like particle vaccines is dependent on induction of neutralizing antibodies. Vaccine 1999; 18: 291-301. [ Links ]
51. Hanke T, Barnfield C, Wee EG, Agren L, Samuel RV, Larke N, Liljeström P, et al. Construction and immunogenicity in a prime-boost regimen of a Semliki Forest virus-vectored experimental HIV clade A vaccine. J Gen Virol 2003; 84: 361-368. [ Links ]
52. Sundback M, Douagi I, Dayaraj C, Forsell MN, Nordstrom EK, McInerney GM, et al. Efficient expansion of HIV-1-specific T cell responses by homologous immunization with recombinant Semliki Forest virus particles. Virology 2005; 341: 190-202. [ Links ]
53. Negri DR, Baroncelli S, Catone S, Comini A, Michelini Z, Maggiorella MT, et al. Protective efficacy of a multicomponent vector vaccine in cynomolgus monkeys after intrarectal simian immunodeficiency virus challenge. J Gen Virol 2004; 85: 1191-1201. [ Links ]
54. Brinster C, Inchauspe G. DNA vaccines for hepatitis C virus. Intervirology 2002; 44: 143-153. [ Links ]
55. Brinster C, Chen M, Boucreux D, Paranhos-Baccala G, Liljeström P, Lemmonier F, et al. Hepatitis C virus non-structural protein 3-specific cellular immune responses following single or combined immunization with DNA or recombinant Semliki Forest virus particles. J Gen Virol 2002; 83: 369-381. [ Links ]
56. Frelin L, Ahlen G, Alheim M, Weiland O, Barnfield C, Liljeström P, et al. Codon optimization and mRNA amplification effectively enhances the immunogenicity of the hepatitis C virus non-structural 3/4A gene. Gene Ther 2004; 11: 522-533. [ Links ]
57. Rollier C, Verschoor EJ, Paranhos-Baccala G, Drexhage JA, Verstrepen BE, Berland JL, et al. Modulation of vaccine-induced immune responses to hepatitis C virus in rhesus macaques by altering priming before adenovirus boosting. J Infect Dis 2005; 192: 920-929. [ Links ]
58. Vidalin O, Fournillier A, Renard N, Chen M, Depla E, Boucreux D, et al. Use of conventional or replicating nucleic acid-based vaccines and recombinant Semliki Forest virus-derived particles for the induction of immune responses against hepatitis C virus Core and E2 antigens. Virology 2000; 276: 259-270. [ Links ]
59. Morris-Downes MM, Phenix KV, Smyth J, Sheahan BJ, Lileqvist S, Mooney DA, et al. Semliki Forest virus-based vaccines: persistence, distribution and pathological analysis in two animal systems. Vaccine 2001; 19: 1978-1988. [ Links ]
60. Lundstrom K. Semliki Forest virus vectors for gene therapy. Expert Opin Biol Ther 2003; 3: 771 -777. [ Links ]
61. Krasemann S, Jürgens T, Bodemer W. Generation of monoclonal antibodies against prion proteins with an unconventional nucleic acid-based immunization strategy. J Biotechnol 1999; 73: 119-129. [ Links ]
62. Keogh B, Atkins GJ, Mills KH, Sheahan BJ. Avirulent Semliki Forest virus replication and pathology in the central nervous system is enhanced in IL-12-defective and reduced in IL-4-defective mice: a role for Th1 cells in the protective immunity. J Neuroimmunol 2002; 125: 15-22. [ Links ]
63. Ivanova L, Schlesinger S, Olivo PD. Regulated expression of a Sindbis virus replicon by herpesvirus promoters. J Virol 1999; 73: 1998-2005. [ Links ]