Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Colombia Médica
On-line version ISSN 1657-9534
Colomb. Med. vol.51 no.4 Cali Oct./Dec. 2020 Epub Dec 29, 2020
https://doi.org/10.25100/cm.v51i4.4511
Articulo de revisión
Sangre total: la nueva alternativa en la resucitación hemostática
1 Hospital Vicente Corral Moscoso, Division of Trauma and Acute Care Surgery, Cuenca, Ecuador.
2 Universidad del Azuay, Escuela de Medicina. Cuenca, Ecuador.
3 Medstar Georgetown University Hospital, Department of Surgery, Washington, D.C., USA
4 Washington Hospital Center. Washington, D.C., USA.
5 Universidad Industrial de Santander, Department of Surgery, Bucaramanga, Colombia.
6 Hospital Manuela Beltrán, Department of Surgery, Socorro, Colombia.
7 Fundación Valle del Lili, Department of Surgery, Division of Trauma and Acute Care Surgery, Cali, Colombia.
8 Universidad del Valle, Facultad de Salud, Escuela de Medicina, Department of Surgery, Division of Trauma and Acute Care Surgery, Cali, Colombia.
9 Universidad Icesi, Cali, Colombia.
10 Broward General Level I Trauma Center, Department of Trauma Critical Care, Fort Lauderdale, FL - USA
11 Fundación Valle del Lili, Centro de Investigaciones Clínicas (CIC), Cali, Colombia
12 Universidad de Chile, Facultad de Medicina, Instituto de Ciencias Biomédicas, Santiago de Chile, Chile.
13 Brigham & Women’s Hospital, Department of Surgery, Center for Surgery and Public Health, Boston, USA
14 Harvard Medical School & Harvard T.H., Chan School of Public Health, Boston - USA
15 Fundación Valle del Lili, Intensive Care Unit, Cali, Colombia
16 Fundación Valle del Lili, Blood Bank and Transfusion Service, Cali, Colombia.
17 Hospital Universitario del Valle, Department of Surgery, Division of Trauma and Acute Care Surgery, Cali, Colombia.
18 Hospital Universitario del Valle, Cali, Colombia.
19 University of Pittsburgh, Critical Care Medicine. Pittsburgh, PA, USA.
El choque hemorrágico y sus complicaciones son la principal causa de muerte en los pacientes con trauma. La resucitación en control de daños ha demostrado una disminución en la mortalidad y mejoría en el manejo del paciente. La resucitación hemostática consiste en la recuperación del volumen con hemoderivados como glóbulos rojos, plasma, crioprecipitado y plaquetas, en proporciones de 1:1:1:1. Sin embargo, esta demanda de hemo componentes podría no aplicarse para toda Latinoamérica u otros países de medianos y bajos ingresos. Las principales barreras para la implementación de esta estrategia serían la escasa disponibilidad de bancos de sangre y de hemoderivados insuficientes para contar con un protocolo de transfusión masiva. Una propuesta para superar estas barreras es el uso de sangre total fresca fría para la resucitación hemostática de los pacientes exsanguinados. Ecuador ha sido pionero en la implementación de esta estrategia con una experiencia ya de seis años, en que han demostrado que la sangre total tiene ventajas sobre la terapia de hemo componentes incluyendo, pero no limitando, la trasfusión de sangre con una razón fisiológica de componentes, fácil transporte y transfusión, menor volumen de anticoagulantes y aditivos trasfundidos al paciente, y menor exposición a donantes. La sangre total es una herramienta con un potencial reemergente que puede ser implementado en centros de trauma civil con óptimos resultados y menor demanda técnica.
Palabras clave: Sangre total; resucitación de control de daños; transfusión soluciones cristaloides; choque hemorrágico; coagulación intravascular diseminada; centros de trauma; seguridad sanguínea; hemostáticos; hipotermia; hipocalcemia; factores de coagulación sanguínea; síndrome de dificultad respiratoria; síndromes compartimentales
Hemorrhagic shock and its complications are a major cause of death among trauma patients. The management of hemorrhagic shock using a damage control resuscitation strategy has been shown to decrease mortality and improve patient outcomes. One of the components of damage control resuscitation is hemostatic resuscitation, which involves the replacement of lost blood volume with components such as packed red blood cells, fresh frozen plasma, cryoprecipitate, and platelets in a 1:1:1:1 ratio. However, this is a strategy that is not applicable in many parts of Latin America and other low-and-middle-income countries throughout the world, where there is a lack of well-equipped blood banks and an insufficient availability of blood products. To overcome these barriers, we propose the use of cold fresh whole blood for hemostatic resuscitation in exsanguinating patients. Over 6 years of experience in Ecuador has shown that resuscitation with cold fresh whole blood has similar outcomes and a similar safety profile compared to resuscitation with hemocomponents. Whole blood confers many advantages over component therapy including, but not limited to the transfusion of blood with a physiologic ratio of components, ease of transport and transfusion, less volume of anticoagulants and additives transfused to the patient, and exposure to fewer donors. Whole blood is a tool with reemerging potential that can be implemented in civilian trauma centers with optimal results and less technical demand.
Keywords: Crystalloid solutions; shock; hemorrhagic; disseminated intravascular coagulation; trauma centers, blood safety; hemostatics; hypothermia; hypocalcemia; blood coagulation factors; respiratory distress syndrome; compartment syndromes
Contribución del estudio
| 1) ¿Por qué se realizó este estudio? |
| Este estudio tiene como objetivo discutir el rol de la sangre total en la resucitación hemostática de los pacientes con trauma severo y shock hemorrágico |
| 2) ¿Cuáles fueron los resultados más relevantes del estudio? |
| El estándar de oro en la resucitación hemostática es un balance de hemocomponentes con una proporción 1:1:1, buscando imitar la composición de la sangre perdida. La sangre total es la nueva estrategia en la resucitación hemostática |
| 3¿Qué aportan estos resultados? |
| La sangre total confiere ventajas practicas sobre la terapia de hemo componentes. |
Introducción
La hemorragia exanguinante constituye la principal causa de muerte prevenible en las primeras 2 a 3 horas en lesiones de causa externa 1-3. Las medidas tempranas de control de daños tienen el potencial de evitar una cuarta parte de las muertes relacionadas con trauma 1. El concepto de cirugía de control de daños se entrelaza con el de reanimación de control de daños. La reanimación de control de daños tiene como objetivo controlar la hemorragia, restaurar la perfusión tisular y mitigar la coagulopatía inducida por el trauma 1,4,5. La reanimación hemostática es un pilar central de la reanimación de control de daños 4 y es el enfoque de esta revisión. Actualmente, la estrategia de resucitación de control de daños se basa en el uso de hemoderivados 2,5-8, teniendo como estándar de tratamiento la transfusión balanceada 1: 1: 1 con concentrados de glóbulos rojos, plasma fresco congelado y plaquetas 2,8,10. La propuesta del grupo de cirugía de trauma y emergencias de Cali integra el ritmo de reanimación ideal que debe ser una proporción de 1:1:1:1, adicionando el crioprecipitado. En los últimos años, se ha desafiado este paradigma sugiriendo que la sangre total es el fluido ideal para la reanimación, en lugar de la terapia de componentes balanceados 4,6,11,12. El objetivo de este trabajo es discutir y presentar nuestra experiencia en el rol emergente de la sangre total en la reanimación hemostática de pacientes con choque hemorrágico.
Este artículo es un consenso que sintetiza la experiencia lograda durante los últimos 30 años en el manejo del trauma, cirugía general y cuidado crítico del grupo de cirugía de Trauma y Emergencias de Cali, Colombia conformado por expertos del Hospital Universitario Fundación Valle del Lili y el Hospital Universitario del Valle “Evaristo García”, con la Universidad del Valle y la Universidad Icesi, en colaboración con la Asociación Colombiana de Cirugía y la Sociedad Panamericana de Trauma, en conjunto con especialistas nacionales e internacionales de EE.UU y Latino América.
Epidemiología
La disponibilidad de hemoderivados tiene un efecto inverso en la mortalidad de pacientes con choque hemorrágico por lesiones de causa externa. Recientemente, en Colombia se describió que la presencia de al menos cuatro bancos de sangre por ciudad se asocia con una disminución en la mortalidad por choque hemorrágico en la atención del trauma 13. Sin embargo, el estudio sobre la seguridad y disponibilidad global de productos sanguíneos de la Organización Mundial de Salud ha estimado que el 61% de los países incluidos no tiene suficientes productos sanguíneos para satisfacer las necesidades de la población 14.
La disponibilidad de hemoderivados varía entre países; las tasas de donación de sangre sirven como un marcador de disponibilidad de sangre dentro de cada país. De los 117.4 millones de donaciones de sangre recolectadas anualmente en todo el mundo, el 42% se recolecta en países de altos ingresos, donde vive solo el 16% de la población mundial. Las tasas de donación de sangre por cada 1,000 personas es de 32.6 en países de altos ingresos, 15.1 en países de ingresos medios-altos, 8.1 en países de ingresos medios bajos y 4.4 en países de bajos ingresos 15.
Para el 2014, la tasa de donaciones de sangre en América Latina y el Caribe fue de 14.84 por 1,000 habitantes 16. La tasa de donación de sangre en Colombia en 2015 fue de 16.07 por 1,000 personas. De las 795,792 donaciones en un año, 725,209 (91.13%) se registraron como donaciones voluntarias y 70,429 (8.85%) se registraron como donaciones de reemplazo 17.
Fisiopatología
La coagulopatía está presente en el 25% de los pacientes con trauma que ingresan al servicio de urgencias 10. MacLeod et al.18, describen que un tiempo inicial de protrombina mayor de 14 segundos y un tiempo parcial de tromboplastina mayor de 34 segundos, fueron predictores independientes de mortalidad con un odds ratio de 1.35 (IC 95%: 1.11-1.68; p <0.001) y 4.26 (IC 95%: 3.23-5.63; p <0.001), respectivamente. La presencia de coagulopatía al ingreso se asocia con un aumento en los requerimientos de transfusión, estancia hospitalaria, soporte ventilatorio invasivo y mayor incidencia de falla orgánica múltiple 19.
La coagulopatía inducida por trauma ocurre por el daño tisular del trauma y los esfuerzos de la reanimación 19 y puede desarrollarse en los primeros 30 minutos 20. Este trastorno ocurre debido a una activación sistémica de la cascada de la coagulación, seguida de una coagulopatía por consumo y un aumento de la fibrinólisis. La coagulopatía inducida por la reanimación se asocia a una infusión excesiva de cristaloides, empeora la acidosis, la hipotermia y la dilución de los factores de coagulación 19. La hipotermia conduce a una disminución en la función de las plaquetas y enzimas. La perfusión tisular inadecuada causa una acidosis láctica que se exacerba aún más, con soluciones cristaloides con alta concentración de cloruro. La actividad de los factores de coagulación se disminuye por el pH acido sanguíneo 20. Una revisión reciente de Ditzel et al. (21, sugieren que el concepto de la "tríada de la muerte" deba actualizarse al del "rombo de la muerte", reconociendo el papel de la hipocalcemia, como predictor independiente de mortalidad y factor que potencia la coagulopatía, la hipotermia y la acidosis 21,22.
En la Figura 1 se resalta la importancia del inicio temprano (15 minutos) de la administración de hemo componentes cumpliendo con la relación 1:1:1, y se demuestra que la administración temprana y balanceada de hemo componentes aumenta la supervivencia y requiere menos número de transfusiones.
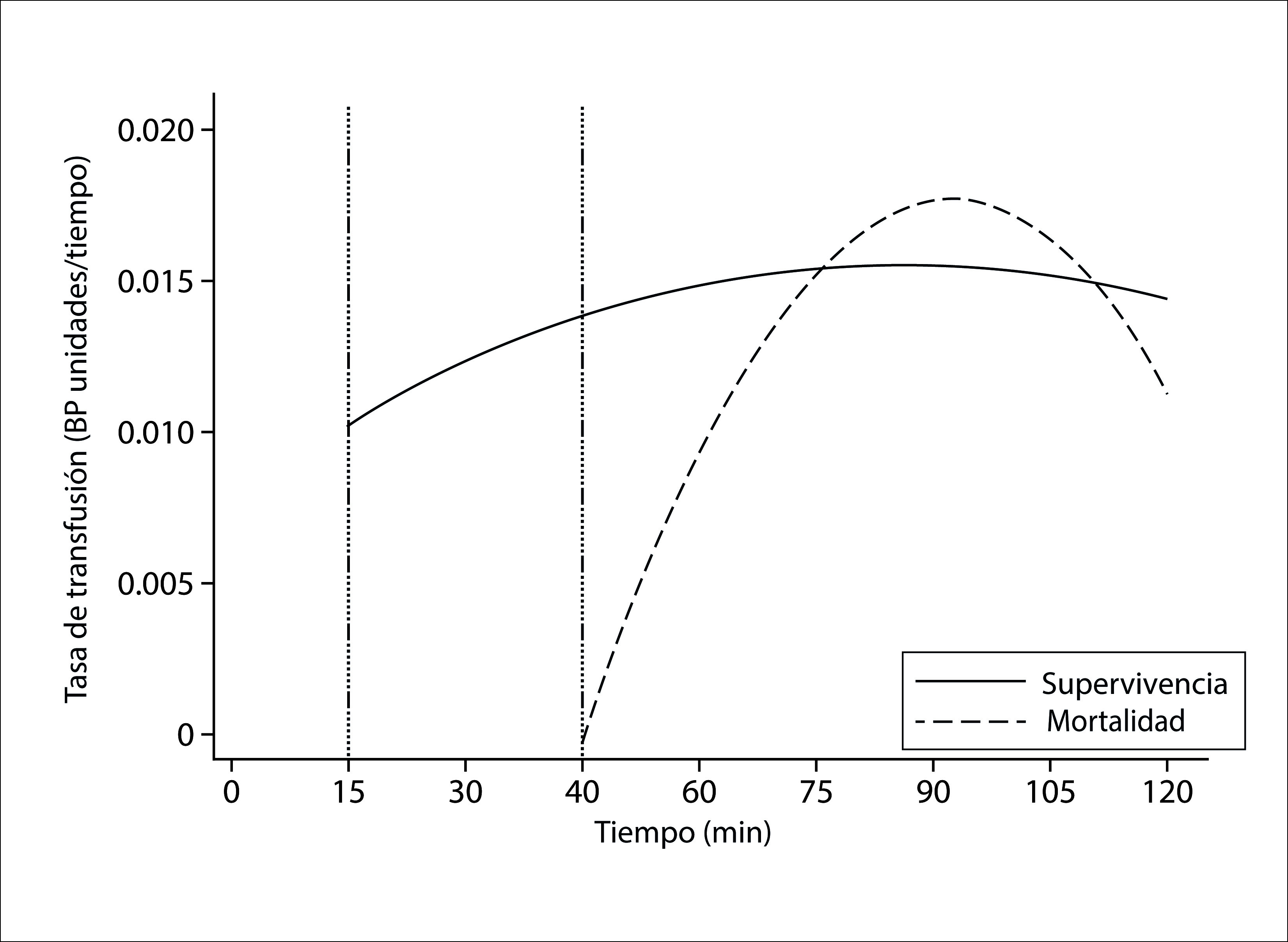
Figura 1 Tasa de hemocomponentes transfundidos según tiempo inicio de cirugía (los supervivientes se asociaron a un inicio de transfusión más temprana y una tasa estable)
Antes de la implementación de la resucitación de control de daños, la reanimación del paciente con trauma fue basada en la administración de grandes volúmenes de cristaloides, con la hipótesis de que mejoraba el gasto cardíaco y el suministro de oxígeno a los tejidos 23. Un estudio realizado por Kasotakis et al.24, pusieron en duda esta práctica, ya que encontraron que la reanimación con cristaloides se asoció al desarrollo de síndrome de distrés respiratorio agudo, falla orgánica múltiple, bacteriemia, infecciones del sitio operatorio, síndrome del compartimiento abdominal y síndrome compartimental de extremidades. Posteriormente, Brickell y Mattox 25 demostraron que la tasa de supervivencia era mayor, si había una disminución en el volumen de cristaloides administrados a los pacientes con trauma. Un análisis multivariado realizado a una muestra de 3,137 pacientes que recibieron reanimación con cristaloides demostró que un volumen de 1.5 L o más, se asocia con un aumento en la mortalidad tanto en adultos mayores como en población joven. 26.
El objetivo de la resucitación de control de daños es la mitigación de los efectos de la coagulopatía inducida por trauma, revertir la acidosis y prevenir la hipotermia 21. Con el reconocimiento de los efectos deletéreos de una estrategia basada en cristaloides, el péndulo ha oscilado hacia una estrategia basada en una administración balanceada de sangre 11. En las últimas dos décadas, los estudios han sugerido que la inclusión de plasma y plaquetas en la reanimación se relaciona con una mayor supervivencia a la hemorragia en pacientes con lesiones traumáticas 9,27. El ensayo PROPPR, encontró que pacientes que recibieron unidades de plaquetas, plasma y glóbulos rojos en una proporción 1:1:1 habían aumentado significativamente la hemostasia y una disminución en la mortalidad en comparación con un grupo tratado con una proporción 1: 1: 2 2. Sin embargo, muchas instituciones en los países de medianos y/o bajos ingresos no tienen acceso a bancos de sangre con suficientes productos sanguíneos para poder administrar hemoderivados en esta proporción. El éxito relativo de la fórmula 1: 1: 1 y el desafío que representa su disponibilidad ha permitido volver a debatir acerca del uso de la sangre total.
¿Qué pacientes se benefician de la reanimación hemostática?
El 1 al 3% de los pacientes que ingresan a un centro de trauma urbano requerirán un protocolo de transfusión masiva, definido como la necesidad de transfusión de más de 10 unidades de sangre en 24 horas 28. Esta definición de transfusión masiva es arbitraria y con sesgo en la estimación de la supervivencia es importante identificar a los pacientes que se podrían beneficiar de la transfusión 28. Aunque muchos cirujanos confían solo en el juicio clínico, un estudio que incluyó 10 centros de trauma de nivel I en EE.UU. determinó que el juicio clínico solo tiene una sensibilidad del 65.6% y una especificidad del 63.8% para identificar pacientes que requieren transfusión masiva 29. Existe una amplia variedad de escalas para ayudar en la decisión de activar o no un protocolo de transfusión masiva. Los puntajes más prácticos se estiman sin cálculos extensos, lo cual facilita la toma de decisiones clínicas en tiempo real, utilizando la evaluación inicial del paciente. Un resumen de algunas escalas para determinar la necesidad de transfusión masiva se describe en la Tabla 1.
Tabla 1 Herramientas utilizadas para predecir si un paciente con choque hemorrágico necesitara transfusión masiva.
| Herramienta | Componentes de la Herramienta | Datos Clínicos | Datos de Imágenes | Datos del Laboratorio | AUROC |
|---|---|---|---|---|---|
| Juicio Clínico 28 | El juicio clínico del cirujano tratante | X | -- | -- | 0.62 |
| Índice de choque 29-31 | IC >0.9 | X | -- | -- | 0.80 |
| McLaughlen 32 | Variables tienen valores de 0 al menos que: FC >105 Lpm, PAS <110 mmHg, Hematocrito <32%, pH <7.25 | X | -- | X | 0.84 |
| Evaluación de la puntuación del consumo de sangre (ABC) 33 | Una puntación de 2 o más, dando 1 puntaje por cada uno de los siguientes: Mecanismo penetrante, FC >120, PAS <90mmHg | X | X | -- | 0.86 |
| Nemotecnia ABCD 8 | Predice transfusión masiva si las 4 variables son presentes: Exceso de base ≥8, Pérdida de sangre >1,500 mL, Hipotermia <35° C, Escala de NISS>35 | X | -- | X | 0.87 |
| TASH 34 | Puntaje >16 predice transfusión masiva, puntaje máximo 27: Las variables evaluadas son: PAS, Hemoglobina, Presencia de líquido intraabdominal, Presencia de fracturas complejas de hueso largo o pélvico, FC, Exceso de base, Género masculino | X | X | X | 0.89 |
*FC: Frecuencia Cardiaca, PAS: Presión Arterial Sistólica.
ABC: Assessment of Blood Consumption score
TASH: Trauma asociado a una hemorragia severa
ABCD: A: Vía aérea B: Respiración C: Circulatoria D: Discapacidad
MTP: Protocolo de transfusión masiva
Si hay disponibilidad de la Tromboelastografía, esta debe ser empleada. La tromboelastografía es una herramienta valiosa para la toma de decisiones en un paciente crítico con choque hemorrágico. Esta evalúa los componentes plasmáticos y celulares involucrados en la formación o lisis de un trombo en su condición actual. Así, esta herramienta permite identificar objetivamente que elemento o elementos, conducen a la coagulopatía 30. Un resumen de las variables reportadas por una tromboelastografía está descrito en la Tabla 2. No obstante, aún existe controversia en la literatura de la aplicabilidad de la tromboelastografía en los pacientes de trauma 31. Un ensayo clínico en 2016 por González et al. (32, demostraron que los pacientes con reanimación guiada por Tromboelastografía, tenían una reducción en la mortalidad (p: 0.049), menor uso de plasma (p: 0.022) y plaquetas (p: 0.041); comparado con los pacientes que tuvieron reanimación convencional 32.
Tabla 2 Resumen de los elementos críticos de una tromboelastografía 38.
| Fase de Hemostasia | Parametro | Valores Normales | Descripción | Interpretación en un paciente hipocoaguloble |
|---|---|---|---|---|
| Activación | R time | 5-10 minutos | Periodo de latencia desde el inicio de la prueba hasta la formación de fibrina inicial | Si R time>10 minutos, se considera: PFC, complejo de protrombina o reversión de anticoagulante |
| Amplificación | K time | 1-3 minutos | Tiempo “cinético” para lograr estabilidad del trombo, equivalente a una amplitud de 20 mm | Si K time >3 minutos, se considera: Concentrado de fibrinógeno o crioprecipitado |
| Propagación | α angle | 53.0-70.0 mm | Angulo entre R y línea imaginaria desde el momento la formación del trombo hasta el punto de trombo máximo, relacionado a K time | Si α angle <53 mm, se considera: Concentrado de fibrinógeno o crioprecipitado |
| Terminación | MA angle | 50-70 mm | Curva máxima que representa la fuerza máxima del trombo | Si MA <50 mm, se considera: Plaquetas |
| Fibrinólisis | LY30 | 0-3% | Porcentaje de la reducción de la amplitud 30 minutos después del MA | Si LY30 >3%, se considera: Acido tranexámico |
La evidencia de sangre total
La meta de la reanimación 1: 1: 1 en un paciente con choque hemorrágico es recuperar la sangre que ha perdido. Si bien falta más evidencia, los estudios en la última década sugieren que la reanimación de control de daños debe buscar imitar la sangre total 4,12.
La sangre total confiere numerosas ventajas prácticas sobre la terapia de componentes. La sangre total tiene una proporción de componentes celulares y de factores coagulación similar al fisiológico. Las unidades por hemoderivados contienen una mayor cantidad de anticoagulantes y aditivos que contribuyen a la coagulopatía general del paciente, en comparación con una unidad de sangre total 33. Se ha reportado que la transfusión adicional de anticoagulantes y aditivos en las primeras 24 horas, aumenta el riesgo de coagulopatía dilucional 34. Un análisis realizado por Hess et al.12, encontraron que la sangre total reconstituida, a través de hemo componentes en una proporción 1: 1: 1 produjo una mezcla diluida con un hematocrito del 29%, recuento de plaquetas de 90,000 y factores de coagulación diluidos al 62% de las concentraciones plasmáticas 12,35. La sangre total de acuerdo al tiempo de almacenamiento puede variar sus concentraciones de hematocrito entre un 35-38%, recuento de plaquetas entre 150,000-200,000 y factores de coagulación en un 85% de los valores previos a la donación 12. El uso de sangre total en el entorno prehospitalario se ha iniciado a proponer que tuviese ventajas respecto a su fácil transporte e inicio temprano de transfusiones (Tabla 3).
Tabla 3 Los beneficios de sangre total comparado a terapia con componentes durante la reanimación de control de daños 37.
| Componentes | Sangre Total |
|---|---|
| Mayor volumen de aditivos y anticoagulantes | Menor volumen de aditivos y anticoagulantes |
| Se requiere la transfusión en 3 bolsas | Se requiere la transfusión de solo 1 bolsa |
| Aplicable en pocos hospitales del mundo | Fácil de replicar |
| Menos accesible en el entorno prehospitalario y en entornos de recursos limitados | Fácil para implementar en el entorno prehospitalario y en entornos de recursos limitados |
| Más costoso | Más económico |
En el servicio de cirugía de trauma y emergencias del Hospital Vicente Corral Moscoso en el sur de Ecuador se implementó un programa de sangre total fresca fría para la reanimación de pacientes críticos 36. Se recolecto sangre completa de los donantes, se examinó y se puso a disposición de los servicios quirúrgicos durante 48 horas, si no se había empleado, la sangre se fracciona en hemo componentes. Las unidades glóbulos rojos y de plasma fresco congelado están disponibles, pero las plaquetas se envían al hospital oncológico local y no están disponibles para transfusiones después del fraccionamiento. Antes de la implementación del centro de trauma y emergencias, las unidades de glóbulos rojos y plasma estaban disponibles de manera inconstante; las plaquetas rara vez estaban disponibles. Esta experiencia demostró la viabilidad del uso de sangre total en una serie de 93 pacientes con choque hemorrágico asociado a trauma o emergencia obstétrica 37.
Mortalidad
La información de la medicina militar en los Estados Unidos proveniente de conflictos recientes en el Medio Oriente se ha centrado en la sangre total fresca ya que los escenarios de combate requieren la recolección de donantes preseleccionados en un "banco de sangre ambulante" en caso de requerirlo. La sangre total fresca se almacena a temperatura ambiente y se usa en un plazo de 72 horas posteriores a la recolección, sin refrigeración 12. Spinella et al. (33, describen una reducción en la mortalidad post trauma a las 24 horas y 30 días en pacientes resucitados con sangre total fresca junto con unidades de glóbulos rojos y plasma adicionales, en comparación con la terapia de hemo componentes, incluidas las plaquetas de aféresis. El grupo de sangre total fresca tuvo una temperatura menor al ingreso en comparación con el grupo de terapia de componentes y una mayor incidencia de transfusión masiva 33. Perkins et al. (38, describieron un aumento de la supervivencia a 24 horas en pacientes tratados con sangre total, a pesar, de que este grupo de estudio se asociaran a una mayor proporción de hipotermia, acidosis, menor recuento plaquetario al ingreso, mayor severidad del trauma medida por ISS y menor tasa de supervivencia predictiva estimada por TRISS. Nessen et al.39, compararon el uso de sangre total fresca versus a la administración únicamente de unidades de glóbulos rojos y plasma. El grupo tratado con sangre total se asocia con una reducción en el riesgo de mortalidad (OR-ajustado: 0.096; IC 95%: 0.02-0.53), a pesar de que el grupo con sangre total fresca tenía mayor severidad del trauma, hipotensión e hipotermia al ingreso comparado con el grupo de hemo componentes 39. Un estudio con población civil prospectivo en Australia, comparó sangre total fresca y la terapia de componentes en pacientes de diversas especialidades que requirieron transfusión masiva, sin encontrar diferencias en la mortalidad a 24 horas o 30 días 40.
La sangre total se puede almacenar a 1-6° C hasta 21 o 35 días, dependiendo del anticoagulante utilizado para mantener la integridad de los glóbulos rojos 12. Los estudios con población civil demuestran una equivalencia o superioridad de la sangre total sobre la terapia de componentes. Un ensayo clínico, aleatorizado, controlado en una sola institución comparó la sangre total modificada (sangre total leuco reducida con transfusión de plaquetas adicional) con la terapia de componentes, sin reportar diferencias en la mortalidad a 24 horas o 30 días. Aunque, este estudio puede tener un sesgo para el grupo de sangre total, ya que no se descartaron las muertes asociadas a trauma craneoencefálico 41. En un estudio retrospectivo que usó controles históricos, se observó una disminución de la mortalidad por traumatismo en pacientes tratados con sangre total almacenada (8.8% en la terapia de componentes versus 2.2% con sangre total,), sin diferencias en la mortalidad a los 30 días 42. Un ensayo prospectivo realizado en entornos prehospitalarios y de sala de emergencias, reportó que la reanimación con sangre total del grupo O con bajos títulos, era un predictor independiente de supervivencia a los 30 días, a pesar de que este brazo del estudio presento choque severo, acidosis e hiperlactatemia comparado con su grupo control 43.
Utilización de productos sanguíneos
Los estudios no describen diferencias en la tasa de utilización de productos sanguíneos entre los pacientes tratados con sangre total en comparación con la terapia de componentes 40,42,44,45. Cotton et al. (41, no encontraron diferencias en el uso de hemo componentes a las 24 horas; pero, en el grupo de sangre total hubo un menor uso de unidades de plasma y plaquetas en las primeras horas. La evaluación de la administración de sangre total prehospitalaria y en sala de emergencias, encontró una reducción de hasta un 50% en el uso de productos sanguíneos después de salir de la sala de emergencia 43.
El rol de la autotransfusión
En centros donde la sangre total no está disponible, la autotransfusión provee una alternativa atractiva. Un estudio de 272 pacientes en dos hospitales de I nivel en EE. UU. demostró que la autotransfusión del hemotórax en pacientes de trauma se asoció con a una disminución en el uso de unidades de glóbulos rojos y de plaquetas, así como una disminución del costo total y no reportó diferencias en las complicaciones. En el proceso de autotransfusión, se recolecta la sangre desde el paciente a un sistema que contiene citrato fosfatasa dextrosa, seguida de la transfusión del producto anticoagulado al paciente directo sin necesidad de realizar un cruce 46. De manera similar, Folkersen et al. (47, describieron una disminución significativa en el uso de unidades de glóbulos rojos y menor drenaje postquirúrgico en pacientes de cirugía de corazón tratados con un auto transfusión de sangre recolectada del mediastino.
Capacidad hemostática de la sangre total
Uno de los dilemas de la sangre total para ser implementada en la esfera civil se relaciona con la falta de información respecto a la eficacia hemostática de las plaquetas guardadas en frío. Los estándares de la Asociación Estadounidense de Bancos de Sangre (American Association of Blood Bank - AABB, por sus siglas en inglés) mantienen que las plaquetas deben almacenarse a 22-24° C con agitación suave y continua durante un máximo de 5 días. El razonamiento detrás de esta pauta es la teoría de que las plaquetas mantienen mejor su función después de la transfusión en estas condiciones. Sin embargo, el almacenamiento a temperatura ambiente aumenta la posibilidad de contaminación bacteriana y conduce a una disminución en la función plaquetaria debido a una disminución en el pH 48. Nuevos estudios sugieren que las plaquetas guardadas en frío conservan la función hemostática hasta por 21 días, y que las plaquetas refrigeradas pueden lograr una hemostasia más efectiva que las plaquetas a temperatura ambiente 12.
El grupo de Cirugía de Trauma y Emergencias en Cali, recientemente ha terminado un proceso de validación de sangre total para ser procesada mediante un sistema ahorrador de plaquetas y leucorredución, evaluando su capacidad de conservar los componentes celulares, los factores de coagulación y su capacidad hemostática hasta por 21 días. Se realizo el análisis de 20 unidades de sangre total de donantes jóvenes hombres y mujeres nulíparas. La sangre fue almacenada en refrigeración sin agitación a temperaturas entre 2º C y 8º C. Se encontró que el conteo de eritroides, hemoglobina y hematocrito se mantuvo estable, el conteo de plaquetas descendió en los primeros seis días, pero se mantuvo mayor a 100,000 celulas/mL, hasta el día 21. Los factores de coagulación, fibrinógeno y proteína C de la coagulación se mantuvieron en rangos normales. Su propiedad hemostática evaluada mediante la Tromboelastografía mostró una leve prolongación en la iniciación y progresión del coagulo, pero tiene una formación estable del coagulo finalmente. Estos resultados preliminares, son el sustento para el desarrollo del ensayo clínico, controlado, aleatorizado WEBSTER, el cual probará este sistema de sangre total, siendo pionero en el mundo en la conservación y aplicación de sangre total en trauma civil 49.
Seguridad de sangre total
En el Hospital Vicente Corral Moscoso en el sur de Ecuador, el grupo O de sangre total sin títulos y sin leucorreducción está disponible para pacientes quirúrgicos que se presentan en choque hemorrágico. En una serie reciente de 93 pacientes exsanguinados de los servicios de trauma y ginecobstetricia, no se observaron reacciones transfusionales asociadas al uso de sangre total. La población en esta región del Ecuador, predominantemente, es un grupo de O +, lo que lo convierte en un lugar ideal para la implementación de un programa de sangre total 37.
No se ha demostrado diferencias en la tasa de reacciones transfusionales en pacientes receptores de sangre total tipo O con bajos títulos, en contraste a pacientes tratados con terapia de componentes. Igualmente, tampoco se han reportado diferencias en pacientes tratados con terapia combinada de hemo componentes y sangre total tipo O con bajos títulos 42,44. Existe un caso reportado acerca de una sobrecarga circulatoria relacionada con la transfusión en un paciente transfundido con sangre total tipo O con bajos títulos 42. No se ha documentado ningún cambio en los marcadores de hemólisis con la administración de hasta cuatro unidades de sangre total 43,45,50.
Conclusión
La reanimación de los pacientes que se presentan con choque hemorrágico por trauma ha evolucionado desde la administración de altos volúmenes de cristaloides, terapia de hemo componentes y nuevamente el de sangre total. La resucitación de control de daños ha implementado una estrategia de reanimación con hemoderivados usando una fórmula balanceada 1:1:1:1, que intenta simular los componentes celulares y factores de coagulación fisiológicos. Sin embargo, tiene una alta demanda técnica y de disponibilidad en el manejo convencional del trauma. La sangre total puede ser factible como una estrategia dentro de la resucitación hemostática que tiene ventajas técnicas y un perfil de resultados superior a la terapia estándar.
References
1. Eastridge BJ, Holcomb JB, Shackelford S. Outcomes of traumatic hemorrhagic shock and the epidemiology of preventable death from injury. Transfusion. 2019;59(S2):1423-8. doi: 10.1111/trf.15161 [ Links ]
2. Holcomb JB, Tilley BC, Baraniuk S, Fox EE, Wade CE, Podbielski JM, et al. Transfusion of plasma, platelets, and red blood cells in a 1:1:1 vs a 1:1:2 ratio and mortality in patients with severe trauma: the PROPPR randomized clinical trial. JAMA. 2015;313(5):471-82. doi: 10.1001/jama.2015.12 [ Links ]
3. Moore SE, Decker A, Hubbard A, Callcut RA, Fox EE, Del Junco DJ, et al. Statistical Machines for Trauma Hospital Outcomes Research: Application to the PRospective, Observational, Multi-Center Major Trauma Transfusion (PROMMTT) Study. PLoS One. 2015;10(8):e0136438. doi: 10.1371/journal.pone.0136438 [ Links ]
4. Spinella PC, Pidcoke HF, Strandenes G, Hervig T, Fisher A, Jenkins D, et al. Whole blood for hemostatic resuscitation of major bleeding. Transfusion. 2016;56 Suppl 2:S190-202. doi: 10.1111/trf.13491 [ Links ]
5. Cap AP, Pidcoke HF, Spinella P, Strandenes G, Borgman MA, Schreiber M, et al. Damage Control Resuscitation. Mil Med. 2018; 183(suppl 2): 36-43. doi: 10.1093/milmed/usy112 [ Links ]
6. Chang R, Holcomb JB. Optimal Fluid Therapy for Traumatic Hemorrhagic Shock. Crit Care Clin. 2017;33(1):15-36. doi: 10.1016/j.ccc.2016.08.007 [ Links ]
7. Woolley T, Thompson P, Kirkman E, Reed R, Ausset S, Beckett A, et al. Trauma Hemostasis and Oxygenation Research Network position paper on the role of hypotensive resuscitation as part of remote damage control resuscitation. J Trauma Acute Care Surg. 2018;84(6S Suppl 1): S3-S13. doi: 10.1097/TA.0000000000001856 [ Links ]
8. Ordoñez CA, Badiel M, Pino LF, Salamea JC, Loaiza JH, Parra MW, et al. Damage control resuscitation: early decision strategies in abdominal gunshot wounds using an easy “ABCD” mnemonic. J Trauma Acute Care Surg. 2012;73(5):1074-8. doi: 10.1097/TA.0b013e31826fc780 [ Links ]
9. Holcomb JB, Fox EE, Wade CE; Group PS. The PRospective Observational Multicenter Major Trauma Transfusion (PROMMTT) study. J Trauma Acute Care Surg. 2013;75(1 Suppl 1):S1-2. doi: 10.1097/TA.0b013e3182983876 [ Links ]
10. Brown JB, Guyette FX, Neal MD, Claridge JA, Daley BJ, Harbrecht BG, et al. Taking the Blood Bank to the Field: The Design and Rationale of the Prehospital Air Medical Plasma (PAMPer) Trial. Prehosp Emerg Care. 2015;19(3):343-50. doi: 10.3109/10903127.2014.995851 [ Links ]
11. Spinella PC, Cap AP. Whole blood: back to the future. Curr Opin Hematol. 2016;23(6):536-42. doi: 10.1097/MOH.0000000000000284 [ Links ]
12. Cap AP, Beckett A, Benov A, Borgman M, Chen J, Corley JB, et al. Whole Blood Transfusion. Mil Med. 2018;183(suppl_2):44-51. doi: 10.1093/milmed/usy120 [ Links ]
13. Muñoz-Valencia A, Bonilla-Escobar F, Puyana JC. Effect of blood bank availability on mortality due to shock after trauma in a middle-income country. San Francisco, CA: American College of Surgeons; 2019. doi: 10.1016/j.jamcollsurg.2019.08.288 [ Links ]
14. Roberts N, James S, Delaney M, Fitzmaurice C. The global need and availability of blood products: a modelling study. Lancet Haematol. 2019;6(12):e606-e15. doi: 10.1016/S2352-3026(19)30200-5 [ Links ]
15. The World Health Organization. Blood safety and availability; 2019. Available from: https://www.who.int/news-room/fact-sheets/detail/blood-safety-and-availability. [ Links ]
16. Pan American Health Association. Latin America and the Caribbean approaching half-way mark toward goal of 100% voluntary blood donation. Pan American Health Association; 2016. Available from: https://www.paho.org/salud-en-las-americas-2017/?tag=en. [ Links ]
17. Pan American Health Organization. Supply of Blood for Transfusion in Latin American and Caribbean Countries 2014 and 2015 Washington D.C.: Pan American Health Organization; 2017. [ Links ]
18. MacLeod JB, Lynn M, McKenney MG, Cohn SM, Murtha M. Early coagulopathy predicts mortality in trauma. J Trauma. 2003;55(1):39-44. doi: 10.1097/01.TA.0000075338.21177.EF [ Links ]
19. Kushimoto S, Kudo D, Kawazoe Y. Acute traumatic coagulopathy and trauma-induced coagulopathy: an overview. J Intensive Care. 2017;5(6). doi: 10.1186/s40560-016-0196-6 [ Links ]
20. Mizobata Y. Damage control resuscitation: a practical approach for severely hemorrhagic patients and its effects on trauma surgery. J Intensive Care. 2017;5(4). doi: 10.1186/s40560-016-0197-5 [ Links ]
21. Ditzel RM, Anderson JL, Eisenhart WJ, Rankin CJ, DeFeo DR, Oak S, et al. A review of transfusion- and trauma-induced hypocalcemia: Is it time to change the lethal triad to the lethal diamond? J Trauma Acute Care Surg. 2020;88(3):434-9. doi: 10.1097/TA.0000000000002570 [ Links ]
22. Ordoñez CA, Parra MW, Serna JJ, Rodríguez HF, García AF, Salcedo A, et al. Damage Control Resuscitation?: REBOA as the New Fourth pillar. Colomb Med (Cali). 2020; 51(4): e-4014353. doi: 10.25100/cm.v51i4.4353. [ Links ]
23. Shoemaker WC, Appel PL, Kram HB, Waxman K, Lee TS. Prospective trial of supranormal values of survivors as therapeutic goals in high-risk surgical patients. Chest. 1988;94(6):1176-86. doi: 10.1378/chest.94.6.1176 [ Links ]
24. Kasotakis G, Sideris A, Yang Y, de Moya M, Alam H, King DR, et al. Aggressive early crystalloid resuscitation adversely affects outcomes in adult blunt trauma patients: an analysis of the Glue Grant database. J Trauma Acute Care Surg. 2013;74(5):1215-21; discussion 21-2. [ Links ]
25. Bickell WH, Wall MJ, Pepe PE, Martin RR, Ginger VF, Allen MK, et al. Immediate versus delayed fluid resuscitation for hypotensive patients with penetrating torso injuries. N Engl J Med. 1994;331(17):1105-9. doi: 10.1056/NEJM199410273311701 [ Links ]
26. Ley EJ, Clond MA, Srour MK, Barnajian M, Mirocha J, Margulies DR, et al. Emergency department crystalloid resuscitation of 1.5 L or more is associated with increased mortality in elderly and nonelderly trauma patients. J Trauma. 2011;70(2):398-400. doi: 10.1097/TA.0b013e318208f99b [ Links ]
27. Borgman MA, Spinella PC, Perkins JG, Grathwohl KW, Repine T, Beekley AC, et al. The ratio of blood products transfused affects mortality in patients receiving massive transfusions at a combat support hospital. J Trauma. 2007;63(4):805-13. doi: 10.1097/TA.0b013e3181271ba3 [ Links ]
28. Savage SA, Zarzaur BL, Croce MA, Fabian TC. Redefining massive transfusion when every second counts. J Trauma Acute Care Surg. 2013;74(2):396-400. doi: 10.1097/TA.0b013e31827a3639 [ Links ]
29. Pommerening MJ, Goodman MD, Holcomb JB, Wade CE, Fox EE, Del Junco DJ, et al. Clinical gestalt and the prediction of massive transfusion after trauma. Injury. 2015;46(5):807-13. doi: 10.1016/j.injury.2014.12.026 [ Links ]
30. Johansson PI, Stissing T, Bochsen L, Ostrowski SR. Thrombelastography and tromboelastometry in assessing coagulopathy in trauma. Scand J Trauma Resusc Emerg Med. 2009;17:45. doi: 10.1186/1757-7241-17-45 [ Links ]
31. Hunt H, Stanworth S, Curry N, Woolley T, Cooper C, Ukoumunne O, et al. Thromboelastography (TEG) and rotational thromboelastometry (ROTEM) for trauma induced coagulopathy in adult trauma patients with bleeding. Cochrane Database Syst Rev. 2015(2):CD010438. doi: 10.1002/14651858.CD010438.pub2 [ Links ]
32. Gonzalez E, Moore EE, Moore HB. Management of Trauma-Induced Coagulopathy with Thrombelastography. Crit Care Clin. 2017;33(1):119-34. doi: 10.1016/j.ccc.2016.09.002 [ Links ]
33. Spinella PC, Perkins JG, Grathwohl KW, Beekley AC, Holcomb JB. Warm fresh whole blood is independently associated with improved survival for patients with combat-related traumatic injuries. J Trauma. 2009;66(4 Suppl):S69-76. doi: 10.1097/TA.0b013e31819d85fb [ Links ]
34. Yazer MH, Cap AP, Spinella PC. Raising the standards on whole blood. J Trauma Acute Care Surg. 2018;84(6S Suppl 1):S14-S7. doi: 10.1097/TA.0000000000001778 [ Links ]
35. Hess JR. Resuscitation of trauma-induced coagulopathy. Hematology Am Soc Hematol Educ Program. 2013;2013:664-7. doi: 10.1182/asheducation-2013.1.664 [ Links ]
36. Sarmiento Altamirano D, Himmler A, Chango Sigüenza O, Pino Andrade R, Flores Lazo N, Reinoso Naranjo J, et al. The successful implementation of a trauma and acute care surgery model in Ecuador. World J Surg. 2020. doi: 10.1007/s00268-020-05435-z [ Links ]
37. Himmler A, Galarza M, Reinoso J, Peña S, Sarmiento D, Flores N, et al. Is the whole greater than the sum of its parts? The implementation and outcomes of a whole blood program in Ecuador. Res Sq, 2020. doi: 10.21203/rs.3.rs-66244/v1. [ Links ]
38. Perkins JG, Cap AP, Spinella PC, Shorr AF, Beekley AC, Grathwohl KW, et al. Comparison of platelet transfusion as fresh whole blood versus apheresis platelets for massively transfused combat trauma patients (CME). Transfusion. 2011;51(2):242-52. doi: 10.1111/j.1537-2995.2010.02818.x [ Links ]
39. Nessen SC, Eastridge BJ, Cronk D, Craig RM, Berséus O, Ellison R, et al. Fresh whole blood use by forward surgical teams in Afghanistan is associated with improved survival compared to component therapy without platelets. Transfusion. 2013; 53 Suppl 1:107S-13S. doi: 10.1111/trf.12044 [ Links ]
40. Ho KM, Leonard AD. Lack of effect of unrefrigerated young whole blood transfusion on patient outcomes after massive transfusion in a civilian setting. Transfusion. 2011;51(8):1669-75. doi: 10.1111/j.1537-2995.2010.02975.x [ Links ]
41. Cotton BA, Podbielski J, Camp E, Welch T, del Junco D, Bai Y, et al. A randomized controlled pilot trial of modified whole blood versus component therapy in severely injured patients requiring large volume transfusions. Ann Surg. 2013;258(4):527-32. doi: 10.1097/SLA.0b013e3182a4ffa0 [ Links ]
42. Hazelton JP, Cannon JW, Zatorski C, Roman JS, Moore SA, Young AJ, et al. Cold-stored whole blood: A better method of trauma resuscitation? J Trauma Acute Care Surg. 2019;87(5):1035-41. doi: 10.1097/TA.0000000000002471 [ Links ]
43. Williams J, Merutka N, Meyer D, Bai Y, Prater S, Cabrera R, et al. Safety profile and impact of low-titer group O whole blood for emergency use in trauma. J Trauma Acute Care Surg. 2020;88(1):87-93. doi: 10.1097/TA.0000000000002498 [ Links ]
44. Yazer MH, Jackson B, Sperry JL, Alarcon L, Triulzi DJ, Murdock AD. Initial safety and feasibility of cold-stored uncrossmatched whole blood transfusion in civilian trauma patients. J Trauma Acute Care Surg. 2016;81(1):21-6. doi: 10.1097/TA.0000000000001100 [ Links ]
45. Seheult JN, Anto V, Alarcon LH, Sperry JL, Triulzi DJ, Yazer MH. Clinical outcomes among low-titer group O whole blood recipients compared to recipients of conventional components in civilian trauma resuscitation. Transfusion. 2018;58(8):1838-45. doi: 10.1111/trf.14779 [ Links ]
46. Rhee P, Inaba K, Pandit V, Khalil M, Siboni S, Vercruysse G, et al. Early autologous fresh whole blood transfusion leads to less allogeneic transfusions and is safe. J Trauma Acute Care Surg. 2015;78(4):729-34. doi: 10.1097/TA.0000000000000599 [ Links ]
47. Folkersen L, Tang M, Grunnet N, Jakobsen CJ. Transfusion of shed mediastinal blood reduces the use of allogenic blood transfusion without increasing complications. Perfusion. 2011;26(2):145-50. doi: 10.1177/0267659110393299 [ Links ]
48. Bahr MP, Yazer MH, Triulzi DJ, Collins RA. Whole blood for the acutely haemorrhaging civilian trauma patient: a novel idea or rediscovery? Transfus Med. 2016;26(6):406-14. doi: 10.1111/tme.12329 [ Links ]
49. Macia C, Guzmán M, Hernández E, Alcala M, García A, Caicedo Y, et al. Whole blood prepared via a platelet-sparing leukoreduction filtration system preserves the hemostatic function for 21 days: early results of a pilot study to expand the use of whole blood for trauma in South America. J Am Coll Surg 2020;231:e64. doi: 10.1016/j.jamcollsurg.2020.08.156. [ Links ]
50. Seheult JN, Triulzi DJ, Alarcon LH, Sperry JL, Murdock A, Yazer MH. Measurement of haemolysis markers following transfusion of uncrossmatched, low-titre, group O+ whole blood in civilian trauma patients: initial experience at a level 1 trauma centre. Transfus Med. 2017;27(1):30-5. doi: 10.1111/tme.12372 [ Links ]
Recibido: 21 de Agosto de 2020; Revisado: 25 de Noviembre de 2020; Aprobado: 18 de Diciembre de 2020











 text in
text in 



