Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Colombia Médica
On-line version ISSN 1657-9534
Colomb. Med. vol.52 no.2 Cali Apr./June 2021 Epub June 30, 2021
https://doi.org/10.25100/cm.v52i2.4777
Articulo de revisión
El cierre de la pared abdominal y torácica: La cenicienta en la cirugía control de daños
1 Fundación Valle del Lili. Department of Surgery. Division of Trauma and Acute Care Surgery, Cali, Colombia.
2 Universidad del Valle, Facultad de Salud, Escuela de Medicina, Department of Surgery. Division of Trauma and Acute Care Surgery, Cali, Colombia.
3 Hospital Universitario del Valle, Department of Surgery. Division of Trauma and Acute Care Surgery, Cali, Colombia.
4 Centro Médico Imbanaco, Cali, Colombia.
5 Hospital Pablo Tobon Uribe, Department of Surgery, Medellín, Colombia.
6 Universidad de Antioquia, Department of Surgery, Medellín, Colombia.
7 Universidad Icesi, Cali, Colombia.
8 Hospital Vicente Corral Moscoso. Department of Surgery. Division of Trauma and Acute Care Surgery, Cuenca, Ecuador.
9 Universidad de Cuenca. Cuenca, Ecuador.
10Medstar Georgetown University Hospital and Washington Hospital Center. Department of Surgery, Washington, D.C., USA.
11 , Fundación Valle del Lili, Centro de Investigaciones Clínicas (CIC)Cali, Colombia
12 Broward General Level I Trauma Center, Department of Trauma Critical Care, Fort Lauderdale, FL - USA
Damage control surgery principles allow delayed management of traumatic lesions and early metabolic resuscitation by performing abbreviated procedures and prompt resuscitation maneuvers in severely injured trauma patients. However, the initial physiological response to trauma and surgery, along with the hemostatic resuscitation efforts, causes important side effects on intracavitary organs such as tissue edema, increased cavity pressure, and hemodynamic collapse. Consequently, different techniques have been developed over the years for a delayed cavity closure. Nonetheless, the optimal management of abdominal and thoracic surgical closure remains controversial. This article aims to describe the indications and surgical techniques for delayed abdominal or thoracic closure following damage control surgery in severely injured trauma patients, based on the experience obtained by the Trauma and Emergency Surgery Group (CTE) of Cali, Colombia. We recommend negative pressure dressing as the gold standard technique for delayed cavity closure, associated with higher wall closure success rates and lower complication and mortality rates.
Key words: Delayed Cavity Closure; Temporary Closure; Open Abdomen; Negative Pressure Dressing; Thoracic Packing; Hemodynamically Unstable; Damage Control Surgery
Contribución del estudio
| 1) ¿Por qué se realizó este estudio? |
| El objetivo de este artículo es presentar las indicaciones y técnicas quirúrgicas para el cierre diferido del abdomen y tórax respecto a la cirugía de control de daños del paciente con trauma severo, a partir de la experiencia del grupo de cirugía de Trauma y Emergencias de Cali, Colombia |
| 2) ¿Cuáles fueron los resultados más relevantes del estudio? |
| Se recomienda el uso de los sistemas de presión negativa como la estrategia ideal para el cierre diferido de la pared abdominal o torácica, que se asocia con una mayor tasa de cierre definitivo, una menor tasa de complicaciones y mejores resultados clínicos. |
| 3¿Qué aportan estos resultados? |
| El cierre diferido de la cavidad abdominal o torácica en el contexto de cirugía de control de daños debe ser un puente para el manejo definitivo, permitiendo en este lapsus la prevención del síndrome compartimental, control de la contaminación y contribuir a una buena cicatrización. El uso de sistemas de presión negativa debe ser la principal estrategia en el cierre diferido. |
Introducción
Los principios de la cirugía de control de daños permiten diferir el manejo de la lesión traumática para lograr una resucitación metabólica temprana en pacientes severamente comprometidos en su fisiología. Esta estrategia consiste en realizar procedimientos abreviados y maniobras de resucitación tempranas que buscan controlar de manera provisional el daño, la hemorragia o la contaminación 1-4. Sin embargo, la respuesta inicial al trauma y a la cirugía, junto con los esfuerzos de resucitación hemostática, ocasionan efectos secundarios sobre los órganos intracavitarios como el edema de los tejidos, el aumento de la presión de la cavidad, las alteraciones hemodinámicas e incluso la falla multiorgánica 4,5. Por esta razón, los síndromes compartimentales abdominal y mediastinal se han descrito como fenómenos que repercuten sobre la morbimortalidad de los pacientes con trauma severo 6,7. Con el paso de los años los cirujanos han desarrollado algunas técnicas para el cierre diferido de la pared, haciendo uso de plásticos o sistemas de presión negativa que logran la contención de la cavidad, y generan una vía de drenaje. No obstante, existen controversias sobre la técnica del cierre quirúrgico tanto en el abdomen, como en el tórax por sus implicaciones que tiene sobre la hemostasia, tasa de complicaciones, evolución de la herida quirúrgica, demandas técnicas y costo-efectividad 8,9. El objetivo de este artículo es presentar las indicaciones y técnicas quirúrgicas para el cierre diferido del abdomen y tórax en la cirugía de control de daños
El presente artículo es un consenso que reúne la experiencia de los últimos 30 años en el manejo del trauma, cirugía general y cuidado crítico del grupo de cirugía de Trauma y Emergencias (CTE) de Cali, Colombia conformado por expertos del Hospital Universitario del Valle “Evaristo García”, el Hospital Universitario Fundación Valle del Lili con la Universidad del Valle y la Universidad Icesi, en colaboración con la Asociación Colombiana de Cirugía y la Sociedad Panamericana de Trauma, en conjunto con especialistas internacionales de EE.UU, Europa, Japón, Suráfrica y Latino América.
Epidemiología
La experiencia reportada en la literatura respecto a las técnicas de cierre diferido abdominal y torácico es variable. Hu et al., presentaron un análisis retrospectivo de 239 pacientes con similar severidad del trauma atendidos con cirugía de control de daños abdominal. La técnica de cierre de la pared abdominal fue en el 58% cierre primario de la piel, 25% Bolsa de Bogotá, 15% ABThera™ VAC System y 2% Barker’s vacuum-packing. No hubo diferencias significativas en cuanto a la severidad del trauma entre los grupos y se encontró que los pacientes manejados con cierre primario de piel tuvieron un lactato y base exceso en promedio menor. Los pacientes tratados con Bolsa de Bogotá tuvieron menor oportunidad de cierre de la fascia, en comparación con los pacientes manejados con ABThera VAC System. Sin embargo, no se reportaron diferencias entre los grupos respecto a la mortalidad, estancia hospitalaria o complicaciones como resangrado o lesión intestinal 10.
O’Connor et al., analizaron 44 pacientes con trauma torácico (2002 y 2012) manejados con cirugía de control de daños. El método de elección de cierre de pared torácica fue a través de la colocación de tubo a tórax y empaquetamiento, a excepción de dos pacientes que fueron manejados con sistema de presión negativa. Un paciente con colocación de tubo a tórax y empaquetamiento torácico desarrolló síndrome compartimental 11.
El grupo de cirugía del Hospital San Vicente Fundación en Medellín, Colombia, no encontraron diferencias en la frecuencia o el tiempo del cierre de la fascia, la estancia hospitalaria, complicaciones o mortalidad en una comparación de pacientes manejados con doble Bolsa de Bogotá y malla (37 pacientes) versus pacientes tratados con un sistema de presión negativa no comercial tipo Backer (38). Las complicaciones más comunes en ambos grupos fueron: absceso abdominal, dehiscencia de la anastomosis y formación de fistula 12.
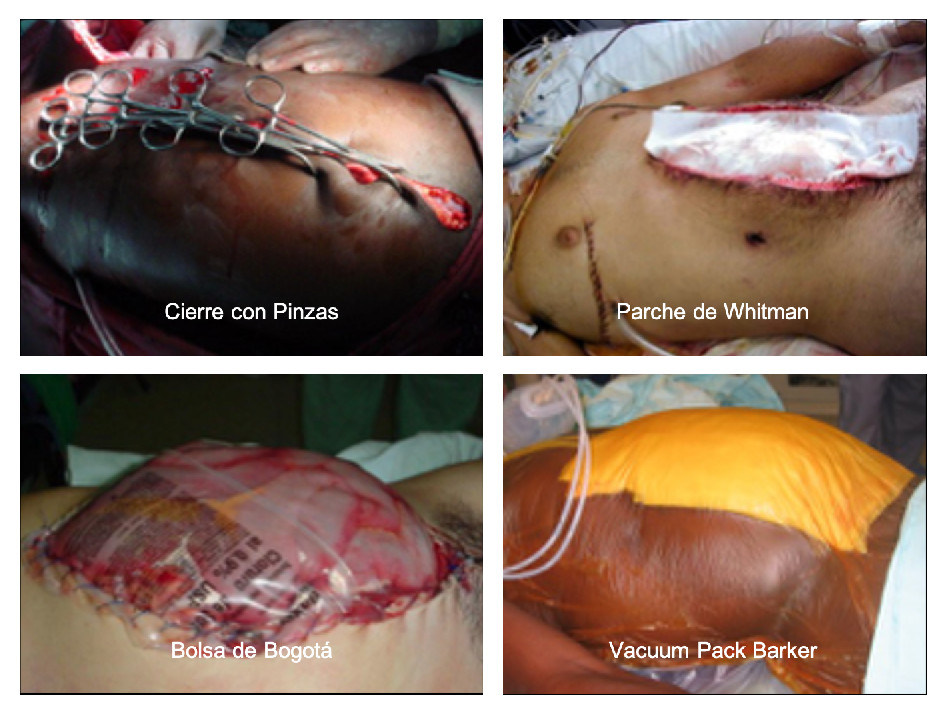
El grupo de Cirugía de Trauma y Emergencias (CTE) de Cali realizó cierre diferido de la pared abdominal a 73 pacientes con trauma severo y cirugía de control de daños entre 2004 y 2011 (Tabla 1). Las técnicas de cierre de pared abdominal tuvieron la siguiente distribución: 52% Vacuum Pack, 25% parche de Wittmann, 11% Bolsa de Bogotá y el 12% cierre primario de piel (Figura 1). Las principales complicaciones asociadas con el cierre diferido fueron sangrado persistente, peritonitis persistente, síndrome compartimental abdominal y fistulas. La mortalidad intrahospitalaria fue del 22%.
Tabla 1 Características generales de pacientes atendidos por el grupo de Cirugía de Trauma y Emergencias (CTE) de Cali, Colombia, mediante cirugía de control de daños y cierre diferido de la pared abdominal.
| Cirugía de Control de Daños y cierre Abdominal Diferido (n = 73) | |
|---|---|
| Edad, años, mediana (RIQ) | 26 (22-38) |
| Masculino, n (%) | 66 (90.4) |
| Injury Severity Score, mediana (RIQ) | 25 (18-34) |
| Abdominal Trauma Index, mediana (RIQ) | 33 (20-43) |
| Mecanismo de Trauma | |
| Penetrante, n (%) | 64 (87.7) |
| Cerrado, n (%) | 9 (12.3) |
| Lesión Anatómica | |
| Cerebral, n (%) | 4 (5.5) |
| Cuello, n (%) | 5 (6.8) |
| Tórax, n (%) | 42 (60) |
| Abdomen, n (%) | 68 (93.2) |
| Extremidades, n (%) | 25 (34.2) |
| Manejo de Abdomen | |
| Empaquetamiento, n (%) | 55 (75.3) |
| Duración, días, mediana (RIQ) | 3 (2-4) |
| Técnica de Cierre | |
| Vacuum Pack, n (%) | 38 (52.1) |
| Parche de Witmann, n (%) | 18 (24.7) |
| Bolsa de Bogotá, n (%) | 8 (11) |
| Cierre de Piel, n (%) | 9 (12.3) |
| Complicaciones | |
| Resangrado, n (%) | 35 (47.9) |
| Peritonitis Persistente, n (%) | 29 (39.7) |
| Síndrome Compartimental Abdominal, n (%) | 29 (39.7) |
| Fistulas, n (%) | 9 (12.3) |
| Evisceración, n (%) | 4 (5.5) |
| Cierre Abdominal Definitivo, n (%) | 46 (63) |
| No. Reintervención, mediana (RIQ) | 4 (2-5) |
| Mortalidad Intrahospitalaria, n (%) | 16 (21.3) |
| Estancia UCI, días, mediana (RIQ) | 10 (6-17) |
| Estancia Hospitalaria, días, mediana (RIQ) | 19 (8-30) |
Consideraciones fisiopatológicas
Cierre de pared abdominal
Existen algunos fenómenos fisiopatológicos que inciden en el éxito del cierre de la pared abdominal o el desarrollo de complicaciones: inflamación peritoneal, aumento del volumen del contenido intraabdominal, cicatrización, formación de adherencias peritoneales y retracción de los bordes de la herida. La hipoxia en la microcirculación intestinal y la inflamación aumentan la permeabilidad celular y produce edema intestinal. Se crea un tercer espacio que puede acumular bacterias y tejido necrótico. Además, genera perdida de células mesoteliales y formación de adherencias peritoneales que producen la retracción del contenido abdominal, favoreciendo el secuestro mecánico y las infecciones intraabdominales. Finalmente, este espacio es rico en citoquinas y mediadores inflamatorios con capacidad de desencadenar una respuesta inflamatoria sistémica 13-15.
Estos fenómenos pueden contribuir al desarrollo de hipertensión abdominal, que se define como la elevación patológica y sostenida de la presión intraabdominal > 12 mm Hg. En el peor de los casos, se puede desarrollar un síndrome compartimental abdominal que se define como una presión intraabdominal sostenida > 20 mm Hg asociada a disfunción orgánica nueva, con repercusiones sobre la mecánica ventilatoria y el retorno venoso 16.
Cierre de pared toráxica
Se ha descrito el síndrome de compartimiento mediastinal en pacientes con cirugía cardiovascular mayor sometidos a cierre esternal 17,18. Este fenómeno de restricción de la cavidad torácica se describió en pacientes que durante el postoperatorio presentaban deterioro del gasto cardíaco y la mecánica ventilatoria. El síndrome de hipertensión torácica se ha descrito como el colapso hemodinámico asociado al cierre de la pared torácica, ocasionado por la presión ejercida sobre la vía aérea y la disminución del retorno venoso, la precarga y el gasto cardiaco. Lo cual, en el caso de persistir, puede ocasionar hipotensión, isquemia subendocárdica y falla multiorgánica 18-20.
Indicaciones para el cierre temporal
Las siguientes son las indicaciones para el cierre temporal de la cavidad abdominal y/o torácica como parte del manejo en la cirugía de control de daños 9,19,21:
Paciente hemodinámicamente inestable o no respondedor transitorio (presión arterial sistólica persistente < 90 mm Hg) con requerimiento de transfusión masiva
Paciente politraumatizado con necesidad de intervención quirúrgica abdominal o torácica urgente
Paciente sometido a cirugía de control de daños que requiera un segundo tiempo quirúrgico para el manejo definitivo del área lesionada
Incapacidad del cierre de la cavidad por edema visceral o riesgo de hipertensión abdominal o torácica
Persistencia de sangrado en la cavidad a pesar de maniobras hemostáticas
Reintervención quirúrgica programada o no, por sangrado o contaminación persistente
Paciente con criterio quirúrgico para seguimiento de la viabilidad de órganos abdominales o torácicos en las siguientes 24 a 48 horas
Metas en el cierre de una cavidad
El cierre diferido de la cavidad en el control de daños es un puente para lograr el manejo definitivo posterior. Sin importar la técnica que se emplee para el cierre de la cavidad abdominal o torácica, el cirujano debe tener en cuenta que este procedimiento debe cumplir con las siguientes metas en el manejo del paciente:
Prevención del Síndrome compartimental
Control de la contaminación
Cicatrización de la herida y cierre diferido de la cavidad
Los estudios que comparan el uso de sistemas de presión negativa versus Bolsa de Bogotá no son concluyentes (Tabla 2). Los grupos de estudio que fueron manejados con bolsa de Bogotá se relacionaron con una tendencia a mayor presión intrabdominal y más días para el cierre definitivo de la cavidad. En cambio, los sistemas de presión negativa tuvieron mejores desenlaces respecto al cierre temprano del abdomen y la progresión de la cicatrización 10,22-26. La composición de los sistemas de presión negativa permite el cumplimiento de las tres metas de manejo, en cambio, la bolsa de Bogotá tiene desventajas respecto al control de la contaminación y del manejo de la cicatrización.
Tabla 2 Estudios recientes que evaluaron el uso de sistema de presión negativa vs Bolsa de Bogotá en el manejo del cierre abdominal diferido
| Tipo de Tratamiento Quirúrgico y Patologías | Sistema de Presión Negativa | Bolsa de Bogotá | ||||||
|---|---|---|---|---|---|---|---|---|
| n | Síndrome compartimental (presión intra abdominal) | Control Contaminación | Cicatrización de la Herida | n | Síndrome compartimental (presión intra abdominal) | Control Contaminación | Cicatrización de la Herida | |
| ECA: Laparotomía descompresiva por Síndrome Compartimental asociado a trauma o cirugía abdominal 26 | 20 | Dia 1 POP: 7.6±2.9 mm Hg Dia 14: 3.5±1.6mm Hg* | Sepsis 2/20 pacientes | Cierre de la herida: 16.9±3.2 días* | 20 | Dia 1 POP: 8.4±3.4 mm Hg. Dia 14: 5.1±2.5 mm Hg* | Sepsis 4/20 pacientes | Cierre de la herida: 20.5±9.9 días* |
| ECP: Cierre temporal abdominal por trauma, sepsis o patología abdominal vascular 25 | 35 | La presión disminuyó más rápido en el grupo tratado con presión negativa | - | Tiempo de Abdomen Abierto: 4(3-5) días ** | 31 | - | Abdomen Abierto: 6 (3-8) días ** | |
| ECP: Cierre temporal abdominal por trauma o patología abdominal 24 | 9 | Ingreso: 10±3 mm Hg. 48 h: 11±3 mm Hg* | - | - | 13 | Ingreso: 13±5 mm Hg. 48h: 11±3 mm Hg* | - | - |
| ECP:Cierre temporal abdominal por trauma o patología abdominal 23 | 163 | - | - | Abdomen abierto: 5±4.1dias* | 117 | - | - | Abdomen abierto: 5±4.4 días* |
| Cierre de fascia: n=83 | ||||||||
| Cierre de fascia: n=98 | ||||||||
| ER: Cierre temporal abdominal por cirugía de control de daños 10 | 36 | - | Absceso intrabdominal: n =10 | Abdomen abierto: 4.6±3.8 días* | 60 | - | Absceso intrabdominal: n =24 | Abdomen abierto: 5.7±5.5 días* |
| Infección de la herida: n =2 | Cierre de fascia: n=34 | Infección de la herida: n =13 | Cierre de fascia: n=50 | |||||
| ER:Cierre temporal abdominal 22 | 15 | - | - | Abdomen abierto: 5(2-69) días*** | 49 | - | - | Abdomen abierto: 4(1-24) días*** |
ECA: Ensayo Clínico Aleatorizado
ECP: Estudio Cohorte Prospectivo
ER: Estudio Retrospectivo
Por otro lado, los sistemas de presión negativa pueden ser de tipo artesanal o comercial. Los dispositivos artesanales son el parche de Wittman o el Barker Vaccuum pack 27,28, que tienen como principio un empaquetamiento de la cavidad que se conecta a un sistema de succión continuo no controlado. Los dispositivos comerciales resuelven problemas que se presentan con los sistemas artesanales respecto a evitar adherencias, control de la presión negativa, disponibilidad de terapia continua e intermitente de presión y el uso de adhesivos que disminuyen el riesgo de lesión tisular. Nosotros evaluamos los pacientes con trauma abdominal sometidos a cierre temporal abdominal con sistemas de presión negativa atendidos entre el 2011 y 2020, comparando aquellos manejados con sistemas comerciales vs artesanales. No hubo diferencias significativas respecto a las complicaciones ni a la mortalidad asociada (Tabla 3). Se determino, que no hubo diferencias en el tiempo de cierre definitivo de la herida entre los dos sistemas (Figura 2).
Tabla 3 Características de los pacientes con trauma abdominal sometidos a cierre diferido con sistemas de Presión Negativa
| Sistema Artesanal | Sistema Comercial | Total | |
|---|---|---|---|
| n (%) | 75 (40.8) | 109 (59.2) | 184 (100.0) |
| Edad, años, mediana (RIQ) | 28 (23 - 38) | 30 (23 - 42) | 29 (23 - 41) |
| Masculino, n (%) | 68 (90.7) | 97 (89.0) | 165 (89.7) |
| Trauma penetrante, n (%) | 65 (86.7) | 93 (85.3) | 158 (85.99 |
| Injury Severity Score (ISS), mediana (RIQ) | 25 (17 - 33) | 21 (16 - 26) | 25 (16 - 31) |
| New-Injury Severity Score (NISS), mediana (RIQ) | 34 (25 - 50) | 38 (25 - 59) | 36 (25 - 50) |
| Falla multiorgánica, n (%) | 30 (40.0) | 42 (39.3) | 72 (39.6) |
| Peritonitis, n (%) | 10 (13.3) | 17 (16.0) | 27 (14.9) |
| Fístula intestinal, n (%) | 11 (14.7) | 15 (13.9) | 26 (14.2) |
| Tiempo de cierre definitivo, días, mediana (RIQ) | 3 (4 - 11) | 3 (4 - 10) | 3 (4 - 11) |
| Mortalidad Intrahospitalaria, n(%) | 1 (1.3) | 4 (3.7) | 5 (2.7) |
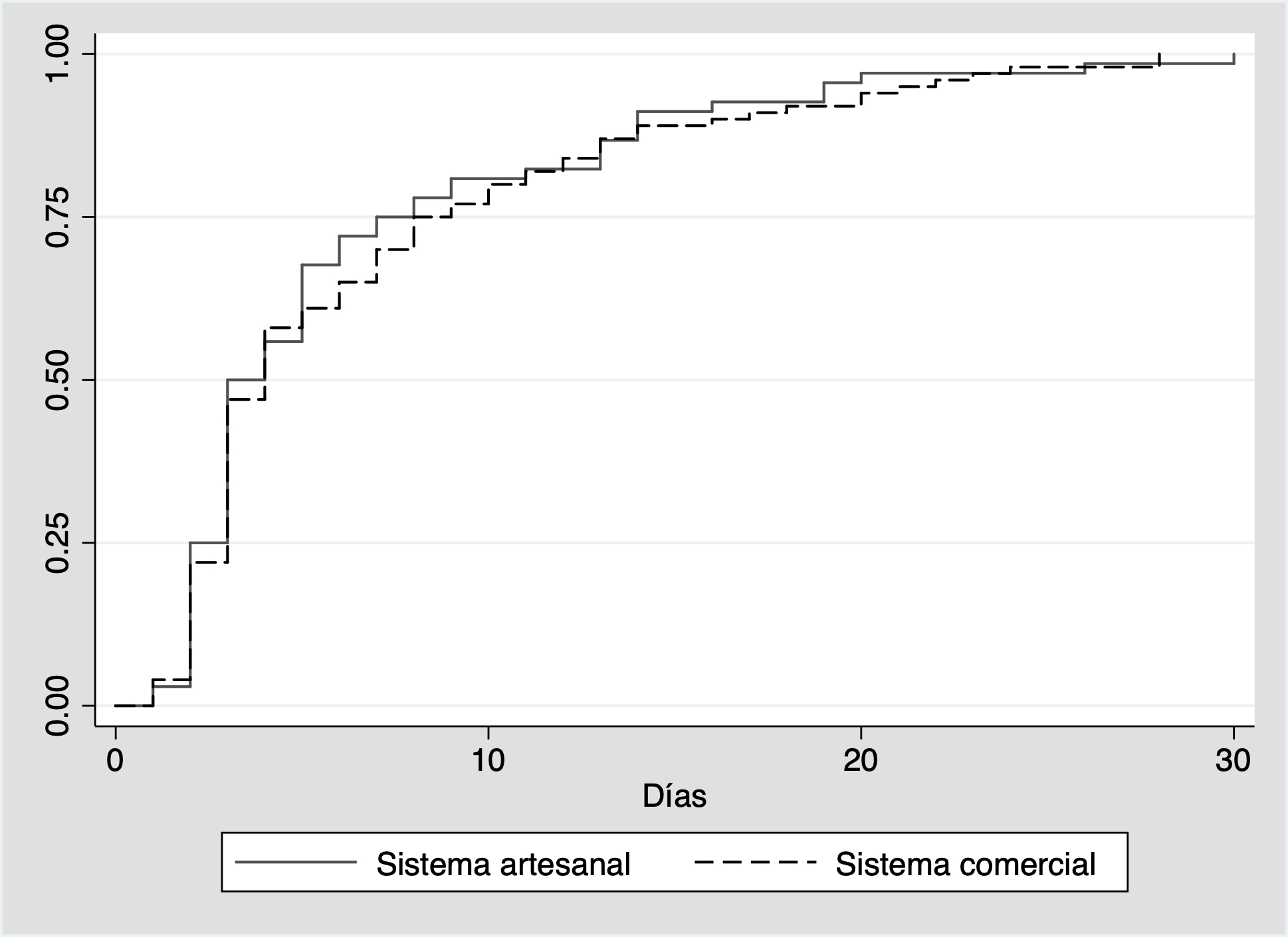
Figura 2 Análisis de Kaplan Meier de tiempo de cierre de la herida respecto al uso de sistemas de presión negativa artesanal y comercial. No hubo diferencia significativa en el tiempo de cierre de la herida entre los sistemas de presión negativa (Log-Rank Test 0.439).
Dado a estos datos y el cumplimiento de las metas de manejo propuestas, el presente artículo propone que la estrategia en el manejo diferido de la cavidad debe ser a través del uso de sistemas de presión negativa.
Manejo quirúrgico
A continuación se presenta un manejo secuencial en el cierre diferido de la cavidad abdominal o torácica, asociado a cirugía de control de daños.
PASO 1 - Cirugía de Control de Daños: Se realiza el control quirúrgico del sangrado y de la contaminación junto con los esfuerzos de resucitación hemostática. Se realizan las intervenciones de control de daños de los órganos o estructuras vasculares comprometidas.
PASO 2 - Asegurar la hemostasia de la herida: Se evalúa si el sangrado ha cedido con la cirugía de control de daños. En el caso de la cavidad torácica, existe la posibilidad de sangrado de una estructura ósea (cuerpo vertebral, costillas o esternón) para lo cual se puede realizar el empaquetamiento de la trayectoria con cera ósea envuelta en hemostático (Surgicel ®). Sin embargo, si persiste el sangrado se puede introducir un catéter con balón (Sonda Foley) directamente por el orificio de la herida ósea, inflar el balón y retraer la sonda suavemente hasta lograr el control de la hemorragia (Figura 3). En caso de una lesión abdominal, se debe realizar el empaquetamiento de la superficie del órgano afectado para lograr un efecto compresivo y hemostático.
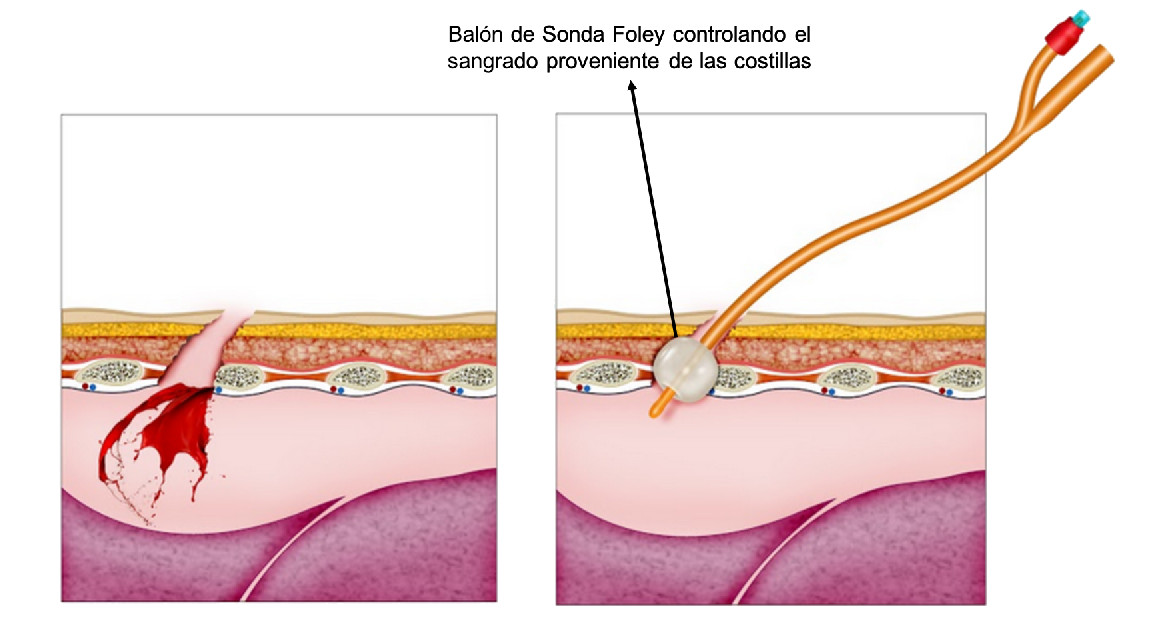
Figura 3 Efecto hemostático sobre la pared torácica con el uso de Sonda Foley. El sangrado persistente que proviene de las estructuras óseas del tórax (cuerpos vertebrales, costillas o esternón) se puede controlar al introducir un catéter con balón (Sonda Foley) directamente por el orificio de la herida ósea, inflar el balón y retraer la sonda suavemente.
PASO 3 - Cierre temporal de la cavidad: Se debe definir entre el uso de técnicas de contención como empaquetamiento y cierre de piel, sistemas de presión negativa o Bolsa de Bogotá. Se proponen los sistemas de presión negativa como el método de elección para el cierre diferido de la cavidad.
Instalar una interfaz de plástico sobre los órganos intraabdominales separándolos de la pared abdominal. Este plástico debe ser permeable hacia el laparaostoma, con perforaciones lineales no mayores a 5 mm para evitar micro-herniaciones de asas. Se pueden usar los plásticos de polipropileno de las bolsas de recolección de tejido para muestras de patología, los cuales deben ser esterilizados y perforados previamente. El plástico debe extenderse sobre los recesos cubriendo completamente la cavidad (Figura 4). El sistema comercial ABThera™ VAC contiene una barrera plástica con una espuma en su interior que cumple dicha función. Debe tener en cuenta que no se debe reducir su tamaño para no dañar el circuito de presión negativa (Figura 5). En caso de no contar con sistemas de presión negativa, se recomienda instalar la bolsa de Bogotá cumpliendo este paso igualmente.
Se deben instalar las espumas o apósitos de transmisión de la presión negativa sobre el plástico fenestrado. En el caso de sistemas comerciales, no se recomienda ubicar compresas bajo la espuma ya que alteran el funcionamiento del sistema (Figura 5). Respecto al manejo del ABThera™ VAC System se deben usar las espumas que contiene el dispositivo, extendiendo la primera espuma detrás de la pared abdominal y sobre el plástico fenestrado, idealmente sin reducirla de tamaño. Posteriormente, se ubica la segunda espuma del kit sobre la primera, cortándola al tamaño del laparostoma, de tal forma que quede al mismo nivel del plano de la pared (Figura 6). En caso del uso de Bolsa de Bogotá, se debe instalar el plástico viaflex suturándolo a los bordes de la pared abdominal.
Se debe sellar el sistema con plástico adhesivo evitando la tracción de los bordes de la herida. Los sistemas comerciales cuentan con suficientes hojas de plástico adherente y permiten aplicar una doble capa de adhesivo que garantiza el adecuado sellado y lo protege del ambiente (Figuras 4 y 5).
Se procede a instalar el dispositivo de succión sobre el plástico adhesivo, recortando y retirando un círculo de plástico entre 3 y 3.5 cm de diámetro que deje expuesta la espuma del kit. Posteriormente, se ubica y adhiere el dispositivo de succión de forma que el tubo de succión y sus canales de sensores queden completamente en contacto con la espuma y con el plástico adhesivo. El tubo de succión se extiende hasta un contenedor de recolección desechable (Figuras 4 y 5).
Realizar la programación y conexión de la fuente de succión. El tubo de succión debe conectarse a una bomba portátil que aplique una presión negativa a la cavidad. Se debe tener en cuenta los parámetros de presión que oscilan entre -50 y -150 mm Hg. Se recomienda idealmente mantener una presión de -125 mm Hg. Algunos sistemas comerciales cuentan además con el control de la intensidad y flujo de la succión. Sin embargo, los sistemas de succión de pared no garantizan la presión de manera precisa ni constante. Se debe vigilar el volumen y cantidad del líquido drenado, igualmente el circuito. La ausencia de drenado con evidencia de distención o dolor debe sospechar que el sistema se encuentra obstruido.
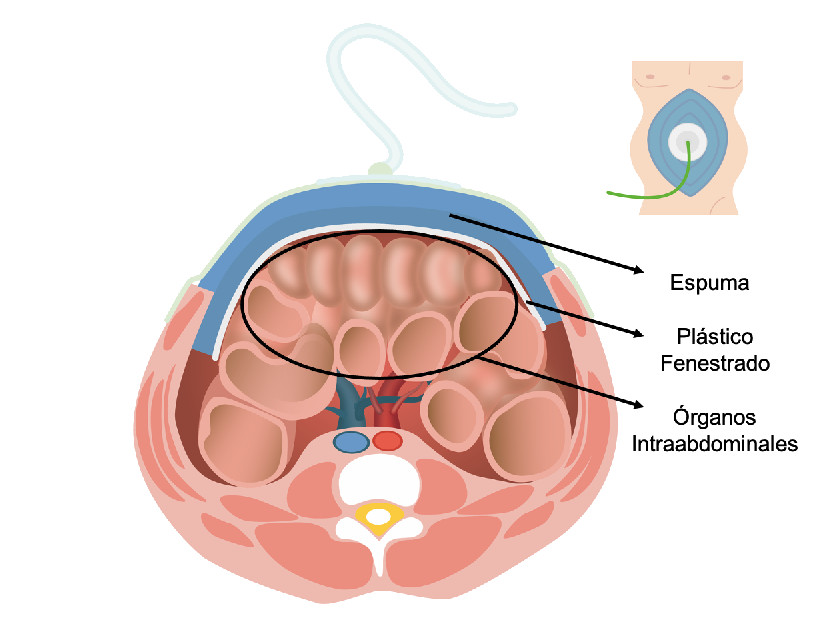
Figura 4 Sistema VAC con interfaz de plástico fenestrado. Un plástico con perforaciones lineales menores de 5 mm debe extenderse por toda la cavidad cubriendo completamente los recesos y separando los órganos intraabdominales de la pared abdominal.
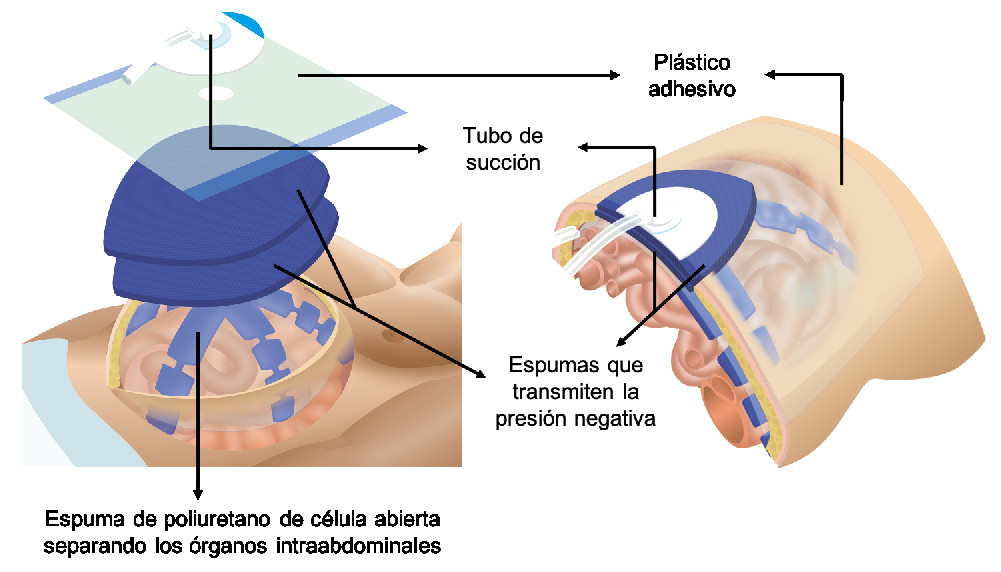
Figura 5 Sistema Comercial ABThera™ VAC. Este sistema contiene una espuma de poliuretano de célula abierta que separa los órganos intraabdominales, 2 espumas que transmiten la presión negativa, varias láminas adhesivas que sellan del sistema y un tubo de succión que se extiende hasta un contenedor de recolección desechable.
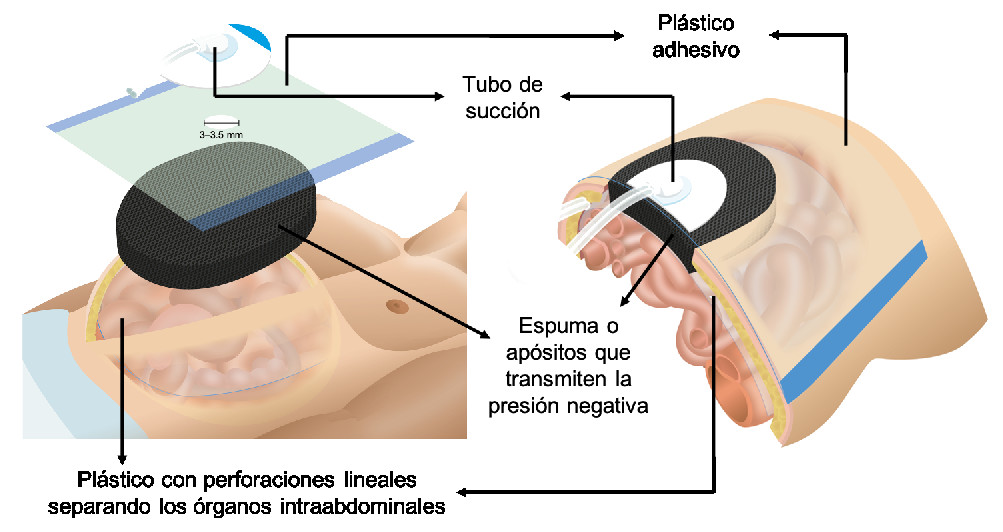
Figura 6 Instalación del sistema de presión negativa. Una interfaz de plástico fenestrado separa los órganos intraabdominales, mientras que las espumas o apósitos se ubican encima y se fijan con una capa doble de plástico adhesivo. El dispositivo de succión se instala sobre el plástico adhesivo recortando un círculo de 3 a 3,5 cm de diámetro.
Cierre de la Pared Torácica: Se deben preparar suficientes fragmentos de espuma que cubran toda el área quirúrgica incluyendo los músculos, el tejido celular subcutáneo y la piel antes de posicionar el sistema de presión negativa. En el caso de un abordaje por toracotomía, se debe asegurar el cubrimiento de las siguientes áreas: bolsillo posterior de la toracotomía formado por los intercostales, serratos y dorsal ancho; costilla superior e inferior en toda su extensión; músculos pectorales; tejido celular subcutáneo y piel. Esta espuma se coloca directamente sobre el área cruenta y se cubre con un apósito impermeable que se conecta al sistema de presión negativa. En caso de no contar con espumas, se puede realizar el sistema de presión negativa con compresas quirúrgicas, pero sin cerrar piel.
Por el contrario, en un abordaje por esternotomía se debe posicionar un plástico perforado en contacto directo con el corazón, seguido de una primera espuma que abarque todo el mediastino y una segunda espuma que cubra los dos bordes de la esternotomía y ocupe el espacio que hay entre ellos. Finalmente, se sella la herida quirúrgica con un plástico adhesivo que se conecta al tubo de succión mediante un orificio cortado en el adhesivo. Se debe asegurar que el efecto de la succión no se interrumpa durante la atención y traslado del paciente hasta su cierre definitivo, pues esta mantiene la hemostasia (Figura 7).
En caso de no contar con un sistema de presión negativa se puede recurrir al empaquetamiento torácico. Si el abordaje fue a través de toracotomía, éste se inicia introduciendo dos compresas en el lugar de mayor sangrado, que corresponde al espacio formado por las costillas, músculos intercostales, serratos y dorsal ancho adyacente. Posteriormente, se abraza cada costilla (superior e inferior) con una compresa y se realiza una sutura continua en la piel con polipropileno 1-0, iniciando ángulo medial y terminando en el ángulo lateral de la incisión quirúrgica. En la medida que avanza la sutura, se va introduciendo una quinta compresa que busca controlar el sangrado de la piel, el tejido celular subcutáneo y los músculos pectorales (Figura 8).
Si se realizó el abordaje del tórax a través de una esternotomía se deben colocar compresas quirúrgicas directamente sobre el corazón hasta ocupar el mediastino completamente. Siempre se debe verificar que no haya cambios hemodinámicos asociados al empaquetamiento. Posteriormente, se coloca un dren (tubo a tórax de pequeño calibre o sonda Levin # 20) y se abrazan los bordes de la esternotomía (derecho e izquierdo) con compresas. Finalmente, se colocan una o dos compresas entre los bordes de la esternotomía y se cierra la piel (Figura 9). Otra alternativa es cubrir ampliamente la herida con un apósito impermeable, dejar el esternón abierto y colocar el dren a succión de manera inmediata.
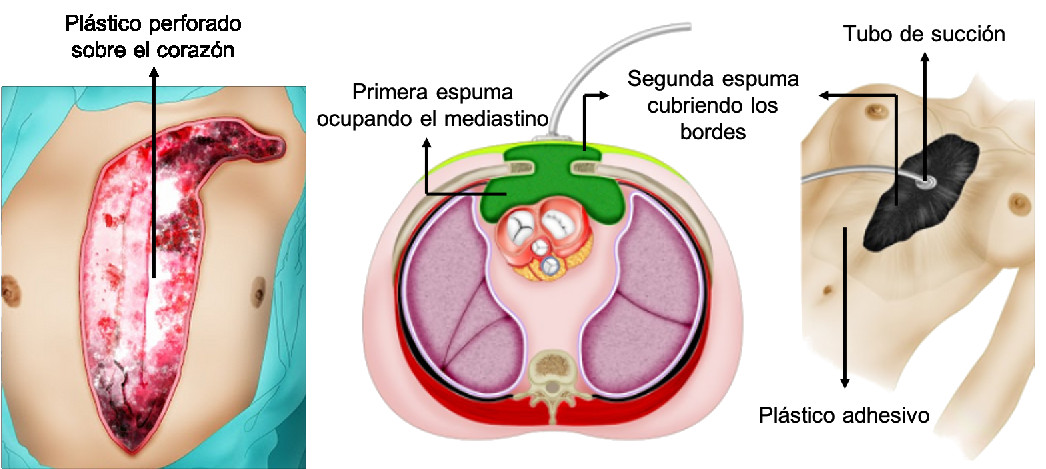
Figura 7 Instalación del sistema de presión negativa en el abordaje por esternotomía. Se extiende un plástico perforado directamente sobre el corazón, seguido de una primera espuma que abarque todo el mediastino y una segunda espuma que cubra los dos bordes de la esternotomía y el espacio entre ellos. Se sella el sistema con un plástico adhesivo, que se conecta al tubo de succión mediante un orificio cortado en el adhesivo.
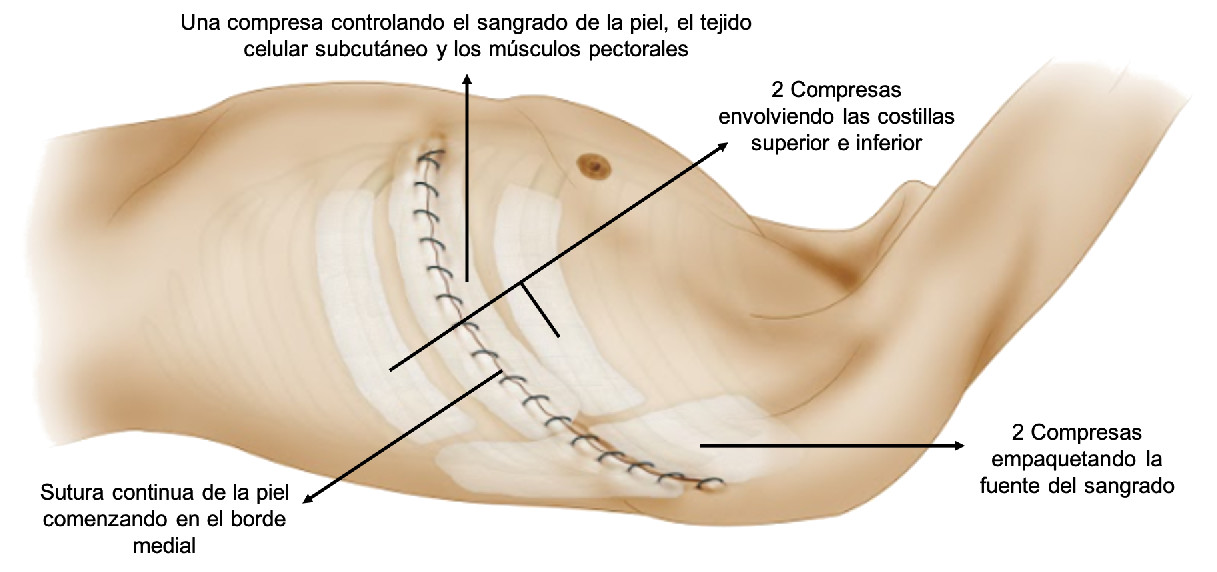
Figura 8 Empaquetamiento torácico en el abordaje por toracotomía. Primero se empaqueta la fuente del sangrado (usualmente costillas o músculos intercostales, serrato o dorsal ancho), seguido de las costillas superior e inferior. Luego se cierra la cavidad con una sutura continúa comenzando en el borde medial e introduciendo una quinta compresa en la herida a medida que avanza la sutura de la piel.
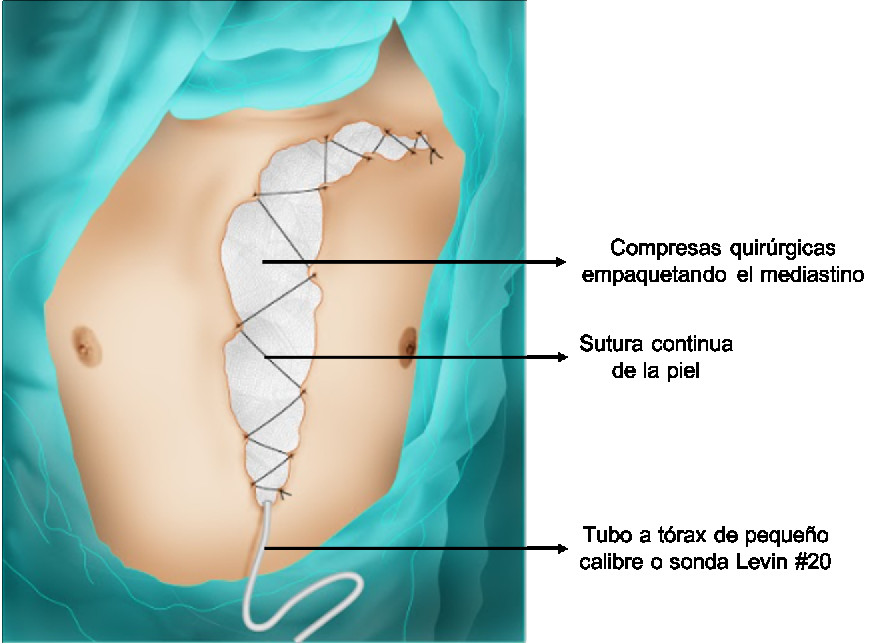
Figura 9 Empaquetamiento torácico en el abordaje por esternotomía mediana. Se sitúan las compresas quirúrgicas directamente sobre el corazón hasta ocupar el mediastino completamente, siempre monitorizando los cambios hemodinámicos. Luego, se ubica un dren, se empaquetan los bordes de la esternotomía y el espacio entre ellos y se cierra la piel.
PASO 4 - Cuidado del cierre temporal: Se debe planear la reintervención en un lapso entre 48 y 72 horas, dependiendo del tipo de trauma. Durante este periodo de tiempo, se debe evaluar la evolución clínica del paciente, mientras se continúa con su resucitación fisiológica en la unidad de cuidados intensivos y se vigilan signos que sugieran un síndrome hipertensivo abdominal o torácico. El monitoreo de la Presión Intraabdominal debe ser el parámetro de evaluación del síndrome compartimental abdominal, junto con una monitoria de la función respiratoria, renal y cardiovascular para identificar a tiempo disfunción orgánica asociada. Hasta la fecha no hay consenso de un parámetro que defina la hipertensión torácica, por lo que el medico debe estar atento a signos de disfunción orgánica no asociada a la hemorragia o procesos infecciosos.
El deterioro clínico del paciente o sangrado persistente en cavidad son indicaciones para una intervención de emergencia con el fin de lograr un control quirúrgico del sangrado o la contaminación. En el caso del seguimiento de un sistema de presión negativa, se recomienda que además de la cantidad y características del fluido drenado se tenga en cuenta la evolución clínica del paciente para determinar la necesidad de una reintervención. Adicionalmente, se debe estar atento al correcto funcionamiento del sistema de presión negativa y a factores como fugas, obstrucciones o problemas técnicos con la bomba.
PASO 5 - Cierre definitivo: Al momento de la reintervención, la espuma o las compresas pueden haberse adherido al tejido de granulación subyacente. Antes de retirarlas, se recomienda realizar una irrigación abundante y constante de la cavidad con líquidos calientes (35 º y 38º C) para disminuir el riesgo de resangrado. Se deben cumplir los siguientes requisitos para el cierre definitivo y seguro de la cavidad:
Discusión
En los últimos años, se han desarrollado importantes avances tecnológicos en los sistemas comerciales de presión negativa logrando mejoras y mayor disponibilidad. Existen múltiples reportes sobre el uso de esta tecnología especialmente en el manejo de pacientes con abdomen abierto. En un subanálisis de los datos recolectados en el International Register of Open Abdomen (IROA) de Italia, se reportó que el sistema de presión negativa fue la técnica más utilizada en aproximadamente el 50% de los casos, seguido de la Bolsa de Bogotá en el 28%. El cierre definitivo de la pared abdominal se logró en el 82% 29.
Poilluci et al., reportaron en un estudio retrospectivo que la mortalidad a 30 días (40.3% del grupo de sistema de presión negativa vs 51.7% del grupo de otros sistemas) y la tasa de colostomías en el trauma colorrectal fue menor en los pacientes manejados con sistema de presión negativa que en aquellos en los que no se utilizó esta tecnología 30. Sibaja y cols., compararon el manejo convencional con Bolsa de Bogotá o parche de Witmann y el uso del sistema de presión negativa con instilación, encontrando en los últimos una r tasa de cierre de fascia del 96%, una mortalidad del 8% sin complicaciones asociadas. 31.
Existen pocas publicaciones que describen el empaquetamiento torácico como medida de control de daños y su impacto en la función cardiorrespiratoria 11,19,32,33. Una cohorte retrospectiva de 61 pacientes, encontró que las presiones pico de las vías respiratorias fueron más bajas en pacientes manejados con empaquetamiento torácico vs. cierre definitivo 33. No obstante, el empaquetamiento torácico se puede asociar a complicaciones tardías tales como neumonía, empiema, mediastinitis, infección del sitio operatorio superficial o profunda, disfunción orgánica, coagulopatía e insuficiencia renal aguda. Los factores asociados al desarrollo de estas complicaciones fueron tiempo quirúrgico prolongado, demora en definir el empaquetamiento y resangrado después de las medidas hemostáticas 34.
Conclusión
El cierre diferido de la cavidad abdominal o torácica en el contexto de cirugía de control de daños debe ser un puente para el manejo definitivo, permitiendo en este lapsus la prevención del síndrome compartimental, control de la contaminación y contribuir a una buena cicatrización. El uso de sistemas de presión negativa debe ser la principal estrategia en el cierre diferido.
Agradecimientos:
Por las ilustraciones y el diseño de la portada al dibujante anatómico Fabian R. Cabrera P. Docente del Departamento de Diseño de la Facultad de Artes Integrada. A Natalia Padilla, Linda M. Gallego y Cindy Natalia Gallego por sus contribuciones en el desarrollo del artículo.
REFERENCIAS
1. Finlay IG, Edwards TJ, Lambert AW. Damage control laparotomy. Br J Surg. 2004; 91: 83-5. Doi: 10.1002/bjs.4434. [ Links ]
2. Benz D, Balogh ZJ. Damage control surgery: Current state and future directions. Curr Opin Crit Care. 2017; 23: 491-7. Doi: 10.1097/MCC.0000000000000465. [ Links ]
3. Giannoudi M, Harwood P. Damage control resuscitation: lessons learned. Eur J Trauma Emerg Surg. 2016; 42: 273-82. Doi: 10.1007/s00068-015-0628-3. [ Links ]
4. Beldowicz BC. The evolution of damage control in concept and practice. Clin Colon Rectal Surg. 2018; 31: 30-5. Doi: 10.1055/s-0037-1602177. [ Links ]
5. Padar M, Blaser AR, Talving P, Lipping E, Starkopf J. Abdominal compartment syndrome: Improving outcomes with a multidisciplinary approach - a narrative review. J Multidiscip Healthc. 2019; 12: 1061-74. Doi: 10.2147/JMDH.S205608. [ Links ]
6. Wall J, Soltero E. Damage control for thoracic injuries. Surg Clin North Am. 1997; 77: 863-78. Doi: 10.1016/S0039-6109(05)70590-9. [ Links ]
7. Roberts DJ, Ball CG, Feliciano D V., Moore EE, Ivatury RR, Lucas CE, et al. History of the innovation of damage control for management of trauma patients: 1902-2016. Ann Surg. 2017; 265: 1034-44. Doi: 10.1097/SLA.0000000000001803. [ Links ]
8. Waibel BH, Rotondo MMF. Cirurgia para o controle de danos: Sua evolução durante os últimos 20 anos. Rev Col Bras Cir. 2012;39:314-21. Doi: 10.1590/S0100-69912012000400012. [ Links ]
9. Coccolini F, Roberts D, Ansaloni L, Ivatury R, Gamberini E, Kluger Y, et al. The open abdomen in trauma and non-trauma patients: WSES guidelines. World J Emerg Surg. 2018; 13: 7. Doi: 10.1186/s13017-018-0167-4. [ Links ]
10. Hu P, Uhlich R, Gleason F, Kerby J, Bosarge P. Impact of initial temporary abdominal closure in damage control surgery: A retrospective analysis. World J Emerg Surg. 2018; 13: 43. Doi: 10.1186/s13017-018-0204-3. [ Links ]
11. O'Connor J V., DuBose JJ, Scalea TM. Damage-control thoracic surgery: Management and outcomes. J Trauma Acute Care Surg. 2014; 77: 660-5. Doi: 10.1097/TA.0000000000000451. [ Links ]
12. Correa JC, Mejía DA, Duque N, J MM, Uribe CM. Managing the open abdomen: negative pressure closure versus mesh-mediated fascial traction closure: a randomized trial. Hernia. 2016; 20: 221-9. Doi: 10.1007/s10029-016-1459-9. [ Links ]
13. Rogers WK, Garcia L. Intraabdominal hypertension, abdominal compartment syndrome, and the open abdomen. Chest. 2018;153:238-50. Doi: 10.1016/j.chest.2017.07.023. [ Links ]
14. Fernandez LG, Sibaja Alvarez P, Kaplan MJ, Sanchez-Betancourt AA, Matthews MR, Cook A. Application of negative pressure wound therapy with instillation and dwell time of the open abdomen: initial experience. Cureus. 2019;11(9): e5667. Doi: 10.7759/cureus.5667. [ Links ]
15. Maluso P, Olson J, Sarani B. Abdominal compartment hypertension and abdominal compartment syndrome. Crit Care Cli. 2016; 32: 213-22. Doi: 10.1016/j.ccc.2015.12.001. [ Links ]
16. Kirkpatrick AW, Roberts DJ, De Waele J, Jaeschke R, Malbrain MLNG, De Keulenaer B, et al. Intra-abdominal hypertension and the abdominal compartment syndrome: Updated consensus definitions and clinical practice guidelines from the World Society of the Abdominal Compartment Syndrome. Intensive Care Med. 2013; 39: 1190-206. Doi: 10.1007/s00134-013-2906-z. [ Links ]
17. Riahi M, Tomatis LA, Schlosser RJ, Bertolozzi E, Johnston DW. Cardiac compression due to closure of the median sternotomy in open heart surgery. Ches.t 1975;67:113-4. Doi: 10.1378/chest.67.1.113. [ Links ]
18. Akay MH, Frazier OH. Thoracic compartment syndrome: A case report. Heart Surg Forum. 2012;15(1): E46-E48. Doi: 10.1532/HSF98.20111071. [ Links ]
19. Caceres M, Buechter KJ, Tillou A, Shih JA, Liu D, Steeb G. Thoracic packing for uncontrolled bleeding in penetrating thoracic injuries. South Med J. 2004;97:637-41. Doi: 10.1097/00007611-200407000-00005. [ Links ]
20. Bouboulis N, Rivas LF, Kuo J, Dougenis D, Dark JH, Holden MP. Packing the chest: A useful technique for intractable bleeding after open heart operation. Ann Thorac Surg. 1994;57:856-60. Doi: 10.1016/0003-4975(94)90189-9. [ Links ]
21. Ordoñez C, Pino L, Badiel M, Sanchez A, Loaiza J, Ramirez O, et al. The 1-2-3 approach to abdominal packing. World J Surg. 2012;36:2761-6. Doi: 10.1007/s00268-012-1745-3. [ Links ]
22. Patel NY, Cogbill TH, Kallies KJ, Mathiason MA. Temporary abdominal closure: Long-term outcomes. J Trauma. 2011;70:769-74. Doi: 10.1097/TA.0b013e318212785e. [ Links ]
23. Coccolini F, Montori G, Ceresoli M, Catena F, Ivatury R, Sugrue M, et al. IROA: International Register of Open Abdomen, preliminary results. World J Emerg Surg. 2017;12: 10. Doi: 10.1186/s13017-017-0123-8. [ Links ]
24. Guetta O, Brotfain E, Shaked G, Sebbag G, Klein M, Czeiger D. Intra-abdominal pressure may be elevated in patients with open abdomen after emergent laparotomy. Langenbeck's Arch Surg. 2020;405:91-6. Doi: 10.1007/s00423-020-01854-7. [ Links ]
25. Batacchi S, Matano S, Nella A, Zagli G, Bonizzoli M, Pasquini A, et al. Vacuum-assisted closure device enhances recovery of critically ill patients following emergency surgical procedures. Crit Care. 2009;13(6):R194. Doi: 10.1186/cc8193. [ Links ]
26. Rencüzogullari A, Dalci K, Eray IC, Yalav O, Okoh AK, Akcam T, et al. Open abdomen yönetiminde erken dönem cerrahi alternatiflerin karsilastirilmasi: Randomize ileriye yönelik çalisma. Ulus Travma ve Acil Cerrahi Derg. 2015; 21: 168-74. Doi: 10.5505/tjtes.2015.09804. [ Links ]
27. Aprahamian C, Wittmann DH, Bergstein JM, Quebbeman EJ. Temporary abdominal closure (TAC) for planned relaparotomy (Etappenlavage) in trauma. J Trauma. 1990; 30: 719-23. Doi: 10.1097/00005373-199006000-00011. [ Links ]
28. Barker DE, Kaufman HJ, Smith LA, Ciraulo DL, Richart CL, Burns RP. Vacuum pack technique of temporary abdominal closure: A 7-year experience with 112 patients. J Trauma. 2000; 48: 201-7. Doi: 10.1097/00005373-200002000-00001. [ Links ]
29. Cicuttin E, Ansaloni L, Ceresoli M, Fugazzola P, Tomasoni M, Sartelli M, et al. Trends in open abdomen management in Italy: a subgroup analysis from the IROA project. Updates Surg. 2020;72:171-7. Doi: 10.1007/s13304-019-00687-4. [ Links ]
30. Poillucci G, Podda M, Russo G, Perri SG, Ipri D, Manetti G, et al. Open abdomen closure methods for severe abdominal sepsis: a retrospective cohort study. Eur J Trauma Emerg Surg. 2020. Doi: 10.1007/s00068-020-01379-0. [ Links ]
31. Sibaja P, Sanchez A, Villegas G, Apestegui A, Mora E. Management of the open abdomen using negative pressure wound therapy with instillation in severe abdominal sepsis: A review of 48 cases in Hospital Mexico, Costa Rica. Int J Surg Case Rep. 2017;30:26-30. Doi: 10.1016/j.ijscr.2016.11.024. [ Links ]
32. Vargo DJ, Battistella FD. Abbreviated thoracotomy and temporary chest closure: An application of damage control after thoracic trauma. Arch Surg. 2001;136:21-4. Doi: 10.1001/archsurg.136.1.21. [ Links ]
33. Lang JL, Gonzalez RP, Aldy KN, Carroll EA, Eastman AL, White CQ, et al. Does temporary chest wall closure with or without chest packing improve survival for trauma patients in shock after emergent thoracotomy? J Trauma. 2011; 70: 705-9. Doi: 10.1097/TA.0b013e31820e89f1. [ Links ]
34. Moriwaki Y, Toyoda H, Harunari N, Iwashita M, Kosuge T, Arata S, et al. Gauze packing as damage control for uncontrollable haemorrhage in severe thoracic trauma. Ann R Coll Surg Engl. 2013; 95: 20-5. Doi: 10.1308/003588413X13511609956057. [ Links ]
Recibido: 16 de Marzo de 2021; Revisado: 18 de Abril de 2021; Aprobado: 30 de Junio de 2021











 text in
text in